Configuration de votre affichage
Vous avez activé le mode de configuration de l'affichage qui permet de sélectionner les informations que vous souhaitez afficher sur la fiche substance. Une fois que vous aurez sélectionné les rubriques à afficher, vous pouvez revenir au mode de consultation de la fiche substance en cliquant à nouveau sur le bouton de filtrage.
1,2,4-Trichlorobenzene (120-82-1)
Introduction
Dernière vérification le 29/03/2024
Dans la période transitoire de mise en cohérence des données du portail, les informations présentées pour cette substance peuvent ne pas être totalement à jour. Nous vous invitons à consulter la substance mère de cette famille : 1,2,3-trichlorobenzène
Informations générales
Dernière vérification le 18/12/2025
Identification
Numero CAS
120-82-1
Nom scientifique (FR)
1,2,4-Trichlorobenzène
Nom scientifique (EN)
Autres dénominations scientifiques (FR)
Autres dénominations scientifiques (Autre langues)
Code EC
204-428-0
Code SANDRE
1283
Numéro CIPAC
-
Formule chimique brute
\(\ce{ C6H3Cl3 }\)
Code InChlKey
Code SMILES
c(ccc(c1Cl)Cl)(c1)Cl
Familles
Familles chimiques
Classification CLP
Type de classification
Harmonisée
ATP insertion
CLP00
Description de la classification
Classification harmonisée selon réglement 1272/2008 ou CLP
| Mention du danger - Code | H302 |
|---|---|
| Mention du danger - Texte | Nocif en cas d'ingestion |
| Classe(s) de dangers | Toxicité aiguë |
| Libellé UE du danger | - |
| Mention du danger - Code | H315 |
|---|---|
| Mention du danger - Texte | Provoque une irritation cutanée |
| Classe(s) de dangers | Corrosion / Irritation cutanée |
| Libellé UE du danger | - |
| Limites de concentration spécifique | - |
| Facteur M | - |
| Estimation de toxicité aigüe | - |
| Mention du danger - Code | H400 |
|---|---|
| Mention du danger - Texte | Très toxique pour les organismes aquatiques |
| Classe(s) de dangers | Danger pour le milieu aquatique |
| Libellé UE du danger | - |
| Mention du danger - Code | H410 |
|---|---|
| Mention du danger - Texte | Très toxique pour les organismes aquatiques, entraîne des effets à long terme |
| Classe(s) de dangers | Danger pour le milieu aquatique |
| Libellé UE du danger | - |
| Limites de concentration spécifique | - |
| Facteur M | - |
| Estimation de toxicité aigüe | - |
Physico-Chimie
Dernière vérification le 29/03/2024
Généralités
Poids moléculaire
181.45 g/mol
Tableau des paramètres
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Bibliographie
Comportement et devenir dans les milieux
Dernière vérification le 29/03/2024
Matrices
Atmosphère
FDTE/VTR Importer Compte tenu de sa pression de vapeur, le 1,2,3-trichlorobenzène se retrouve principalement sous forme de vapeurs dans l'atmosphère.
Milieu eau douce
FDTE/VTR Importer La majeure partie du 1,2,3-trichlorobenzène est adsorbée sur les particules en suspension. La phase non-adsorbée se volatilise en suivant la loi de Henry. La demi-vie du 1,2,3-trichlorobenzène dans l'eau, estimée à partir de modèles de rivières et de lacs, varie de 5 à 135 heures (Lyman et al., 1990).
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Milieu sédiment eau douce
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Milieu terrestre
FDTE/VTR Importer La mobilité du 1,2,3-trichlorobenzène est faible. La valeur du coefficient de partage (log Koc ) mesurée dans le sol et dans les sédiments est estimée entre 3,4 et 4,8. La volatilisation à partir de sols secs ne constitue pas une voie de dissémination importante vers l'atmosphère (Shiu et Mackay, 1997). La volatilisation à partir de sols humides est estimée à partir de la constante de Henry (0,98.10-3 atm.m3.mol-1 à 25 °C).
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Persistance
Biodégradabilité
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Dégradabilité abiotique
FDTE/VTR Importer Sous forme de vapeur, le 1,2,3-trichlorobenzène est dégradé par réaction photochimique due aux radicaux hydroxyles libres. Sa demi-vie est estimée à 57 jours. Que ce soit dans les eaux de surface, souterraines ou interstitielles, l'hydrolyse du 1,2,3-trichlorobenzène ne se produit pas en raison de l'absence de groupes fonctionnels hydrolysables.
Milieu eau douce
FDTE/VTR Importer La biodégradation du 1,2,3-trichlorobenzène dans les eaux est lente, et la demi-vie estimée varie de plusieurs semaines à plusieurs mois (Wang et Jones, 1994 ; Masunga et al., 1996 ; Peijnenburg et al., 1992).
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Milieu terrestre
FDTE/VTR Importer La biodégradation du 1,2,3-trichlorobenzène dans les sols est lente, et la demi-vie estimée varie de plusieurs semaines à plusieurs mois (Wang et Jones, 1994 ; Masunga et al., 1996 ; Peijnenburg et al., 1992). La biodégradation du 1,2,3-trichlorobenzène dans les sols a été démontrée par plusieurs auteurs (Marinucci et Bartha, 1979). Schwarzenbach et Westall (1981) ont mis en évidence que la biodégradation du 1,2,3-trichlorobenzène dans les sols suivait les voie aérobie et anaérobie. Les principaux produits de biodégradation sont les phénols chlorés et les catéchols. Les résultats publiés de biodégradation dans les boues de station d’épuration (STEP) sont contradictoires. Mais plusieurs auteurs s'accordent pour indiquer que ce type de biodégradation est favorisée lorsque les consortiums bactériens sont adaptés (Wang et Jones, 1994). Des sols amendés par des boues de STEP ont montré une amélioration de la biodégradation du 1,2,3-trichlorobenzène (Masunga et al.,1996). Dans le cas où la microflore n'est pas adaptée, un temps de latence de 2 à 6 mois a été rapporté (Bosma et al., 1988).
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Bioaccumulation
Organismes aquatiques
FDTE/VTR Importer La bioconcentration du 1,2,3-trichlorobenzène chez les poissons est élevée. Des facteurs de bioconcentration (BCF) ont été rapportés par divers auteurs et varient de 130 à 1200 chez la carpe (Masunga et al. 1996 ; Wang et Jones, 1994 ; Peijnenburg et al., 1992 ; CITI, 1992).
Une valeur moyenne de BCF de 430 a été rapportée chez la gambusie Gambusia affinis exposée au 1,2,3-trichlorobenzène (Chaisukant et Connel, 1997).
Chez la truite, le BCF varie en fonction du degré de développement. La bioaccumulation semble être 10 fois plus élevée chez les larves que chez les alevins (Galassi et Calamari, 1983).
Des données de bioaccumulation mesurées chez les organismes aquatiques sont disponibles dans la littérature, et sont présentées dans le tableau suivant.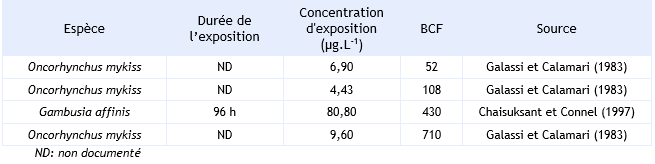
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Organismes terrestres
FDTE/VTR Importer Le 1,2,3-trichlorobenzène a été détecté, mais non quantifié, dans des aiguilles de pins en Slovénie (Jan et al., 1994). Des résidus de 1,2,3-trichlorobenzène ont été mesurés à des concentrations moyennes de 0,01 mg.kg-1 dans des œufs de héron prélevés dans la rivière Detroit (Struger et al. 1985). Aucun résultat d'essai valide permettant de déterminer des facteurs de bioconcentration du 1,2,3-trichlorobenzène dans les plantes n'a pu être trouvé dans la littérature.
Bibliographie
Toxicologie
Dernière vérification le 29/03/2024
Introduction
FDTE/VTR Importer L'ensemble des informations et des données toxicologiques provient de diverses monographies publiées par des organismes reconnus pour la qualité scientifique de leurs documents (OMS IPCS, 1991 ; CE, 2003 ; US EPA – IRIS, 1996). Les références bibliographiques aux auteurs sont citées pour permettre un accès direct à l’information scientifique mais n’ont pas fait l’objet d’un nouvel examen critique par les rédacteurs de la fiche. Une recherche bibliographique, réalisée dans les bases de données électroniques, n’a identifiée aucune nouvelle étude concernant les effets toxicologiques des trichlorobenzènes. La plupart des données concernant les trichlorobenzènes sont souvent réduites à celles concernant le 1,2,4-trichlorobenzène qui est l’isomère le plus largement utilisé. Très peu de données sont disponibles chez l’homme.
Toxicocinétique
Chez l'homme
Absorption
FDTE/VTR Importer Très peu d’informations sont disponibles. L’absorption du 1,2,4-trichlorobenzène par voie orale est rapide et importante ; les niveaux d’absorption par inhalation n’ont pas fait l’objet de mesures spécifiques (CE, 2003). Cependant, les études chroniques ou sub-chroniques réalisées laissent supposer une bonne absorption par cette voie, probablement similaire à celle de la voie orale.
Distribution
FDTE/VTR Importer Les trichlorobenzènes se distribuent majoritairement au niveau des graisses.
Élimination
FDTE/VTR Importer L’excrétion est principalement urinaire.
Chez l'animal
Absorption
FDTE/VTR Importer Les trichlorobenzènes sont lentement absorbés par voies cutanée et respiratoire.
Distribution
FDTE/VTR Importer Compte tenu de leur importante lipophilie, ils sont stockés principalement au niveau des graisses. Ils sont retrouvés dans de nombreux organes, dont le foie.
Métabolisme
FDTE/VTR Importer Le métabolisme du 1,2,4-trichlorobenzène varie d’une espèce à l’autre. Les métabolites des trichlorobenzènes sont excrétés dans les urines, l’air expiré et les fèces. Chez le rat, les métabolites urinaires sont des trichlorophénols, du 2,4,5-trichlorothiophénol, du 3,4,6-trichlorocatéchol et, dans une moindre mesure, des conjugués (sulfhydrile, méthylthiol, méthylsulfoxyde et méthylsulfone). Dans l’air, les trichlorobenzènes sont retrouvés tels quels.
Élimination
FDTE/VTR Importer L’élimination des trichlorobenzènes est rapide : 85 % du 1,3,5 et 92 % du 1,2,3 sont éliminés dans les 24 premières heures, après administration de 10 mg.kg-1, par voie orale.
Chez le lapin, l’isomère 1,2,3 est le plus rapidement métabolisé : 62 % du produit est éliminé dans les urines, pendant les cinq jours suivants l’administration par voie orale, sous forme de dérivés conjugués. Cette élimination est de 38 % pour l’isomère 1,2,4 et de 23 % pour l’isomère 1,3,5. Chez le rat, 66 % du 1,2,4-trichlorobenzène administré par voie orale (50 mg.kg-1) sont excrétés dans les urines, 17 % dans les selles et 2 % dans l’air expiré.
Autre
FDTE/VTR Importer Mécanisme d’action :
Les trichlorobenzènes sont des inducteurs des enzymes microsomiales hépatiques : ils induisent surtout les cytochromes P450 de type phénobarbital. Par cette action, ils sont capables de modifier le métabolisme d’autres xénobiotiques.
Synthèse
FDTE/VTR Importer Chez l’homme, l’absorption est rapide par voie orale et probablement similaire par inhalation.
Chez l’animal, l’absorption est lente par voie cutanée et respiratoire. Que cela soit chez l’homme ou chez l’animal, les trichlorobenzènes se distribuent majoritairement au niveau des graisses et leur excrétion est principalement urinaire, après métabolisation.
Toxicité aiguë
Chez l'homme
Synthèse
FDTE/VTR Importer Il n’existe pas de données publiées concernant l’homme. Seul le caractère irritant pour les yeux, la peau et les voies aériennes semble avéré (CE, 2003).
Chez l'animal
Inhalation
FDTE/VTR Importer Il n’y a pas de CL50 disponibles par inhalation pour la durée standard de 4 heures. Seule une étude rapporte une CL50 pour 7 heures d’exposition au 1,2,4-trichlorobenzène, supérieure à 1 800 ppm soit 13,6 mg.L-1 (Kociba et al., 1981).
Voie orale
FDTE/VTR Importer Différentes études ont cherché à établir des DL50 chez le rat et la souris, elles sont reprises dans le tableau ci-après. Le rat et la souris ont une sensibilité équivalente lors de l’exposition par la voie orale au 1,2,4-trichlorobenzène. Le 1,2,4-trichlorobenzène est plus actif seul qu’en mélange avec le 1,2,3-trichlorobenzène. L’administration par voie orale induit des effets supérieurs à ceux par voie cutanée ou intra-péritonéale. Lors de l’administration par voie cutanée la souris est l’espèce animale la plus sensible (Cf tableau ci-après).
Une excitation motrice et des convulsions apparaissent avant la mort des animaux. Une irritation de la peau, des muqueuses oculaires et respiratoires, ainsi qu’une atteinte neurologique centrale, sont observées lors des études réalisées (CE, 2003).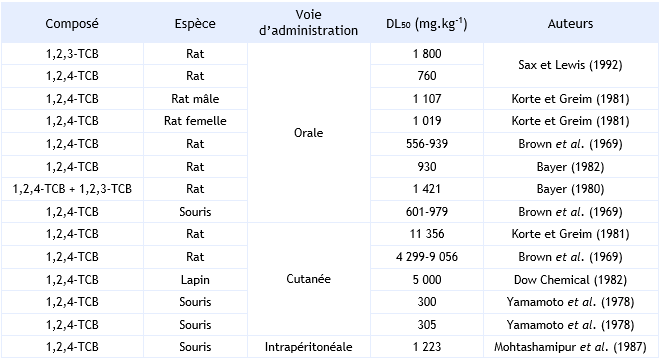
Synthèse
FDTE/VTR Importer Chez les animaux, la toxicité aiguë du 1,2,4-trichlorobenzène est faible, quelle que soit la voie d’exposition considérée. Elle se traduit par une irritation des muqueuses et de la peau et une atteinte du système nerveux central. Aucune information n’est disponible chez l’homme, mise à part la confirmation du potentiel irritant.
Toxicité à doses répétées
Effets généraux
Chez l'homme
Toutes voies
FDTE/VTR Importer Les données épidémiologiques sont très limitées (Lauwerys, 1999). Une étude, réalisée chez des travailleurs exposés à différents dérivés chlorés du benzène dont le 1,2,4-trichlorobenzène, ne met en évidence aucun effet au niveau du foie ou du sang (Erlicher, 1968). Seul un cas d’anémie aplasique est rapporté chez une femme de 68 ans, ayant été exposée aux trichlorobenzènes lors du nettoyage de vêtements de travail, mais des coexpositions sont plus que probables (Girard et al., 1969).
Chez l'animal
Inhalation
FDTE/VTR Importer Dans une étude réalisée chez le singe et le lapin (mâles uniquement), l'inhalation de différentes concentrations de 1,2,4-trichlorobenzène pouvant atteindre 100 ppm (754 mg.m-3) pendant 7 heures par jour, 5 jours par semaine pendant 26 semaines, n’induit pas d’effet systémique statistiquement significatif (Coate et al., 1977). Cependant, dans la même étude, des rats mâles ont été sacrifiés après 4 et 13 semaines d’exposition et des modifications histopathologiques de type hépatocytomégalie et des inclusions hyalines au niveau des reins sont observées. De cette étude, une LOAEC de 25 ppm (188 mg.m-3) est établie.
Une autre étude a été réalisée par inhalation de 1,2,4-trichlorobenzène aux concentrations de 0, 30 et 100 ppm chez le rat, le lapin et le chien (Kociba et al., 1981), 7 heures par jour, 5 jours par semaine, sur une période de 44 jours (ce qui correspond à 30 expositions). Elle montre une augmentation statistiquement significative du poids du foie chez le chien à 100 ppm, une diminution significative du poids du foie par rapport au poids corporel pour les deux concentrations étudiées chez le lapin. Une augmentation significative du poids du foie et des reins est observée pour la plus forte concentration chez le rat. Ceci est associé à une augmentation de l’excrétion urinaire des porphyrines pour les concentrations de 30 et 100 ppm. De cette étude, une LOAEC de 30 ppm (226 mg.m-3) de 1,2,4 trichlorobenzène est établie pour le rat.
Une augmentation de l’excrétion des porphyrines urinaires a aussi été mise en évidence chez le rat suite à une exposition à 10 ppm de 1,2,4-trichlorobenzène pendant 90 jours. Cet effet est réversible et n’est pas retrouvé pour une exposition à 3 ppm. Une NOAEC de 3 ppm (22,6 mg.m-3) est ainsi déterminée (Watanabe et al., 1977).
Une exposition chez le rat par inhalation d’un mélange de 1,2,4-trichlorobenzène contenant jusqu’à 20 % de 1,2,3-trichlorobenzène, à des concentrations de 0, 148, 519 ou 1484 mg.m-3, 6 heures par jour, 5 jours par semaine, pendant 3 ou 4 semaines, induit une léthargie et un diminution de la prise de poids pour les concentrations les plus élevées. Des larmoiements sont observés à 519 mg.m-3. Aucun effet n’est observé pour la concentration la plus basse (Gage, 1970).
Il semble que l’isomère 1,3,5-trichlorobenzène soit moins toxique que le 1,2,4-trichlorobenzène. Ceci serait lié à une plus faible absorption du 1,3,5-trichlorobenzène, très peu volatil. Les seuls effets notables observés lors de l’exposition à long terme de rats (6 heures par jour, 5 jours par semaines, pendant 13 semaines) à des concentrations de 1,3,5-trichlorobenzène pouvant atteindre 1 000 mg.m-3, sont une métaplasie épidermoïde et une hyperplasie de l’épithélium nasal pour la dose la plus élevée (NOEC de 100 mg.m-3) (Sasmore et al., 1983). Pour une exposition plus courte de 4 semaines, dans des conditions expérimentales identiques, une augmentation du ratio du poids du foie sur le poids corporel est observée pour la concentration la plus élevée de 1 000 mg.m-3.
Voie orale
FDTE/VTR Importer Différentes études réalisées chez le rat ou la souris ont mis en évidence l’effet du 1,2,4-trichlorobenzène sur le foie et les reins lors de l’administration par voie orale. Il s’agit d’altérations biochimiques, fonctionnelles et histopathologiques. A doses élevées, les trichlorobenzènes peuvent aussi être à l’origine d’une porphyrie hépatique. Quelques études se sont également intéressées à la thyroïde (altérations histopathologiques) ou aux glandes surrénales (augmentation pondérale). Des LOAEL et des NOAEL ont été établis. Il apparaît clairement une différence de sensibilité entre les deux sexes, le mâle étant plus sensible que la femelle. Les niveaux retrouvés dans ces différentes études sont du même ordre de grandeur et sont repris dans le tableau ci-dessous.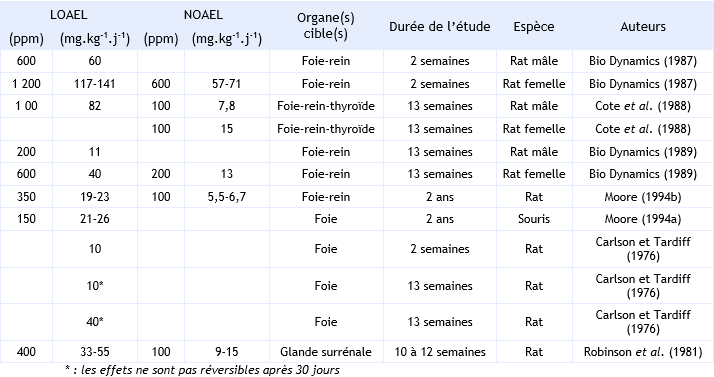
L’étude de l’évolution du poids des souris, exposées au 1,2,4-trichlorobenzène via l’alimentation pendant 13 semaines, a permis d’établir un NOAEL de 195 ppm soit 80 mg.kg-1 par jour pour les femelles et un LOAEL de 220 ppm (62 mg.kg-1.j-1) pour les mâles (Hiles, 1989).
Les rares études qui se sont intéressées aux autres isomères du trichlorobenzène montrent que le 1,2,3-trichlorobenzène est responsable d'une dégénérescence limitée des cellules hépatiques ou d’une nécrose focalisée dans les régions centrales, médianes ou périportales. Ces effets sont accompagnés d’une perte de poids et d’appétit (Rimington et Ziegler, 1963). Les doses maximales utilisées dans cette étude étaient de 785 mg.kg-1.j-1, pendant 7 jours, l’administration étant réalisée par gavage dans 1 % de cellofas.
Une étude réalisée par gavage chez les rats a permis de comparer les effets des 3 isomères séparément. Les doses testées sont les suivantes : 0 – 1 – 10 – 100 et 1 000 mg.kg-1 diluées dans de l’huile de maïs, ce qui correspond à 0 - 0,07/0,08 - 0,78/0,81 - 7,6/7,8 et 78/82 mg.kg-1.j-1 pour les mâles et à 0 - 0,11/0,13 - 1,3/1,5 – 12/17 et 101/146 mg.kg-1.j-1 pour les femelles. La durée de l'étude est de 13 semaines (Cote et al., 1988). Les effets observés sont une diminution statistiquement significative du gain de poids des mâles pour les concentrations de 10 ou 1 000 mg de 1,2,3-trichlorobenzène.kg-1 (l’absence d’effet lors de l’exposition à 100 mg demeure non expliquée) et une néphrose chez un mâle exposé à 1 000 mg de 1,2,4-trichlorobenzène.kg-1. De plus, une augmentation significative du ratio poids du foie sur poids corporel est retrouvée pour la plus forte concentration lors de l’exposition à chacun des 3 isomères. Des effets qualitatifs sont observés pour le foie, les reins et la thyroïde : ils ne sont statistiquement significatifs que chez les mâles et pour la plus forte concentration. Les effets hépatiques sont faibles à modérés et correspondent à une augmentation du volume cytoplasmique et à une anisocaryose des hépatocytes. Chacun des 3 isomères induit des infiltrations graisseuses dont les effets les plus importants sont observés pour une exposition à 1 000 mg de 1,2,4-trichlorobenzène.kg-1. Des altérations faibles à modérées sont observées au niveau de la thyroïde (rats mâles seulement) pour les lots exposés aux concentrations les plus élevées, ces altérations correspondent à une diminution de la taille des follicules, une augmentation de la taille de l’épithélium et une réduction de la densité de colloïde. Au niveau rénal, des altérations modérées des tubules sont retrouvées chez les mâles exposés à 1 000 mg de 1,3,5-trichlorobenzène.kg-1.
A partir de cette étude, un NOAEL de 7,7 mg.kg-1.j-1 est proposé pour le 1,2,3-trichlorobenzène, un NOAEL de 7,8 mg.kg-1.j-1 est proposé pour le 1,2,4-trichlorobenzène et un NOAEL de 7,6 mg.kg-1.j-1 est proposé pour le 1,3,5-trichlorobenzène.
Voie cutanée
FDTE/VTR Importer Lors de l’administration par voie cutanée de 450 mg de 1,2,4-trichlorobenzène.kg-1.j-1, des effets hépatiques et une excrétion de coproporphyrines sont observés (Rao et al., 1982). De cette étude, un LOAEL de 450 mg.kg-1.j-1 et un NOAEL de 150 mg.kg-1.j-1 sont établis pour le 1,2,4-trichlorobenzène, suite à une exposition de 4 semaines.
L’application cutanée chez le lapin entraîne une irritation avec acanthose et hyperkératose, sans chloracné (Powers et al., 1975).
Synthèse
FDTE/VTR Importer Seuls les effets chez les animaux ont été étudiés. Il s’agit principalement d’atteintes hépatiques, rénales (altérations biochimiques, fonctionnelles et histopathologiques) et de la thyroïde, retrouvées pour chacun des isomères, et, dans une moindre mesure, d’effets au niveau des glandes surrénales (1,2,4-trichlorobenzène) ou de l’épithélium nasal (1,3,5-trichlorobenzène).
Effets cancérigènes
Classifications
| Organisme | Classification | Année |
|---|---|---|
| UE | FDTE/VTR Importer non classé | 2001 |
| US EPA | FDTE/VTR Importer 1,2,4-trichlorobenzène : groupe D : substance non classifiable quant à sa cancérogénicité pour l'homme. |
1991 |
Chez l'homme
Synthèse
FDTE/VTR Importer Aucune donnée concernant l’homme n’est disponible.
Chez l'animal
Voie orale
FDTE/VTR Importer Par voie orale, deux études sont disponibles. Chez la souris B6C3F1, l’administration du 1,2,4-trichlorobenzène dans l’alimentation pendant deux ans provoque des effets cancérogènes. Il s’agit de tumeurs hépatocellulaires qui sont retrouvées pour les doses les plus élevées, 700 ppm et 3 200 ppm (Moore, 1994a). Un NOAEL pour les effets cancérogènes a été déterminé à des niveaux d’exposition de 150 ppm qui correspondent à 21-26 mg de 1,2,4-trichlorobenzène par kg de poids corporel par jour pour la souris B6C3F1. Toutefois, cette souche de souris est connue pour présenter une incidence élevée de carcinomes hépatocellulaires lors de son exposition à des substances ayant une action toxique au niveau du foie (CE, 2003).
Chez le rat Fisher, une étude menée dans des conditions analogues pour des doses de 5,5, 18,9, et 66,7 mg.kg-1 de 1,2,4 trichlorobenzène par jour montre une augmentation non statistiquement significative des tumeurs de la glande de Zymbal (Moore, 1994b).
Voie cutanée
FDTE/VTR Importer Par voie cutanée, une étude a été réalisée chez la souris par application d’une solution à 30 ou 60 % de 1,2,4-trichlorobenzène dans l’acétone. Les souris sont exposées deux fois par semaine pendant 2 ans à 0,03 mL de cette solution. Il n’y a pas d’augmentation de l’incidence d’un type particulier de tumeur et aucune différence significative entre les lots témoins et exposés n’est observée (Yamamoto et al., 1982). Toutefois, c’est à partir de cette étude que l’US EPA a établi sa classification.
Synthèse
FDTE/VTR Importer Seule une augmentation de l’incidence de carcinomes hépatocellulaires chez des souris, par voie orale, a été observée pour le 1,2,4-trichlorobenzène. Les trichlorobenzènes ont été évalués par l’Union européenne mais n’ont pas été classés par insuffisance de données ; ils sont dans le groupe D de l’US EPA.
Effets génotoxiques
Classifications
| Organisme | Classification | Année |
|---|---|---|
| UE | FDTE/VTR Importer non classé | 2001 |
In vitro
Organismes procaryotes
FDTE/VTR Importer Les quelques tests in vitro disponibles, réalisés sur S. typhimurium sont négatifs (Schoeny et al., 1979).
Synthèse
FDTE/VTR Importer Les trichlorobenzènes ne sont pas génotoxiques et n’ont pas été classés au niveau européen.
Effets sur la reproduction
Classifications
| Organisme | Classification | Année |
|---|---|---|
| UE | FDTE/VTR Importer non classés | 2001 |
Chez l'homme
Synthèse
FDTE/VTR Importer Des données concernant l’homme ne sont pas disponibles.
Chez l'animal
Voie orale
FDTE/VTR Importer Plusieurs études ont cherché à identifier un effet du 1,2,4-trichlorobenzène sur la reproduction. Seule une diminution du poids des organes de reproduction a été observée, aussi bien chez les mâles que chez les femelles, pour des gammes de doses comprises entre 1 ppm et 1 800 ppm chez le rat (Cote et al., 1988 ; Bio-dynamics, 1989 ; Moore, 1994b) et entre 150 et 7 700 ppm chez la souris (Hiles, 1989 ; Moore, 1994a). Cependant, dans l’étude de Moore (1994a), une dégénérescence unilatérale ou bilatérale des testicules, ainsi qu’une diminution des sécrétions des vésicules séminales, sont rapportées pour des expositions à 700 et 3 200 ppm de 1,2,4-trichlorobenzène, incorporé dans la nourriture pendant 104 semaines.
L’étude de la fertilité et de la toxicité sur le développement sur 2 générations a été effectuée chez le rat exposé à des doses de 25, 100 ou 400 ppm de 1,2,4-trichlorobenzène dans l’eau de boisson, ce qui équivaut à des doses de 1,2,4-trichlorobenzène de 2,5, 8,9 et 33 mg.kg-1 pc.j-1 pour les mâles et 3,7, 14,8 et 53,6 mg.kg-1 pc.j-1 pour les femelles (Robinson et al., 1981). Aucun effet n’est observé sur la fertilité, la viabilité, la croissance, l’activité locomotrice et les analyses chimiques sanguines. Pour la dose la plus élevée, une augmentation statistiquement significative du poids des glandes surrénales est rapportée. De cette étude, un NOAEL de 400 ppm (correspondant à 33 et 53 mg.kg-1 pc.j-1 respectivement pour les mâles et pour les femelles) est défini pour la toxicité sur le développement et la fertilité.
Effets sur le développement
Généralités
FDTE/VTR Importer Résumé:
Concernant les effets reprotoxiques, une dégénérescence des testicules et une augmentation du poids des glandes surrénales sont observées chez les animaux exposés au 1,2,4-trichlorobenzène. Des lésions du cristallin, un retard dans le développement embryonnaire ainsi que des malformations sont aussi rapportées pour le 1,2,4 et le 1,3,5 trichlorobenzène. Aucune donnée n’est disponible chez l’homme.
Chez l'homme
Toutes voies
FDTE/VTR Importer Des données concernant l’homme ne sont pas disponibles.
Chez l'animal
Voie orale
FDTE/VTR Importer Des lots de 13 à 14 rates en gestation ont été exposés à 0, 75, 150 et 300 mg.kg-1 de 1,2,4-trichlorobenzène en solution dans de l’huile de maïs, administré par gavage, du sixième au quinzième jour de gestation (Black et al., 1988). Une diminution non significative du poids corporel est observée pour la dose la plus élevée. Un examen post-mortem des mères montre de légères atteintes hépatiques correspondant à une augmentation de l’éosinophilie cytoplasmique péri-portale et une légère anisocaryose des noyaux des hépatocytes lors de l’exposition à 150 mg.kg-1.j-1. Une diminution significative des taux de l’hémoglobine et de l’hématocrite ainsi qu’une augmentation de la quantité de protéines et de l’activité de l’aminopyrine-N-déméthylase hépatique sont identifiées pour les doses de 150 mg.kg-1.j-1 et au delà. De plus, une augmentation du poids du foie est retrouvée pour le lot exposé à 300 mg.kg-1.j-1. Chez les fœtus, des lésions histologiques sont observées au niveau du cristallin pour des niveaux d’exposition intermédiaires. Ces effets sont considérés par les auteurs comme un indicateur possible des premières étapes de développement vers une cataracte. De cette étude, un NOAEL de 75 mg.kg-1.j-1 est déterminé pour les mères et les fœtus.
Dans une autre étude, des lots d’au moins six rates en gestation ont été exposés à des doses de 0, 36, 120, 360 ou 1 200 mg de 1,2,4-trichlorobenzène.kg-1.j-1. L’administration est réalisée par gavage du neuvième au treizième jour de gestation (Kitchin et Ebron, 1983). Les animaux sont sacrifiés au quatorzième jour de gestation ; les effets au niveau du foie et de la reproduction sont évalués chez les mères. Les premiers signes d’une hépatotoxicité sont observés dès 120 mg.kg-1.j-1. A 360 mg.kg-1.j-1, l’augmentation du poids corporel des mères est retardée et une légère augmentation de la mortalité est observée. Pour une exposition de 1 200 mg.kg-1.j-1, toutes les femelles meurent avant la fin de l’étude. A la dose de 360 mg de 1,2,4-trichlorobenzène.kg-1.j-1, un retard du développement embryonnaire est observé alors que le nombre de fœtus vivants et l’incidence des malformations ne sont pas modifiés. Cette fœtotoxicité apparaît pour des doses où une toxicité maternelle est aussi observée. De cette étude, un NOAEL de 36 mg.kg-1.j-1 est proposé pour les mères.
Plus récemment, Yokoyama et Akita (2000) ont confirmé l’impact du 1,2,4-trichlorobenzène sur le développement embryonnaire mais ont aussi mis en évidence l’apparition de malformations (œdème, fente labiale, perturbation dans le développement du cerveau ou des mains) consécutives à l’exposition d’embryons de rats à 10 µg.dL-1 de trichlorobenzène pendant 48 heures.
Deux études ont cherché à identifier les effets sur le développement des 3 isomères du trichlorobenzène pris séparément (Ruddick et al., 1983 ; Black et al., 1988). L’exposition a été réalisée par gavage dans de l’huile de maïs, du sixième au quinzième jour de la gestation. Les doses utilisées sont 0, 75, 150, ou 300 mg.kg-1.j-1 pour le 1,2,4-trichlorobenzène, 0, 150, 300 ou 600 mg.kg-1.j-1 pour le 1,2,3-trichlorobenzène et le 1,3,5-trichlorobenzène. Chez les mères, les différents effets suivants sont observés : diminution du poids corporel pour 600 mg/kg de 1,3,5-trichlorobenzène, augmentation du poids du foie pour 600 mg.kg-1.j-1 de 1,2,3- et de 1,3,5-trichlorobenzène, et pour 300 mg.kg-1.j-1 de 1,2,4-trichlorobenzène, et enfin une diminution des niveaux d’hémoglobine et d’hématocrite pour les doses les plus élevées de chacun des 3 isomères. De plus, une diminution du nombre de globules rouges est observée à la dose de 300 mg.kg-1 lors de l’exposition au 1,2,3- trichlorobenzène, aux doses de 150 et 300 mg.kg-1.j-1 lors de l’exposition au 1,2,4-trichlorobenzène et aux doses de 150 et 600 mg.kg-1.j-1 lors de l’exposition au 1,3,5-trichlorobenzène
Pour chacun des 3 isomères, les doses intermédiaires induisent des modifications histopathologiques de la rate, du foie, de la thyroïde. Des altérations du cristallin des nouveau-nés sont retrouvées pour toutes les doses lors de l’exposition au 1,3,5-trichlorobenzène et à 75 mg.kg-1.j-1 lors de l’exposition au 1,2,4-trichlorobenzène.
De ces études, seul un LOAEL de 600 mg.kg-1.j-1 pour les mères est proposé pour le 1,3,5-trichlorobenzène.
Valeurs accidentelles
Autres seuils accidentels
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Valeurs réglementaires
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Valeurs de référence
Valeurs de l'ANSES et/ou de l'INERIS
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Autres valeurs des organismes reconnus
Description
FDTE/VTR Importer Effets à seuil - Exposition chronique par inhalation :
Le RIVM propose, pour chaque isomère du trichlorobenzène, une TCA provisoire (pTCA) de 5.10-2 mg.m-3 pour une exposition chronique par inhalation (Baars et al., 2001).
Cette valeur était celle recommandée par l’OMS IPCS pour le 1,2,4- trichlorobenzène (1991) mais qui n’est plus en vigueur aujourd’hui. Elle est basée sur une étude de toxicité subchronique chez le rat, exposé par inhalation au 1,2,4-trichlorobenzène durant 3 mois et pour laquelle un NOAEL de 22,3 mg.m-3 a été établi pour des effets urinaires (Watanabe et al., 1977). L’OMS IPCS (1991) a également défini une valeur de 0,2 mg.m-3 pour le 1,3,5-trichlorobenzène, à partir de l'étude de Sasmore et al. (1983), qui a défini une NOAEC de 100 mg.m-3 pour les effets sur les voies nasales chez le rat. Dans les deux cas, un facteur d'incertitude de 500 a été appliqué. Aucune donnée n'existe pour le 1,2,3-trichlorobenzène.
Le RIVM a choisi d'appliquer la valeur la plus basse de l'OMS IPCS (celle de l'isomère 1,2,4) à tous les isomères du trichlorobenzène.
Selon le RIVM, la fiabilité de cette valeur est faible.
Effets à seuil - Exposition chronique par voie orale :
Le RIVM propose, pour chaque isomère du trichlorobenzène, une TDI de 8.10-3 mg.kg-1.j-1 pour une exposition chronique par voie orale (Baars et al., 2001).
Cette valeur a été calculée à partir d'une étude expérimentale chez le rat, exposé durant 13 semaines aux trois isomères du trichlorobenzène de manière séparée, via l'alimentation (Cote et al., 1988). Les effets critiques observés étaient une augmentation du poids relatif du foie et des changements histopathologiques légers à modérés au niveau du foie, de la thyroïde et des reins. Des NOAELs de 7,8, 7,7 et 7,6 mg.kg-1.j-1 ont été établis pour respectivement les isomères 1,2,4-, 1,2,3- et 1,3,5- du trichlorobenzène et la valeur moyenne a été prise comme NOAEL de départ.
Facteurs d'incertitude : un facteur 10 a été appliqué pour l'extrapolation de l'animal à l'homme, un facteur 10 pour la variabilité au sein de la population humaine et un facteur 10 pour le manque de données chroniques.
Calcul : 7,7 mg.kg-1.j-1 x 1/1 000 = 8.10-3 mg.kg-1.j-1
Selon le RIVM, la fiabilité de cette valeur est moyenne.
L’US EPA (IRIS) propose une RfD de 10-2 mg.kg-1.j-1 pour le 1,2,4-trichlorobenzène (1992).
Cette valeur a été établie à partir d’une étude expérimentale de reproduction sur plusieurs générations chez le rat (Robinson et al., 1981). Des mâles et des femelles ont été exposés à des doses de 25, 100 ou 400 ppm de 1,2,4-trichlorobenzène dans l’eau de boisson. L’étude de la fertilité chez les rats de la génération F0 et F1 ne montre pas d’effet. Un LOAEL de 400 ppm (53,6 mg.kg-1.j-1) a été établi suite à l’augmentation significative du poids de la glande surrénale chez les mâles et les femelles des générations F0 et F1. La valeur expérimentale de 100 ppm (14,8 mg.kg-1.j-1) est considérée comme un NOAEL.
Facteurs d’incertitude : un facteur de 10 est appliqué pour tenir compte de l’extrapolation de l’animal à l’homme, un facteur de 10 est utilisé pour tenir compte des différences de sensibilité des sous populations humaines et enfin un autre facteur de 10 pour combler le manque de données lors d’études chroniques.
Calcul : 14,8 mg.kg-1.j-1 x 1/1 000 = 10-2 mg.kg-1.j-1********Selon l’US EPA, la confiance accordée à cette valeur est moyenne.
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Bibliographie
Ecotoxicologie
Dernière vérification le 29/03/2024
Introduction
FDTE/VTR Importer L'objectif de cette rubrique est d'estimer les effets à long terme sur la faune et la flore, les résultats nécessaires à cette évaluation sont présentés. Lorsqu'un nombre suffisant de résultats d'écotoxicité chronique est disponible, les résultats d'écotoxicité aiguë ne sont pas fournis. Lorsque l'écotoxicité chronique n’est pas suffisamment connue, les résultats d'écotoxicité aiguë sont présentés et peuvent servir de base pour l'extrapolation des effets à long terme. L'ensemble des informations et des données de ce chapitre provient de diverses revues bibliographiques publiées par des organismes reconnus pour la qualité scientifique de leurs documents. Les références bibliographiques aux auteurs sont citées pour permettre un accès direct à l’information scientifique mais n’ont pas fait systématiquement l’objet d’un nouvel examen critique par les rédacteurs de la fiche. Les références bibliographiques ayant été évaluées sont indicées d’une valeur en fonction de leur recevabilité selon les critères définis ci-dessous : - Recevabilité 1 : le résultat peut être utilisé pour le calcul de la PNEC vis-à-vis des organismes aquatiques sans restriction, - Recevabilité 2 : le résultat peut être utilisé pour le calcul de la PNEC vis-à-vis des organismes aquatiques mais dans une seconde étape. Généralement ces résultats proviennent de protocoles comportant des dérives par rapport aux normes des essais (durée d’exposition, composition des milieux, températures d’exposition …), - Recevabilité 3 : Le résultat ne peut pas être utilisé pour le calcul de la PNEC. Il peut être utilisé pour conforter des résultats. Ces résultats proviennent d’essais pour lesquels l’organisme testé n’est pas un organisme dulçaquicole, ou que le protocole n’est pas disponible, ou que le protocole comporte des modifications majeures par rapports aux normes en vigueurs (durée d’exposition trop courtes …), - Non classés : Le résultat est provient d’une citation dans un article.
Dangers
Valeurs de danger
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Synthèse
Eau douce
FDTE/VTR Importer Paramètres d’écotoxicité aiguë :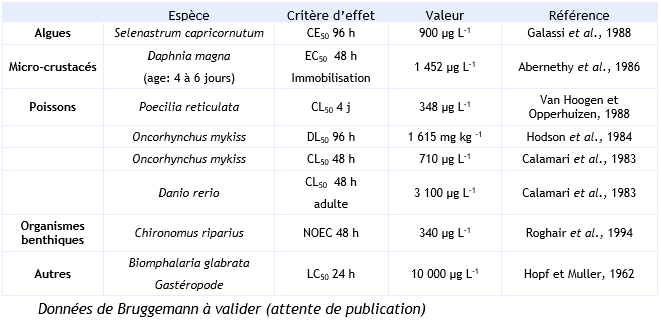
Paramètres d’écotoxicité chronique :
Aucune donnée fiable de toxicité chronique n'est disponible pour les algues.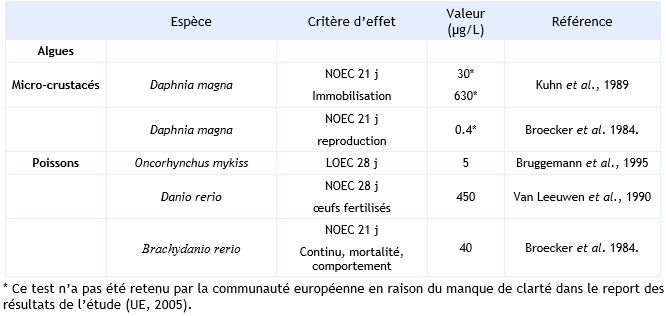
Sol
FDTE/VTR Importer Aucune donnée fiable n'a été trouvée dans la littérature pour les organismes terrestres.
Valeurs écotoxicologiques
Valeurs guides
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Synthèse
FDTE/VTR Importer On dispose de trois résultats d'essais à long terme sur trois niveaux trophiques différents (algues, daphnies et poissons). Le calcul de la PNECeau se fait donc en considérant la donnée la plus faible affectée d'un facteur de sécurité de 10. La donnée la plus faible a été obtenue sur Brachydanio rerio (NOEC : 40 µg.L-1 ).
D’où :
PNECeau = 4 µg L-1
Cette valeur a été retenue dans le cadre de la mise en œuvre de la Directive cadre sur l’eau comme norme de qualité pour la protection des organismes aquatique (UE, 2005).
Bibliographie
Données technico-économiques
Dernière vérification le 29/03/2024
Tableaux de synthèse
Généralités
| CAS | 120-82-1 |
|---|---|
| SANDRE | 1283 |
| Substance prioritaire dans le domaine de l’eau (DCE) | non |
| Substance soumise à autorisation dans Reach | non |
| Substance soumise à restriction dans Reach | oui |
| Substance extrêmement préoccupante (SVHC) | non |
| Réglementations |
FTE 2005 Importer Le trichlorobenzène est couvert par plusieurs textes réglementaires :
|
| Classification CLP | Voir la classification CLP |
Production et utilisation
Production et ventes
Données économiques
FTE 2005 Importer
Actuellement le TCB commercial est du 1,2,4 TCB pur à 99,8 %. Précédemment le TCB commercial était un mélange de deux isomères : entre 80 et 100 % de 1,2,4 TCB et entre 0 et 20 % de 1,2,3 TCB. Le 1,3,5 TCB n'est que très faiblement utilisé (environ 200 tonnes par an en Europe), en tant qu'intermédiaire. [Eurochlor, 2002]
Les TCB sont obtenus par chloration directe du benzène, en même temps que des dichlorobenzènes. Ils peuvent également être obtenus lors de la production de lindane. En effet le lindane est le isomère de l'hexachlorocyclohexane (HCH). Or le HCH brut contient seulement 20 % de cet isomère. Les 80 % restants (isomères , , etc.) sont pyrolysés avec formation de TCB et d'acide chlorhydrique, qui sont récupérés. [Eurochlor, 2002]
D'après Corden (2000), on répertoriait deux producteurs de 1,2,4 TCB dans l'Union européenne qui en produisaient 7 000 tonnes par an en 1994 1995 : Bayer (en Allemagne) et Rhodia (en Belgique). D'après ces deux producteurs, entre 70 % et 90 % de la production était exportée (80 % en moyenne). [Hansen et al., 2003] Un troisième producteur a commencé à en fabriquer en 1997 1998, avec une production d'environ 3 000 tonnes par an (ce qui a réduit légèrement la production des deux autres). 80 % de la production sont exportés hors de l'Union européenne. [Corden, 2000]
Coûts d'une interdiction du TCB
Sur la base d'expériences danoises, l'Agence danoise de protection de l'environnement (2002), estime que le coût moyen de reformulation d'une recette est inférieur à 15 000 €. Cela comprend le développement d'une nouvelle formule, une phase de test et la certification du nouveau produit. L'Agence estime qu'au total un maximum de 50 recettes devraient être reformulées et re certifiées en cas d'interdiction du 1,2,4 TCB. Les coûts maxima de reformulation peuvent être estimés à 750 000 €. À ces coûts, il est possible que s'ajoutent notamment des coûts liés au fait que les produits remplaçant le TCB sont susceptibles d'être plus chers (actuellement le TCB est relativement peu cher).
Utilisations
utilisations
FTE 2005 Importer
Utilisateurs intentionnels
D'après Eurochlor (2002), le 1,2,3 trichlorobenzène et le 1,2,4 trichlorobenzène sont utilisés en tant qu'intermédiaire dans divers produits de chimie fine, particulièrement pour certains herbicides, pigments et teintures. Ils sont également utilisés comme agents de teinture et comme solvants de procédés. L'Europe a cessé d'utiliser les TCB comme solvants dans les fluides diélectriques (application qui fut importante). Le 1,2,3 TCB est en outre utilisé comme intermédiaire dans la production de pesticides (production de 2,3,4 trichloronitrobenzène).
À cause des importantes exportations, seules 1 400 tonnes par an de 1,2,4 TCB étaient utilisées dans l'Union européenne en 1994 1995. Les principales utilisations étaient les suivantes :
- comme intermédiaire chimique, particulièrement pour certains herbicides, des benzènes plus chlorés, pigments et teintures (1 100 tonnes par an, soit 79 % de l'utilisation totale) ;
- comme solvant de procédé (200 tonnes par an, 14 % du total) ; d'après le principal utilisateur, cet usage du 1,2,4 TCB a été arrêté en 1997 dans son usine ;
- comme solvant, lubrifiant et additif (100 tonnes, 7 % du total) ;
- comme agent de teinture dans l'industrie du textile (1,4 tonnes, 0,1 %) ; le CSTEE1 (2001), s'appuyant sur des données des industriels, affirme que cette substance n'est plus utilisée dans l'industrie du textile dans l'Union européenne ;
- en outre, du 1,2,4 TCB est encore présent dans les équipements électriques existants, comme fluide diélectrique, solvant, moyen de transfert de chaleur ; une évaluation pessimiste estimait que la quantité de TCB liée à ces applications dans l'Union européenne s'élevait à 5 000 tonnes. [Danish Environmental Protection Agency, 2002]
Tableau 1. Production et utilisation du TCB en Europe occidentale entre 1983 et 1995 (en tonnes) (Source : Srour, 1989 et 1996 ; in Hansen et al., 2003)

[1] Scientific Committee for Toxicity, Ecotoxicity, and the Environment.
L'Agence danoise de protection de l'environnement (2002) liste également les utilisations suivantes, sans doute d'importance mineure, et pour lesquels les quantités employées ne sont pas connues :
- fluide de travail des métaux ;
- peinture anticorrosion et produits de maintenance ;
- inhibiteur de corrosion dans des sprays ;
- additif pour la production d'isolant à haute performance pour des câbles ;
- produit de mélange pour certaines substances utilisées pour les bains de plomb/étain.
Il semble être utilisé en outre dans certains produits pharmaceutiques. Depuis cette époque, les deux producteurs européens de cette période disent avoir arrêté de vendre du 1,2,4 TCB pour les usages à l'air libre. L'utilisation comme agent de teinture a également été volontairement éliminée. [Corden, 2000]
Production non intentionnelle
Le TCB est également formé lors de la combustion de substances organiques en présence de chlore (incinération de déchets, PVC et autres substances organiques) et lors de la production du lindane [Eurochlor, 2002].
Rejets dans l’environnement
Rejets dans l'environnement
FTE 2005 Importer
Le TCB peut être émis dans l'environnement lors de la production, la préparation et l'utilisation de la substance. Un sondage effectué en 1997 auprès de 78 sites européens produisant ou utilisant du TCB estimait les émissions dans l'eau à 553 kg.an-1 et celles dans l'air à 351 kg.an-1. Les émissions dans l'eau ont été réduites de 97 % entre 1985 et 1997 [Eurochlor, 2002].
L'Agence danoise de protection de l'environnement (2002) estime les émissions totales de TCB en Europe à environ 16 tonnes par an.
D'après l'Agence danoise de protection de l'environnement (2002), il semblerait que les principales sources de 1,2,4 TCB en Europe soient :
- la production et l'utilisation du 1,2,4 TCB ;
- les fluides diélectriques ;
- la biodégradation et la photo dégradation du HCB, du lindane et de ses isomères ;
- les émissions des décharges et des sites contaminés.
En comparaison de ces sources, les émissions dues aux procédés de combustion ou à certaines usines de production de papier sont sans doute d'importance mineure. Dans la mesure où certaines réglementations actuelles demandent la destruction du PCB et d'autres composés chlorés dans les fluides diélectriques des équipements électriques, ces émissions sont en train de diminuer. [Danish Environmental Protection Agency, 2002]
La base de données EPER2 répertorie deux installations comme émettrices de TCB dans l'Union européenne en 2001, mais aucune en France. Ces deux usines, situées en Allemagne, produisent des produits de chimie inorganique et des engrais. Elles ont émis chacune entre 30 et 40 kg de TCB dans l'air en 2001.
D'après la DRIRE Rhône Alpes, les rejets de TCB de 168 établissements industriels de la région, parmi les plus émetteurs, se sont élevés à 8 137 g.j-1 en 1993 et à 4 804 g.j-1 en 1998. Ceux de 1,2,4 TCB se sont élevés à 17 897 g.j-1 en 1993 et à 3 254 g.j-1 en 1998. En 1998, pour le TCB comme pour le 1,2,4 TCB, ces rejets proviennent à plus de 99 % des 47 établissements du secteur de la chimie/pétrochimie (notamment de l'usine Atofina de Jarrie qui doit faire une auto surveillance journalière pour les TCB, la plate forme Rhodia de Pont de Claix et l'usine Rhodia organique à Saint Fons). Une part marginale provient de cinq établissements de traitement de déchets/régénération de solvants, de quatre stations d'épuration, de huit établissements de peinture et de trois tanneries. En 1993, 26 établissements de textile émettaient des quantités importantes de TCB (15 % des rejets totaux de 1,2,4 TCB et 42 % de ceux des TCB) mais ils n'en émettaient plus en 1998. [DRIRE Rhône Alpes, 2001]
En Midi Pyrénées, la pelleterie (tannerie) Rial à Briatexte (81) émettait 305 g.j-1 de 1,2,4 TCB en 1997 (PEC/PNEC > 1) [DRIRE Midi Pyrénées, 1998].
Présence environnementale
Synthèse
FTE 2005 Importer
Dans le Rhin, le TCB est considéré comme substance prioritaire depuis 1987. Chaque année, entre 1990 et 2000, les concentrations en 1,2,3 TCB, 1,2,4 TCB et 1,3,5 TCB dans le Rhin ont été sensiblement inférieures aux objectifs de référence (la valeur de percentile de 90 %, ou le double de la valeur du percentile de 50 %, est inférieure à la moitié de l'objectif de référence), sauf en 1993 et 1994 pour le 1,2,4 TCB, pour lequel les concentrations étaient alors proches des objectifs de référence. [Braun et al., 2003]
Les concentrations de fond dans les grandes rivières de France et d'autres pays européens (Allemagne, Pays Bas et Royaume Uni) sont généralement inférieures à 0,4 Bg.l-1. [Eurochlor, 2002]
En 1995, deux études ont mesuré la concentration en TCB dans la Seine : l'Agence de bassin a trouvé une concentration inférieure à 0,4 Bg.l-1 à Honfleur (1996) ; la base de données
[2] http://www.eper.cec.eu.int.
COMMPS fait part d'une concentration inférieure à 0,02 Bg.l-1 dans l'estuaire (1998) [Eurochlor, 2002].
Lors d'une campagne de mesure dans les eaux du Rhône (1993 1997), on a observé un résultat positif sur 153 échantillons. Le seuil de détection était de 1 ou de 10 Bg.l-1. Pour les matières en suspension et les sédiments, il y avait six résultats positifs sur 153. Le seuil de détection variait entre 10 et 100 Bg/kg. La concentration moyenne était de 5,1 Bg/kg dans les sédiments et de 34,3 Bg/kg dans les matières en suspension. [Banque nationale de l'eau, 1998 ; in Hansen et al., 2003]
Lors d'une campagne de mesure dans le Rhin et la Meuse en 1997, les concentrations en 1,2,4 TCB étaient inférieures au seuil de détection (0,02 Bg.l-1) pour les 88 mesures. Une autre campagne de mesure dans le Rhin et la Meuse (1992 1996) a permis d'estimer que la concentration moyenne de 1,2,4 TCB était de 3,4 Bg/kg dans les sédiments et de 8,2 Bg/kg (poids sec) dans la matière en suspension. [Agence de l'eau Rhin Meuse, 1998 ; in Hansen et al., 2003].
Perspectives de réduction
Réduction des rejets
Interdiction
FTE 2005 Importer
D'après Bayer et Rhodia, il n'existe pas de substitut au 1,2,4 TCB pour la production de pesticide. Actuellement, la production de pesticide avec du 1,2,4 TCB a lieu aux États Unis. [Danish Environmental Protection Agency, 2002]
L'Agence danoise de protection de l'environnement (2002), recommande une interdiction de tous les usages ouverts et des importations de produits contenant du 1,2,4 TCB. Elle estime en effet que l'effet des émissions de TCB dues aux usages ouverts est assez élevé et que l'impact économique sur l'industrie est probablement modéré.
Alternatives aux usages
Produits de substitution
FTE 2005 Importer
D'après les principaux producteurs, de nombreux substituts au TCB comme agent de teinture existent : biphényl (CAS no 92 52 4), n butyl phthalamide (CAS n° 1515 72 6), esters d'acide o crésotinique (par exemple le méthylester d'acide 2 hydroxy 3 méthyl benzoïque, CAS n° 23287 26 5), alkylbenzènes en C3 et C4, diméthylphthalate, 2 méthyl naphtalène, etc. Parmi ces produits, certains ont des impacts sur l'environnement et la santé qui les rendent sans doute inappropriés pour se substituer au TCB : biphényl, certains alkylbenzènes en C3 et C4 ; d'autres sont encore trop peu connus pour que l'on puisse déterminer s'ils peuvent convenablement remplacer le TCB : n butyl phthalamide, 2 méthylnaphtalène, esters d'acide o crésotinique. [Danish Environmental Protection Agency, 2002]
Le principal producteur de TCB recommande de remplacer le 1,2,4 TCB comme solvant de procédé par du nitrobenzène [Danish Environmental Protection Agency, 2002].
Il est sans doute difficile de trouver des substituts pour le trichlorobenzène utilisé dans l'industrie pharmaceutique. [Corden, 2000]
Conclusion
FTE 2005 Importer
Les trichlorobenzènes ne sont plus produits en France. Il reste encore deux, peut être trois, producteurs importants de ces produits en Europe. Ils exportent hors d'Europe environ 80 % de leur production.
Les trichlorobenzènes sont encore utilisés, principalement comme intermédiaire chimique (particulièrement pour certains herbicides, des benzènes plus chlorés, pigments et teintures), comme solvant de procédé, comme lubrifiant et comme additif. La production et la consommation de ces substances ont respectivement baissé de 64 % et de 81 % entre 1983 et 1995 en Europe occidentale.
Les rejets de ces substances ont également beaucoup diminué depuis le début des années 1980, notamment grâce à l'arrêt de leur utilisation comme fluide diélectrique.
De nombreux substituts aux TCB semblent exister. Ils ne sont toutefois pas forcément toujours préférables aux TCB d'un point de vue environnemental. En outre, pour certains usages des TCB (fabrication de pesticides, industrie pharmaceutique), il ne semble pas exister encore de substituts viables.
Les diverses sources de TCB sont variées et, prises individuellement, émettrices de quantités relativement faibles de TCB. Il est sans doute possible d'atteindre des rejets négligeables d'ici 2015. L'obtention d'émissions nulles d'ici à 2015 est toutefois rendue délicate à cause de la difficulté d'identifier clairement les responsables des rejets de TCB. D'après l'Agence de protection de l'environnement, une mesure radicale comme l'interdiction d'utiliser des produits contenant des TCB pourrait permettre d'atteindre cet objectif à un coût raisonnable.
Archives
Dernière vérification le 29/03/2024
Documents
Exporter la substance
Choisissez le format de l'export :










