Configuration de votre affichage
Vous avez activé le mode de configuration de l'affichage qui permet de sélectionner les informations que vous souhaitez afficher sur la fiche substance. Une fois que vous aurez sélectionné les rubriques à afficher, vous pouvez revenir au mode de consultation de la fiche substance en cliquant à nouveau sur le bouton de filtrage.
Chlorure de zinc (7646-85-7)
Introduction
Dernière vérification le 29/03/2024
Dans la période transitoire de mise en cohérence des données du portail, les informations présentées pour cette substance peuvent ne pas être totalement à jour. Nous vous invitons à consulter la substance mère de cette famille : Zinc
Informations générales
Dernière vérification le 18/12/2025
Identification
Numero CAS
7646-85-7
Nom scientifique (FR)
Chlorure de Zinc
Nom scientifique (EN)
Autres dénominations scientifiques (FR)
Autres dénominations scientifiques (Autre langues)
Code EC
231-592-0
Code SANDRE
-
Numéro CIPAC
-
Formule chimique brute
\(\ce{ Cl2Zn }\)
Code InChlKey
Code SMILES
Cl[Zn]Cl
Familles
Familles chimiques
Classification CLP
Type de classification
Harmonisée
ATP insertion
CLP00
Description de la classification
Classification harmonisée selon réglement 1272/2008 ou CLP
| Mention du danger - Code | H314 |
|---|---|
| Mention du danger - Texte | Provoque de graves brûlures de la peau et de graves lésions des yeux. |
| Classe(s) de dangers | Corrosion / Irritation cutanée |
| Libellé UE du danger | - |
| Limites de concentration spécifique |
STOT SE 3;H335: C ≥ 5 % |
| Facteur M | - |
| Estimation de toxicité aigüe | - |
| Mention du danger - Code | H302 |
|---|---|
| Mention du danger - Texte | Nocif en cas d'ingestion |
| Classe(s) de dangers | Toxicité aiguë |
| Libellé UE du danger | - |
| Limites de concentration spécifique |
STOT SE 3;H335: C ≥ 5 % |
| Facteur M | - |
| Estimation de toxicité aigüe | - |
| Mention du danger - Code | H400 |
|---|---|
| Mention du danger - Texte | Très toxique pour les organismes aquatiques |
| Classe(s) de dangers | Danger pour le milieu aquatique |
| Libellé UE du danger | - |
| Mention du danger - Code | H410 |
|---|---|
| Mention du danger - Texte | Très toxique pour les organismes aquatiques, entraîne des effets à long terme |
| Classe(s) de dangers | Danger pour le milieu aquatique |
| Libellé UE du danger | - |
| Limites de concentration spécifique |
STOT SE 3;H335: C ≥ 5 % |
| Facteur M | - |
| Estimation de toxicité aigüe | - |
Physico-Chimie
Dernière vérification le 29/03/2024
Généralités
Poids moléculaire
136.28 g/mol
Tableau des paramètres
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Bibliographie
Toxicologie
Dernière vérification le 29/03/2024
Valeurs accidentelles
Autres seuils accidentels
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Valeurs réglementaires
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Bibliographie
Données technico-économiques
Dernière vérification le 29/03/2024
Introduction
FTE 2015 Importer
Le zinc est un métal, son numéro CAS est 7440-66-6. Les principaux composés du zinc, étudiés dans cette fiche, sont le chlorure de zinc (CAS 7646-85-7), le sulfate de zinc (CAS 7733-02-0), le sulfure de zinc (1314-98-3), l'oxyde de zinc (CAS 1314-13-2), le phosphure de zinc (CAS 1314-84-7), le chromate de zinc (CAS 13530-65-9) et le stéarate de zinc (557-05-1).
Le zinc est un métal ubiquitaire, très répandu dans la croûte terrestre. Les sources de zinc sont à la fois naturelles et anthropiques. La majorité du zinc naturel provient des minerais.
Le zinc est utilisé dans différents secteurs industriels : la galvanisation, le laiton, les alliages, les demi-produits, les usages chimiques.
En France, le zinc dans l'environnement est principalement d'origine anthropique.
La production mondiale de zinc était, en 2012, de 13 604 milliers de tonnes de zinc, et de 732 milliers de tonnes pour l'Union européenne en 2011.
Les émissions françaises industrielles de zinc vers l'environnement sont, tous milieux confondus, selon IREP, d'environ 756 tonnes en 2012 en France. De plus, de nombreux sites industriels sont recensés comme contaminés ou ayant été contaminés au zinc, dans toutes les régions françaises, d'après la base de données BASOL.
Les émissions diffuses de zinc proviennent essentiellement du secteur routier pour le milieu atmosphérique, et de l'agriculture pour le milieu terrestre.
De par ses propriétés physico-chimiques, le zinc s'adsorbe en milieu aquatique sur les matières en suspension. Les sédiments d'eau douce constituent donc un stock potentiel de zinc.
Différents substituts du zinc sont mis en œuvre à l'heure actuelle, notamment dans les domaines des produits phytosanitaires, des toitures. D'autre part, des techniques de réduction des émissions industrielles existent pour les effluents aqueux et gazeux, comme par exemple des techniques de filtration.
Zinc is a metal, its CAS number is 7440-66-6. The main compounds of zinc, which are studied in this report, are zinc chlorite (CAS 7646-85-7), zinc sulphate (CAS 7733-02-0), zinc sulphur (CAS 1314-98-3), zinc oxide (CAS 1314-13-2), trizinc diphosphide (CAS 1314-84-7), zinc chromate (CAS 13530-65-9) and zinc stearate (CAS 557-05-1).
Zinc is a ubiquitous metal, very common in the Earth's crust. Zinc sources are both natural and anthropogenic. Most of natural zinc comes from ores.
Zinc is used in different industrial applications: galvanization, brass, alloys, semi products and chemicals.
In France, zinc in the environment is mainly anthropogenic.
In 2012, the global production of zinc was 13 604 thousand tons and 732 thousand tons for European Union in 2011.
According to IREP, the French industrial emissions of zinc to environment were about 756 tons for all medias for 2012 in France. Moreover, according to the database BASOL, many industrial sites are registered as polluted by zinc or having been polluted by zinc in all regions.
Diffuse emissions of zinc come mainly from road transport for the atmosphere and from agriculture for terrestrial.
By its physic-chemical properties, zinc is adsorbed on suspended solids in aquatic environment. Freshwater sediments are therefore a potential stock of zinc.
Different substitutes of zinc are currently used, especially in pesticides or roofing. On the other hand, techniques exist to reduce industrial emissions in aqueous and gaseous effluents, like for example techniques of filtration.
Tableaux de synthèse
Généralités
| CAS | 7646-85-7 |
|---|---|
| Substance prioritaire dans le domaine de l’eau (DCE) | non |
| Substance soumise à autorisation dans Reach | non |
| Substance soumise à restriction dans Reach | non |
| Substance extrêmement préoccupante (SVHC) | non |
| Réglementations |
FTE 2015 Importer TEXTES GENERAUXLe règlement 1907/2006 concernant l'enregistrement, l'évaluation et l'autorisation des substances chimiques (REACH) oblige les producteurs et les importateurs de substances en quantité supérieure à une tonne à soumettre une demande d'enregistrement. Ces substances sont ensuite pour certaines évaluées, et éventuellement leur usage est ensuite soumis à autorisation. Le zinc et nombre de ses composés sont concernés par le règlement REACH. Le zinc et ses composés ne sont pas cités dans la liste de l'annexe I du règlement (CE) 649/2012 relatif à l'export et à l'import de substances dangereuses. Ils ne sont donc pas soumis aux notifications d'exportations. [3] Données d'enregistrement dans REACH consultées sur le site de l'European Chemicals Agency : (consulté en mai 2014). http://echa.europa.eu/fr/ DIRECTIVE-CADRE SUR L'EAULe zinc et ses composés ne sont pas cités dans la directive n°2013/39/UE du 12 août 2013 modifiant les directives 2000/60/CE et 2008/105/CE en ce qui concerne les substances prioritaires pour la politique dans le domaine de l'eau. De ce fait il n'a pas été fixé de normes de qualité environnementale (NQE) pour le zinc et ses composés. NOMENCLATURE DES INSTALLATIONS CLASSEES (IC)En France, le zinc est concerné par les rubriques suivantes de la Nomenclatures des Installations Classées (selon le Décret n°53-578 du 20 mai 1953 relatif à la nomenclature des installations classées pour la protection de l'environnement). Les rubriques ICPE relatives au zinc sont mentionnées ci-dessous de façon indicative : cette liste ne se veut donc pas exhaustive quant aux secteurs industriels où le zinc et ses composés sont ou peuvent être rencontrés4 :
[4] (consulté en janvier 2014). http://www.ineris.fr/aida/sites/default/files/gesdoc/30296/Nomenclature_octobre.pdf [5] Cette rubrique est une rubrique de définition et non une rubrique de classement. Elle sert à préciser le classement dans d'autres rubriques. En conséquence, aucune installation ne peut être classée sous la rubrique 1430.
SEUILS DE REJETS POUR LES INSTALLATIONS CLASSEESL'arrêté du 26 décembre 2012 modifiant l'arrêté du 31 janvier 2008 concerne le registre et la déclaration annuelle des émissions polluantes et des déchets. L'exploitant de l'installation doit déclarer ces rejets dès lors que les seuils d'émissions décrits dans l'annexe II de cet arrêté sont dépassés. Les seuils de rejets du zinc et composés6 (exprimés en tant que Zn) sont :
L'arrêté du 2 février 1998 modifié relatif aux prélèvements et à la consommation d'eau ainsi qu'aux émissions de toute nature des installations classées pour la protection de l'environnement soumises à autorisation indique que : Pollution de l'airRejets d'antimoine, chrome, cobalt, cuivre, étain, manganèse, nickel, vanadium, zinc, et de leurs composés6 : si le flux horaire total d'antimoine, chrome, cobalt, cuivre, étain, manganèse7 , nickel, vanadium, zinc7 et de leurs composés8 dépasse 25 g/h, la valeur limite de concentration est de 5 mg.m-3 (exprimée en Sb+Cr+Co+Cu+Sn+Mn+Ni+V+Zn). Pollution des eaux superficiellesLes rejets respectent les valeurs limites de concentrations suivantes : Zinc et ses composés (en Zn) 2 mg.L-1 si le rejet dépasse 10 g.j-1. [6] L'arrêté ne précise pas les composés du zinc concernés. [7] En cas de fabrication de monoxyde de zinc (ZnO) et de bioxyde de manganèse (MnO2), la valeur limite de concentration pour respectivement le zinc et le manganèse est de 10 mg.m-3 . [8] L'arrêté ne précise pas les composés concernés. Epandage des bouesL'annexe I de l'arrêté précise les seuils à respecter en éléments-traces pour l'épandage des boues issues du traitement des eaux usées. Ces seuils sont présentés dans le Tableau 3. Le Tableau 3 présente les teneurs limites en éléments-traces dans les boues, les valeurs limites en éléments-traces dans les sols et le flux maximum en éléments-traces apporté par les déchets ou effluents pour les pâturages ou sols de pH inférieurs à 6. Tableau 3. Seuils de zinc applicables aux épandages de boues issues du traitement des eaux usées sur les sols agricoles, d'après l'arrêté du 2 février 1998 modifié.  UTILISATION ET SURVEILLANCE EN AGRICULTURELa Directive 91/414/CEE du Conseil liste les substances actives dont l'incorporation dans les produits phytopharmaceutiques est autorisée. Les seuls composés autorisés du zinc sont :
Cas de l'élevage et de l'agriculture biologiqueLe règlement CE/889/2008 du 5 septembre 2008 autorise l'utilisation de l'oxyde de zinc et du sulfate de zinc en agriculture biologique en tant qu'additif pour l'alimentation des animaux. Ce même règlement autorise l'utilisation de déchets ménagers en tant qu'engrais, dans la limite de 200 g Zn/kg de matière sèche. Cas de l'alimentation animale au sein des élevagesLe règlement CE/1334/2003 du 25 juillet 2003 modifie les conditions d'autorisation de plusieurs additifs (dont le zinc) appartenant au groupe des oligoéléments dans l'alimentation animale. Désormais, la teneur maximale de l'élément zinc en mg/kg d'aliment complet est présentée dans le Tableau 4 ci-après en fonction de l'animal. Tableau 4. Conditions d'autorisation du zinc en tant qu'additif dans l'alimentation animale, d'après le règlement CE/1334/2003.  ACTIONS DE RECHERCHE RSDELe zinc et ses composés sont cités dans l'annexe 1 de la circulaire du 5 janvier 2009 relative à la mise en œuvre de la 2ème phase de l'action RSDE pour les ICPE soumise à autorisation. Cette annexe regroupe les listes par secteurs d'activité industrielle des substances dangereuses. Le zinc et ses composés sont cités pour tous les secteurs d'activité, à l'exception de la fabrication de colles et adhésifs. Le zinc appartient aussi à la liste des micropolluants à mesurer dans les stations de traitement des eaux usées traitant une charge brut de pollution supérieure ou égale à 600 kg DBO5/jour12 (Circulaire du 29 septembre 2010 relative à la surveillance de la présence de micropolluants dans les eaux rejetées au milieu naturel par les stations de traitement des eaux usées). NANOPARTICULESCertains composés du Zinc, notamment l'oxyde de zinc, peuvent être employés sous forme nanoparticulaire (par exemple, dans des textiles pour ses propriétés biocides). Le décret n° 2012-232 du 17 février 2012 relatif à la déclaration annuelle des substances à l'état nanoparticulaire précise que le seuil de la déclaration est fixé à 100 g/an pour la fabrication, l'importation ou la mise sur le marché de nanomatériaux. ENGRAISPour les engrais organiques, divers seuils en métaux lourds sont fixés par les législations européennes et nationales. Les seuils pour le zinc sont repris dans le Tableau 513 . [12] DBO5: demande biochimique en oxygène. [13] (consulté en février 2014). http://ec.europa.eu/enterprise/sectors/chemicals/files/fertilizers/annexes_16jan2012_en.pdf Tableau 5. Seuils de zinc pour les engrais organiques.  Pour les engrais minéraux, il n'existe pas de règlementation européenne, néanmoins l'évaluation du règlement CE 2003/2003 relatif aux engrais16 préconise d'inclure dans le règlement des dispositions concernant les teneurs maximales en métaux lourds. AUTRES TEXTESLe zinc appartient à la liste des 823 substances du plan micropolluants 2010-201317 . Le zinc ne fait pas partie de la liste OSPAR18 . [14] European Compost Network. [15] Joint Research Center. [16] (consulté en février 2014). http://ec.europa.eu/enterprise/sectors/chemicals/files/fertilizers/final_report_2010_en.pdf [17] (consulté en févirer 2014). http://www.developpement-durable.gouv.fr/IMG/pdf/plan_micropolluants_dv.pdf [18] Convention OSPAR: Convention pour la protection du milieu marin de l'Atlantique du nord-est : (consulté en mars 2014). http://www.ospar.org/content/content.asp?menu=30950304450153_000000_000000 Protocole relatif à la protection de la mer Méditerranée19 : Le zinc est cité dans la liste des substances et matières nuisibles ou nocives dont le rejet dans la zone du protocole est assujetti à permis spécial |
| Classification CLP | Voir la classification CLP |
| Valeurs et normes appliquées en France |
FTE 2015 Importer VALEURS UTILISEES EN MILIEU DE TRAVAILD'après l'INRS (2012), les valeurs moyennes d'exposition pour certains composés du zinc sont les suivantes : 3 VME(chlorure de zinc, fumées) : 1 mg/m(en Zn) ; 9 [9] VME : Valeur Moyenne d'Exposition. VALEURS UTILISEES POUR LA POPULATION GENERALEValeurs de références dans la population générale :Le zinc est présent naturellement dans le corps humain. Selon l'INRS (2009), les valeurs de références des substances10 présentes dans les urines et le sang sont précisées ci-dessous : Valeur de référence du zinc dans le sang : 4-7,5 mg.L-1 ; Qualité de l'eau de consommation :La Directive 98/83/CE du conseil du 3 novembre 1998 relative à la qualité des eaux destinées à la consommation humaine n'indique pas de valeurs spécifiques pour le zinc. Le Décret n°2001-1220 du 20 décembre 2001 relatif aux eaux brutes destinées à la consommation humaine (consolidé par la version du 27 mai 2003) indique que la limite de qualité des eaux brutes et des eaux douces superficielles utilisées pour la production d'eau destinées à la consommation humaine est de 5 mg (en Zn) /L. Qualité des rejets d'eau résiduaire urbaine :L'Arrêté du 2 février 1998 relatif aux rejets des eaux résiduaires dans le milieu naturel indique que les rejets de zinc et de ses composés doivent respecter la valeur limite de concentration suivante : 2 mg (en Zn)/L si le rejet dépasse 20 g.j-1. Produits alimentaires :Le Règlement 10/2011 précise que les matériaux et objets en matière plastique destinés à entrer en contact avec les denrées alimentaires ne peuvent pas libérer plus de 25 mg Zn/kg de denrée alimentaire. De plus, l'oxyde de zinc, le sulfure de zinc et l'hydroxyde de zinc sont autorisés comme additif ou auxiliaire de production de polymères, mais sont interdits comme monomère11 ou substance de départ. [10] Les substances concernées sont le chlorure de zinc, le diphosphure de trizinc, l'oxyde de zinc, le sulfate et le sulfure de zinc. [11] Un monomère est une substance à la base d'un polymère, qui consiste en un assemblage d'un ou plusieurs monomères. |
Production et utilisation
Production et ventes
Données économiques
FTE 2015 Importer
MINERAIS
Selon Vignes (2013)23 , la teneur moyenne de l'écorce terrestre en zinc est de 80 mg/kg. Dans les minerais, le zinc est très souvent associé au plomb et au cadmium, ainsi qu'au fer, cuivre, bismuth, antimoine, arsenic, germanium, indium, or et argent.
Le zinc et ses composés sont présents naturellement dans la croûte terrestre à des concentrations de l'ordre de 40 à 120 mg/kg dans les roches magmatiques, les sédiments argileux24 et les schistes (ATSDR, 2005 ; Agence de l'eau Seine-Normandie, 2009).
Les principaux minerais du zinc sont les suivants :
- les minerais sulfurés (blende, ZnS ou sulfure de zinc macroscopiquement associé à du sulfure de plomb) ;
- les minerais carbonatés (smithsonite, ZnCO3) ;
- les minerais silicatés et oxydés (hémimorphite, Zn4SiO7(OH)2, H2O et willémite, Zn2SiO4) regroupés sous le nom de calamine (Techniques de l'ingénieur, 1988).
PRODUCTION MINIERE
Selon Vignes (2013), la production mondiale de zinc, très majoritairement à base de blende, était, en 2012, de 13 604 milliers de tonnes de zinc contenu et de 732 milliers de tonnes (5 %) pour l'Union européenne en 2011.
Selon cette même source, en 2012, les réserves mondiales étaient estimées à 250 millions de tonnes de zinc contenu. La répartition de ces réserves est la suivante (en millions de tonnes) : Australie : 70, Chine : 43, Pérou 18, Mexique : 16, Inde : 12, Etats-Unis : 11, Kazakhstan : 10 et Canada : 8.
Il existe encore des mines en Europe, la plus importante étant en Irlande. Lors de cette étude, nous n'avons pas identifié de mine en France.
[23] (consulté en février 2014). http://www.societechimiquedefrance.fr/extras/Donnees/acc.htm
[24] Dans ces sédiments argileux, le zinc est présent à des concentrations comprises entre 80 et 120 mg/kg.
PROCEDES
La production de zinc est réalisée par extraction à partir des minerais de zinc. Les sources principales sont les minerais sulfurés (blende), les minerais carbonatés (smithsonite), les minerais silicatés et oxydés (hémimorphite et willémite) (Techniques de l'ingénieur, 1988). Ces derniers sont en voie d'épuisement (CNUCED, 2009 ; Techniques de l'ingénieur, 2000).
Selon la CNUCED (2009), la transformation du minerai en un produit commercialisable est constituée de 2 étapes principales :
- le minerai est broyé puis traité chimiquement afin de séparer les impuretés et les différents concentrés de zinc ;
- l'affinage permet d'obtenir du métal brut. Deux procédés sont utilisés pour cette étape, l'hydrométallurgie et la pyrométallurgie. Ces deux procédés sont détaillés dans le paragraphe suivants, les informations sont issues de CNUCED (2009) et des Techniques de l'ingénieur (2000).
Hydrométallurgie (extraction par voie humide ou électrolyse)
Selon nos informations, l'hydrométallurgie semble bien développée pour la production de métaux tels que le zinc. Ce procédé est principalement utilisé pour le traitement des roches riches en fer. Il se réalise en 4 étapes.
L'étape 1 est le grillage consistant à transformer le sulfure de zinc en oxyde (cf. Figure 1 pour les réactions). Cette oxydation dégage du SO2 qui est transformé en SO3, puis en acide sulfurique H2SO4. Le procédé utilisé est un procédé de contact à double catalyse. L'oxyde de zinc issu du grillage est appelé calcine.
(2)
Figure 1. Réactions lors du procédé de contact à la double catalyse – catalyseur V2O5, d'après Vignes (2013).
L'étape 2 est la lixiviation qui consiste à solubiliser le zinc et à précipiter le fer. La première lixiviation est neutre. On obtient une solution de sulfate de zinc à 150 g.L-1. Puis la lixiviation acide avec une solution d'acide sulfurique (180 à 190 g.L-1) traite les résidus de la lixiviation neutre. Le fer est précipité sous forme de goethite. A cette étape, la solution de zinc contient encore des impuretés.
L'étape 3 est une purification de la solution. La cémentation25 va permettre l'élimination d'impuretés comprenant du cuivre, du cobalt et du cadmium. Cette élimination nécessite l'utilisation de poudre de zinc récupérée ensuite par filtration. La solution de sulfate de zinc est alors purifiée.
L'étape 4 est l'électrolyse de la solution purifiée. Dans la cellule d'électrolyse du zinc massif se dépose sur la cathode d'aluminium. Il est récupéré par pelage ou stripping et est ensuite raffiné par fusion. Le zinc obtenu est très pur (99,995 %) et contient principalement du plomb comme impureté.
A ce stade, le zinc est fondu et moulé en plaque pour acquérir sa forme commerciale.
Pyrométallurgique (l'extraction par voie sèche ou voie thermique)
La pyrométallurgie est la technique traditionnelle d'extraction des métaux. Elle permet de purifier le minerai au moyen d'énergie thermique. Elle est constituée de 3 étapes.
Comme pour l'hydrométallurgie, l'étape 1 est le grillage. L'objectif de l'oxydation du minerai en calcine (cf. Figure 2 pour les réactions) est de préparer le minerai pour un rendement approprié à l'étape 2. La teneur en soufre total (sulfure et sulfate) doit être inférieure à 0,5 % et la porosité du minerai importante.
(1)
(2)
- (1)Réaction exothermique qui s'amorce à environ 700°C.
- (2)Réaction parasite menant à la production de ZnSO4.
Figure 2. Réaction d'oxydation catalytique par voie sèche (Techniques de l'ingénieur, 1998 ; CNUCED, 2009).
A ce stade, l'anhydride sulfureux issu des gaz est transformé par oxydation catalytique en de l'anhydride sulfurique et de l'acide sulfurique.
L'étape 2 est la réduction de l'oxyde avec du carbone et de l'oxyde de carbone selon les réactions ci-après.
[25] Dans le domaine de la métallurgie, la cémentation est un traitement thermochimique de diffusion. La cémentation superficielle de l'acier par le carbone (cémentation la plus employée) permet de durcir la surface de diverses pièces mécaniques : engrenages, axes, cames, arbres, etc.
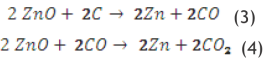
- (3)Température de la réaction 950°C.
- (4)Température de la réaction entre 1 300 et 1 400°C.
Figure 3. Réduction de l'oxyde de zinc (Techniques de l'ingénieur, 1998 ; CNUCED, 2009).
La température de réduction de l'oxyde de zinc est supérieure à la température d'ébullition du métal. Le zinc étant gazeux lors de sa formation, il se sépare de la gangue du minerai26 .
Le zinc issu de cette étape a une pureté d'environ 98,5 %, la production du zinc métal pourrait s'arrêter à cette étape. Cependant, ce taux de pureté limite l'utilisation à la galvanisation au trempé.
L'étape 3 est l'affinage du zinc brut. Les métaux plomb, fer, plus rarement cadmium, arsenic, antimoine et cuivre sont encore présents. L'affinage peut se faire dans un four à liquidation et/ou dans une colonne à distiller. A la sortie du four, 3 produits sont récupérés :
- le zinc purifié à 99 % ;
- le plomb zincifère (5 à 6 % de zinc) ;
- les mattes27 (5 à 6 % de fer).
La distillation fractionnée permet d'obtenir des métaux plus purs. Le zinc ainsi obtenu a une pureté de 99,995 %.
Production des principaux composés du zinc
Le chlorure de zinc est principalement produit par traitement de matières premières secondaires (ou de récupération). Ces dernières sont d'abord dissoutes dans de l'acide chlorhydrique, avant purification et raffinage de la solution. Lors de la production sont également produites des boues contenant soit du plomb, soit d'autres métaux lourds (cuivre, cadmium). Ces boues sont précipitées puis séparées, procurant par là-même des matières premières secondaires (Commission Européenne, 2008c).
[26] La gangue est constituée des mineraux sans valeur commerciale enveloppant le minerai convoité.
[27] Les mattes de zinc sont générées lors de la décantation des composés insoluble (Zn et Fe) qui forment des cristaux de FeZn7.
Le sulfate de zinc est produit à partir de matériaux contenant du zinc, tels que des cendres de zinc, du carbonate de zinc. Le zinc est d'abord séparé des matériaux de départ par lixiviation à l'acide sulfurique, suivie de divers procédés de purification. Les sulfates de plomb sont séparés par précipitation et vendus comme matières premières secondaires. Les autres métaux lourds et impuretés (cuivre, cadmium, manganèse) sont séparés par précipitation. Le sulfate de zinc pur est cristallisé (Commission Européenne, 2008b).
L'oxyde de zinc est produit par des procédés directs et indirects. Pour le procédé direct, le réactif de départ est constitué de minerais contenant du zinc, que l'on oxyde pour former de l'oxyde de zinc. Dans le procédé indirect, le réactif est du zinc métal (de pureté 92-99,995 %). Le métal est vaporisé et les vapeurs sont oxydés pour produire de l'oxyde de zinc. Des procédés différents, ainsi que des variations de procédés et de matières premières, résultent une grande variété de types d'oxydes de zinc, chacun avec des particules de taille différentes et contenant des impuretés. L'oxyde de zinc produit par le procédé direct est moins pur que celui produit par le procédé indirect (Commission Européenne, 2008f).
Le phosphure de zinc est produit par réduction électrothermique de l'oxyde de zinc en présence de carbone et de phosphate (Bettermann, 1986).
Le chromate de zinc peut être produit soit par la réaction d'oxyde de zinc finement broyé dans l'acide sulfurique concentré, soit par la réaction d'un sel de zinc soluble dans l'eau (ZnCl2 ou ZnSO4) avec du dichromate de potassium ou d'ammonium (Anger, 1986).
Le stéarate de zinc peut être produit par trois méthodes : la méthode de double décomposition, le procédé de transformation directe et le procédé de fusion. Seul le premier de ces procédés génère des eaux usées.
Dans la méthode de double décomposition, on ajoute à de l'acide stéarique de la soude pour former un alkalistéarate. Il est ensuite ajouté à cet alkalistéarate du chlorure de zinc. Le stéarate de zinc précipite et est séparé par filtration, puis lavé et séché.
Dans le procédé de transformation directe, de l'acide stéarique et de l'oxyde de zinc sont mélangés avec de l'eau. La température du mélange réactionnel est juste en dessous de la température de fusion des réactifs. La réaction a lieu selon la réaction suivante :
L'eau est ensuite éliminée.
Le procédé de fusion est similaire à celui de transformation directe. L'unique différence est la température du mélange réactionnel, qui est au-delà de la température de fusion des réactifs. L'eau formée est évaporée durant la réaction (Commission Européenne, 2008e).
RECYCLAGE
Le zinc recyclé représente environ 40 % de la consommation mondiale. En 2012, aux Etats-Unis, la production de zinc secondaire était de 150 000 tonnes, contre 115 000 tonnes pour la production primaire.
Le zinc recyclé provient soit de produits en fin de vie, soit de chutes et de déchets des usines métallurgiques. Le zinc récupéré est soit réutilisé directement, soit réemployé après refusion, soit retraité en suivant le circuit de la métallurgie de 1ère fusion, d'après Vignes (2013).
D'après cette même source, en 2003, dans le monde occidental, les principales sources de zinc recyclé étaient l'industrie du laiton (42 %), la galvanisation (27 %), la fonderie (16 %), le zinc laminé (6 %), les poussières d'aciéries (6 %) et l'industrie chimique (2 %).
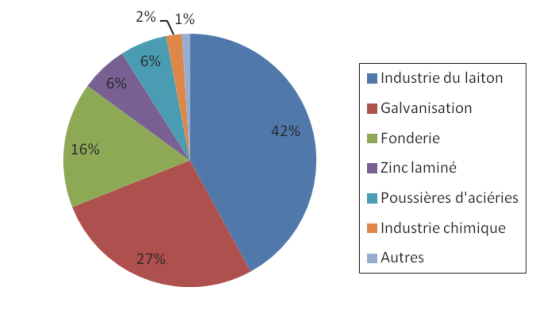
Figure 4. Principales sources de zinc recyclé par secteur industriel en 2003, d'après Vignes (2013).
D'après la CNUCED28 , la consommation mondiale de zinc se situe au quatrième rang des métaux après celle du fer, de l'aluminium et du cuivre. Il est exploité dans de nombreuses régions. Les principaux pays producteurs représentant 65 % de la production mondiale sont la Chine, l'Australie, le Pérou, le Canada et les Etats Unis.
Selon Vignes (2013), la dernière mine exploitée en France a fermé en décembre 1993.
Néanmoins, s'il n'y a plus d'exploitation, la France continue à produire du zinc, à partir de minerai importé et de recyclage. En 2012, la production française de zinc était de 161 000 tonnes (Vignes, 2013).
[28] Conférence des Nations Unies sur le Commerce et le Développement : (consulté en février 2014). http://r0.unctad.org/infocomm/francais/zinc/marche.htm
Selon l'INSEE29 , sur une base de production de 100 % en 2005, la production de « plomb, zinc, étain » a diminué en France jusqu'en 2008 où elle ne représentait plus que 71 % et 31 % de la production en 2005, puis est remontée. En 2012, elle représente 81 % de la production de 2005.La Figure 5 ci-après présente les variations de la production de plomb, zinc, étain.
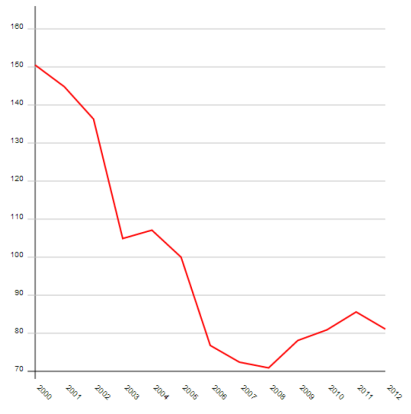
Figure 5. Production de «Plomb, Zinc et Etain» 30 de 2000 à 2012 en France (Base 100 : 2005), d'après l'INSEE.
[29] Institut National de la Statique et des Etudes Economiques : (consulté en mai 2014). http://www.bdm.insee.fr/bdm2/affichageSeries.action?anneeDebut=2000&anneeFin=2012&page=graphique&recherche=idbank&codeGroupe=960&idbank=001563495
[30] En France, le secteur du zinc est représenté par le code NAF 27.4F (Production de plomb, de zinc ou d'étain) :
- la production de plomb, de zinc et d'étain (première ou deuxième fusion);
- la production d'alliages de plomb, de zinc et d'étain.
dans
la
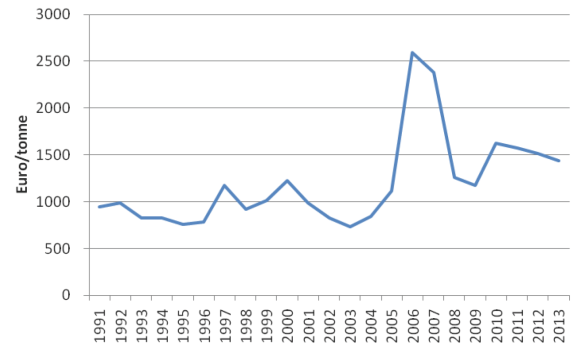
Figure 6. Prix du zinc brut sur le marché de Londres (LME) en euro/tonne (AGORIA31).
Le prix moyen en janvier 2014 du zinc brut était d'environ 1 500 euro/tonne. Les cotations du zinc laminé sont présentées dans la Figure 7 ci-après.
[31] (consulté en février 2014). http://www.agoria.be/FR/Mercuriale-des-materiaux-tableaux-synoptiques-67005?vWebsessionID=65599&vUserID=999999
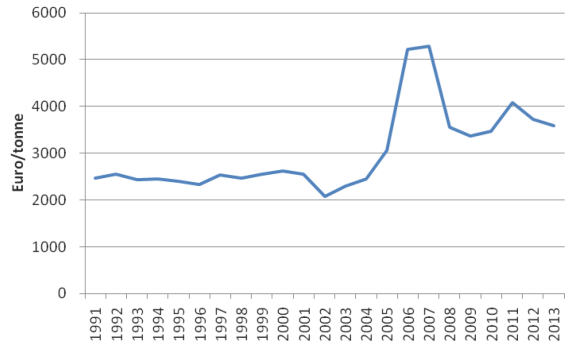
Figure 7. Prix du zinc laminé en euro/tonne (AGORIA).
Le prix moyen du zinc laminé, qui suit à une translation d'environ + 2 200 €/tonne celui du zinc brut, était d'environ 3 700 euro/tonne en janvier 2014.
Le Tableau 7 ci-après présente les prix des principaux composés du zinc trouvés sur le site commercial Alibaba32 .
[32] (consulté en mai 2014). http://www.alibaba.com/
Tableau 7. Prix des principaux composés du zinc en mai 2014, d'après Alibaba.
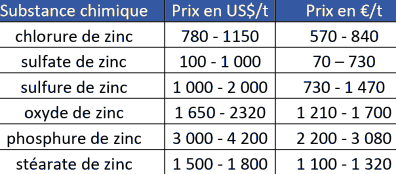
cours au 26 mai 201433 : 1 US$ = 0,733€
Utilisations
UTILISATIONS
FTE 2015 Importer
En 2003, le zinc est utilisé à 75 % sous forme métallique. Les autres 25 % sont très majoritairement constitués des oxydes de zinc et des sulfures de zinc (CNUCED, 2009). Les secteurs d'utilisation sont détaillés dans les paragraphes ci-dessous : zinc métal et composés du zinc.
UTILISATIONS DU ZINC
FTE 2015 Importer
D'après Vignes (2013), en 2012, à l'échelle mondiale, les principaux secteurs d'utilisation du zinc sont la galvanisation : 50 %, le laiton : 17 %, les autres alliages : 17 %, les demi produits : 6 %, les usages chimiques : 6 % et les autres produits : 4 %. D'après la CNUCED, de manière générale, à l'échelle internationale, en 2003, le zinc métal est utilisé à 45 % dans la construction, 25 % dans les transports, 23 % dans les produits domestiques et biens électriques et 7 % dans les machines.
Le zinc métal est principalement utilisé pour les revêtements, dans les alliages tels que le laiton, les alliages moulés sous pression et le zinc plaqué ou forgé. Il est également utilisé pour produire des composés du zinc, des pigments et d'autres produits chimiques (Commission Européenne, 2008a). La répartition de la consommation du zinc est illustrée dans le Tableau 8 ci après, pour le Monde, les Etats-Unis et la France.
[33] Banque Central Européenne : (consulté en mai 2014). http://www.ecb.europa.eu/stats/exchange/eurofxref/html/eurofxref-graph-usd.en.html
Tableau 8. Consommation du zinc métal pour chaque secteur industriel, d'après Vignes (2013).
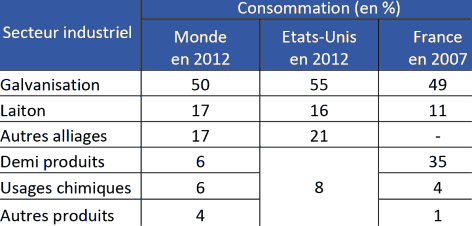
Revêtement
Le zinc métal est utilisé dans les revêtements anticorrosion des métaux par les techniques de galvanoplastie, métallisation ou immersion et dans les peintures (ATSDR, 2005 ; INRS, 2002). Il protège les métaux de la rouille et les bâtiments des altérations (INRS, 2002).Dans le secteur de la protection des métaux, le zinc en lui-même n'est pas très stable thermodynamiquement. Cependant il est utilisé, car il libère des ions Zn2+ qui en précipitant forment des produits protecteurs tels que le carbonate de zinc, un hydroxycarbonate de zinc et l'hydroxyde de zinc (Techniques de l'ingénieur, 2004).
Batteries
Il est utilisé dans les cellules de batteries sèches (ATSDR, 2005). Le zinc et/ou ses composés sont utilisés dans de nombreuses piles électriques :
- Zinc-carbone ;
- Zinc-chlorure ;
- Alkaline (zinc et dioxyde de manganèse) ;
- Nickel oxy hydroxyde ;
- Zinc-air ;
- Argent oxyde (argent et zinc ; pile rechargeable) (d'après le site de l'IZA34).
[34] International Zinc Association : (consulté en mars 2014). http://www.zincworld.org/index.html
Autres
Les pièces de monnaie (y compris certaines pièces d'euro) peuvent être réalisées à partir de l'alliage de zinc et de cuivre d'après le site ECB35 . Il est également utilisé pour préparer des alliages de fonderie type Zamak36 (INRS, 2002).
VUE D'ENSEMBLE DES COMPOSES CHIMIQUES DU ZINC ET LEUR UTILISATION
FTE 2015 Importer
Les composés du zinc ayant été enregistrés dans REACH (selon la base publique de l'ECHA, consultée en février 2014), pour des usages autres que des intermédiaires de synthèse, et à des tonnages supérieurs à 100 tonnes37 , sont présentés dans le Tableau 9 ci-après.
Tableau 9. Composés du zinc et tonnages, d'après l'ECHA (2014).

[35] European Central Bank : (consulté en mars 2014). http://www.ecb.europa.eu/ecb/html/index.en.html
[36] Le Zamak est un alliage de zinc, d'aluminium et de magnésium et parfois de cuivre.
[37] Quant à lui, le Pentazinc chromate octahydroxide est enregistré pour des tonnages inférieurs à 100 tonnes.
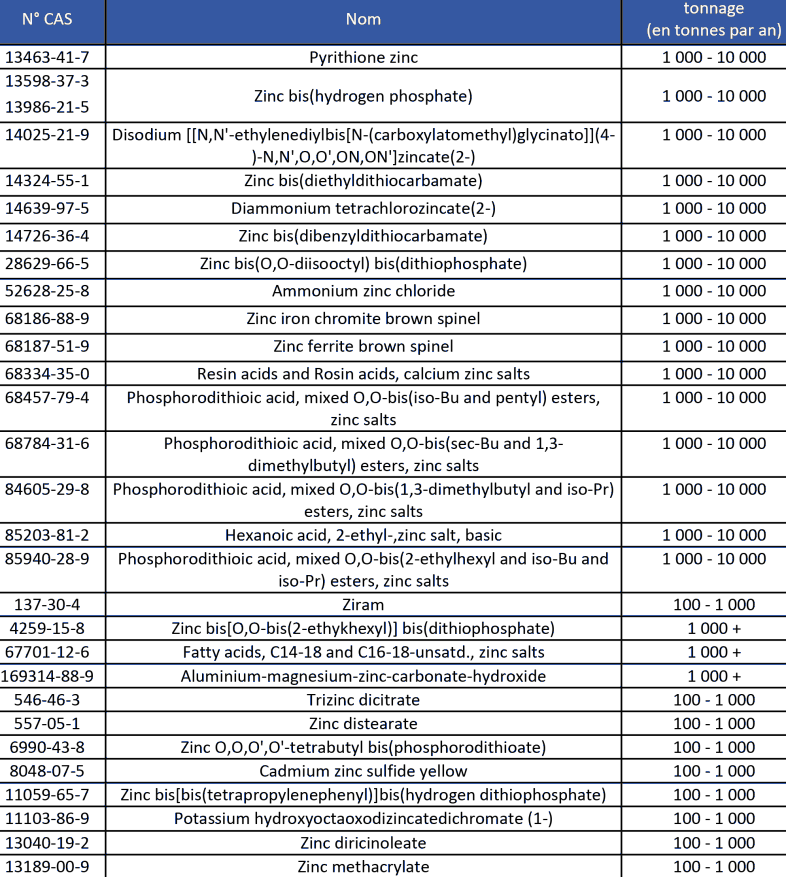
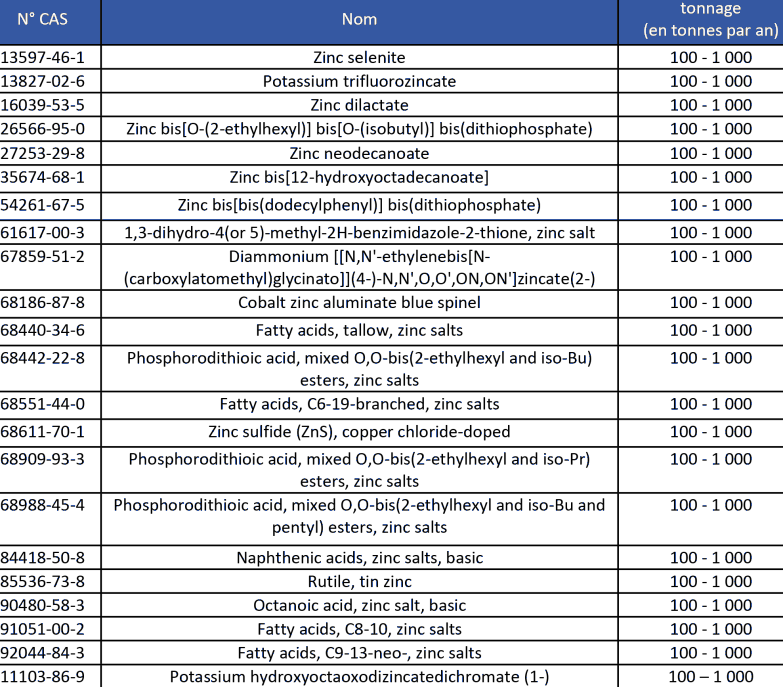
Les composés du zinc sont utilisés dans l'industrie des peintures, des caoutchoucs, des teintures, dans les produits de conservation du bois et dans les produits pharmaceutiques. Les secteurs d'utilisation des composés du zinc tels que reportés dans l'ATSDR (2005), l'INRS (2002), les Techniques de l'ingénieur (2004) et la CNUCED (2009) sont détaillés (de façon non exhaustive) ci-après pour les principaux composés de cet élément.
Le chlorure de zinc (ZnCl2) est utilisé dans l'industrie chimique (régulateur de process, catalyseurs) (37 %), le secteur de la galvanisation (28 %), l'industrie des piles (électrolyte) (15 %), dans l'industrie agroalimentaire (en tant que fongicide) (13 %) et l'industrie des peintures et colorants (7 %). Il est aussi utilisé dans l'industrie textile et papetière, dans le secteur pharmaceutiques et vétérinaires et dans le secteur du bois (agent de conservation pour ce dernier) (Commission Européenne, 2008c).
Le sulfate de zinc (ZnSO4) est utilisé dans les revêtements anticorrosion des métaux par les techniques de galvanoplastie, métallisation ou immersion et dans les peintures (en tant que pigments et/ou de substances anticorrosion). Il est aussi utilisé dans l'industrie textile, papetière, pour la conservation du bois et des peaux, pour la fabrication d'engrais et de pesticides (60 %), de produits pharmaceutiques et vétérinaires (tels que des additifs d'aliments pour animaux) (20 %) (Commission Européenne, 2008b). Le sulfate de zinc est employé par l'industrie chimique (20 %).
Le sulfure de zinc (ZnS) est utilisé dans la réalisation d'écrans de télévision et de lampes fluorescentes (tubes cathodiques). Il est aussi utilisé dans la fabrication de pigments pour peintures, émaux, matières plastiques et caoutchouc.
L'oxyde de zinc (ZnO) est employé dans la fabrication des caoutchoucs et plastiques (36 %), dans l'industrie du verre et de la céramique (27 %), dans les produits tels que les varistors, les aimants en ferrite et en tant que catalyseur (12 %), dans l'industrie agroalimentaire (complément alimentaire pour animaux) (9 %), des peintures (4,5 %), dans la production des composés du zinc (borate de zinc, phosphate de zinc, silicate de zinc, stéarate de zinc, thiocarbamate de zinc, diacrylate de zinc)38 (4,5 %), dans les carburants en tant qu'additif (4,5 %), dans le secteur pharmaceutique et cosmétique (2 %). Son utilisation dans la fabrication des produits à base de caoutchouc a pour objectif d'accélérer la vulcanisation39 . Pour l'industrie de la céramique et du verre, l'oxyde de zinc est employé pour réduire la fissuration et pour améliorer l'opacité. Dans les peintures, l'oxyde de zinc agit contre les moisissures et comme biocide38 . Le zinc est également utilisé dans les encres d'impression, les textiles, dans les savons et les produits nettoyants (Commission Européenne, 2008f).
Le chromate de zinc (ZnCrO4) est principalement utilisé dans les traitements de surface pour la chromatation. Il est également utilisé dans les peintures pour métaux (peinture d'apprêt anticorrosion) et les vernis ; comme pigment pour peintures automobiles, colorant pour artistes et comme agent anticorrosion dans les stratifiés époxy (INRS, 2005).
[38] (consulté en juin 2014). http://www.zn-oxide.com/
[39] La vulcanisation est un exemple de réticulation c'est-à-dire de création de liaison entre les macromolécules.
Le stéarate de zinc (C36H72O4Zn) est principalement utilisé dans l'industrie des polymères (en tant que stabilisateur, lubrifiant) (55 %), dans l'industrie des peintures, laques et vernis en tant que qu'agent décapant (18 %), dans l'industrie du bâtiment (agent imperméable du ciment) (5 %), dans l'industrie du carton, papier et du textile (agent imperméable) (2 %), dans le secteur pharmaceutique et cosmétique (1 %), dans l'industrie chimique (1 %) et dans le secteur des métaux (1 %) (Commission Européenne, 2008e).
Les Dialkyldithiophosphates de zinc sont utilisés comme additif des lubrifiants de toute nature (automobiles, moteurs, pompes,…). Les quantités en jeu peuvent être importantes, puisque ils sont présents dans la plupart des lubrifiants présents sur le marché40 .
Les carbonates et hydroxydes de zinc tels que le ZnCO3, Zn(OH)2 et Zn5(CO3)2(OH)6 sont utilisés dans les revêtements anticorrosion des métaux et des peintures.
Les scories (slags, lead-zinc smelting) sont utilisées comme additifs dans la production de matériaux de construction et comme agent de fluidification dans les procédés pyrométallurgiques41 .
Ces composés ainsi que de nombreux autres composés du zinc sont utilisés en tant que catalyseur par l'industrie chimique. Face à la multiplicité de ces usages, il n'est pas possible de les citer dans cette fiche.
LES NANOPARTICULES
FTE 2015 Importer
D'après l'ANSES42 (2013), seuls deux composés nanoparticulaires du zinc ont été enregistrés dans le cadre du registre français sur les nanoparticules, l'oxyde de zinc et le stéarate de zinc. Leurs usages sont repris dans le Tableau 10 ci-après.
[40] (consulté en septembre 2015). http://apps.kemi.se/flodessok/floden/kemamne_eng/zinkdialkyl_eng.htm
[42] Bilan 2013 de déclarations des substances importées, fabriquées ou distribuées en France en 2012. (consulté en mars 2014). http://www.developpement-durable.gouv.fr/IMG/pdf/Rapport_public_format_final_20131125.pdf
Tableau 10. Composés nanoparticulaires du zinc, d'après l'ANSES (2013).

Un exemple d'utilisation potentielle des nanoparticules de zinc est le secteur de la santé : Pour lutter contre les infections contractées en milieu hospitalier elles pourraient être utilisée fabriquer des textiles antibactériens pour les hôpitaux.
C'est l'objectif du projet SONO, («A pilot line of antibacterial and antifungal medical textiles based on a sonochemical process») qui a été financé par l'UE. Il se base sur un processus de laboratoire récemment breveté et éprouvé, en une étape, pour imprégner des textiles par des nanoparticules d'oxydes de zinc et de cuivre43 .
PRECISIONS SUR LES USAGES DU ZINC EN METTALURGIE
FTE 2015 Importer
Les paragraphes ci-après apportent des informations quant à la galvanisation et aux alliages ayant recours au zinc.
[43] (consulté en juin 2014). http://cordis.europa.eu/result/brief/rcn/11169_fr.html
Galvanisation
La galvanisation est un procédé de revêtement des métaux ferreux, dont l'acier. Le recouvrement peut se faire par immersion des pièces dans un bain de zinc fondu (galvanisation à chaud), ou par électrolyse (galvanisation à froid) (CNUCED, 2009). Ces deux procédés détaillés ci-après permettent notamment une protection contre la corrosion liée à l'air et l'eau.
Les produits les plus souvent galvanisés sont l'acier en feuilles, les tubes, les fils et les câbles métalliques (CNUCED, 2009).
D'après Vignes (2013), en 2007, en France, les produits en acier galvanisés sont utilisés dans le bâtiment, la construction (40,0 %), le mobilier urbain (16,5 %), l'énergie (6,2 %), l'agriculture (14,2 %), l'équipement industriel (10,0 %), les transports (12,0 %) et la visserie (1,1 %).
Galvanisation à chaudLa galvanisation à chaud nécessite de préparer soigneusement la surface à recouvrir, les premières étapes sont le dégraissage, le décapage, puis le fluxage qui permet de réoxyder la surface de façon homogène. Ensuite la pièce est immergée dans un bain de zinc fondu. Ce procédé crée un alliage entre le zinc et l'acier.
Selon l'association Galvazinc44 , les secteurs d'utilisation de la galvanisation à chaud de produits finis sont principalement le bâtiment-construction à 45,7 %, le mobilier urbain à 15,3 % et l'agriculture et horticulture à 13 %.
Galvanisation à froid ou électrozingageLa galvanisation à froid (i.e. la galvanoplastie) est basée sur le principe de l'électrolyse : c'est-à-dire la réalisation d'un dépôt de zinc métallique sur un objet mis à la charge négative immergé dans une solution de sels de zinc (notamment les chlorures et sulfates de zinc) (CNUCED, 2009).
Alliages
L'alliage de zinc le plus connu est le laiton. Il est utilisé pour remplacer le cuivre en raison du moindre prix du zinc, il présente une bonne résistance à la corrosion et peut recevoir des traitements de surface. Il peut également être moulé, travaillé à chaud et à froid. De plus il supporte les déformations importantes. Il existe différents laitons :
[44] (consulté en mars 2014). http://www.galvazinc.com/la-galvanisation/la-galvanisation-%C3%A0-chaud/march%C3%A9.html
- les laitons simples : contenant de 5 à 45 % de zinc et de 55 à 95 % de cuivre, utilisés dans la quincaillerie, la cartoucherie, la bijouterie, les douilles de lampes, les instruments de musique, la visserie, la serrurerie et les appareils sanitaires ;
- les laitons au plomb : contenant 1 à 3,7 % de plomb et 35 à 40 % de zinc, utilisés pour la fabrication de pièces décolletées45 ;
- les laitons spéciaux : contenant de l'aluminium (moins de 3 % du mélange) destiné à augmenter la résistance des alliages utilisés dans la plomberie, ou de l'étain (moins de 2 % du mélange) pour que les alliages utilisés dans l'industrie navale résistent à la corrosion causée par le sel de mer d'après la CNUCED et Vignes (2013).
D'autres alliages moins fréquemment rencontrés contiennent du zinc notamment le maillechort ou argentant, le métal anglais, tombac et le zamak46 , d'après la CNUCED.
[45] Pièces usinées par enlèvement de matière à partir de barres de métal.
[46] Maillechort ou Argentan: alliage inaltérable de cuivre, de zinc et de nickel. On l'utilise notamment dans la fabrication de pièces d'orfèvrerie ou d'instruments scientifiques, d'après la CNUCED. Métal anglais : alliage à base de zinc et d'antimoine. Ce mélange contient entre 70 et 94 % de zinc, 5 à 24% d'antimoine, du cuivre jusqu'à concurrence de 5% et parfois du plomb jusqu'à 9%. Il est notamment employé dans la fabrication de services de table, de couverts ou de théières, d'après le CNUCED. Tombac : ce nom est donné à différents alliages à base de cuivre et de zinc (laitons) contenant plus de 80% de cuivre et pouvant renfermer de petites quantités d'étain. Il possède une couleur proche de celle de l'or. Il est souvent utilisé en bijouterie sous forme de bandes ou de fils, d'après la CNUCED. Zamak : (nom déposé) c'est la dénomination commerciale désignant un alliage à base de zinc, d'aluminium (3,9 à 4,3%), de magnésium (0,03 à 0,06%) et éventuellement de cuivre (1 à 3%). Dans l'industrie automobile, il est utilisé dans la fabrication de poignées, de corps de pompe et de carburateurs. Dans l'industrie radio-électrique et de la téléphonie mobile, il sert à réaliser des pièces de petite taille. Enfin, il trouve un large éventail de débouchés dans la serrurerie et la quincaillerie, d'après la CNUCED.
Rejets dans l’environnement
Sources naturelles
FTE 2015 Importer
Le zinc et ses composés sont présents naturellement dans la croûte terrestre à des concentrations de l'ordre de 40 à 120 mg/kg dans les roches magmatiques, les sédiments argileux21 et les schistes (ATSDR, 2005 ; Agence de l'eau Seine-Normandie, 2009).
Les apports naturels de zinc se font principalement par transport éolien de particules du sol, émissions liées aux éruptions volcaniques, génération d'aérosols marins et par émissions suite aux feux de forêts (Agence de l'eau Seine-Normandie, 2009 ; INERIS, 2005 ; Commission Européenne, 2008f, 2008a).
[21] Dans ces sédiments argileux, le zinc est présent à des concentrations comprises entre 80 et 120 mg/kg.
Le FOREGS22 construit des cartes (qui sont présentées paragraphe 4.2) montrant les concentrations en zinc dans 26 pays européens et dans différents milieux (sol couche profonde et de surface, sédiments de cours d'eau et de plaines alluviales et cours d'eau). Ces cartes montrent de grandes différences entre les régions. Les régions présentant de faibles concentrations en zinc sont la Pologne, les pays baltes et la Finlande. Les régions présentant de fortes concentrations sont l'Angleterre, l'Autriche et la République tchèque.
La France présente des concentrations assez fortes en ce qui concerne les couches profondes et superficielles des sols, ainsi que les sédiments de plaines alluviales, les concentrations dans les cours d'eau et les sédiments de cours d'eau sont plus faibles.
Sources non-intentionelles
FTE 2015 Importer
Sans objet
[22] Forum of the European Geological Surveys : Atlas Géochimique de l'Europe : (consulté en janvier 2014). http://weppi.gtk.fi/publ/foregsatlas/
Émissions anthropiques totales
FTE 2015 Importer
Les émissions de zinc et de ses composés dans l'environnement peuvent être d'origine naturelle ou anthropique.
Les apports de zinc anthropique ont principalement pour origine :
- les activités industrielles qui émettent majoritairement dans les milieux aquatiques et les sols ;
- les bâtiments et mobiliers urbains et le trafic routier qui émettent principalement dans l'atmosphère et dans les milieux aquatiques ;
- les activités agricoles (les épandages des fumiers et lisiers de bovins, porcins et de volailles ; les traitements phytosanitaires des cultures et notamment des vignes) qui émettent principalement vers les sols (ADEME-SOGREAH, 2007).
Le suivi du zinc émis depuis les industries dans l'environnement est régi par la réglementation française et européenne. Les émissions sont donc recensées dans l'environnement au niveau français par différents organismes et registres (Agences de l'eau, DRIRE, BASOL, IREP, IFEN, BRGM) et au niveau européen (E-PRTR (U27), FOREGS).
En France, les secteurs industriels de traitement des métaux sont des émetteurs importants de zinc et de ses composés. Pour ces secteurs, parmi tous les rejets, les rejets vers les milieux aquatiques sont les plus importants d'après l'IREP. Parmi les autres émissions, les processus de galvanisation et de zingage de l'acier génèrent des résidus riches en zinc. La fusion des ferrailles d'acier galvanisé produit des poussières contenant du zinc, d'après le site Galvazinc .
Ces secteurs sont cohérents avec les utilisations recensées et la présence ubiquitaire de zinc dans l'environnement hormis le secteur « pétrole et gaz » qui n'avait pas été identifié dans les utilisations. A ce jour, nous n'avons pas relié les émissions de ce secteur à une source de zinc clairement identifiée.
Une synthèse des rejets industriels français connus est proposée dans le Tableau 11 ci-après pour les trois compartiments environnementaux.
De plus, pour l'IREP comme pour l'E-PRTR, seuls les rejets supérieurs à un seuil donné sont soumis à déclaration (seuil défini substance par substance) ; de façon globale, les seuils appliqués par l'E-PRTR sont plus hauts que ceux appliqués par l'IREP. Les informations issues de ces deux bases de données ne peuvent donc pas être considérées comme exhaustives.
Tableau 11. Rejets industriels français du zinc et ses composés, d'après l'IREP.

En 2012, en France, les émissions vers le sol (environ 390 tonnes) et vers les eaux (environ 250 tonnes) sont plus importantes que celles vers l'air (environ 115 tonnes). En effet les émissions vers le sol et les eaux représentent respectivement environ 50 % et 30 % du total des émissions industrielles de zinc et de ses composés recensées par le registre IREP en France. La Figure 8 ci-dessous représente la répartition de ces émissions vers le sol, l'air et les eaux.
[47] Dans la base de l'IREP,une valeur d'émission vers l'air de 1 030 000 kg.an-1 a été donné par Tarnaise des Panneaux SAS. Cette valeur semble aberrante et a donc été exclue.

Figure 8. Répartition des rejets de zinc et de ses composés en 2012 d'après l'IREP.
La France a une place importante dans les émissions de zinc à l'échelle de l'Union Européenne. Les émissions vers le sol, l'eau et l'air représentaient respectivement 99 %, 9 % et 12 % du total des émissions déclarées dans l'UE (27) en 2011 d'après l'E-PRTR. Pour les émissions vers les sols, ce chiffre doit plus être vu comme un bon renseignement de la base de données de l'E-PRTR par la France, plutôt que comme un indicateur de l'importance des rejets.
Émissions atmosphériques
FTE 2015 Importer
En France, selon l'INS48 , les émissions de zinc, toutes sources confondues, en 2007 étaient réparties sur le territoire comme le montre la Figure 9 ci-après.
[48] Inventaire National Spatialisé : (consulté en mars 2014). http://90.83.82.201/ins-webapp/

Figure 9. Répartition des émissions de zinc en France en 2007, d'après l'INS.
Les départements ayant les émissions de zinc les plus importantes, sont le Nord, le Pas-de-Calais, les Ardennes, la Moselle, la Seine-Maritime, les Yvelines, la Seine-et-Marne, la Saône-et-Loire, la Loire, la Savoie, l'Isère, les Bouches-du-Rhône, la Gironde et les Landes.
Parmi les dix premiers émetteurs industriels français répertoriés par l'IREP, un est situé dans les Bouches-du-Rhône, un en Moselle, trois dans le Nord et un en Savoie, ce qui explique que ces départements enregistrent des émissions importantes de zinc.

Figure 10. Secteurs émettant du zinc en France en 2007, d'après l'INS.
Les deux secteurs émettant le plus de zinc en France en 2007 étaient les procédés de production (43 %) et la combustion dans l'industrie manufacturière (26 %).
Selon l'INS, les émissions totales de zinc vers l'atmosphère étaient en 2007 de 201 523 kg, tandis que les émissions industrielles de l'IREP étaient cette même année de 164 495 kg, soit environ 80 % des émissions de l'INS. Précisons que, pour le zinc, l'INS, ne tient pas compte des émissions liées au transport (L. Létinois, communication personnelle).
Selon le CITEPA, le zinc et ses composés sont principalement rejetés dans l'atmosphère par les sous-secteurs suivants (sous-secteurs prépondérants en 2011 pour la France métropolitaine) :
Ces mêmes données peuvent être présentées sous forme graphique (Figure 11).

Figure 11. Secteurs responsables des rejets atmosphériques de zinc et de ses composés, d'après les données du CITEPA.
Selon cette même source, les rejets atmosphériques de zinc en France ont atteint 441 tonnes en 2011. Ce chiffre représente une augmentation de 1,9 % par rapport à 2009 (rejets les plus bas enregistrés depuis 1990), ce qui est comparable avec les chiffres de l'IREP, pour ce qui est de la part industrielle. La diminution observée de 1990 à 2011 équivaut à -79,6 %.
Selon les chiffres publiés par le CITEPA, les rejets de zinc dus à l'industrie manufacturière ont diminué de 93 % entre 1990 et 2011. Ces émissions sont notamment dues à la métallurgie des métaux ferreux (57 % des émissions de l'industrie manufacturière en 2011). La baisse des émissions est due à la mise en place de techniques de réduction dans les aciéries électriques et à la fermeture d'un important site de métallurgie de métaux non ferreux en 2003. Les émissions de zinc du secteur routier proviennent d'une part de la remontée d'une partie de l'huile moteur dans la chambre de combustion et d'autre part de l'abrasion des routes, des pneus et des freins.
La Figure 12 ci-après montre les émissions de zinc dans l'air entre 1990 et 2012 selon différents secteurs.

Figure 12. Emissions de zinc dans l'air en France métropolitaine, en tonnes, d'après CITEPA.
- En France, d'après les données E-PRTR de l'année 2011, les secteurs industriels dont les émissions de zinc vers l'atmosphère sont les plus importants sont :
- Production de fonte et d'acier y compris en coulée continue (52,0 %) ;
- Fonderies de métaux ferreux (14,7 %) ;
- Centrales thermiques et autres installations de combustions (5,9 %) ;
- Production de métaux non-ferreux bruts à partir de minerais, de concentrés ou matériaux de récupération (5,7 %).
Notons que ces estimations de zinc vers le compartiment aérien varient d'une source à l'autre, néanmoins, cette variabilité est à mettre en regard avec l'importance des émissions de zinc vers l'atmosphère qui, selon IREP ne représentent que 15 % des émissions totales à l'environnement.
Émissions vers les eaux
FTE 2015 Importer
A L'ECHELLE DE LA FRANCE
Selon l'Agence de l'eau Seine Normandie (2009), l'origine du zinc dans la Seine à Poses (estuaire) en 2006 est :
- urbaine (65 %) ;
- naturelle (15 %) ;
- autre, dont industrielle (20 %).
D'après les données RSDE49 , près de 90 % des flux totaux de zinc proviennent des centrales thermiques de production d'électricité.
Selon le projet de recherche AMPERES (2009), le zinc fait partie des composés toujours détectés (c'est-à-dire dans plus de 90 % des cas) en entrée des STEP et en sortie de STEP (traitements secondaires). Suite à un traitement tertiaire, le zinc peut être éliminé (cf 5.1.6).
Les métaux représentent 82 % en masse du flux total de micropolluants et le zinc représente 5,5 % du flux total de micropolluants en entrée par équivalent habitant (médianes du flux total pour toutes les STEPs étudiées durant ce projet de recherche). En sortie de STEP, les métaux représentent 97,4 % en masse du flux total de micropolluants et le zinc représente 7 % du flux total de micropolluants par équivalent habitant.
Ce même projet, indique que le zinc est majoritairement adsorbé dans les eaux résiduaires brutes alors que ce même élément est majoritairement dissous dans les eaux résiduaires traitées.
Nous n'avons pas de précision sur le type de traitements utilisés dans les STEPs étudiées au cours de ce projet.
[49] Réduction des Substances Dangereuses dans l'Eau, consulté le 16 juin 2014.
L'IREP différencie les émissions directes dans l'eau de celles qui sont indirectes. Un rejet direct est défini comme un rejet isolé, après station d'épuration interne au site industriel ou directement dans le milieu naturel, un rejet indirect est défini comme un rejet raccordé à une station d'épuration extérieure à l'installation industrielle émettrice. Ces deux types de rejets sont explicités dans les paragraphes 3.3.1.1 et 3.3.1.2 ci-après.
Rejets directs
En France, en 2012, 169 établissements ont déclarés des rejets directs vers les eaux de zinc, ces rejets atteignaient 232 392 kg.an-1. Les rejets directs vers les eaux représentent environ 31 % des rejets totaux de zinc vers l'environnement et 93 % des rejets vers les eaux. Les 10 premiers émetteurs nationaux émettaient entre 3 300 et 58 400 kg.an-1. Ces 10 premiers émetteurs sont les STEP de plus de 100 000 habitants, la sidérurgie, métallurgie et coke et la chimie et parachimie et le traitement des déchets d'après l'IREP.
Il a été estimé aux Pays-Bas que les rejets de zinc dans les eaux de surface, dus aux toitures en zinc, étaient de l'ordre de 40 tonnes/an pour une surface d'environ 33 km2 . En France, les toitures en zinc sont essentiellement situées en région parisienne ; à Paris la surface de toitures en zinc est estimée à 5 km2 , on peut donc estimer que les rejets dus aux toitures sont de l'ordre de 6 tonnes/an en France.
Rejets indirects
Selon ces mêmes déclarations, les émissions dans l'eau de zinc et ses composés par rejets indirects atteignaient en France 17 688 kg.an-1 en 2012. Les rejets indirects vers les eaux représentent environ 2 % des rejets totaux de zinc vers l'environnement et 7 % des rejets vers les eaux Les 10 premiers émetteurs nationaux émettaient entre 140 et 12 600 kg.an-1. Les secteurs concernés sont la chimie et parachimie, le traitement des déchets, la mécanique et traitement de surface, et l'agro-alimentaire et boissons d'après l'IREP. Ces secteurs semblent cohérents avec ceux recensés précédemment en termes d'utilisation.
A L'ECHELLE DE L'UNION EUROPEENNE
En Europe, en 2011, selon l'E-PRTR, les principaux émetteurs (en termes de sources fixes couvertes par ce registre) sont l'Allemagne, la Pologne, le Royaume-Uni, la France et l'Italie. Ils représentent respectivement 17 % (293 tonnes), 14 % (245 tonnes), 10 % (173 tonnes), 9 % (166 tonnes) et 9 % (163 tonnes) des émissions industrielles européennes50 vers les milieux aquatiques.
[50] Les données européennes considérées ci-dessus sont issues des données provenant des 27 membres actuels de l'Union Européenne.
Selon cette même source, à l'échelle de l'UE 27, les sources ponctuelles les plus émettrices de zinc et de ses composés en 2011 correspondent aux stations de traitement des eaux résiduaires urbaines (48,2 %). Les autres sources ponctuelles majeures sont l'exploitation minière souterraine et les opérations connexes (14,4 %), la production de fonte et d'acier y compris en coulée continue (6,3 %), la production de pulpe à partir de bois ou d'autres matériaux fibreux similaires (5,4 %), les centrales thermiques et autres installations de combustion (4,1 %), la production à l'échelle industrielle de produits chimique inorganiques (3,4 %), la production à l'échelle industrielle de produits chimique organiques (3,4 %), la production de métaux non-ferreux bruts à partir de minerais, de concentrés et de matériaux de récupération (2,6 %) et la mise en décharge des déchets non dangereux (2 %).
Émissions vers les sols
FTE 2015 Importer
En France, les déclarations pour l'année 2012 indiquent que les émissions de zinc et ses composés atteignaient 390 850 kg.an-1, ce qui représente environ 52 % des émissions de zinc dans l'environnement. Les 10 premiers émetteurs nationaux émettaient entre 3 500 et 133 000 kg.an-151 . Ces 10 premiers émetteurs sont dans le secteurs de l'agroalimentaire et des boissons, du bois, du papier et du carton, du traitement des eaux usées (STEP de plus 100 000 habitants), des déchets et des traitements, d'après l'IREP.
En Europe, en 2011, d'après l'E-PRTR (2014), le principal émetteur est la France, qui représente 99 % (346 955 kg) des émissions industrielles européennes vers les sols. Le principal secteur est le traitement et la transformation de matières animales et végétales dans la production d'aliments et de boissons (78,7 %). Néanmoins, ce chiffre soit plutôt être lu comme un indicateur de remplissage de la base de données et non pas comme un indicateur de l'importance des rejets.
Selon l'ADEME52 et SOGREAH (2007), les apports annuels sur les sols agricoles en France de zinc et de ses composés sont estimés à environ 15 200 tonnes/an. Ils proviennent des
[51] Les rejets dans le sol repertoriés dans IREP sont issus des déchets traités en milieu terrestre (par exemple : épandage de boue, biodégradation de déchets liquides ou de boues dans les sols...) ou liés à des injections en profondeur (par exemple : injection des déchets pompables dans des puits, des dômes de sel ou des failles géologiques naturelles...). Les effluents d'élevage ne sont pas soumis à cette obligation. En cas d'épandage de boues industrielles, seules les substances n'ayant pas d'intérêt agronomique avéré pour les sols ou pour la nutrition des cultures (tels que métaux, substances dangereuses...) devront être déclarées, dès lors qu'elles sont rejetées en quantité supérieure aux seuils.
[52] (consulté en février 2014). http://www2.ademe.fr/servlet/KBaseShow?sort=-1&cid=96&m=3&catid=15725
traitements phytosanitaires (3 %, soit environ 462 tonnes en 2013, d'après le BNV-D53), des engrais minéraux (2 %), des déjections animales (78 %), des amendements calciques et magnésiens (1 %), des boues et composts (7 %) et des retombées atmosphériques (11 %). L'importance des déjections animales dans les émissions de zinc vers les sols agricoles est soulignée par la Commission Européenne (2008a).
D'après l'ADEME et SOGREAH (2010), l'utilisation du zinc dans les produits phytosanitaires est essentiellement vouée aux traitements des vignes (99 %), et minoritairement aux laitues, pommes de terre et tomates.
Pollutions historiques et accidentelles
FTE 2015 Importer
BASOL est une base de données française sur les sites et sols pollués ou potentiellement pollués appelant une action des pouvoirs publics, à titre préventif ou curatif. Le site internet de cette base de données permet d'effectuer des recherches par substance : la recherche (effectuée en mars 2014) des sites ou sols pollués (ou potentiellement pollués) par du zinc aboutit à un résultat de 367 localisations en France, dont :
- 19 sites traités et libres de toute restriction ;
- 224 sites traités avec surveillance et/ou restriction d'usage ;
- 51 sites en cours de travaux ;
- 64 sites en cours d'évaluation ;
- 9 sites mis en sécurité et devant faire l'objet d'un diagnostic ;
- 191 sites ayant abouti à un impact dans les eaux souterraines (teneurs anormales) ;
- 2 sites ayant abouti à l'arrêt d'un captage AEP54 .
La base de données BASOL recense 5 587 sites pour 26 types de polluants (pour donner un ordre d'idée, cinq fois moins de sites industriels sont recensés pour le cuivre).
[53] Banque nationale des ventes de produits phytopharmaceutiques par les Distributeurs agréés : (consulté en juin 2014). https://bnvd.ineris.fr
[54] Captage AEP : captage destiné à l'alimentation en eau potable.
Présence environnementale
Atmosphère
FTE 2015 Importer
Le zinc dans l'atmosphère est principalement lié aux aérosols. Le zinc gazeux compte pour moins de 1 % de la totalité du zinc atmosphérique. Les particules de zinc trouvées dans l'air sont le sulfure de zinc, le phosphure de zinc, le chlorure de zinc et le zinc métallique (Commission Européenne, 2008a).
Aquatique
FTE 2015 Importer
Dans le milieu aquatique, un pH faible est nécessaire à la dissolution du zinc et ses composés dans les eaux. La solubilité du zinc, du triphosphate de zinc et de l'oxyde de zinc est nulle ou négligeable. La solubilité de sulfate de zinc et du chlorure de zinc dans l'eau douce est respectivement moyenne et forte. Le stockage dans les sédiments et l'adsorption sur les matières en suspension sont beaucoup plus importants dans l'eau douce que dans la mer. La volatilité du zinc et ses composés est négligeable.
Le chlorure de zinc, une fois rejeté dans l'environnement, se dissocie en cations Zn2+ et anion Cl-, en raison de sa grande solubilité dans l'eau. La spéciation du zinc (complexation, précipitation et sorption) dépend ensuite des conditions environnementales (Commission Européenne, 2008c).
Le zinc dans l'eau douce et l'eau de mer peut être présent sous forme dissoute ou en suspension. En eau douce, le zinc peut être divisé en plusieurs classes, comme par exemple des ions hydratés, des ions complexés sur des ligands organiques, du zinc adsorbé. La forme dominante des composés du zinc dans l'eau dépend du pH et du potentiel redox. L'adsorption sur des matières en suspension et dans les sédiments est aussi un facteur important du comportement du zinc dans le milieu aquatique (Commission Européenne, 2008a).
Dans l'Union européenne, les teneurs en zinc mesurées dans les cours d'eau sont comprises entre inférieure à 0,09 et 310 µg.L-1 avec une valeur médiane de 2,68 µg.L-1.

Figure 13. Distribution géographique du zinc dans les cours d'eau entre 1997 et 2001, d'après le FOREGS.
En France, on note une forte concentration en zinc dans les cours d'eau en Bretagne, le reste de la France présentant ces valeurs plus moyennes.
Les sédiments de la Seine (en amont du barrage de Poses) et de la Garonne (en amont de Bordeaux) ont été analysés, les teneurs minimum et maximum en zinc sont respectivement de 267 à 1 749 µg.L-1 et 167 à 1 013 µg.L-1 (IFEN, 2009).
Dans l'Union européenne, les teneurs en zinc dans les sédiments de la plaine alluviale varient entre 6 et 4 910 mg/kg avec une valeur médiane de 65 mg/kg.
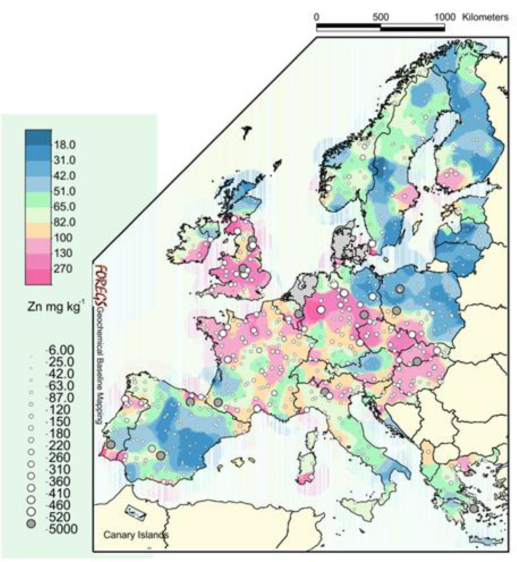
Figure 16. Distribution géographique du zinc dans les sédiments de la plaine alluviale entre 1997 et 2001, d'après le FOREGS.
En France, des concentrations importantes en zinc dans les sédiments de la plaine alluviale sont présentes dans le nord-ouest de la France.
Dans l'Union européenne, les teneurs en zinc dans les sédiments de cours d'eau varient entre 4 et 13 900 mg/kg avec une valeur médiane de 71 mg/kg.
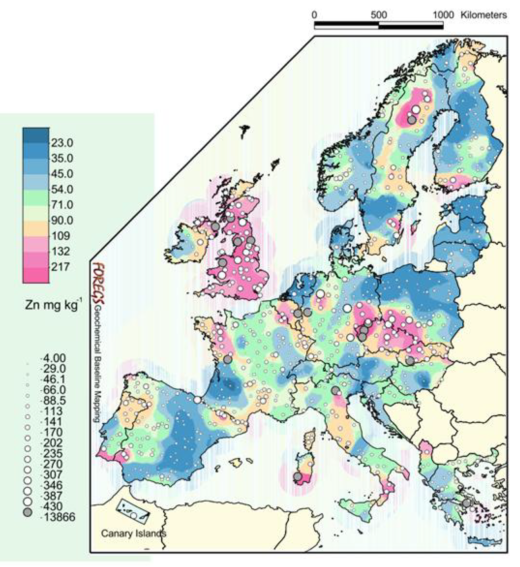
Figure 17. Distribution géographique du zinc dans les sédiments de cours d'eau entre 1997 et 2001, d'après le FOREGS.
Le sud-ouest de la France présentent une faible concentrations en zinc, tandis que la Bretagne présente la plus forte concentration en zinc française.
Terrestre
FTE 2015 Importer
Le zinc dans les sols est distribué entre différentes fractions :
- dissous dans les eaux interstitielles (ce qui inclut de nombreuses espèces) ;
- échangeable, lié à des particules du sol ;
- échangeable, lié à des ligands organiques (en petite partie dans la fraction dissoute et en grande partie dans la fraction solide) ;
- présent dans des minéraux argileux et des oxydes et hydroxydes métalliques ;
- présent dans des minéraux primaires.
Le zinc tend à être plus adsorbé à pH élevé qu'à faible pH. La solubilité du zinc dans les sols diminue avec le pH. La mobilité du zinc dans les sols dépend du degré d'adsorption et de paramètres tels que le pH (Commission Européenne, 2008a).
Dans l'Union européenne, les valeurs médianes des teneurs en zinc sont 47 et 52 mg/kg pour respectivement la couche profonde du sol et la couche superficielle. Les teneurs mesurées varient entre inférieure à 3 et 3 060 mg/kg pour la couche profonde du sol et inférieure à 3 et 2 900 mg/kg pour la couche superficielle.
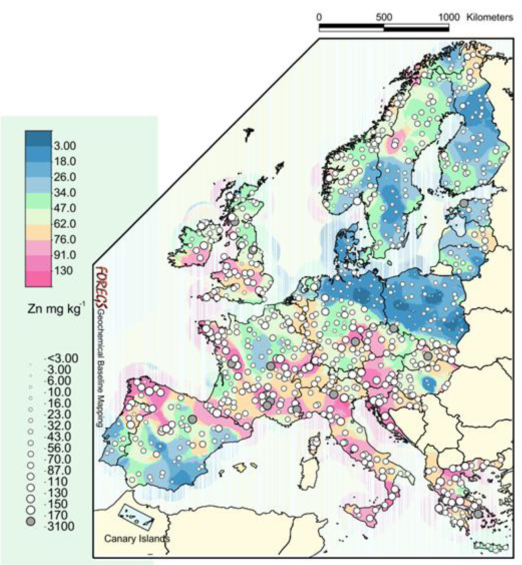
Figure 14. Distribution géographique du zinc dans la couche profonde du sol entre 1997 et 2001, d'après le FOREGS.
En France, des concentrations importantes en zinc dans la couche profonde du sol ont été relevées dans plusieurs régions : en Bretagne et dans le sud-est de la France.

Figure 15. Distribution géographique du zinc dans la couche superficielle du sol entre 1997 et 2001, d'après le FOREGS.
Des concentrations importantes en zinc en France ont été relévées dans le nord et l'est de la France, ainsi que d'une ligne allant de la Bretagne au sud-est de la France.
Perspectives de réduction
Réduction des rejets
REDUCTION DES EMISSIONS
FTE 2015 Importer
La réduction des émissions industrielles peut être réalisée par la valorisation et le recyclage des résidus et poussières, tels que la valorisation des poussières des aciéries électriques (Techniques de l'ingénieur, 2000), le traitement des résidus d'épuration de fumées d'incinération d'ordures ménagères (Pasquini, 2002), la valorisation de résidus riches en zinc et en sulfates (Roth et Bontemps, 2008) et le recyclage du zinc à partir d'acier galvanisé (Galvazinc Association, 2009).
A l'échelle mondiale, 40 % du zinc produit est issu d'une filière de recyclage. Sur la base d'estimations fondées sur des données historiques de consommation et les cycles de vie des produits, 60 % du zinc disponible pour le recyclage serait effectivement recyclé, d'après l'IZA (2011).
Le recyclage des métaux non ferreux (MNF) est une activité industrielle traditionnelle. Les métaux non ferreux recyclés sont Zn, Al, Cu, Pb et Ni. Ils sont issus des chutes de production, des chutes de l'industrie de transformation et des produits en fin de vie après collecte ou en premier traitement (sortie de l'incinération ou du 1er broyage). Il n'y a pas de différence entre le métal raffiné (produit à partir du minerai) et le métal affiné (métal secondaire) (Miquel, 1999).
Les produits de fin de vie représentent 50 % des ressources de MNF55 . La récupération de ces produits est organisée à travers une organisation professionnelle. Par exemple, le zinc de toiture est recyclé à hauteur de 95 % (Miquel, 1999).
La récupération fournit 37 % des besoins nationaux en MNF, 20 % correspondent à la récupération des produits en fin de vie. La production de minerai a disparu en France, l'importation ou la récupération sont les solutions actuelles de gestion des MNF. Le procédé de récupération du zinc permet d'économiser 90 % de l'énergie nécessaire à le produire à partir de minerai ce qui revient 3 à 4 fois moins cher (Miquel, 1999).
[55] MNF: Métaux Non Ferreux.
RECYCLAGE DES CHUTES DE PRODUCTION DE LA FILIERE HYDRO-METALLURGIQUE, VALORISATION DE RESIDUS RICHES EN ZINC ET EN SULFATES
Plusieurs procédés dont certains brevetés (US4, 072,503 ; WO2005/005674 et WO2002/068700) décrivent les techniques de traitement et de valorisation des résidus issus de l'extraction hydro-métallurgique du zinc. Ces procédés sont différents mais le principe général est proche. Il comprend, soit une étape de désulfuration par oxydation des sulfures en sulfates puis une réduction des oxydes par un réducteur carboné ; soit une réduction par un réducteur carboné suivie d'une fusion oxydante. Les produits résultant sont la fonte, le laitier (contenant du fer), un mélange d'oxydes contenant des métaux Zn, Pb, Ag, In, Ge, Ga et des fumées formées par des particules et des gaz. Les produits valorisables sont la fonte, le laitier stable et inerte utilisable dans la fabrication des ciments ou comme ballast et le mélange d'oxydes.
Le procédé développé par Roth and Bontemps (2008), a l'avantage de recycler quasiment l'intégralité des résidus. Le zinc et le fer sont recyclés, répondant ainsi aux exigences environnementales et aux exigences économiques pour la valorisation des métaux non ferreux.
RECYCLAGE DU ZINC A PARTIR D'ACIER GALVANISE
Les filières concernées sont le recyclage des ferrailles d'acier galvanisé et des résidus de galvanisation.
Dans la filière des ferrailles d'acier galvanisé, les produits proviennent des chutes de production et des ferrailles en fin de vie (automobiles, réfrigérateurs,). Les produits qui arrivent en fin de vie et/ou de conception obsolète et ne sont pas corrodés, sont alors recyclés.
Dans la filière de la galvanisation, les résidus sont les mattes de galvanisation (produites par la réaction du zinc avec l'acier) et les cendres écumées en surfaces des bains de galvanisation (produit par oxydation du zinc au cours du processus). Ces résidus de procédé sont actuellement recyclés (Galvazinc Association, 2009).
L'acier et le zinc combinés dans l'acier galvanisé et les tôles d'acier électro-zinguées sont des matériaux séparables de par l'importante volatilité du zinc. Le zinc est alors récupéré dans les poussières de cheminée d'un four électrique (Galvazinc Association, 2009).
VALORISATION DE POUSSIERES DES ACIERIES ELECTRIQUES
Selon les Techniques de l'ingénieur (2000), les aciéries européennes émettent 600 000 tonnes de poussières d'acier qui comprennent 20 à 25 % de zinc, 5 % de plomb, 20 à 25 % de fer, 5 % de sels et de la chaux. Les métaux sont sous forme d'oxydes et de ferrites. Afin d'éviter l'enfouissement de ces poussières en tant que déchets ultimes, deux procédés de recyclage ont été conçus. Ils permettent de séparer le zinc, le plomb et le résidu du traitement. Le traitement nommé EZINEX est développé par Engitec56 Inpianti. Le traitement nommé REZEDA a été développé par le groupe Usinor (aujourd'hui Arcelor-Mittal). Les deux procédés de traitements ont quelques différences mais ils ont le même principe de conception, ils sont tout les deux constitués des 3 étapes suivantes : la lixiviation des poussières, la cémentation et l'électrolyse.
Selon les Techniques de l'ingénieur (2000), les deux procédés sont rentables et concurrentiels, ils recyclent la solution appauvrie issue de l'électrolyse et produisent du cément de plomb, de la poudre de zinc et des cathodes de zinc massif.
TRAITEMENT DES RESIDUS D'EPURATION DE FUMEES D'INCINERATION D'ORDURES MENAGERES
Une tonne d'ordures ménagères génère 200 à 250 kg de mâchefer, environ 30 kg de cendres volantes nommées REFIOM (Résidus d'Epuration des Fumées d'Incinération d'Ordures Ménagères). Ces REFIOM sont collectés au niveau de la filtration des gaz et sont riches en éléments métalliques tels que le mercure, le plomb, le cadmium ou encore le zinc. En raison de leur dangerosité, ces résidus doivent être stabilisés et enfouis dans les CET57 appropriés. La vitrification est une des méthodes de stabilisation permettant de limiter la lixiviation des métaux toxiques dans l'environnement. D'après l'ADEME (2010b), les autres techniques de stabilisation des REFIOM sont la solidification à base de liants hydrauliques (ciments, chaux) et l'encapsulation qui enveloppe le déchet afin qu'il soit imperméable et chimiquement inerte vis-à-vis de l'extérieur (PVC, PET, bitume…).
Un procédé breveté (EP 0 779 082 A1) permet d'augmenter ou de diminuer le taux de métaux lourd dont le zinc dans le vitrifiat. Dans le premier cas, le vitrifiat enrichi en métaux permet de limiter la quantité de déchets ultimes lors du traitement total des REFIOM à moins de 1 % du total des déchets. L'autre cas peut amener à la production d'un vitrifiat appauvri en éléments métalliques et un solide valorisable dans le secteur métallurgique. Ce solide est assimilable à un minerai riche en métaux valorisables en pyrométallurgie ou en hydrométallurgie. Dans le premier cas, le vitrifiat obtenu contient 0,2 % de zinc au lieu de 2,3 % sans ajout de carbone (Pasquini, 2002).
[56] (
[57] CET : Centre d'Enfouissement Technique.
ELIMINATION DU ZINC DANS LES FUMEES
Dans l'atmosphère, le zinc est essentiellement sous forme particulaire. D'après un fabricant d'installations de traitement des fumées, l'épuration des poussières (PM 2,558) dans les fumées est d'environ 40 %.
Suite à la filtration par des filtres à manche et des électrofiltres, les poussières sont récupérées et valorisées.
ELIMINATION DU ZINC DANS LES EFFLUENTS
Le zinc est recherché dans le cadre du projet AMPERES59 . Il a été quantifié dans plus de 90 % des eaux usées brutes étudiées. Les concentrations moyennes en zinc varient entre 100 et 1 000 µg.L-1. Le zinc a été quantifié dans plus de 70 % des eaux traitées secondaires à des concentrations comprises entre 10 et 100 µg.L-1 et dans plus 70 % des eaux traitées tertiaires à des concentrations comprises entre 10 et 100 µg.L-1 (Coquery, 2011).
Au cours du passage en STEP, plusieurs substances sont retenues sous forme particulaire et transférées dans les boues. Le zinc est quantifié dans plus de 70 % des boues à des concentrations comprise entre 100 et 1 000 mg/kg (Coquery, 2011).
Deux rendements sont disponibles :
- le rendement de la filière eau traduit la diminution de la concentration entre l'entrée et la sortie de la STEP : il est en moyenne de 57 % pour le zinc ;
- le rendement d'élimination global prend en compte le flux de micropolluants transférés vers la filière boues et le flux de micropolluants réintroduits dans la filière eau par le retour en tête. Ce rendement permet d'évaluer si la substance est transformer ou simplement stocké dans les boues : il est inférieur à 30 % pour le zinc (Choubert, 2011).
CONCLUSIONS SUR LES DEMARCHES DE RECYCLAGE DU ZINC METAL
Ces démarches de recyclage du zinc métal semblent déjà bien installées au niveau français. A partir de nos informations il est difficile de savoir si l'intensification de cette approche permettrait une diminution significative des rejets de zinc dans l'environnement.
[58] Particules dont le diamètre est inférieur à 2,5 µm.
[59] Analyse de micropolluants prioritaires et émergents dans les rejets et les eaux superficielles.
Alternatives aux usages
ALTERNATIVES AUX USAGES
FTE 2015 Importer
DIFFICULTE DE LA SUBSTITUTION
Pour les applications actuelles, le zinc n'est pas concurrencé par d'autres matériaux (Techniques de l'ingénieur, 1988). Nous n'avons pas trouvé mention d'alternatives au zinc et à ses composés pour les principaux secteurs d'application. Notons que, pour certaines applications, le zinc est déjà employé en tant que substitut à d'autres composés chimiques. Par exemple, dans le secteur du traitement de surface, le zinc-nickel alcalin sans acide60 est une alternative performante à l'usage du Chrome VI dans les passivations bichromatées. Ce procédé va de pair avec l'élimination du PFOS61 dans les bains de placage de métaux tel que le chrome hexavalent (Commission Européenne, 2005).
L'évolution du parc automobile vers des voitures électriques favoriserait l'utilisation des batteries en zinc plus performantes que les systèmes actuels au plomb (CNUCED, 2009).
Dans le secteur de l'informatique, l'utilisation de batteries « zinc-air » remplace progressivement les piles à mercure. Outre la substitution du mercure, ces batteries permettraient une meilleure autonomie. De plus, elles ont l'avantage d'être recyclables sans perte de leurs qualités chimiques et physiques (CNUCED, 2009).
PISTES DE REDUCTION DES EMISSIONS
Les produits phytosanitaires
Le Tableau 13 ci–après présente la liste des produits phytosanitaires contenant du zinc, leurs applications et le nombre de leurs possibles substances de substitution.
[60] Le zinc-nickel alcalin sans acide est un revêtement électrolytique de zinc allié à du nickel à hauteur de 12 à 15%.
[61] Le PFOS ou le SPFO est le sulfonate de perfluorooctane.
Tableau 13. Liste des produits phytosanitaires contenant du zinc, leurs applications et le nombre de leurs possibles substances de substitution (ACTA, 2014; E-phy, 2014).

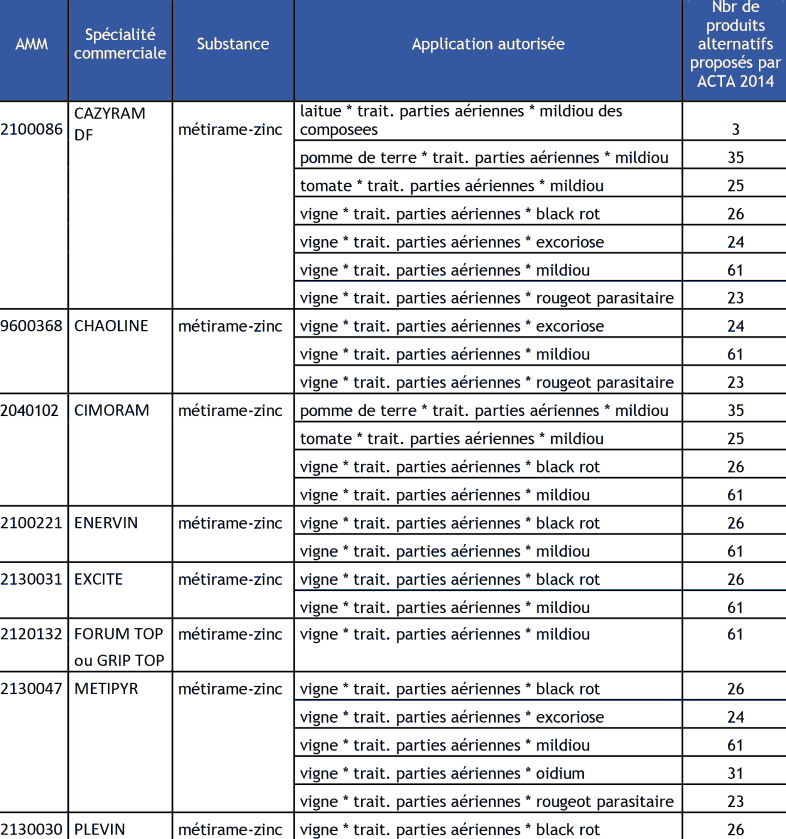

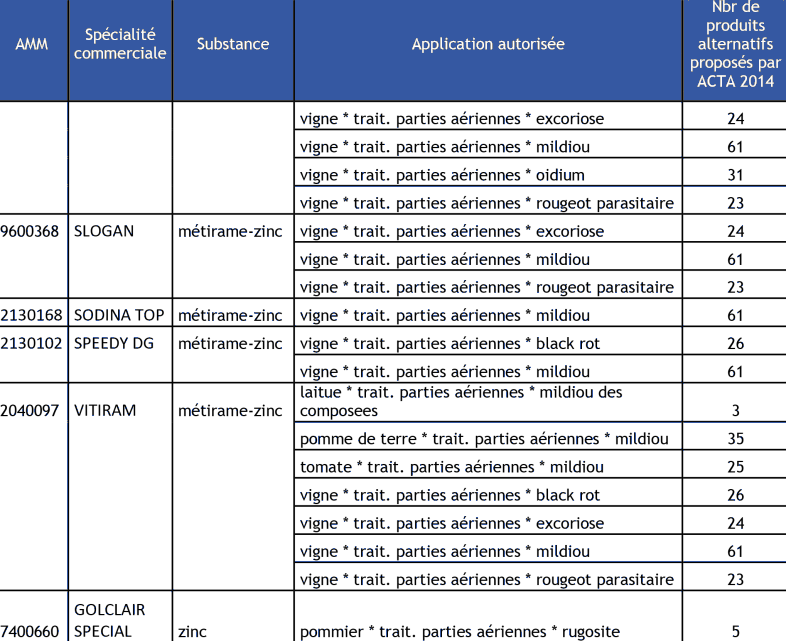
D'après ACTA (2014), de nombreuses substitutions sont possibles quant à l'usage du zinc en tant que substance active de produits phytosanitaires ou en tant qu'additif. Sans porter de jugement sur la portée agronomique de ces alternatives, notons que des substituts sans zinc sont identifiés pour les toutes les applications citées dans le Tableau 13.
Les toitures
Le zinc est utilisé dans les toitures pour le revêtement complet ou partiel par la jonction de tôle de zinc.
Le remplacement du zinc par un autre métal est une solution alternative coûteuse. En effet, la réalisation d'une toiture neuve avec un recouvrement de toiture en cuivre reviendrait à 120 €/m2 alors qu'un un recouvrement de toiture en zinc reviendrait à environ 90 €/m2 . De plus, le cuivre fait aussi l'objet de l'action de réduction des substances dangereuses dans l'eau dite RSDE (notons qu'une fiche technico-économique sur le cuivre est également disponible). Ce matériau est donc difficilement envisageable comme substituant au zinc.
Une autre solution rapportée pour substituer le zinc dans les toitures consiste en l'emploi d'autres matériaux non-métalliques tels que les bardeaux d'asphalte, de bois, de plastique et de fibres de verre, les tuiles traditionnelles, les tuiles de plastique, les tuiles de béton, … Mais certaines au moins de ces alternatives ont des inconvénients puisqu'elles ont recours à d'autres substances chimiques : HAP pour les asphaltes, additifs et monomères pour les plastiques, …
Les couvertures de toiture alternatives aux revêtements en zinc sont généralement moins chères que l'usage du zinc :
- tuiles de terre cuite (50 à 60 €/m2) ;
- les tuiles Sneldek (environ 30 €/m2)62 ;
- ...
Les lisiers animaux
Les lisiers animaux sont responsables d'une partie des apports diffus en zinc aux sols. Un contrôle plus strict des quantités de cet élément administré aux animaux en tant que supplément alimentaire pourrait être à étudier.
En effet, les lisiers animaux représentant près de 12 tonnes/an de zinc en France (cf. paragraphe 3.4), la mise en œuvre d'une telle mesure pourrait permettre le gain de plusieurs tonnes de rejet de zinc par an vers les sols.
Les chauffages individuels au bois
La consommation de bois libère le zinc contenu dans la biomasse par des fumées de combustion. La réduction de ces émissions peut donc s'envisager par le remplacement de ces systèmes de chauffage, notamment en privilégiant la combustion de bois non transformé(ADEME 2010a, DGEMP 2010).
[62] Les prix indicatifs de toitures et zingueries viennent du site : (consulté en mars 2014). http://www.livios.be/fr/etapes-de-construction/gros-oeuvre/toiture/prix-indicatifs-toiture/
Autres produits ou utilisation du zinc
Le chromate de zinc est utilisé dans la fabrication de peintures anticorrosion. D'après l'INRS (2011), il est possible de le substituer dans la plupart de ses applications. Les substituts envisagés sont :
- phosphates mixte de zinc-aluminium ;
- phosphate de zinc ;
- phosphate de calcium ;
- phosphate de magnésium ;
- molybdate de zinc ;
- ferrite de calcium…
Néanmoins de nombreux substituts possibles au chromate de zinc sont aussi des composés du zinc.
Le chlorure de zinc est utilisé comme agent de conservation pour le bois. D'après le TURI, le chlorure de zinc peut être substitué par l'acétate de cuivre, le carbonate de cuivre, le citrate de cuivre ou l'oxyde cuprique63 .
63
(consulté en juin 2014). http://www.turi.org/TURI_Publications/TURI_Chemical_Fact_Sheets/Arsenic_and_Arsenic_Compounds_Fact_Sheet/Arsenic_and_Arsenic_Compounds_Facts/Alternatives
Conclusion
FTE 2015 Importer
Le zinc et ses composés sont naturellement présents dans la croûte terrestre. Leur présence dans l'eau, le sol et l'air a également une origine anthropique.
Les secteurs d'activités principalement concernés sont la sidérurgie, la métallurgie et le coke. Les émissions sont majoritairement des émissions vers les sols (50 %) et des émissions vers les milieux aquatiques (30 %). Le secteur industriel de l'agroalimentaire et des boissons, et le secteur agricole (émissions dues aux déjections animales et à l'usage de produits phytosanitaires) sont émetteurs du zinc et de ses composés dans les sols. Les émissions dans l'eau sont principalement dues aux secteurs du traitement d'eau urbaine, la sidérurgie, la métallurgie et le coke, la chimie et la parachimie, les déchets et les traitements des déchets, la mécanique et les traitements de surfaces ; et au secteur du textile, habillement, teinture, impression et laverie. Les émissions vers l'air représentent environ 20 % des émissions totales et sont majoritairement dues à l'activité de la métallurgie des métaux ferreux. L'usure des toitures, des gouttières et des pneus contenant du zinc et la consommation de bois de chauffage induit également des émissions de zinc vers les eaux et vers l'air.
Nous n'avons pas identifié de substitut générique au zinc et à ses principaux composés pour leurs principaux secteurs d'utilisation. Néanmoins, des pistes alternatives sont disponibles pour un grand nombre de secteurs d'utilisation directs ou indirects de ces substances :
- Usages phytosanitaires ;
- Usages comme matériaux de couverture ;
- Combustion pour la production d'énergie ;
- …
D'autre part, des techniques de réduction des émissions industrielles existent, ce sont le traitement des effluents industriels aqueux, le recyclage des chutes de production de la filière hydro-métallurgique, la valorisation des résidus riches en zinc et en sulfates, le recyclage du zinc à partir d'acier galvanisé, la valorisation de poussières des aciéries électriques et le traitement des résidus d'épuration des fumées d'incinération d'ordures ménagères.
Bibliographie
Archives
Dernière vérification le 29/03/2024
Documents
Exporter la substance
Choisissez le format de l'export :










