Configuration de votre affichage
Vous avez activé le mode de configuration de l'affichage qui permet de sélectionner les informations que vous souhaitez afficher sur la fiche substance. Une fois que vous aurez sélectionné les rubriques à afficher, vous pouvez revenir au mode de consultation de la fiche substance en cliquant à nouveau sur le bouton de filtrage.
Jaune d'oxyde d'antimoine, de nickel (8007-18-9)
Informations générales
Dernière vérification le 29/03/2024
Identification
Numero CAS
8007-18-9
Nom scientifique (FR)
Jaune d'Oxyde d'Antimoine, de Nickel Et de Titane
Code EC
232-535-3
Code SANDRE
-
Numéro CIPAC
-
Formule chimique brute
\(\ce{ (Ti, Ni, Sb) O2 }\)
Familles
Familles chimiques
Physico-Chimie
Dernière vérification le 29/03/2024
Tableau des paramètres
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Bibliographie
Comportement et devenir dans les milieux
Dernière vérification le 29/03/2024
Persistance
Biodégradabilité
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Ecotoxicologie
Dernière vérification le 29/03/2024
Dangers
Valeurs de danger
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Bibliographie
Données technico-économiques
Dernière vérification le 29/03/2024
Introduction
FTE 2015 Importer
Le nickel est un métal, son numéro CAS est 7440-02-0. Les principaux composés du nickel, étudiés dans cette fiche, sont le nickel tétracarbonyle (CAS 13463-39-3), l'acétate de nickel (CAS 373-02-4), l'oxyde de nickel (CAS 1313-99-1), l'hydroxyde de nickel (CAS 12054-48-7), le carbonate de nickel (CAS 3333-67-3), le chlorure de nickel (CAS 7718-54-9), le nitrate de nickel (CAS 13138-45-9), le sulfure de nickel (CAS 12035-72-2) et le sulfate de nickel (CAS 7786-81-4).
Le nickel est un métal ubiquitaire, très répandu dans la croûte terrestre. Les sources de nickel sont à la fois naturelles et anthropiques. La majorité du nickel naturel provient des minerais.
Le nickel est utilisé dans de nombreux secteurs : les aciers inoxydables (contenant 8 à 12 % Ni), les alliages de nickel (contenant 25 à 100 % Ni), le traitement de surface (nickelage), les aciers alliés (contenant moins de 4 % Ni), les batteries (Cd-Ni, NiMH1), la monnaie, la chimie (catalyseur).
En France, la source principale de nickel dans l'environnement est une source anthropique, liée aux activités industrielles.
La production mondiale de nickel était, en 2011, de 1 897.103 tonnes de nickel, dont 58.103 tonnes dans l'Union européenne.
Les émissions françaises de nickel vers l'environnement sont répertoriées par différents organismes : le CITEPA pour les émissions atmosphériques, l'IREP et l'E-PRTR pour les données des industriels aux émissions atmosphériques, vers les eaux et les sols. Tous milieux confondus, selon E-PRTR, les émissions industrielles étaient d'environ 60 tonnes en 2011.
De nombreux sites industriels sont recensés comme contaminés ou ayant été contaminés au nickel, dans toutes les régions françaises, d'après la base de données BASOL.
Le nickel est présent sous forme d'ions Ni2+ dans les systèmes aquatiques. En présence de soufre et en milieu anaérobie, il se forme du sulfate de nickel. Dans les sols, la mobilité du nickel augmente aux pH faibles, en milieu alcalin, le nickel est majoritairement adsorbé. Le nickel, bien que pouvant parcourir de grandes distances via le compartiment atmosphérique, est peu présent dans les particules en suspension.
[1] Ni-Cd : Nickel-Cadmium, NiMH : Nickel Métal Hydrure.
Le nickel est à l'heure actuelle difficilement substituable. Des techniques de réductions des émissions industrielles existent pour les effluents aqueux, notamment dans les domaines de la chimie et des traitements de surface. Il existe aussi des techniques de réductions des émissions lors des opérations minières ou du traitement des minerais.
Nickel is a metal, its CAS number is 7440-02-0. The main compounds of nickel, which are studied in this sheet, are nickel tetracarbonyl (CAS 13462-39-3), nickel acetate (CAS 373-02-4), nickel oxide (CAS 1313-99-1), nickel hydroxide (CAS 771854-9), nickel chloride (CAS 7718-54-9), nickel nitrate (CAS 13138-45-9), nickel sulphide (CAS 12035-72-2) and nickel sulphate (CAS 7786-81-4).
Nickel is a ubiquitous metal, very common in the Earth's crust. Nickel sources are both natural and anthropogenic. Most of natural nickel comes from ores.
Nickel is used in many applications: stainless steels (containing 8 to 12% Ni), nickel alloys (containing 25 to 100% Ni), surface treatment (nickel plating), steel (containing less than 4% Ni), batteries (NiCd, NiMH2), mint, chemistry (catalyser).
In France, the main source of nickel in environment is an anthropogenic source, related to industries.
In 2011, the global production of nickel was 1897 thousand tons of nickel and 58 thousand tons for the European Union.
The French emissions of nickel to environment are registered by different organizations: the CITEPA for atmospheric emission, IREP and E-PRTR for emissions to atmosphere, water and soil. According to E-PRTR, industrial emissions were about 60 tons for all medias for 2011.
According to the database BASOL, many industrial sites are registered as polluted by nickel or having been polluted by nickel in all regions.
Nickel is present as ions Ni2+ in aquatic systems. With sulfur and in anaerobic conditions nickel sulfate is formed. In soil nickel mobility is greater at low pH. In alkaline environment nickel is mainly adsorbed. Even if nickel can travel on long distance via atmosphere, it is not very present in particles.
At the moment, nickel is hardly substitutable. Techniques exist to reduce industrial emissions in aqueous effluents, mainly in chemistry and surface treatment. There are techniques to reduce emissions during mining operations and ore treatment.
[2] NiCd: Nickel Cadmium, NiMH: Nickel –metal hydride.
FTE 2015 ImporterL'Antimoine, élément chimique n°51 de symbole (Sb) et de numéro CAS 7440-36-0, est un métalloïde ubiquitaire que l'on trouve généralement sous forme minérale de stibine (Sb2S3) dans la nature en relative faible abondance.
La Chine est le principal fournisseur mondial de minerais d'antimoine, extrait seul ou issu de la coproduction d'autres métaux, avec près de 75% d'un marché représentant environ 143 000 tonnes en 2016.
L'antimoine est rarement utilisé en tant que tel et subit généralement des transformations chimiques avant d'être réutilisé le plus souvent sous forme de trioxyde d'antimoine (Sb2O3) dont la Chine est aussi le principale fournisseur.
L'antimoine est utilisé dans une gamme très variée de produit textiles, plastiques, alliages métalliques. Il est principalement utilisé en tant que retardateur de flamme (≈45-60%) dans l'industrie plastique et textile. On le retrouve aussi en grande partie (≈30%) dans les batteries Plomb-acide bien qu'il s'agisse d'un usage en déclin. Enfin on le retrouve dans de multiples usages mineurs tel que la plasturgie des polymères, les munitions, l'électronique, les peintures et céramiques…
La plupart des rejets dans l'environnement sont majoritairement atmosphériques et d'origine anthropogénique, et sont associés aux exploitations minières, métallurgiques, à la combustion de charbon dans le secteur de l'énergie, l'abrasion des plaquettes de freins, à l'incinérations des déchets municipaux. Les rejets vers les sols et les milieux aquatiques proviennent des stations d'épuration et de l'ensemble du cycle de vie des produits et matériaux contenant de l'antimoine (plastiques, textiles, peintures, alliages métalliques, scories).
L'antimoine présente peu d'alternatives soutenables et sa demande est en constante augmentation alors que seule la filière des batteries Plomb-Antimoine valorise ses déchets à l'heure actuelle. Ainsi, rien ne laisse prévoir une réduction des émissions dans l'environnement à court ou moyen terme.
Antimony, a chemical element n°51 and CAS n°7440-36-0, is a ubiquitous metalloid mainly found under its mineral shape named stibnite (Sb2S3) in a relative low abundance.
Either retrieved alone or as a by product during others metals mining process, China is the main supplier of the world antimony ores market, representing a share of ≈75% out of an overall volume estimated around 143 000 tonnes in 2016.
Antimony is rarely consumed in its basic state and is usually undergoing chemical process. Its most common compound is Antimony Trioxide (Sb2O3) which is also mainly produced in China as well.
Antimony is employed in a wide variety of end-uses such as textiles, plastics or alloys. Its main application will be found in flamme-retardant market (≈45-60%) for plastics and textiles. Lead-acide batteries market do also request antimony accounting for ≈30% of global use, even though it is a declining market. Finally, antimony finds application in plenty other minor market such catalyst/heath-stabilizer for polymeres, ammunitions, electronics, painting and coating, ceramics…
Most of its release within the environment arises from anthropogenic sources polluting atmosphere linked to mining activities, metallurgy, coal combustion for energy purpose, brake wear, municipal waste incineration. Waters and Soils contamination occurs from sewage treatment plant and antimony containing products life-cycle as a whole (plastics, textiles, paints, alloys, slags).
Antimony does not exhibit much sustainable alternatives, its demand is not forecast to lower while only lead-antimony batteries sector performs effective recycling (≈90%), thus we do not expect antimony emissions to decline in the upcoming years.
Tableaux de synthèse
Généralités
| CAS | 8007-18-9 |
|---|---|
| Substance prioritaire dans le domaine de l’eau (DCE) | non |
| Substance soumise à autorisation dans Reach | non |
| Substance soumise à restriction dans Reach | non |
| Substance extrêmement préoccupante (SVHC) | non |
| Réglementations |
FTE 2015 Importer Textes générauxL'usage du nickel est interdit dans les (alliages pour) bijoux dans le cadre de REACH (Annexe XVII). Les composés du nickel ne sont pas actuellement dans la liste des SVHC de REACH, mais des analyses préliminaires sont en cours qui pourraient éventuellement conduire à leur inclusion future (notamment des études conduites en France par l'ANSES pour l'oxyde et le sulfate de Nickel). Le nickel et ses composés ne sont pas cités dans la liste de l'annexe I du règlement (CE) 689/2008 relatif à l'export et à l'import de substances dangereuses. Ils ne sont donc pas soumis aux notifications d'exportations. Certains composés du nickel étant carcinogènes (NiO), les dispositions générales relatives à ces composés, notamment en matière de protection des travailleurs, s'appliquent, et des limites spécifiques peuvent exister dans des règlementations nationales dans l'UE (voir 1.3.1 ci-dessous pour les valeurs limites en France). Nomenclature des Installations classées (IC)En France, le nickel est concerné par les rubriques suivantes de la Nomenclature des Installations Classées (selon le Décret n°53-578 du 20 mai 1953 relatif à la nomenclature des installations classées pour la protection de l'environnement, mis à jour par le Ministère de l'Ecologie et du Développement Durable)5 :
5La liste des rubriques mentionnée est indicative et ne se veut pas exhaustive. (consulté en décembre 2013). http://www.ineris.fr/aida/sites/default/files/gesdoc/30296/Nomenclature_octobre.pdf  -2565 : Revêtement métallique ou traitement (nettoyage, décapage, conversion, polissage, attaque chimique, etc.) de surface (métaux, matières plastiques, semi-conducteurs, etc.) par voie électrolytiques ou chimique. Seuils de rejets pour les installations classéesL'arrêté du 26 décembre 2012 modifiant l'arrêté du 31 janvier 2008 concerne le registre et la déclaration annuelle des émissions polluantes et des déchets. L'exploitant de l'installation doit déclarer ces rejets dès lors que les seuils d'émissions décrits dans l'annexe II de cet arrêté sont dépassés. Les seuils de rejets de nickel et ses composés (exprimés en tant que Ni) sont :
Le nombre d'établissements rejetant du nickel est donné au paragraphe 3.3. L'arrêté du 2 février 1998 relatif aux prélèvements et à la consommation d'eau ainsi qu'aux émissions de toute nature des installations classées pour la protection de l'environnement soumises à autorisation indique que : Pollution de l'air Rejets d'antimoine, chrome, cobalt, cuivre, étain, manganèse, nickel, vanadium et zinc, et de leurs composés : si le flux horaire total d'antimoine, chrome, cobalt, cuivre, étain, manganèse6 , nickel, vanadium, zinc6 et de leurs composés (gazeux et particulaires) dépasse 25 g/h, la valeur limite de concentration est de 5 mg.m-3 (exprimée en Sb+Cr+Co+Cu+Sn+Mn+Ni+V+Zn). Pollution des eaux superficielles Les rejets respectent les valeurs limites de concentrations suivantes : nickel et ses composés (en Ni) 0,5 mg.L-1 si le rejet dépasse 5 g.j-1. Dans le cas de la fabrication ou de la transformation de nickel, la valeur limite de concentration est 2 mg.L-1. Epandage des boues L'annexe I de l'arrêté précise les seuils à respecter en éléments-traces pour l'épandage des boues issues du traitement des eaux usées. Ces seuils sont présentés dans le Tableau 3. Le Tableau 3 précise les teneurs limites en éléments-traces dans les boues, les valeurs limites en éléments-traces dans les sols et le flux maximum en éléments-traces apporté par les déchets ou effluents pour les pâturages ou sols de pH inférieurs à 6. [6] En cas de fabrication de monoxyde de zinc (ZnO) et de bioxyde de manganèse (MnO2), la valeur limite de concentration pour respectivement le zinc et le manganèse est de 10 mg.m-3 . Tableau 3. Seuils de nickel applicables aux épandages de boues issues du traitement des eaux usées sur les sols agricoles.  Actions de recherche RSDELe nickel et ses composés sont cités dans l'annexe 1 de la circulaire du 5 janvier 2009 relative à la mise en œuvre de la 2ème phase de l'action RSDE pour les ICPE soumise à autorisation. Cette annexe regroupe les listes par secteurs d'activité industrielle des substances dangereuses. Le nickel et ses composés sont cités pour tous les secteurs d'activité. Le nickel appartient aussi à la liste des micropolluants à mesurer dans les stations de traitement des eaux usées traitant une charge brute de pollution supérieure ou égale à 600 kg DBO5/jour (Circulaire du 29 septembre 2010 relative à la surveillance de la présence [9] «PM 10»: particules en suspension dont le diamètre aérodynamique est inférieur à 10 µm. [10] Conditions ambiantes: température de 25°C et pression de 100 kPa. de micropolluants dans les eaux rejetées au milieu naturel par les stations de traitement des eaux usées). Directive-Cadre sur l'EauLe nickel et ses composés sont cités dans la directive n°2013/39/UE du 12 août 2013 modifiant les directives 2000/60/CE et 2008/105/CE en ce qui concerne les substances prioritaires pour la politique dans le domaine de l'eau. Ils sont listés en tant que substances prioritaires mais pas en tant que substances prioritaires dangereuses. La directive précédemment citée fixe des normes de qualité environnementale (NQE) pour le nickel et ses composés :
EngraisPour les engrais organiques, divers seuils en métaux lourds sont fixés par les législations européennes et nationales. Les seuils pour le nickel sont repris dans le Tableau 411 . [11] (consulté en février 2014). http://ec.europa.eu/enterprise/sectors/chemicals/files/fertilizers/annexes_16jan2012_en.pdf Tableau 4. Seuils de nickel pour les engrais organiques.  Pour les engrais minéraux, il n'existe pas de règlementation européenne, néanmoins l'évaluation du règlement CE 2003/2003 relatif aux engrais14 préconise d'inclure dans le règlement des dispositions concernant les teneurs maximales en métaux lourds. NanoparticulesLe décret n° 2012-232 du 17 février 2012 relatif à la déclaration annuelle des substances à l'état nanoparticulaire précise que le seuil de la déclaration est fixé à 100 g/an pour la fabrication, l'importation ou la mise sur le marché de nanomatériaux. Autres textesLe nickel appartient à la liste des 823 substances du plan micropolluants 2010-201315 . [12] European Compost Network. [13] Joint Research Center. [14] (consulté en février 2014). http://ec.europa.eu/enterprise/sectors/chemicals/files/fertilizers/final_report_2010_en.pdf Le nickel est cité dans la liste des substances et matières nuisibles ou nocives dont le rejet dans la zone du protocole est assujetti à permis spécial. Il s'agit du protocole relatif à la protection de la mer Méditerranée contre la pollution résultant de l'exploration et de l'exploitation du plateau continental, du fond de la mer et de son sous-sol auquel l'Union européenne a adhéré par la décision n°2013/5/UE du 17 décembre 2012. Le nickel ne fait pas partie des substances potentiellement préoccupantes définies par OSPAR16 . FTE 2015 ImporterTEXTES GENERAUXREACHDans le cadre du règlement REACH concernant la mise sur le marché des substances chimiques1 , l'antimoine (Sb) et ses composées ne font pas à l'heure actuelle partie de la liste des substances soumises à restrictions quant à leurs fabrication, mise sur le marché et utilisations (Annexe XVII), ni de la liste des substances soumises à autorisation (Annexe XIV). Cependant, l'antimoniate de plomb (O7Pb2Sb2), aussi appelé « Jaune de Naples » est inscrit sur la liste des SVHC2 de REACH étant donné son caractère reprotoxique. De plus, l'antimoine et certains de ses composés, au vu des diverses sources de dangers reportées et ou suspectées par des entreprises auprès de l'ECHA, font partie du programme CoRAP (Community rolling action plan) et des investigations sont réalisées en 20183 par le BAuA (Institut fédéral de la sécurité et de la santé au travail allemand) en particulier sur l'antimoine (Sb), le trisulfure d'antimoine (SB2S3), le trioxyde de diantimoine (Sb2O3), le trichlorure d'antimoine (Cl3Sb). RÈGLEMENT (CE) 689/2008L'antimoine et ses composés ne figurent pas dans la liste des substances soumises aux notifications d'importations et d'exportations issue du règlement (CE) 689/2008 (Annexe I). [1] En application du Règlement (CE) n° 1907/2006 du 18/12/06 concernant l'enregistrement, l'évaluation et l'autorisation des substances chimiques, ainsi que les restrictions applicables à ces substances (REACH), instituant une agence européenne des produits chimiques [2] « Substances of Very High Concern”, candidates à une inscription sur la liste des substances soumises à autorisation. [3] Les résultats ne sont pas connus à la date de publication de cette fiche, ainsi on ne sait pas si cette évaluation peut déboucher à terme sur une inscription à la liste des SVHC. DIRECTIVE SUR LES EMISSIONS INDUSTRIELLESLa Directive relative aux émissions industrielles du 24 novembre 2010 (2010/75/UE) prolonge les actions menées par l'Europe en matière de contrôle et de réductions de la pollution émise par ces installations, et établit des valeurs limites par secteur industriel sur des rejets de substances avérées et ou soupçonnées d'être dangereuses pour l'homme et/ou son environnement. L'antimoine et ses composés font l'objet de plages de rejets associés aux Meilleures Techniques Disponibles 4 dans plusieurs secteurs (notamment installations d'incinération ou co-incinération des déchets, grandes installations de combustion, industrie des métaux non-ferreux…) Par exemple, dans le secteur de l'incinération, ces plages de rejets associées aux MTD sont les suivantes :
DIRECTIVE CADRE EAU (DCE)L'antimoine (Sb) ainsi que ses composées ne font pas partie de la liste des substances prioritaires. REGLEMENTATION D'USAGESRÉGLEMENTATION DES PRODUITS COSMÉTIQUESLa Réglementation européenne en matière de produit cosmétique s'appuyant sur le texte CE n°1223/2009 visant à assurer un niveau élevé de protection de la santé indique que l'antimoine et ses composés sont interdits dans la conception des produits cosmétiques. [4] L'ensemble des conclusions relatives aux Meilleures Techniques Disponibles est consultable sur https://aida.ineris.fr/guides/directive-ied/documents-bref REGLEMENTATION CONCERNANT LA MISE SUR LE MARCHE DES JOUETSConformément à la directive 2009/48/EC du 18 juin 2019 encadrant la sécurité relative à la mise en marché des jouets au sein de l'Union Européenne, les acteurs de la filière sont tenus de respecter des limites de migration pour les jouets et leurs composants. Ces limites de migration sont les suivantes pour l'antimoine5 :
Ces valeurs limites ne s'appliquent pas aux jouets ou composants de jouets qui, en raison de leur accessibilité, de leur fonction, de leur volume ou de leur masse, excluent tout danger par succion, léchage, ingestion ou contact prolongé avec la peau. REGLEMENTATION DES MATERIAUX PLASTIQUES EN CONTACT AVEC LES DENREES ALIMENTAIRESLe règlement européen (EU) N°10/2011 du 14 janvier 2011 établit un cadre concernant les matières plastiques, ainsi que les substances chimiques participant à leur composition, et leur entrée en contact avec les aliments. Or le trioxyde d'antimoine (Sb203), est utilisé en raison de ses propriétés ignifugeantes dans la fabrication de polymères et plus précisément de matières plastiques éventuellement destinées à entrer en contact avec des denrées alimentaires. Etant donné le danger du trioxyde d'antimoine6 celui-ci fait l'objet d'une valeur limite7 concernant la composition des matières plastiques entrant en contact avec les denrées alimentaires fixée à 0,04 mg/Kg. [5] Aucune précision sur les composés d'antimoine. [6] Voir la section CLP ainsi que la fiche INRS dont le trioxyde d'antimoine fait l'objet [7] Valeur limite de migration de la substance en mg vers la denrée alimentaire en Kg. REGLEMENTATION DES ADDITIFS ALIMENTAIRESLe règlement européen (EU) No 231/2012 du 9 Mars 2012 établit un cadre légal concernant l'utilisation d'additifs alimentaires. Ainsi, des limites spécifiques visant l'antimoine s'appliquent dans certains additifs :
REGLEMENTATION DU TRANSPORT DES DECHETSLe règlement européen (CE) N°1013/2006 du 14 juin 2006 encadrant le transfert des déchets à risque et notamment en dehors de la communauté européenne s'inscrit dans la lignée de la Convention de Bâle du 22 mars 1989. Dans cet effort de contrôler les flux de déchets dangereux et d'en protéger les pays en développement n'ayant les moyens de les valoriser, des procédures de notifications et de restrictions ont été établies. Ainsi les déchets contenant de l'antimoine et ses composés sont interdits à l'exportation (article 36 et Annexe VIII convention de Bâle) 8 . |
| Valeurs et normes appliquées en France |
FTE 2015 Importer Valeurs utilisées en milieu de travailEn France, les valeurs utilisées pour la qualité de l'air en milieu de travail sont publiées par l'INRS7 : VME8 = 1 mg.m -3 (en Ni) pour le nickel (métal et grillage de mattes), l'oxyde de nickel, l'hydroxyde de nickel, le carbonate de nickel et le sulfure de nickel. -3 VME = 0,12 mg.m (en Ni) pour le tétracarbonyle de nickel. [7] INRS 2012 – Valeurs limites d'exposition professionnelle aux agents chimiques en France (consulté en décembre 2013). [8] VME : valeurs moyennes d'exposition. Valeurs utilisées pour la population généraleQualité de l'air Le décret 2010-1250 du 21 octobre 2010 relatif à la qualité de l'air fixe pour le nickel une valeur cible de 20 ng.m-3 de nickel en moyenne calculée sur une année civile du contenu total de la fraction « PM 109 », avec un volume d'échantillonnage mesuré dans les conditions ambiantes10 . Cette valeur est la même que celle de la règlementation européenne correspondante. Qualité des eaux de consommation Le décret 2001/1220 du 20 décembre 2001 impose, de même qua la règlementation européenne correspondante, une limite de qualité aux eaux destinées à la consommation humaine. Les eaux doivent respecter une valeur inférieure ou égale à 20 µg.L-1 de nickel. Contact avec la peau L'annexe XVII « Restrictions applicables à la fabrication, à la mise sur le marché et à l'utilisation de certaines substances dangereuses et de certaines mélanges et articles dangereux » du règlement européen REACH impose des restrictions l'usage de nickel ou ses composés pour la fabrication de produits ayant un contact prolongé avec la peau. Ainsi les boucles d'oreilles et les piercings ne doivent pas entraîner des transferts dans l'organisme supérieurs à 0,2 µg.cm -2 par semaine. Les bijoux (y compris les montres), les fermetures éclairs, les boutons et rivets métalliques destinés à l'habillement sont interdits s'ils entraînent des transferts supérieurs à 0,5 µg.cm -2 par semaine. L'oxyde de nickel est interdit dans les cosmétiques par la règlementation européenne de ce secteur. FTE 2015 ImporterNOMENCLATURE DES INSTALLATIONS CLASSEESL'antimoine est concerné par des textes, notamment pour les rubriques suivantes de la Nomenclature des Installations Classées9 :
[8] A l'exception des débris métalliques (y compris alliages), propres, non contaminés, sous forme de produits finis (feuilles, tôles, poutrelles, fil machine, etc.) et sur dérogation suite à l'étude d'un dossier. [9] Mise à jour par le Ministère de l'Ecologie et du Développement Durable, version consultée en décembre 2018. SEUILS DE REJETS POUR LES INSTALLATIONS CLASSEES ET EXPLOITANTS DE STATION D'EPURATION D'EAUX URBAINES.L'antimoine et ses composés sont visés par l'arrêté du 26 décembre 2012 modifiant l'arrêté du 31 janvier 2008 concernant le registre et la déclaration annuelle des émissions polluantes et des déchets en provenance des installations classées pour la protection de l'environnement et exploitants de station d'épuration d'eaux urbaines. L'exploitant d'une installation définie dans l'annexe I doit déclarer ses rejets lorsque ceux-ci dépassent le seuil indiqué dans l'annexe II soit :
Pour les installations d'incinération de déchets non dangereux et les installations d'incinération de déchets dangereux, ce seuil est fixé à 0. L'arrêté du 14 février 2007 fixe une valeur limite s'appliquant aux rejets d'antimoine et ses composés dans les eaux naturelles ou dans un réseau d'assainissement collectif urbain en provenance des installations classées relatives au travail chimique du verre (rubrique n° 2531). Celles-ci doivent respecter une valeur limite de concentration de 0,3 mg.l-110 . L'arrêté du 2 février 1998 relatif aux prélèvements et à la consommation d'eau ainsi qu'aux émissions de toute nature des installations classées pour la protection de l'environnement soumises à autorisation indique que l'exploitant prend toutes les dispositions nécessaires dans la conception et l'exploitation des installations pour réduire la pollution de l'air à la source. Les seuils suivants s'appliquent :
Les émissions directes ou indirectes d'antimoine et de ses composés sont interdites dans les eaux souterraines, à l'exception de celles dues à la réinjection dans leur nappe d'origine d'eaux à usage géothermique, d'eaux d'exhaure des carrières et des mines ou d'eaux pompées lors de certains travaux de génie civil, conformément aux dispositions de l'arrêté ministériel du 10 juillet 1990 modifié. Cette interdiction ne s'applique pas aux eaux pluviales. [10] Moyenne quotidienne, de plus aucune valeur instantanée ne doit dépasser le double des valeurs limites de concentration. NORMES ET VALEURS APPLIQUEES A LA QUALITE DES EAUXComme développé précédemment, l'antimoine ne faisant pas partie de la liste des substances prioritaires pour la qualité de l'eau, aucune Norme de Qualité Environnementale n'est disponible pour l'eau. L'INERIS publie des Valeurs-guide environnementales (VGE) pour la qualité de l'eau : Tableau 2 : Valeurs Guide Environnementale (INERIS) 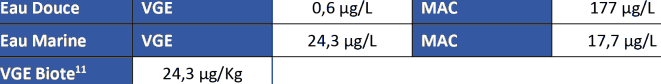 VGE = Valeur Guide Environnementale MAC = Concentration maximale Acceptable dans l'Eau NORMES ET VALEURS APPLIQUEES EN EAU POTABLELes concentrations limites pour les eaux destinées à la consommation humaine sont issues de l'arrêté du 11/01/07 relatif aux limites et références de qualité des eaux brutes et des eaux destinées à la consommation humaine12 . Pour l'antimoine, la limite de qualité des eaux destinées à la consommation humaine est de 5 µg.L-1. VALEURS UTILISEES DANS LE CADRE PROFESSIONNELEn France, l'Institut national de recherche et de sécurité pour la prévention des accidents du travail et des maladies professionnelles (INRS) publie des valeurs limites d'exposition professionnelles, celles qui concernent des composés de l'antimoine figurent dans le Tableau 3 : [11] Fondée sur la proposition de norme de qualité pour la santé humaine via la consommation de produits de la pêche. [12] Arrêté du 11/01/07 relatif aux limites et références de qualité des eaux brutes et des eauxdestinées à la consommation humaine mentionnées aux articles R. 1321-2, R. 1321-3, R. 1321-7 et R.1321-38 du code de la santé publique Tableau 3 : Valeurs limites professionnelles d'expostion 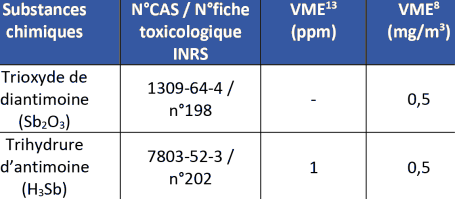 AUTRES TEXTESMICROPOLLUANTS ET CONTROLE DE LA QUALITE DES EAUXDans le cadre de l'application de la directive européenne cadre sur l'eau (DCE) et des réglementations et efforts européens de contrôle des polluants qui ont suivi, la France planifie au travers du code de l'environnement le contrôle de la qualité des eaux (article L212-2). L'antimoine fait partie de la liste des substances pertinentes à surveiller dans les eaux de surface et souterraines (Arrêté du 7 août 2015 modifiant R. 212-22). De plus, L'antimoine fait partie de la liste initiale des substances pertinentes à surveiller dans le cadre de la circulaire 29/09/10 relative à la surveillance de la présence de micropolluants dans les eaux rejetées au milieu naturel par les stations de traitement des eaux usées (STEU). Il n'est pas retenu dans la note technique sur les STEU (12/08/16) prise dans le cadre de l'action de recherche RSDE. CONVENTION DE BARCELONEDans le cadre de la convention de Barcelone, la directive n°2013/5/UE du 17 décembre 2012 fixe un cap pour la protection du milieu marin et du littoral de la Méditerranée contre la pollution résultant de l'exploration et de l'exploitation du plateau continental, du fond de la mer et de son sous-sol. A ce titre, l'antimoine est inscrit à la liste des substances et matières nuisibles ou nocives dont le rejet dans la zone du protocole est assujetti à permis spécial. [13] VME = Valeur moyennes d'exposition RÈGLEMENTATION AUX ETATS UNISL'antimoine fait partie de la liste des substances prioritaires de l'ATSDR14 (Agency for Toxic Substances and Disease Registry). L'antimoine et ses composés fait également partie de la liste des 188 substances toxiques ou fortement soupçonnées de la section 112 du CAA (Clean Air Act) émise par l'EPA (Agence pour l'Environnement aux Etats-Unis). CLASSIFICATION ET ETIQUETAGEDans le cadre d'une réglementation européenne commune des substances chimiques, le règlement CLP (Classification, Labelling & Packaging) établit la réglementation relative à la classification, à l'étiquetage et à l'emballage des substances chimiques qui s'appuie sur le système GHS15 des nations unies. Celui-ci est régulièrement mis à jour par l'ECHA à partir du travail conjoint des industriels de la chimie et des institutions de contrôle, la dernière version en date étant le règlement (UE) 2018/669 du 16 avril 2018. L'Antimoine et certains de ses composés faisant partie du CoRAP en raison des risques qu'ils représentent, et faisant l'objet de notifications auprès de l'ECHA, les informations relatives à leur classification CLP produites ci-dessous en l'état actuel des connaissances sont probablement amenées à changer dans les années à venir. Les libellés des codes de risque associés à l'antimoine et ses composés figurent dans le tableau 4 sur la page suivante. [14] https://www.atsdr.cdc.gov/spl/resources/1992_atsdr_substance_priority_list.html [15] GHS = Globally Harmonized System of Classification and Labelling of Chemicals Tableau 4 : Descriptif des mentions de dangers liées à l'antimoine et ses composés  ANTIMOINEL'antimoine (Sb) n'est pas dans le règlement CLP mais à l'étude (CoRAP). En attendant les recommandations en matière de CLP suivantes sont suggérées par la communauté européenne au travers de notifications (nombre de notifications reçues mentionnées dans le dossier CoRAP entre parenthèses) :  H300 (28), H301 (22), H302 (137), H332 (155), H310 (28), H335 (3), H373 (17), H351 (70), H411 (176) TRISULFURE D'ANTIMOINELe trisulfure d'antimoine (SB2S3) n'est pas dans le règlement CLP mais à l'étude (CoRAP). En attendant les recommandations en matière de CLP suivantes sont suggérées par la communauté européenne au travers de notifications (nombre de notifications reçues mentionnées dans le dossier CoRAP entre parenthèses) :  H302 (149), H315 (1), H319 (1), H332 (149), H335 (1), H351 (6), TRIOXYDE DE DIANTIMOINELe trioxyde de diantimoine (Sb2O3), est inclus dans le règlement CLP pour les mentions suivantes :  Classification : H351 De plus, il fait l'objet d'un dossier CoRAP mentionnant les dangers suivants : H302, H318, H315, H319, H332, H360D, H372, H373, H412 TRIHYDRURE D'ANTIMOINELe trihydrure d'antimoine (H3Sb) ne fait pas partie à part entière du règlement CLP, cependant il est inclus dans la catégorie des composés de l'antimoine dans ce règlement et à ce titre les mentions de risque minimales suivantes s'appliquent en attendant des recherches supplémentaires (Fiche toxicologique 202 INRS) :  Classification : H302, H332, H411 Il est aussi concerné par le même dossier CoRAP que l'antimoine (Sb). TRICHLORURE D'ANTIMOINELe trichlorure d'antimoine (Cl3Sb) fait partie du règlement CLP qui lui attribue les mentions de danger suivantes :  Classification : H314, H411 Il fait l'objet d'un dossier CoRAP mentionnant les dangers additionnels suivant notifiés par les industriels : H318, H335, H341, H350 ANTIMONIATE DE PLOMB OU « JAUNE DE NAPLES »L'antimoniate de plomb (O7Pb2Sb2), Pigment Yellow 41 ou antimony lead yellow (« Jaune de Naples ») ne fait pas partie à part entière du règlement CLP, cependant il est inclus dans la catégorie des composés de l'antimoine dans ce règlement et à ce titre les mentions de risque minimales suivantes s'appliquent en attendant des recherches supplémentaires :  Classification : H302, H332, H411 On rappelle qu'il est inscrit à la liste SVHC de Reach et notamment au motif de son danger potentiel pour la reproduction (Repr. 1A) : H360D CHLORURE D'OXYDE D'ANTIMOINELe chlorure d'oxyde d'antimoine (Sb4Cl2O5) ne fait pas partie à part entière du règlement CLP, cependant il est inclus dans la catégorie des composés de l'antimoine dans ce règlement et à ce titre les mentions de risque minimales suivantes s'appliquent en attendant des recherches supplémentaires :  Classification : H302, H332, H411 ARSENIATE D'ANTIMOINEL'arseniate d'antimoine (AsO4Sb) ne fait pas partie à part entière du règlement CLP, cependant il est inclus dans la catégorie des composés de l'antimoine ainsi que de l'arsenic dans ce règlement et à ce titre les mentions de risque minimales suivantes s'appliquent en attendant des recherches supplémentaires :  Classification : H301, H302, H331, H332, H400, H410, H411 JAUNE TITANATE NICKEL ANTIMOINELe jaune titanate nickel antimoine (Ti, Ni, Sb) O2 ou Pigment Yellow 53 ne fait pas partie à part entière du règlement CLP, cependant il est inclus dans la catégorie des composés de l'antimoine dans ce règlement et à ce titre les mentions de risque minimales suivantes s'appliquent en attendant des recherches supplémentaires :  Classification : H302, H332, H411 PENTACHLORURE D'ANTIMOINELe pentachlorure d'antimoine (Cl5Sb) fait partie du règlement CLP qui lui attribue les mentions de danger suivantes :  Classification : H314, H411 TRIBROMURE D'ANTIMOINELe tribromure d'antimoine (Br3Sb) ne fait pas partie à part entière du règlement CLP, cependant il est inclus dans la catégorie des composés de l'antimoine dans ce règlement et à ce titre les mentions de risque minimales suivantes s'appliquent en attendant des recherches supplémentaires :  Classification : H302, H332, H411 TRIFLUORURE D'ANTIMOINELe trifluorure d'antimoine (F3Sb) fait partie du règlement CLP qui inclut les mentions de danger suivantes :  Classification : H301, H311, H331, H411 En addition de ces mentions obligatoires, certaines entreprises suggèrent en attendant des recherches supplémentaires le signalement suivant en raison des soupçons de cancérogénicité qui pèsent sur la substance :  Associé au danger suivant : H351 |
Volume de production
| France |
FTE 2015 Importer 0 t (Sb) ≈7000 t (Sb203) t.an-1 |
|---|---|
| UE |
FTE 2015 Importer 0 t (Sb) t.an-1 () |
| Monde |
FTE 2015 Importer 143000 (Sb) t.an-1 |
Consommation
| Volume de consommation en France |
FTE 2015 Importer Pas d'information t.an-1 |
|---|
Présence dans l'environnement
| Eaux de surface |
FTE 2015 Importer Eaux de surface marines : 184 ± 45 ng.l-1 en moyenne (filella et al, 2002) Eaux douces : quelques ng.l-1 a quelques µg.l-1 (moyenne 0,23 µg.l-1 en eau douce en France en moyenne entre 2015 et 2017) |
|---|---|
| Eaux souterraines |
FTE 2015 Importer Eaux de pluie et eaux souterraines : < 1 µg.L-1 (ATSDR, 2017) |
| Air |
FTE 2015 Importer < 1 ng.m-3 (ATSDR, 2017) |
| Sols |
FTE 2015 Importer Abondance de 0,2 ppm dans la croûte terrestre (BRGM) |
Production et utilisation
Production et ventes
Données économiques
FTE 2015 Importer
Minerais
Selon le site internet de la Société Chimique de France (SCF), la teneur moyenne de l'écorce terrestre en nickel est de 75 ppm. Dans les minerais, le nickel est souvent associé au fer (Fe), au cuivre (Cu), au chrome (Cr) et au cobalt (Co).
De plus, d'après cette source et European Commission (2001a), on distingue deux principaux types de minerais :
- Les minerais sulfurés (65 % de la production), sous forme de pentlandite, (Ni,Fe)9S8, associée, en général, à de la pyrrhotite (Fe7S8), de la pyrite (FeS2) et de la chalcopyrite (CuFeS2). Les exploitations minières de ce type de minerais sont, en général, souterraines.
Ces minerais ont des teneurs de 0,7 à 3 % de nickel et contiennent du cuivre (environ 1 %), des platinoïdes, du cobalt, de l'argent et de l'or, qui sont récupérés. Le nickel est concentré par flottation à des teneurs de 10 à 15 % de Ni.
Ces minerais sont principalement exploités en Australie de l'Ouest, en Russie, au Canada (Manitoba, Labrador et Ontario19), en Chine, en Afrique Australe, en Finlande.
- Les minerais oxydés (35 % de la production de Ni). Ces minerais sont exploités à ciel ouvert et ne peuvent pas être concentrés par voie physique. Ils ne contiennent pas de cuivre ni de métaux précieux, mais renferment du cobalt. Parmi eux, on distingue :
- Les minerais silicatés (saprolites) qui se forment par substitution du magnésium de la serpentine (3MgO,2SiO2,2H2O) par du nickel : on obtient ainsi de la garniérite. Ce minerai est caractéristique de la Nouvelle-Calédonie où l'on observe le plus important gisement mondial de minerais oxydés, sa teneur en nickel est de 2,3 à 3 % et le minerai contient, outre le magnésium et la silice, 10 à 30 % de fer et de cobalt. Ces minerais sont également exploités à des teneurs plus faibles en Indonésie, en République Dominicaine, aux Philippines, au Brésil, …
- Les latérites nickelifères (limonites) dans lesquelles le nickel se substitue au fer dans la goethite (FeOOH). Ces minerais se caractérisent par leur pauvreté en nickel (de 1 à 1,5 %) et en cobalt (0,1 à 0,2 %) et une relative richesse en fer (40 à 50 %) et en chrome (2 à 5 %). Ils sont exploités à Cuba, en Australie (Queensland), en Grèce et sont présents en couverture de tous les gisements de minerais silicatés. Ils sont exploités, depuis 1987, par des "petits mineurs" de Nouvelle Calédonie20 , par Eramet et par Vale, la production étant exportée en Australie pour être traitée par hydrométallurgie ou transformée en Calédonie à Goro (ouverte en 2010).
[19] La mine de Sudbury constitue le plus important gisement mondial de minerais sulfurés. Les réserves prouvées sont de 59,8 millions de tonnes de minerai tout-venant.
[20] Le terme « petits mineurs » désigne, les sociétés autres que la SLN qui travaillent dans les mines. Elles exploitent des concessions et vendent par elles-mêmes le minerai à des acheteurs étrangers ou bien elles le revendent à la SLN voire même, elles exploitent une mine pour le compte de la SLN (Société Le Nickel).
Production minière
Selon Eramet via la SCF, la production mondiale de nickel était en 2011 de 1 897 000 tonnes de nickel contenu (dont 58,0.103 pour l'Union européenne et 122,9.103 pour la Nouvelle-Calédonie). Selon la SCF, la production métallurgique mondiale de nickel toujours en 2011 atteignait 1 589 000 tonnes de nickel contenu dans le nickel raffiné, les sels et les ferronickels (dont 119 000 pour l'Union européenne et 40 000 pour la Nouvelle-Calédonie).
De même, depuis le milieu des années 1990, plus d'un million de tonnes de nickel sont produites annuellement. Ce chiffre de production est dix à douze fois plus faible que pour le cuivre, et 800 fois plus faible que pour l'acier (site internet CNUCED21).
Selon le site internet de la Société Chimique de France en 2012, les réserves mondiales sont estimées à 75 millions de tonnes de métal contenu (dont 60 % de minerais latéritiques et 40 % de minerais sulfurés). La répartition de ces réserves en 2012 est la suivante (en millions de tonnes) : Australie : 20, Nouvelle-Calédonie : 12, Brésil : 7,5, Russie : 6,1, Cuba : 5,5, Indonésie : 3,9, Afrique du Sud : 3,7, Canada : 3,3, Chine : 3,0 et Madagascar : 1,6.
La Nouvelle-Calédonie représenterait le quart des réserves mondiales de minerai latéritique, d'après le site internet du CNUCED.
Variations de l'offre et de la production
Le paragraphe suivant est repris du site internet CNUCED :
« L'offre mondiale est parfois difficile à prévoir, notamment pour le nickel en provenance de Fédération de Russie. Ce pays possède en effet des stocks de métal importants et leur écoulement aléatoire influence fortement le marché à court terme. Mais l'offre varie également en fonction des mises en chantier d'usines, de la découverte de nouveaux gisements ou encore en raison de sanctions spécifiques telles que celles pratiquées dans le cadre de la loi américaine Helms-Burton concernant Cuba.
En outre, des facteurs exogènes tels que les prix des déchets d'inox, produits substituables au nickel primaire, les grèves dans un certain nombre d'entreprises ou les changements dans les volumes des stocks (…) contribuent à l'instabilité de l'offre. »
Nouvelle-Calédonie
Selon le site internet de la SCF, en 1995, l'exploitation et le traitement du nickel représentaient 30 % du PIB du Territoire et employaient environ 3 000 personnes.
[21] Conférence des Nations Unies sur le Commerce et le Développement : (consulté en décembre 2013). http://r0.unctad.org/infocomm/francais/nickel/plan.htm
Toujours selon la SCF, en 2012, la production de la Nouvelle-Calédonie a été de 131 816 tonnes de nickel contenu (soit 9,7 millions de tonnes de minerai humide).
Les exportations de minerais, en croissance, sont estimées à 61 250 tonnes de nickel contenu (soit 4,65 millions de tonnes de minerai). Elles sont dirigées principalement vers la Corée du Sud, l'Australie et le Japon. Les exportations sont effectuées, en grande partie par des mineurs indépendants de la Société le Nickel (SLN(. Le minerai en provenance de Nouvelle Calédonie représente la moitié de l'approvisionnement des producteurs japonais de ferronickel.
Depuis le début de l'exploitation des gisements de Nouvelle-Calédonie, 155 millions de tonnes de minerai ont été extraites (3,3 millions de tonnes de Ni). L'extraction a culminé en 1971 avec 7,7 millions de tonnes de minerai (jusqu'en 1950, la teneur exploitée dépassait 5 %, actuellement la teneur est comprise entre 2,3 et 2,8 %).
La SLN exploite les mines de Thio, de Kouaoua, de Népoui Kopéto, de Tiébaghi et depuis 2007 de Poum. La production a été en 2012 de 3,8 millions de tonnes de minerai. D'autres producteurs exploitent des gisements à Ouaco, Poya, Nakety, Kouaoua et Goro. Le gisement de la SLN de Kaala-Gomen est exploité par des sous-traitants. Au total, il y a 13 centres miniers (Figure 1). La société Inco détient 85 % (le BRGM 15 %) des droits d'exploitation de la zone de Goro (sud de l'île) dont les réserves seraient de 165 millions de tonnes de minerai à 1,57 % de nickel et 0,16 % de cobalt.
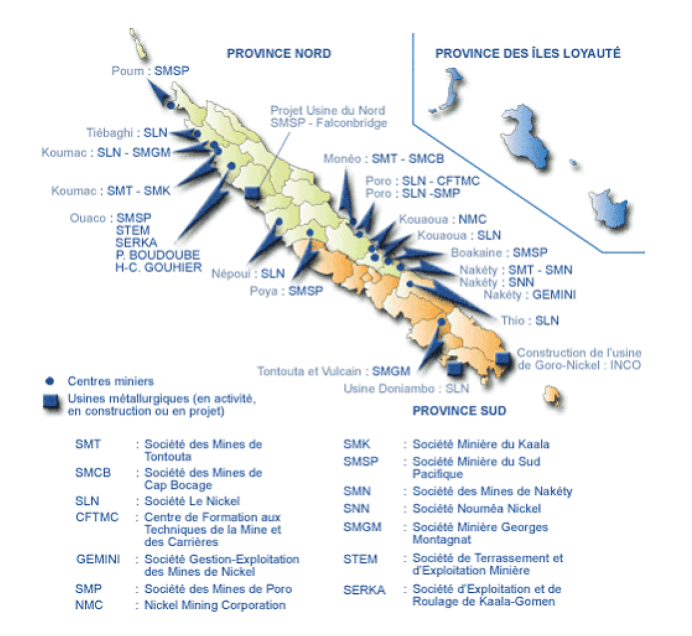
Figure 1. Les mines de nickel en Nouvelle-Calédonie, d'après le site internet de la SCF reprenant un document du Sénat : projet de loi de finances pour 2007 : outre-mer.
Selon le site internet CNUCED : « Les secteurs minier et métallurgique représentent 80 % de la valeur des exportations calédoniennes. Dans ce contexte, il est à noter que seuls 45 % du minerai extrait est traité sur place (…). Afin d'encourager les investissements, notamment d'infrastructures de traitement du nickel sur l'île, le Congrès de Nouvelle-Calédonie a adopté à l'unanimité le 27 juin 2001 une loi mettant en place un régime fiscal propice aux investissements dans la métallurgie du nickel. »
Métallurgie
Le BREF sur les métaux non-ferreux (Commission Européenne, 2001a) propose une schématisation du principe général de production du nickel à partir de minéraux oxydés.

Figure 2. Principe de production du nickel à partir de minerais oxydés, d'après European Commision (2001a).
Un schéma analogue existe également pour les minerais sulfurés. Mais comme ces derniers ne sont pas exploités en France ce document n'est pas repris dans cette fiche. De plus, selon le site internet de la SCF et dans le cas précis du minerai oxydé de Nouvelle-Calédonie, le process est détaillé dans les paragraphes suivants (§2.2.5.1 à 2.2.5.6).
Réduction du minerai :
Le minerai, riche en eau (25 %), est séché, puis, après ajout de 50 kg d'anthracite par tonne de minerai sec, calciné à 1000°C dans des fours rotatifs. Une première réduction des oxydes métalliques a ainsi lieu, à l'état solide.
Le minerai est ensuite réduit (désulfuration et soufflage d'oxygène), en phase liquide, dans des fours électriques22 . Le métal (ferronickel de 1ère fusion) sur lequel surnagent des scories est coulé : les scories sont granulées à l'aide d'eau de mer et utilisées pour des remblaiements.
Production de ferronickel
L'affinage du ferronickel de 1ère fusion consiste à enlever des proportions variables de carbone, de soufre et de silice élémentaire selon la qualité désirée de ferronickel, et le fer pour l'obtention des mattes.
Une tonne de minerai donne 110 kg de ferronickel (contenant de 24 à 29 kg de Ni).
Selon le site de la SCF, en 2012, les exportations calédoniennes de ferronickel correspondent à 44 858 tonnes de Ni contenu.
Production de mattes (destinées à l'élaboration de Ni)
La production de mattes s'effectue à partir du minerai réduit en phase liquide par sulfuration et déferrage par injection de soufre liquide. Cette étape aboutit à une "matte synthétique" (contenant de 10 à 15 % de soufre).
Un affinage secondaire, donne des mattes de "qualité industrielle" constituées de sulfure de nickel (75 % de Ni et 25 % de S). Les mattes contiennent en outre un peu de fer et du cobalt qui est récupéré lors de l'élaboration du nickel.
Exemple de production industrielle
En 2012, l'usine de Doniambo (société SLN, de Nouméa en Nouvelle-Calédonie), consommait 3 à 4 millions de t.an-1 de minerais bruts et 900 000 MWh.an-1 d'électricité.
Cette usine possédait en 2012 une capacité de production de 75 000 t.an-1 de Ni contenu (contre 55 000 en 1996) (dont 80 % en ferronickel et 20 % en matte). Cette usine fonctionne avec un personnel de 1 400 personnes.
[22] Le rendement des fours typiquement utilisés est de 97% et la consommation électrique est de 19 000 kWh.t-1 de Ni.
Exportations de la production industrielle
La totalité du ferronickel calédonien (44 858 tonnes en 2012) est exportée. La société Eramet est le 2ème producteur mondial de ferronickel.
La totalité des mattes est exportée vers la métropole pour être transformée à l'usine SLN/Eramet de Sandouville (situé à 10 km du Havre). Cette installation, qui date de 1978, a traité, en 2012, 13 417 tonnes de mattes calédoniennes dont 10 800 tonnes de cathodes et 2 080 tonnes de Ni pour la production de chlorure de nickel cristallisé et en solution (effectifs : 200 personnes).
Schématisation de la filière calédonienne
L'ensemble du process décrit ci-dessus en repris de façon schématique dans la Figure 3 ci-après.
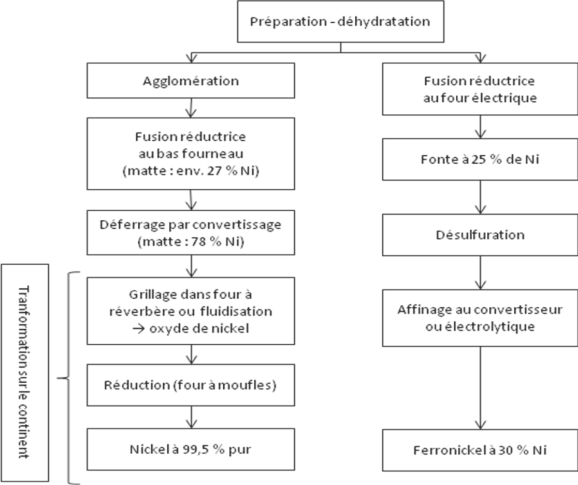
Figure 3. Schématisation de la filière néo-calédonienne de production de nickel, d'après le site internet CNUCED.
Recyclage
Le recyclage du nickel recouvre environ 25 % de la demande totale de nickel (RPA, 2000). De plus, selon le site internet de la SCF, le recyclage fournit 50 % du nickel destiné à la production des aciers inoxydables (le Ni contenu dans les aciers inoxydables est réutilisé lors du recyclage de ces aciers) et 20 % des autres utilisations.
Selon le site internet de la SCF, en 2012, aux Etats-Unis, le recyclage a représenté 95 100 tonnes, soit 43 % de la consommation. Dans l'Union européenne ; le taux de recyclage est de 45 %.
Selon Eramet (2005), le recyclage s'effectue directement chez les utilisateurs (cas de l'industrie sidérurgique pour ce qui concerne les chutes et les meulures d'acier inoxydable) ou par l'intermédiaire des industriels de la récupération (cas des catalyseurs usagés).
Place de la substance dans l'économie française
Consommation française
Selon le site internet de l'ENIA, en 2002, la consommation française de nickel équivalait à 90.103 tonnes (soit 13 % de la consommation européenne). Sur ces 90.103 tonnes, 40 % sont originaire de la filière de recyclage.
Evolution de la production française
La Figure 20 (repris du site internet de la société Eramet) présente l'évolution de l'offre de nickel dans le monde occidental. Cette figure permet de visualiser la relative stabilité dans le temps de la production de nickel en Nouvelle-Calédonie.
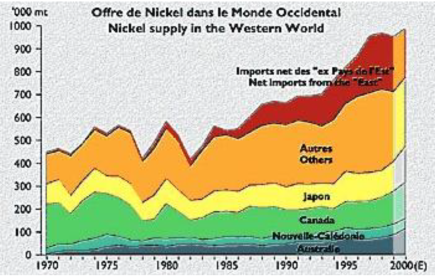
Figure 20. Offre de nickel dans le monde occidental, d'après le site internet d'Eramet.
Place dans l'économie française
Selon le site internet de l'ENIA, la totalité de la valeur ajoutée71 créée par les industries du nickel primaire, intermédiaire et de produits manufacturés est estimée à 6 G€.an-1 selon la répartition indiquée au Tableau 14. Ce secteur industriel emploie 105 000 salariés français.
Tableau 14. Répartition de la valeur ajoutée du nickel par secteur industriel, selon le site internet de l'ENIA.

Place dans l'économie européenne
Selon le site internet Nickel Institute73 , la totalité de la valeur ajoutée créée par les industries du nickel primaire, intermédiaire et de produits manufacturés est estimée à 40 G€ en 2004 selon la répartition indiquée Tableau 15. Ce secteur industriel emploie 465 000 salariés européens.
[71] Augmentation du prix d'un article à chaque étape de sa fabrication à l'exception du coût initial du nickel (site internet de l'ENIA).
[72] La totalité de ces emplois n'est probablement pas attribuable au seul nickel. 73 (consulté en janvier 2014). http://www.nickelinstitute.org/~/media/Files/SocioEconomicWeinbergReports/SocioEconomicImpactNickel-29Jan04-FinalReport-logo_.ashx
Tableau 15. Répartition de la valeur ajoutée du nickel par secteur industriel en 2004, selon le site internet de Nickel Institute.

Prix du marché du nickel
Selon Eranet (2005), le cours du nickel au LME74 connaît depuis une trentaine d'années des fluctuations parfois rapides et de grande amplitude (du fait des phénomènes de spéculation et d'amplification propres aux marchés des matières premières) : cf. Figure 21. En 2004, le prix moyen du marché était de 13,9 $.kg-1 ou 11,4 €.kg-1 .
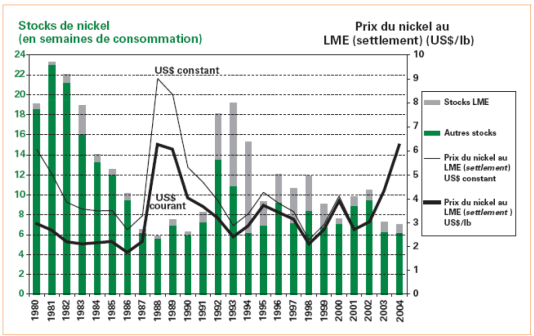
Figure 21. Prix du nickel au London Metal Exchange, d'après Eramet, 2005.
[74] LME : London Metal Exchange ou Bourses des Métaux de Londres.
Selon le site internet CNUCED :
« A court terme, la volatilité des prix du nickel est très importante (environ 16,5 % entre janvier 1998 et janvier 2006). Un certain nombre de facteurs sous-tendent cette instabilité. Au niveau de l'offre : les incertitudes liées aux approvisionnements et en particulier ceux relatifs à la situation de Cuba, de la Fédération de Russie ou encore des Philippines, ainsi que le nombre limité de producteurs ont un impact sur le prix du nickel. Dans ce cadre également, l'impact des arrêts momentanés de production de certains grands groupes pour cause de négociations d'accords collectifs tend à renforcer cette volatilité. Du coté de la demande, la situation d'autres secteurs tels que celui de la sidérurgie influence fortement le développement des cours du nickel. La substitution possible avec les déchets d'inox pour certaines applications peut également jouer un rôle en cas de forte variation des prix de ces deux produits. Finalement, dans un marché étroit (au niveau de l'offre) et relativement segmenté, la variabilité des stocks est une source importante d'instabilité des cours. Cette volatilité inhérente à la situation spécifique du marché du nickel attire ponctuellement les fonds d'investissements, renforçant encore ce phénomène et engendrant un développement parfois erratique des cours. ».
Evolution du marché de la métallurgie
Depuis 1950, la consommation de nickel dans le monde occidental croit de 4 % par an. La consommation mondiale suit cette même croissance depuis 1992. Eramet (2005) indique que la plus forte croissance de l'usage du nickel lié à la production d'aciers inoxydables (5 %.an-1) est compensée par une croissance plus faible des autres secteurs (construction, monnaie, superalliages pour l'aéronautique et alliages à base de nickel destinés aux industries électroniques).
Cette croissance de 4 %.an-1 devrait se maintenir dans les années à venir. En effet, les usages de cet élément pour la fabrication des aciers inoxydables devraient s'intensifier (RPA, 2000). De plus, la majorité des moteurs d'avion sont constitués à plus de 30 % de nickel et ce secteur est supposé connaître une croissance annuelle de 5,3 % jusqu'en 2015 (Anyadike, 1999).
Données sur les producteurs français de nickel
Le principal producteur de nickel français (nickel électrolytique) est la société Eramet, en 2013, cette société et ses filiales (Le Nickel SLN ; Erasteel) étaient responsables de :
- la production de la moitié du nickel produit en France et en Nouvelle-Calédonie ;
- la production de la quasi-totalité du nickel sous forme de produits finis en France et en Nouvelle-Calédonie.
Ainsi, en 2012, cette société était à l'origine de la production de 56 447 tonnes de nickel (ferronickel et matte) pour un effectif moyen de 3 000 personnes, un chiffre d'affaires de 898 M€75 et des investissements de 146 M€.
En Nouvelle-Calédonie, sa filiale SLN exploite d'importants gisements de minerai. Elle transforme le minerai dans son usine métallurgique de Doniambo, à proximité de Nouméa. En France, la raffinerie de Sandouville près du Havre, produit du nickel de haute pureté et des sels de nickel à partir d'un produit intermédiaire (la matte de nickel) élaborée à Doniambo (site internet d'Eramet).
Données sur les projets de production de nickel en France
La société Inco développe actuellement un projet de site industriel de production de nickel en Nouvelle-Calédonie. Ce projet, initié en 2001, porte le nom de "Goro Nickel" et porte sur la construction d'une unité de traitement hydrométallurgique des latérites du Sud néo-calédonien par la lixiviation du minerai à l'acide sulfurique sous pression. L'objectif affiché pour ce site industriel est la production annuelle de 54 000 tonnes de nickel et ce pour une durée d'une vingtaine d'années.
L'impact économique de ce projet correspond à la création de 2 500 emplois directs ou induits, soit 5 % de la population active, et l'équivalent de 10 à 12 % du produit intérieur brut (PIB) annuel du territoire, grâce aux importations et aux exportations (Pitoiset, 2003).
Une demande "d'autorisation d'exploiter des installations classées" a été publiée en 2004 (Goro Nickel, 2004). A ce jour, suite à des modifications dans le projet industriel, une nouvelle demande d'autorisation est en cours de rédaction.
Données sur les producteurs français d'aciers inoxydables
D'après le site internet de l'ENIA, environ 106 t d'acier inoxydable et d'autres alliages sont produites en France pour une valeur de 1,6 G€.an-1 .
D'après le site internet de la SCF, les producteurs français d'aciers inoxydables sont Aperam (transformation d'acier inoxydable brut en tôles laminées), Industeel (production des tôles hyper lourdes et d'aciers inoxydables), Ugitech (production d'acier inoxydable brut et de produits longs) et Aubert & Duval.
[75] Chiffre uniquement lié à l'activité «nickel ».
Batteries Ni-Cd
La société française SAFT est un acteur majeur du marché des accumulateurs Ni-Cd. Seul fabricant français, elle emploie 4 000 personnes dans le monde, dont 2 000 en France réparties sur trois sites. Son chiffre d'affaires global est d'environ 598 millions d'euros ; la moitié environ est réalisée en France. La production d'accumulateurs Ni-Cd pour l'industrie représente 50 % à 60 % de son activité (premier rang en Europe). L'emploi du couple Ni-Cd subsiste pour des piles et batteries rechargeables grand public, mais est désormais marginal pour des batteries de téléphones mobiles et d'ordinateurs portables. En revanche, leur emploi reste important pour les outils portables (Drag, 2000 dans Brignon et al., 2005).
Impact économique des mesures de réduction ou de substitution
Aucune information n'a été obtenue à ce sujet.
Coût de l'impact sur la santé humaine des émissions
Une estimation de coût des dommages globaux des émissions atmosphériques de nickel a été effectuée par Rabl (2005) : 3,8 € par kg de nickel valeur comprise (entre 0,3 et 20 €.kg-1). L'auteur précise que 95 % du coût des dommages sont imputables aux impacts sur la santé, soit 3,6 €.kg-1 de nickel émis.
FTE 2015 ImporterINFORMATIONS MINERALOGIQUES
L'Antimoine (Sb) est présent en relative faible quantité, avec une abondance moyenne de 0,2 ppm dans la croute terrestre ce qui est comparable au cadmium mais jusqu'à 10 fois inférieur à l'arsenic d'après le BRGM. Cela la positionne donc au 65iéme rang par ordre d'abondance.
Rarement présent sous sa forme native, il existe plus d'une centaine de minerais contenant de l'antimoine. En effet, l'antimoine étant chalcophile il a tendance à s'associer au souffre ainsi qu'aux métaux lourds (Anderson, 2012). La forme la plus courante est le trisulfure d'antimoine (Sb2S3) ou plus communément stibine :
Figure 1 : Photographie de Stibine, Vendée16

L'antimoine peut aussi être retrouvé sous ses formes oxydées (III et V) telles que le trioxyde d'antimoine (Sb2O3).
[16] Source illustration (
Aussi, Les gisements d'antimoine contenant de faibles volumes, il est également récupéré en tant que coproduit de l'extraction des métaux auxquels on le retrouve associé tel que l'or, le plomb, zinc, fer…
Tableau 5 : Récapitulatif des principaux minerais antimoniés

(Source : BRGM)
Du fait de la faiblesse des réserves d'antimoines connues, d'un nombre d'acteurs restreint et fournissant peu d'informations (Chine, Russie…), de son importance économique, du manque d'alternatives identifiées à ses usages, la Commission Européenne l'inclut dans la liste des matières premières en situation critique17 .
[17] Report on critical raw materials for the EU, Avril 2014, Commission Européenne Une version plus récente (2017) de la liste existe et dresse un constat similaire tout en ajoutant d'autres matériaux
PRODUCTION MINIERE
Figure 2 : La filière de l'antimoine dans le monde
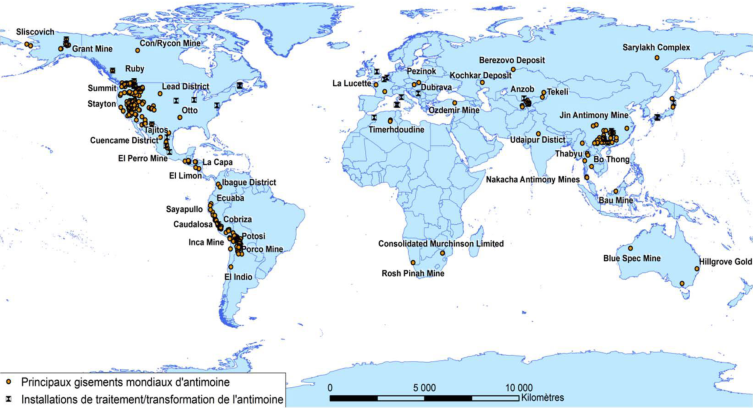
(Source : BRGM)
La plupart des sources d'information sur les minéraux (BRGM, BGS, USGS…) attire notre attention sur le manque d'informations et de transparence concernant la production, les réserves et la consommation d'antimoine. Certains chiffres sont le résultat d'estimations et peuvent être sous-évalués.
PRODUCTION MINIERE CONTEMPORAINE
L'antimoine, retrouvé en grande majorité sous forme de minerais, doit être séparé des autres métaux post-extraction à l'aide de techniques métallurgiques.
Les minerais sont broyés puis flottés, ce qui génère des concentrés de sulfures et sulfosels.
Ils sont à leur tour grillés afin de produire du trioxyde d'antimoine réduit par la suite en antimoine sous forme de métal.
L'antimoine, en tant que coproduit notamment de la production du plomb, peut être récupéré lors de l'affinage de celui-ci par oxydation afin d'en éliminer les impuretés.
Les réserves mondiales sont estimées à 1 800 000 t d'équivalent antimoine (Dupont, Arnout, Jones, & Binnemans, 2016), et la Chine en compte à elle seule 950 000 t d'après les chiffres publiés par l'état. Elle est suivie par la Russie, 350 000 t, et la Bolivie 310 000 t.
La production minière est principalement concentrée en Chine à près de 75 % ce qui en fait l'acteur majeur du marché. Les autres producteurs notables sont le Tadjikistan et la Russie. Bien qu'il ait existé des mines produisant de l'antimoine par le passé en Union européenne, il n'y a désormais plus aucun producteur, ce qui place l'UE dans une position de déficit commercial vis-à-vis de cette ressource.
Figure 3 : Production mondiale minière d'antimoine en 2016 (en tonne de métaux)
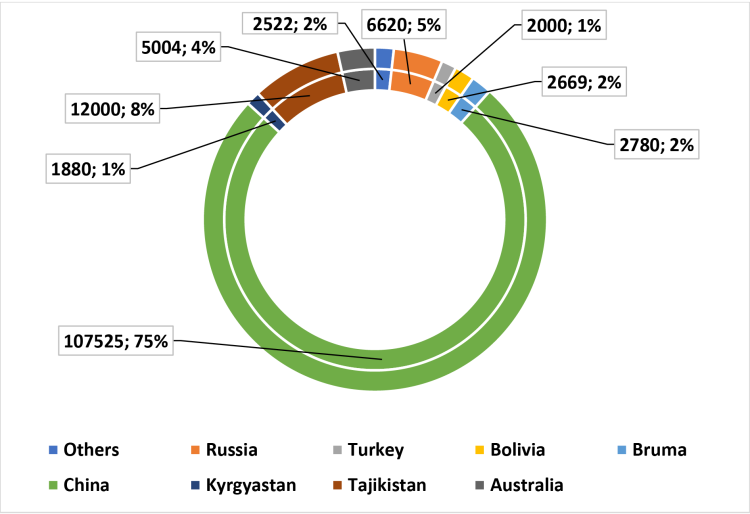
Source : British Geological Survey 2012-2016
Figure 4 : Evolution de la Production Mondiale minière d'Antimoine (en tonne d'antimoine)
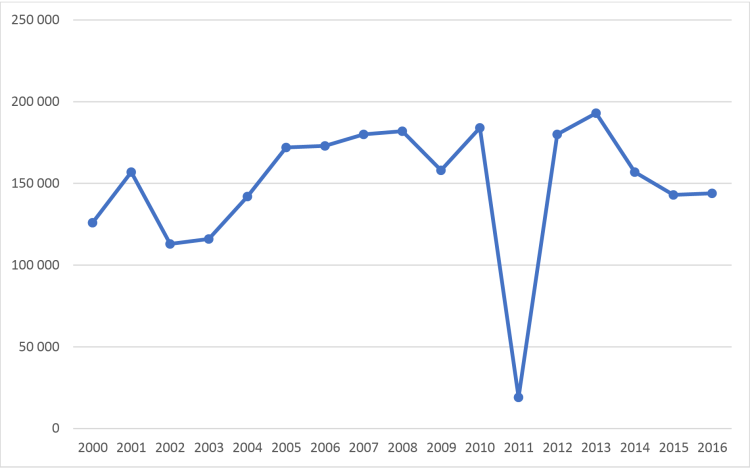
Source : USGS
PRODUCTION MINIERE HISTORIQUE EN FRANCE
Jusqu'en 1991 la France a extrait de ses sols de l'antimoine pour une production totale cumulée de 154 900 t (BRGM, Avril 2015). En effet, la France fut même au premier rang de la production minière mondiale d'antimoine entre 1890 et 1908. Le principal site se situant à la Lucette (53) avec une production historique de 42 000 t. Dans les sites notables on retrouvera aussi les sites de Brioude-Massiac (43/15) et de Rochetréjoux (85). Quelques tentatives d'exploitation perdureront dans les années 80-90 jusqu'à la fermeture du site de Les Brouzils en Vendée.
Figure 5 : Potentiel des gites et gisements français d'antimoine
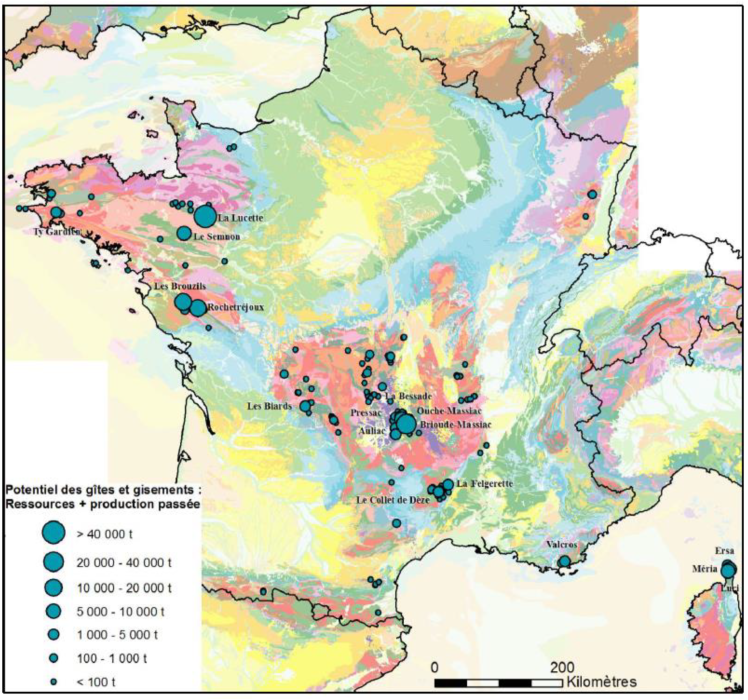
(Source : BRGM , 2011)
PRODUCTION SECONDAIRE D'ANTIMOINE
L'antimoine est utilisé dans des alliages avec d'autres métaux (Plomb, Zinc, Etain, Fer, Nickel…) pour augmenter leur durabilité, notamment dans la confection de batteries plomb-acide et dans une moindre mesure dans les munitions, tôles, tuyaux, câbles, paliers à roulement… Ainsi l'antimoine à l'instar des autres métaux fait l'objet d'un marché secondaire principalement basé sur le recyclage des batteries plomb-acide contenant de l'alliage Pb-Sb qui représente environ 25 % de la consommation d'antimoine (pour un taux de recyclage des batteries se situant autour de 85%). Les batteries sont fondues puis les différents éléments sont récupérés à la suite d'un processus d'affinage.
Celui-ci a été motivé par l'accroissement des prix observé autour de 2010 résultant d'une régulation plus importante des licences d'exploitations et des quotas d'exportations chinois de la production minière d'antimoine.
Figure 6 : Production secondaire d'antimoine aux États-Unis (T/Sb)
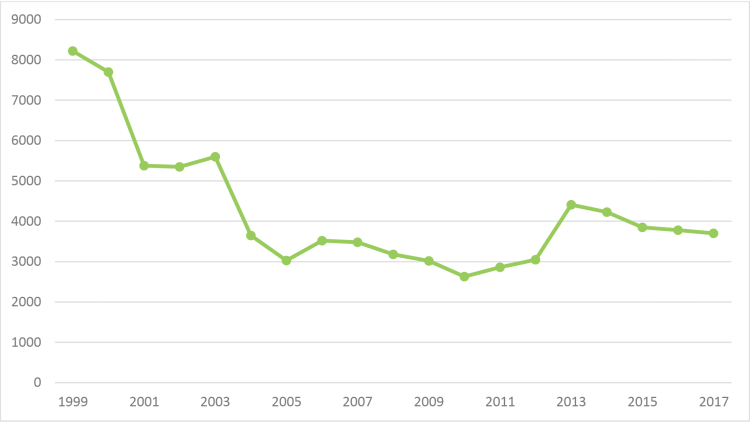
(Source : USGS)
Auparavant un ralentissement de la production secondaire avait été observé au début des années 2000 qui pourrait s'expliquer par la baisse du prix de la source d'antimoine primaire principalement venu de Chine. On observe actuellement, une stabilisation de la production secondaire d'antimoine illustrée par l'exemple des Etats-Unis (Figure 6) qui pourrait s'expliquer par la demande croissante en composés de l'antimoine du secteur des retardateurs de flamme.
L'offre de déchets antimoniés recyclables pourrait se réduire au fur à mesure du remplacement des batteries plombs-antimoine par des batteries plomb-calcium (USGS, 2013). Une tendance d'autant plus marquée par la réduction des doses d'antimoine dans les produits finaux18 (Roskill, 2018). Enfin l'émergence de substituts à la batterie plomb-acide notamment motivée par le marché de l'automobile électrique pourrait entrainer de lourds changements sur la production secondaire d'antimoine.
PRODUCTION DES COMPOSES D'ANTIMOINE
L'antimoine est couramment vendu aussi sous forme manufacturée de sels, poudres et notamment sous forme oxydée (Sb2O3) qui répond à son usage principal en tant que retardateur de flamme dans les textiles et plastiques. Le trioxyde d'antimoine peut être produit par grillage de trisulfure d'antimoine, par combustion d'antimoine dans l'air ou dans l'oxygène, par hydrolyse alcaline de composés halogènes d'antimoine (trichlorure, tribromure ou triiodure), ou par hydrolyse du trisulfure d'antimoine avec de la vapeur surchauffée19 .
Tout comme l'antimoine, la majorité de la production de ses composés émane de la Chine. En effet, la production de trioxyde d'antimoine est assurée à plus de moitié par la Chine seule (BRGM, 2011). Cependant, contrairement à la production minière, la production de trioxyde d'antimoine, de sulfures ou encore de chlorures d'antimoine est également établie en Europe. Un rapport du BRGM (2011) s'appuyant sur les données de l'USGS estimait la production du trioxyde d'antimoine mondiale à 107 500 t (masse brute) pour l'année 2006 dont 7500 t pour la France. Malheureusement, il n'existe pas de source d'information publique de la production des autres composés
http://www.sica-chauny.com/fr/http://www.pcdlucette.com/ Deux sites situés en France assurent la production de Sb2O3 ainsi que de catalyseurs nécessaires à la plasturgie : la Société Industrielle et Chimique de l'Aisne (SICA) (02) également 1ier producteur européen de trioxyde d'antimoine avec une production annoncée à plus de 10 000 t par an () et la Société des Produits Chimiques de la Lucette (SPDL) (53) (). Ces deux sites sont des filiales de la société belge Sudamin.
[18] https://roskill.com/market-report.an-1timony/
[19] Fiches toxicologiques et environnementales des substances chimiques, INERIS 2007
COMMERCE MONDIAL ET BALANCE COMMERCIALE FRANÇAISE
ECHANGES INTERNATIONAUX ET COURS DE L'ANTIMOINE
L'illustration ci-dessous synthétise les échanges commerciaux relatif à l'antimoine, qui à l'image de la production sont centrés sur la Chine.
Figure 7 : Commerce international de l'antimoine

Figure 8 : Cours de l'antimoine basé sur le London Exchange Market index, référence du marché mondiale des métaux non ferreux (US$/t).
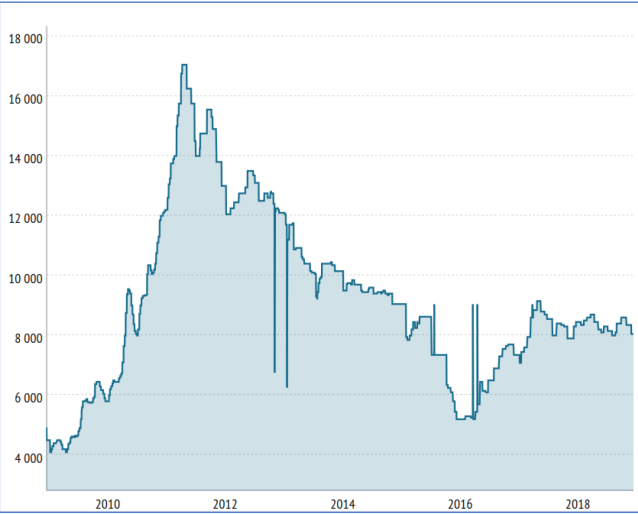
Source : Les Echos investir20 (2018)
L'accroissement des prix autour de 2010 pourrait s'expliquer par la mise en place de quotas sur les exportations chinoises 21 . Roskill 22 estime qu'une diminution de la demande est à prévoir dans le secteur des batterie plomb-acide et inversement une augmentation pour la demande dans l'industrie des plastique et textiles (Catalyseurs et Retardateur de flamme)
[20] https://investir.lesechos.fr/cours/matiere-premiere-antimoine-9965pc,wmpcb,ant,ant,opid.html
[21] https://www.globaltradealert.org/state-act/7830
[22] https://roskill.com/market-report.an-1timony/
BALANCE COMMERCIALE FRANÇAISE
D'après le département des statistiques et des études du commerce extérieur23 , en 2017 :
- Les importations de minerais d'antimoine et leurs concentrés représentent 90 milliers d'euros pour une masse totale de 13 tonnes dont 83% depuis la Chine et 14% depuis les Pays-Bas. On ne relève aucune exportation, car il n'y a pas de production.
- Le trioxyde d'antimoine représente une valeur d'exportation de l'ordre de 47 millions d'euros soit 6 596 tonnes avec pour principaux partenaires l'Allemagne (34%), l'Italie (14%), l'Espagne (13%) et le Royaume-Unis (9%). Les importations représenteraient un volume de 979 tonnes pour une valeur de 7 millions € avec pour principal fournisseur la Belgique (80%).
- Le plomb antimonié représenterait un volume d'exportations de l'ordre de 6 752 tonnes pour une valeur de 16 millions € avec pour principaux clients l'Allemagne (67%), la Thaïlande (20%) et la Hongrie (10%). Les importations représentent un volume de 34 807 tonnes pour une valeur de 50 millions € avec pour fournisseurs le Royaume-Uni (77%) et la Belgique (23%).
[23] http://lekiosque.finances.gouv.fr/site_fr/NC8/recherche.asp?t=2&iter=2&CS=antimoine
Les avis concernant les perspectives économiques font état d'une diminution future de la production minière chinoise qui représente la majeure partie de la production mondiale et est donc au centre des attentions des acteurs du marché (Roskill, 2018)29 . Exceptée la consommation dans le marché des batteries au Plomb, la plupart des usages semble en constante augmentation (European Commission, 2014). De nouveaux usages mineurs soumis à forte concurrence se développent, dans la plasturgie (catalyseur pour les polymères, stabilisateurs de chaleur…), les semi-conducteurs, condensateurs miniaturisés, générateurs thermoélectriques, technologies infrarouges, couches conductrices (ATO) (USGS, 2013) (BRGM, 2011).
[29] https://roskill.com/market-report.an-1timony/
Même si de nouveaux sites miniers pourraient voir le jour (Arménie, Australie, Canada, Géorgie, Italie, Laos, Russie, and Turquie) (USGS, 2013) l'UE a ajouté l'antimoine à la liste des matières premières critiques faisant l'objet d'une surveillance accrue dont la recherche d'alternatives est encouragée (European Commission, 2014) en raison de sa rareté, de l'absence de production minière européenne et du quasi-monopole chinois, de l'augmentation constante de notre consommation globale et du manque de substituts soutenables (puisque souvent les alternatives présentent des caractéristiques similaires).
Procédés de production
FTE 2015 Importer
Selon European Commision (2001a) et INERIS (2005), le nickel est obtenu principalement à partir de minerais de nickel sulfurés (pyrrhotite, nickeliferreuse, pentlandite, chalcopyrite) dans lesquels sont également présents le fer et le cuivre. Le minerai est broyé, enrichi par flottation et séparation magnétique suivie d'un grillage et d'une fusion. La matte obtenue est ensuite traitée par un procédé pyrométallurgique (grillage de l'oxyde et réduction en métal) ou hydrométallurgique (formation d'une solution de sel de nickel et réduction en métal).
Le nickel brut obtenu peut ensuite être purifié par une méthode électrolytique ou par un procédé dans lequel le métal brut et l'oxyde de carbone réagissent à 200/300°C pour former du nickel carbonyle qui se décompose sélectivement d'abord en nickel et monoxyde de carbone puis dans des délais plus longs en carbonyles des autres éléments présents. Ce procédé permet d'obtenir du nickel pur à plus de 99,9 %.
Le nickel tétracarbonyle est formé par réaction du monoxyde de carbone avec de la poudre de nickel à 50°C.
L'oxyde de nickel est obtenu en chauffant du nickel à une température supérieure à 400°C en présence d'oxygène.
L'acétate de nickel est produit par réaction de l'oxyde noir de nickel avec l'acide acétique.
Le chlorure de nickel est formé par réaction de l'acide chlorhydrique avec le nickel.
Le nitrate de nickel est obtenu par réaction entre l'acide nitrique fumant et le nitrate de nickel hexahydraté.
Le sulfate de nickel est formé par dissolution d'oxyde ou d'hydroxyde de nickel dans de l'acide sulfurique.
Le sulfure de nickel ou sous sulfure de nickel est obtenu lors de la production de nickel à partir de minerais sulfurés.
Utilisations
Introduction (varitétés d'utilisations)
FTE 2015 Importer
Comme de nombreux autres métaux, les applications du nickel à l'état pur sont beaucoup moins importantes que celles sous forme d'alliage avec d'autres composants (site internet CNUCED). Ainsi, le nickel est utilisé pour la fabrication de plus de 300 000 produits repartis entre les secteurs industriels, militaires, des transports, de la marine, de l'architecture et des produits destinés au public.
D'après le site ESIS de la Commission Européenne23 , le nickel a été rapporté par les industriels de l'Union européenne comme substance HPV (high production volume). Il s'agit de substances produites ou importées à plus de 1 000 tonnes par an.
Selon le site de la SCF, en 2011 et dans le monde, les différents secteurs d'utilisation de nickel sont :
[23] (consulté en décembre 2013). http://esis.jrc.ec.europa.eu/index.php?PGM=hpv

Figure 4. Répartition de la consommation mondiale de nickel primaire par secteur, d'après le site internet de la SCF.
De plus, toujours d'après Eramet (2005), le nickel est consommé à 64 % sous forme de métal (électrolytique, briquettes, billes), 22 % de ferronickel, 12 % d'oxyde métallurgique et produits dérivés et 2 % de produits spéciaux (poudres, sels, produits pour la galvanoplastie).
Le nickel entre dans la composition de nombreux alliages en raison de ses caractéristiques de dureté et de résistance à la corrosion. De plus, selon le site internet d'Environnement Canada, outre l'exploitation minière, la fonte, l'affinage de métaux, la production d'alliages et le recyclage de métaux, le nickel et ses principaux composés sont utilisés dans une vaste gamme d'applications industrielles dans les secteurs de la fabrication d'automobiles et de la construction navale ainsi que dans les industries électrique, pétrolière, alimentaire et chimique.
Selon l'INERIS (2005), le nickel est associé au cuivre, au fer et au manganèse pour fabriquer du monel24 , au fer et au chrome pour donner des aciers inoxydables et du chromel ou inconel25 , à l'aluminium, au chrome et au soufre pour obtenir l'alumel26 .
[24] Le monel est un alliage d'une grande robustesse et d'une excellente résistance à la corrosion dans de nombreuses situations acides et alcalines, il convient en particulier aux conditions de réductions. Il possède également une bonne ductilité et une bonne conductivité thermique. Parmi ses applications on compte : l'ingénierie navale, le traitement chimique et des hydrocarbures, les échangeurs de chaleur,
Selon l'INRS27 (2009), le nickel est également employé dans la production d'alliages non ferreux utilisés par exemple dans la fabrication de pièces de monnaie, d'outils, d'ustensiles de cuisine et de ménage… Par exemple, il est associé au cuivre et au zinc pour fabriquer du maillechort28 . De plus, cet élément est utilisé dans la fabrication de pigments minéraux pour métaux et céramiques ainsi que pour réaliser des revêtements électrolytiques des métaux (nickelage).
Selon le site internet du Nickel Institute29 , le nickel est également employé minoritairement dans les secteurs de la fabrication :
- de réacteurs et turbines d'avions ;
- de structures de véhicules (tels que les trains, avions, métros, …) ;
- de métaux à mémoire de forme ;
- d'équipements pour la cuisine et la salle de bain ;
- d'équipements pour les industries pétrochimiques et pharmaceutiques ;
- d'instruments médicaux ;
- de CD, DVD et disques Blue-ray.
les soupapes et les pompes (consulté en janvier 2014). http://www.alloywire.com/french/monel_alloy_400.html
[25] L'inconel est un alliage d'une bonne résistance à l'oxydation et à la corrosion à températures élevées utilisé notamment pour les composants de fours, le traitement chimique et alimentaire et le ingénierie nucléaire : (consulté en janvier 2014). http://www.alloywire.com/french/inconel_alloy_600.html
[26] L'alumel est un alliage d'une bonne résistance à l'oxydation et à températures élevées utilisé notamment pour constituer l'élément négatif du thermocouple de type K. Ce thermocouple peut être utilisé jusqu'à 1250°C dans des atmosphères oxydantes et est probablement le thermocouple le plus commun : (consulté en janvier 2014). http://www.goodfellow.com/catalogue/GFCat4I.php?ewd_token=noyssmFfhxYcc4gPLY7zXdMHtYFyoi&n=Hl6EK9Xcyg17YI66cDowFdpJuFTinL&ewd_urlNo=GFCat411&Catite=NI100260&CatSearNum=1
[27] (consulté en janvier 2014). http://www.inrs.fr/accueil/produits/bdd/doc/fichetox.html?refINRS=FT%2068
[28] Bonne usinabilité, excellent pour travail à froid et excellente soudabilité. Son comportement lors d'un formage à chaud est médiocre. Ses applications comprennent rivets, visserie, fermeture éclair, éléments optiques et bijoux fantaisie : (consulté en janvier 2014). http://www.goodfellow.com/catalogue/GFCat4I.php?ewd_token=orQCg5DJj2qub4t7rz0ggtpvgorWEk&n=jXAlfgv6DwtfneBxEY64315imQ2IQN&ewd_urlNo=GFCat4B11&Catite=CU100400&CatSearNum=2
[29] (consulté en janvier 2014). http://www.nickelinstitute.org/NickelUseInSociety/AboutNickel/WhereWhyNickelIsUsed.aspx
Vue d'ensemble des composés chimiques du nickel et de leur utilisation
FTE 2015 Importer
Les composés du nickel ayant été enregistrés dans REACH (selon la base publique de l'ECHA consultée en Février 2014), pour des usages autres que des intermédiaires de synthèse et à des tonnages supérieurs à 100 tonnes sont présentés dans le tableau ci-après.
Tableau 6. Composés du nickel enregistré dans REACH.
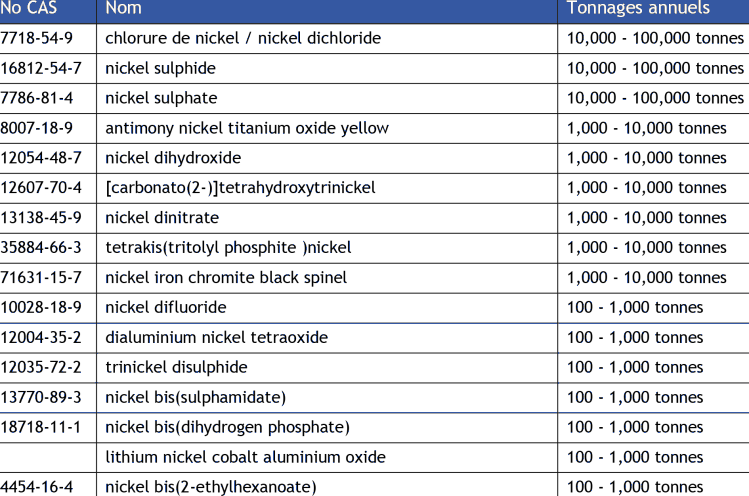
Plus en détail, le nickel tétracarbonyle est employé dans la fabrication de poudre de nickel de haute pureté. Il est également utilisé comme catalyseur en synthèse organique. Plusieurs autres composés du nickel (par exemple le nickel bis(2-éthylhexanoate) sont utilisés comme catalyseurs, notamment catalyseurs de polymérisation (Rieger, 2006).
L'acétate de nickel est utilisé comme mordant30 pour les textiles, comme intermédiaire dans la fabrication d'autres composés de nickel et comme catalyseur.
L'oxyde de nickel est utilisé dans la fabrication de sels de nickel, dans la fabrication de ferrites utilisées dans l'industrie électronique, dans la production de catalyseurs et pour le nickelage. Il est également employé comme colorant pour le verre, utilisé dans les peintures sur porcelaine, dans des composants électroniques et comme catalyseur.
L'hydroxyde de nickel est utilisé dans le domaine des batteries.
Le carbonate de nickel est employé (à hauteur de 2700 tonnes/an de nickel dans l'UE en 2000) pour la fabrication de catalyseurs (25 %), le nickelage électrolytique (75 %) et d'autres usages (5 %) (Danish EPA, 2008c31). Il est utilisé, selon les données SIDS (Screening Information Dataset) de l'OCDE32 , en Europe de l'Ouest, dans le nickelage, la production de catalyseurs, la production de pigments et dans les composants électroniques.
Le chlorure de nickel est employé (à hauteur de 1670 t Ni/an dans l'UE en 2001) pour le nickelage électrolytique, pour la production de catalyseurs (72 % des tonnages), en tant qu'intermédiaire pour la production de nickel par électrolyse (26 %), et divers autres usages (Danish EPA, 2008b33) (pour fabriquer des encres sympathiques et comme réactif de laboratoire). Il sert également à piéger l'ammoniac dans les masques à gaz. Selon les données SIDS (Screening Information Dataset) de l'OCDE, en Europe de l'Ouest, le chlorure de nickel est utilisé à 71 % pour le nickelage et à 29 % pour la production de catalyseurs.
Le nitrate de nickel est employé (à hauteur de 3 300 tonnes/an de nitrate de nickel dans l'UE en 2002) pour la production de catalyseurs (76 % des tonnages), comme intermédiaire dans la production de batteries nickel-cadmium (12 % des tonnages) et dans le prétraitement chimique des métaux (12 % des tonnages) (Danish EPA, 2008d34). Selon les données SIDS (Screening Information Dataset) de l'OCDE, en Europe de l'Ouest, la production de catalyseurs et les batteries représentent 92,5 % de la production total de nitrate de nickel de l'Union européenne.
[30] Dans l'industrie textile, le mordant est un composé chimique qui joue le rôle de lien entre la fibre textile et le colorant naturel : (consulté en janvier 2014). http://www.scrd.net/scrd_new/francais/textile_colorants_naturels_intro.html
[31] (consulté en février 2014). http://www.mst.dk/NR/rdonlyres/2929A8CB-8A5B-43C9-BB67-506D847E960E/0/Ni_carbonate_EU_RAR_HH
[32] (consulté en janvier 2014). http://webnet.oecd.org/HPV/UI/handler.axd?id=9ce00cf2-296e-459f-a92e-aec0c9771a7b
[33] (consulté en février 2014). http://www.mst.dk/NR/rdonlyres/BD706A72-29DD-4021-ABAE-BE3D66FD9BAE/0/Ni
[34] (consulté en février 2014). http://www.mst.dk/NR/rdonlyres/21D4A773-AA98-4160-91CA-BB1444238BC9/0/Ni_nitrate_EU_RAR_HH_March_2008_finaldraft.pdf
Le sulfate de nickel est utilisé dans les bains de nickelage souvent conjointement avec le chlorure de nickel. Une alternative à ce mélange est celui constitué de fluoborate de nickel, ou le sulfamate de nickel (et d'usage important notamment pour la fabrication de robinetterie en « nickel-chrome ») (Danish EPA, 2008e). Le sulfate de nickel est aussi employé comme intermédiaire dans la fabrication de carbonate de nickel et de sulfate d'ammonium et de nickel. C'est le principal intermédiaire pour la fabrication de sels de nickel. Il sert à produire des catalyseurs et est employé comme mordant13 pour les textiles. Il est également employé pour le noircissement du zinc et du bronze. Il est utilisé 3 400 tonnes/an de nickel en 2000 de sulfate de nickel dans l'UE (Danish EPA, 2008e 35).
Le sulfure de nickel est utilisé dans la production de catalyseurs et dans l'hydrogénation des composés de soufre en pétrochimie.
Le nickel bis(dihydrogen phosphate) est notamment un composant de produits pour le traitement de surface de métaux (phosphatation).
Le nickel bis(sulphamidate) est utilisé en traitement de surface des métaux, pour la production de batteries, ainsi que celle d'autres sels de nickel, d'après le site internet Nickel Consortia.
Certains pigments (comme le antimony nickel titanium oxide yellow) contiennent du nickel, et peuvent être employés dans la coloration de matériaux comme des plastiques.
Enfin, les scories de la production de ferronickel, produites en grandes quantités, qui étaient considérées principalement comme des déchets, tendent à être progressivement réutilisées dans plusieurs domaines :
- matériau abrasif pour procédés de sablage industriel ;
- additifs améliorant les caractéristiques mécaniques du ciment ou de céramiques ;
- additifs d'asphaltes, employé pour apporter des propriétés antidérapantes.
Les scories de ferronickel ont été enregistrées, à la date de rédaction de ce document, dans le cadre de REACH par deux sociétés européennes pour des bandes de tonnage importantes (100 000 – 1 000 000 tonnes).
[35] (consulté en février 2014). http://www.mst.dk/NR/rdonlyres/8DBA0CD9-5845-4C3D-832F-70E12B87F27C/0/Ni_sulfate_EU_RAR_HH_March_2008_finaldraft.pdf
Les nanoparticules
FTE 2015 Importer
D'après l'ANSES36 (2013), les composés nanoparticulaires du nickel ayant été enregistrés dans le cadre de la réglementation sur les nanoparticules, ainsi que leurs usages, sont les suivants :
Tableau 7. Composé nanoparticulaires du nickel, d'après l'ANSES (2013).
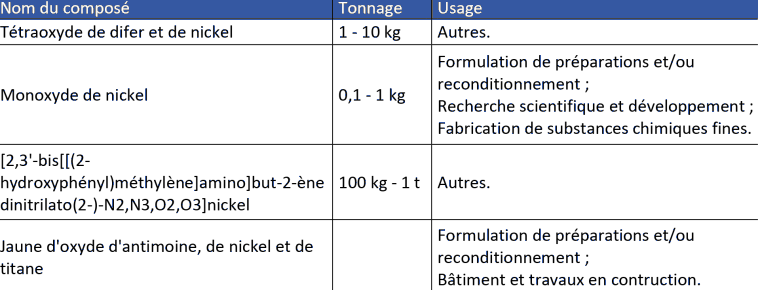
Réalisation d'alliages contenant du nickel
FTE 2015 Importer
Selon le site internet CNUCED, le nickel est actuellement l'additif le plus répandu dans les alliages modernes. La proportion de nickel dans l'alliage est très variable selon les propriétés souhaitées. Le Tableau 8 présente quelques-uns de ces alliages ainsi que la proportion de nickel contenu.
[36] Bilan 2013 de déclarations des substances importées, fabriquées ou distribuées en France en 2012. (consulté en mars 2014). http://www.developpement-durable.gouv.fr/IMG/pdf/Rapport_public_format_final_20131125.pdf
Tableau 8. Proportions de nickel contenu dans différents types d'alliages, selon le site internet CNUCED.

A ce jour, plus des quatre cinquièmes de la production mondiale de nickel sont utilisés dans la fabrication d'alliages. Plus de 3000 sortes d'alliages sont recensés, leurs qualités tant physiques que mécaniques ou chimiques sont très variables et modulables en fonction du domaine et de l'emploi que l'on souhaite en faire.
Aciers inoxydables
FTE 2015 Importer
Généralités
Selon le site internet de la SCF, les aciers inoxydables sont des aciers alliés présentant une résistance élevée à la corrosion à chaud ou à froid dans de nombreux milieux. Cette résistance chimique est due à la présence de chrome (à des teneurs supérieures à 10,5 %), qui protège, par passivation (formation d'oxyde Cr2O3 à l'interface alliage-film passif), la surface de l'alliage. La résistance à la corrosion atmosphérique est multipliée par cent par rapport aux aciers courants.
Il existe deux principaux types d'aciers inoxydables : les aciers au chrome ainsi que les aciers au chrome-nickel.
- Aciers au Chrome-Nickel : la nuance de base contient 18 % de Cr et 10 % de Ni (nuance 18-10). Ils allient une grande résistance à la corrosion avec une bonne aptitude à la déformation facilitant la mise en forme. Ce sont les aciers inoxydables les plus utilisés, dans les industries chimiques, alimentaires, les couverts de table... Ils représentent 76 % de la production d'aciers inoxydables du monde occidental.
- Les aciers austéno-ferritiques contiennent 4 à 7 % de Ni. Ils sont surtout utilisés pour élaborer des aciers moulés.
Production et utilisation d'acier inoxydable
- Production 2011 (Source ISSF37 via le site internet de la SCF) : France 300.103 tonnes, Monde 33 991.103 tonnes et Union européenne 7 528.103 tonnes.
- Utilisation (en % de la consommation mondiale de nickel) : Europe 34 % (Figure 5 d'après le site internet de la société Eramet, chiffres de 2000).
Figure 5. Consommation d'acier inoxydable par zone en 2000, d'après le site internet d'Eramet.
- Secteurs d'utilisation en 2011, dans le monde (site internet de la SCF38) :

[37] International Stainless Steel Forum.
[38] (consulté en janvier 2014). http://www.societechimiquedefrance.fr/extras/Donnees/mater/acin/cadacin.htm
Utilisations diverses :
- Chimie : l'utilisation des aciers inoxydables a débuté en 1920, dans l'industrie de l'acide nitrique ;
- Equipements ménagers : tambours de lave-linge, éviers, couverts, plats, casseroles, ...
- Pièces de monnaie : utilisation mondiale d'environ 180 000 t.an-1 ;
- Bâtiment : en France, 3 millions de m 2 de toits sont recouverts d'inox. En France, le bâtiment représente 10 % de la consommation d'aciers inoxydables ;
- Véhicules et transports : trains, métro, pots d'échappements, ...
- Agro-alimentaire : industries du chocolat, des produits laitiers, cuves et fûts des brasseries, cuves viticoles (17 % du vin français est stocké dans de l'acier inoxydable ; 70 % des fûts à bière sont en acier inoxydable). En Europe de l'Ouest, le marché est de 3,7 millions de cuves par an dont 250 000 en France. La consommation mondiale d'acier inoxydable dans ce secteur est de 30 000 t.an-1 ;
- Nucléaire : outre la cuve principale du réacteur Super Phénix l'acier inoxydable est également utilisé dans l'industrie nucléaire pour stocker des déchets à haute et moyenne activité. La consommation d'acier inoxydable dans ce secteur est, en France, de 7 500 t.an-1 .
Superalliages
FTE 2015 Importer
Selon le site internet de la SCF, ces alliages résistent mécaniquement et chimiquement à de hautes températures. Ils sont, par exemple, à la base du développement des turboréacteurs utilisés en aéronautique39 .
Ces superalliages sont en général destinés à l'aéronautique, aux réacteurs chimiques, à la cryogénie et aux centrales thermiques (site internet CNUCED). Selon le site internet de la SCF, ils constituent plus de 50 % de la masse des moteurs aéronautiques où ils sont présents dans :
- les disques de compresseurs et de turbines, et certains arbres, dont les températures de fonctionnement atteignent 650°C ;
- les aubes dont la température est portée à 1000°C ;
- les chambres de combustion où la température peut atteindre 1500-1800°C.
[39] L'amélioration du rendement des turbines aéronautiques est liée à l'accroissement de la température d'entrée de la turbine. L'accroissement moyen de cette température depuis 1970 a été d'environ 15°C.an-1 , la contribution relative aux matériaux étant d'environ 7°C.an-1 .
Nickelage
FTE 2015 Importer
Selon le site internet CNUCED, le nickel possède comme qualité d'être inoxydable à l'air dans des conditions normales et d'offrir un bel éclat. Il peut donc être employé afin de nickeler des pièces en fer (qui s'oxydent à l'air), en cuivre ou en laiton (qui perdent facilement leur éclat).
Selon le site internet de la SCF, les pièces appelées « chromées » sont en fait essentiellement nickelées. Elles sont constituées d'acier recouvert par une couche de 20 à 30 mm de nickel sur laquelle est déposée une mince pellicule de chrome (de 0,2 à 0,3 mm) ou parfois d'un autre métal destinée uniquement à faciliter l'entretien. Selon le site internet de SFTS40 , les principaux secteurs d'activité dans lesquels le nickelage intervient sont :
- les équipements collectifs ;
- les équipements médicaux (lits, fauteuils, …) ;
- les cycles ;
- les équipements publicitaires (présentoirs, …) ;
- l'outillage ;
- les équipements de loisir ;
- les équipements de manutention ;
- l'automobile et les poids-lourds ;
- la ventilation ;
- l'électronique ;
- la tôlerie ;
- le bâtiment ;
- la tringlerie ;
- les équipements agro-alimentaires ;
- la mécanique ;
- le matériel agricole ;
- …
[40] Société Forézienne de Traitement de Surface.
Le nickelage a lieu selon deux méthodes (électrolytique ou chimique) :
- Nickelage par électrolyse : méthode la plus courante. La pièce à revêtir constitue la cathode, l'anode est formée de "carrés" de nickel pur placés dans des paniers en titane. La solution du bain d'électrolyse contient des composés du nickel, notamment du sulfate et du chlorure de Ni2+ .
- Nickelage par réduction chimique : les pièces à revêtir sont immergées dans une solution d'ions Ni2+ contenant un réducteur. On obtient ainsi des dépôts très durs, d'épaisseur uniforme.
En France comme dans les autres pays de l'UE, l'activité de production d'acier traité zinc-nickel a augmenté de façon continue entre 1992 et 2001 et connu une légère baisse en 2002 (European Commission, 2005a).
Autres aciers
FTE 2015 Importer
Selon le site internet de la SCF, du nickel peut également être incorporé à d'autres aciers (aciers de construction) afin d'en augmenter la résistance mécanique. Par exemple :
- 9 % de nickel sont introduits dans les aciers afin de les rendre résistants au froid ;
- 36 % de nickel sont introduits afin d'obtenir un acier possédant un coefficient de dilatation nul.
Ainsi, selon le site de la SCF, d'autres utilisations minoritaires du nickel métallique peuvent être rapportées, par exemple :
- Cupro-nickel : Cu et Ni sont miscibles en toutes proportions. Ces alliages possèdent une excellente résistance à la corrosion par l'eau de mer. Leurs propriétés mécaniques et chimiques sont d'autant meilleures que la teneur en Ni est plus élevée. Les cupronickels à 40-45 % de Ni ont leur résistivité qui ne varie pas en fonction de la température (utilisation dans les thermocouples) ;
- Maillechorts : de 9 à 26 % de Ni (et de 17 à 28 % de Zn). Leurs propriétés sont intermédiaires entre celles des laitons et des cupronickels et ils sont utilisés en orfèvrerie ;
- Alliages Ni-Cr : 60 % de Ni (Cr : 35 %, Si : 2 %, Mo : 1 %, Fe : 1 %) utilisés pour réaliser des couronnes et bridges dentaires ;
- Alliages Inconel 600 : alliages à base de Ni (contenant au minimum 72 % de Ni + Co, 14 à 17 % de Cr et 6 à 10 % de Fe selon le site internet Special Metals41). Ces alliages qui étaient utilisés pour certaines pièces des réacteurs nucléaires à eau pressurisée des centrales françaises sont sensibles à la corrosion sous contrainte et les pièces présentent des fissures. Ils sont remplacés par l'Inconel 690 (contenant au minimum 58 % de Ni, 27 à 31 % de Cr et 7 à 11 % de Fe selon le site internet Special Metals42) ;
- Développement de l'utilisation d'un alliage Zn-Ni (à 13 % de Ni) pour la galvanisation de tôles pour automobiles ;
- Alliages divers : pièces de monnaie de l'Union européenne de 1 et 2 € : la pièce de 1 € est laiton de nickel pour l'anneau extérieur et comporte trois couches (cupro-nickel, nickel, cupro-nickel) pour la partie centrale, la pièce de 2 € est en cupro-nickel pour l'anneau extérieur et comporte trois couches (laiton de nickel, nickel, laiton de nickel) pour la partie centrale (site internet de l'Euro43) ;
- Catalyseur (Ni-Al) d'hydrogénation pour la fabrication de l'acide adipique ;
- Alliages (Ni-Ti) à mémoire de forme : l'alliage TiNi (50/50 atomique) a été le premier alliage à mémoire de forme fabriqué industriellement.
Batteries
FTE 2015 Importer
Dans le cadre de l'arrêté du 26 juin 2001, l'ADEME a été chargée de la mise en place de l'Observatoire des piles et accumulateurs. Chaque année, les acteurs de la filière doivent transmettre une déclaration relative aux flux mis sur le marché, collectés, valorisés ou éliminés. Les données issues des déclarations pour l'année 2012 sont les suivantes. Plus de 141 millions d'accumulateurs de moins de 1 kg (dits portables), soit plus de 8 708 tonnes ont été mis sur le marché. 2 160 tonnes sont des accumulateurs Ni-Cd (Nickel -Cadmium), 952 tonnes des accumulateurs Ni-Cd (Nickel -Cadmium), 865 tonnes des accumulateurs au plomb, 1 740 tonnes des accumulateurs NiMH (Nickel Métal Hydrure) et 5 114 tonnes des accumulateurs Li-ion (Lithium-ion). Ces deux dernières technologies se développent très rapidement.
[41] (consulté en janvier 2014). http://www.specialmetals.com/documents/Inconel%20alloy%20600%20(Sept%202008).pdf
[42] (consulté en janvier 2014). http://www.specialmetals.com/documents/Inconel%20alloy%20690.pdf
[43] (consulté en janvier 2014). http://www.ecb.europa.eu/euro/coins/common/html/index.fr.html
Batteries Ni-Cd
Selon le site de la SCF, dans le domaine des accumulateurs (piles rechargeables) Ni-Cd, la matière constituant l'anode est un mélange pulvérulent d'hydroxyde de nickel et de graphite, celle constituant la cathode est un mélange d'hydroxyde de cadmium mélangé à d'autres substances.
Selon Robert et Alzieu (2005), il apparaît que les performances techniques de l'accumulateur nickel-cadmium sont assez largement comparables à celles des accumulateurs au plomb. Néanmoins, ce bilan est influencé défavorablement par deux facteurs. Les prix du nickel et du cadmium, ainsi que ceux des procédés de fabrication, conduisent à un coût de l'énergie stockée largement supérieur à celui associé à l'accumulateur au plomb. Enfin, la manipulation du cadmium n'est pas sans danger pour la santé et la mise au rebut des batteries usagées présente un risque pour l'environnement. Dans ces conditions, pour l'Europe de l'Ouest, le marché de l'accumulateur nickel-cadmium représente aujourd'hui environ 10 % de celui de l'accumulateur au plomb.
Les applications grand public sont en décroissance rapide, alors que les applications industrielles (ferroviaire, aviation, véhicules électriques) se maintiennent. Les accumulateurs Ni-Cd ne représentent cependant que 2 % des accumulateurs industriels, leur immense majorité étant au plomb (Commission européenne, 2003).
La société française SAFT est un acteur majeur de ce marché. Seul fabricant français, elle emploie 4 000 personnes dans le monde. Son chiffre d'affaires global est d'environ 598 millions d'euros pour l'année 2012 (site internet SAFT). La production d'accumulateurs Ni-Cd pour l'industrie représente 50 % à 60 % de son activité (premier rang en Europe).
L'emploi du couple Ni-Cd subsiste pour des piles et batteries rechargeables grand public, mais est désormais marginal pour des batteries de téléphones mobiles et d'ordinateurs portables. En revanche, leur emploi reste important pour les outils portables (Noréus, 2000).
Batteries Ni-Fe
Selon Robert et Alzieu (2005), l'accumulateur nickel-fer a des performances spécifiques et une durée de vie comparables à celles du couple nickel-cadmium, mais l'accumulateur nickel-fer est pénalisé par un rendement de charge faible, une autodécharge importante et un comportement médiocre à basse température. Par contre, le fer est un matériau plus pratique d'emploi que le cadmium du fait de son faible prix et de son absence de toxicité.
Dans cette situation contrastée, le développement de l'accumulateur nickel-fer a été lent et limité à quelques pays, dont les États-Unis, tandis que ses applications se sont longtemps identifiées à celles du nickel-cadmium (stationnaire, installations de secours et d'alarme, traction lourde...). Elles se sont étendues, quelques années durant, de façon limitée, au véhicule électrique. Aujourd'hui, ce type d'accumulateur n'a plus les faveurs des acteurs influents du domaine.
Batteries Ni-hydrure métallique
Selon Robert et Alzieu (2005), cet accumulateur est habituellement désigné par le symbole Ni-MH. Un gain significatif en énergie volumique favorise le développement du système Ni-MH au détriment du système Ni-Cd. Cela étant, l'accumulateur Ni-MH est le siège d'une autodécharge et est médiocrement adapté aux régimes rapides en charge comme en décharge. Par contre, l'accumulateur Ni-MH fait beaucoup mieux en régime impulsionnel (utile dans le domaine du véhicule hybride44).
Dans le domaine des équipements autonomes ou portables et des voitures électriques, les accumulateurs Ni-MH, après avoir dépassé, aussi bien en nombre d'unités qu'en capacité globale, les accumulateurs Ni-Cd, sont aujourd'hui en perte de vitesse devant le Li-ion.
Batteries Ni-Zn
Une société a récemment mis en service une unité pilote de production de batteries nickel-zinc. Bien que la composition de ce type de batterie reste confidentielle, l'évolution du marché45 ainsi que les qualités affichées par le producteur46 suggèrent de suivre l'évolution de ce type de batteries dans les années à venir.
Selon France ST (2005), ce nouveau type de batterie parvient à éviter la dissolution du zinc pendant la phase de décharge (qui, jusqu'à présent, se reformait de manière anarchique pendant la recharge, ce qui avait pour conséquence d'encrasser la batterie et de provoquer des courts-circuits).
Batteries ZEBRA47
Les batteries ZEBRA (Zero Emission Batteries Research Activity) sont à base de chlorure de nickel pour l'électrode positive et de sodium pour l'électrode négative. Cette technologie a été mise au point pour les applications véhicules électriques, transport lourd et transport
[44] Le développement du véhicule hybride paraît plus probable aujourd'hui que celui du véhicule électrique, l'adoption de l'accumulateur Ni-MH suppose des gains en puissance spécifique. Cette perspective n'est pas irréaliste, car l'accumulateur Ni-MH, plus récent que les deux autres systèmes, dispose certainement d'une marge de progression. Les véhicules hybrides, aujourd'hui commercialisés, portent d'ailleurs témoignage de ces progrès (Robert et Alzieu, 2005).
[45] le marché des batteries pèse 20 milliards d'euros en 2004 et devrait atteindre 70 milliards d'ici 2014-2019 (Barbotin, 2004).
[46] Performances approchant celle de batteries lithium pour un coût inférieur.
[47] (
public. Elle semble réservée à des marchés de niche et est considérée par certains promoteurs de cette filière comme une technologie de transition.
Usage du nickel dans le secteur de l'automobile (hors batteries)
FTE 2015 Importer
Selon le site internet de la SCF, les automobiles produites aux États-Unis contiennent environ 1 kg de nickel ainsi, l'industrie automobile représente de 6 à 8 % de la consommation de Ni du monde (pièces nickelées et alliages).
Ainsi, selon le site euro-inox48 , l'acier inoxydable et les pièces dites chromées sont couramment utilisés dans l'échappement automobile. Des pièces diverses telles que des tuyaux flexibles et des colliers de serrage sont utilisés dans le compartiment moteur où la résistance à la corrosion est d'une importance primordiale. Par ailleurs, il existe un potentiel de développement dans les applications structurales. Grâce à leurs remarquables caractéristiques mécaniques, les composants en acier inoxydable peuvent être plus légers que leurs homologues réalisés en « alliage léger ». Leur aptitude à la consolidation permet également d'améliorer l'absorption d'énergie.
De nos jours les pièces "chromées" sont très fortement concurrencées par les plastiques (en particulier pour les pièces chromées esthétiques : pare-chocs). Néanmoins, pour les années à venir, un certain usage des pièces nickelées en automobile devrait se maintenir via le phénomène « tuning ».
Chimie
FTE 2015 Importer
Selon le site internet de Nickel Institute et European Commission (2003), le rôle du nickel comme catalyseur dans des processus chimiques est peut-être la moins connue de ses utilisations. Plusieurs composés du nickel sont aussi utilisés comme catalyseurs, dont notamment le chlorure de nickel, le sulfure de nickel, le sulfate de nickel, le nitrate de nickel, le disulfure de nickel, le nickel bis(2-ethylhexanoate), l'oxyde de nickel et le nickel tétracarbonyle. Cependant, les catalyseurs à base de nickel finement divisé sont indispensables à plusieurs réactions importantes, y compris l'hydrogénation d'huiles végétales, la reformulation des hydrocarbures ainsi que la production d'engrais, de pesticides et des fongicides.
Plus en détail, le site internet de la SCF présente l'exemple d'un catalyseur (Ni-Al) destiné à l'hydrogénation pour la fabrication de l'acide adipique. De même, on rapporte également l'hydrogénation de l'acide oléique (acide cis-9-octadecenoïque C17H33COOH), liquide, en acide stéarique (acide octadecanoïque C17H35COOH), solide, sur du nickel finement divisé. Cette hydrogénation est encore largement utilisée de nos jours dans de nombreux domaines
[48] (consulté en janvier 2014). http://www.euro-inox.org/
(alimentation, pharmacie, savonnerie, parfumerie, peinture,...) et le nickel reste le catalyseur phare.
La liste complète des réactions réalisées en présence d'un catalyseur contenant du nickel est impossible à dresser dans le cadre de cette fiche, néanmoins, on peut se reporter au rapport publié en 2003 (European Commission) pour plus de détails. On peut toutefois donner un aperçu des composés organiques qui font intervenir le nickel comme catalyseur :
- Alcools (ethylhexanol, isopropanol, oxo alcools);
- Amines aliphatiques (ethyl et isopropylamines) et amines aromatiques ;
- Nitriles ;
- Toluène Di Isocyanate (TDI) ;
- Cyclohexane.
Dans le cas de l'ethylhexanol, on emploie de l'ordre d'un kg de nickel par tonne de produit, et les pertes de catalyseur, inférieures à 0,4 kg par tonne de produit, sont recyclées pour récupérer le nickel.
Dans le cas du cyclohexane, le procédé en phase aqueuse utilise quelques tonnes de recyclage par an pour une usine typique, qui est recyclé pour récupérer le métal.
Le nickel est employé comme catalyseur dans l'oxydation catalytique des COV (European Commission, 2002).
En dehors de l'emploi comme catalyseur, le nickel est aussi utilisé comme réactifs pour produire des composés organométalliques, comme des dithiocarbamates métalliques. Ce composé (nickel dithiocarbamate), est utilisé comme additif antidégradant pour caoutchoucs, et protège les pièces en caoutchouc pendant leur durée de vie contre les dégradations liées à l'oxygène de l'air ou à l'ozone. Il est produit en France par MLPC International (Groupe Arkema) sur le site de Lesgor en Aquitaine.
Enfin, le nickel est présent, en combinaison avec du graphite, dans certains élastomères conducteurs à base de silicone.
UTILISATIONS
FTE 2015 Importer
L'Europe représentait 19% de la consommation d'antimoine en 2011, devancée par l'Asie (59%) et à égalité avec l'Amérique du Nord (15%) (European Commission, 2014).
L'antimoine sous ses différentes formes est utilisé dans une grande variété de secteurs en vertu de ses propriétés chimiques (résistance à la corrosion, mauvais conducteur d'électricité et de chaleur) :
Figure 9 : Répartition de la consommation d'antimoine en UE (2011)

RETARDATEURS DE FLAMME ET PLASTURGIE
L'antimoine, sous sa forme oxydée (Sb2O3 et Sb2O5), est principalement utilisé dans le secteur des retardateurs de flamme servant dans les plastiques, l'électronique ou encore les vernis (Dupont, Arnout, Jones, & Binnemans, 2016). Il n'est généralement pas utilisé seul mais en tant qu'ignifugeant secondaire ou dans la préparation d'une substance dont la synergie des composants donnera les propriétés ignifugeantes voulues.
Ainsi l'antimoine sera régulièrement associé avec des halogènes (Trifluorure d'antimoine, Tribromure d'antimoine, trichlorure d'antimoine) comme les retardateurs de flamme bromés (RFB) (Gensch, Baron, Blepp, Bunke, & Moch, 2014) entrant dans la composition de nombreux polymères (PVC, PE, Polyester…).
On le trouvera notamment dans la confection des gaines isolantes servant dans la plupart des appareils électroménagers et dans l'industrie automobile (BRGM 2011). On peut le retrouver aussi dans la confection de film plastiques, packaging, bouteilles, vêtements, tapis et rideaux, prises électriques, parechocs, matériaux pour l'aérospatiale, résines, adhésifs par exemple (BRGM 2011) (Gensch, Baron, Blepp, Bunke, & Moch, 2014).
En plus de ces applications en tant que retardateur de flamme dans la plasturgie, on va également retrouver l'antimoine en tant que catalyseur dans les processus d'estérification des fibres et résine de PET (Polytéréphtalate d'éthylène) et comme stabilisateur de chaleur, par exemple dans le processus de fabrication du PVC bien qu'il s'agisse d'un marché un peu plus restreint mais en augmentation constante (BRGM, 2011).
BATTERIE PLOMB-ACIDE ET ALLIAGES METALLIQUES
L'antimoine est aussi utilisé dans la fabrication des batteries plomb-acide, en effet il va permettre de durcir le plomb et d'augmenter sa résistance à la corrosion. On parle ici d'une teneur de 10 à 12%. Il s'agit d'un marché amené à se réduire avec la baisse des teneurs en antimoine dans les batteries pour des raisons d'efficience au profit du calcium, de l'étain, ou encore de l'aluminium (Dupont, Arnout, Jones, & Binnemans, 2016).
L'antimoine entre dans la composition de nombreux autres alliages avec des métaux accroissant leur durabilité comme le zinc, l'étain, le cuivre, le fer pour ne citer qu'eux. En plus des batteries, on va aussi le retrouver dans la confection de tôles, tuyaux, soudures, paliers à roulement, ceinture de convoyage, « métal anglais » (couverts), matériaux antifrictions, munitions, dans le brunissage du fer, les piles thermoélectriques ou encore les semi-conducteurs (électrodes, transistors…) pour l'électronique (allié à l'Indium ou encore l'étain) et autrefois les caractères d'imprimerie (BRGM, 2011).
L'utilisation dans les munitions pourrait donner lieu à des émissions dans l'environnement (munitions de chasse actuelles, ou anciennes zones de conflit).
PEINTURES, CÉRAMIQUES, VERRES ET AUTRES
L'antimoine entre dans la fabrication des pigments (Jaunes de Naples, Jaune Titane…) et de vernis pour la peinture, notamment les peintures à l'eau (INRS, 2005). Il s'agit donc d'un usage pouvant donner particulièrement lieu à des émissions vers les réseaux d'eau usée et les milieux aquatiques.
Dans le secteur militaire, Il entre aussi dans la confection de peintures réfléchissant les infra-rouges (Douay, et al., 2008) (Anderson, 2012).
Dopé à l'oxyde d'étain, l'antimoine entre dans la coloration des composants électroniques (BRGM, 2011). Il entre aussi dans la confection d'émail durcissant et ignifugeant pour la poterie mais aussi d'agent opacifiant pour les porcelaines (BRGM, 2011). Outre les céramiques et les peintures, on peut le retrouver dans la verrerie comme agent opacifiant (INERIS, 2007) ou décolorant pour les verres optiques des appareils photos, photocopieuses, jumelles ou encore les tubes fluorescents (Dupont, Arnout, Jones, & Binnemans, 2016). Enfin il est utilisé en très petite quantité (<1%) dans la confection des tubes cathodiques pour les anciens écrans de télévision, d'ordinateur qui sont supplantés par les écrans à LED (BRGM, 2011).
L'antimoine trouve encore d'autres applications mineures telles que (BRGM, 2011) :
- Médicaments émétiques antiparasitaires contre la leishmaniose (glucantime, pentostam) (BRGM, 2011).
- Sous forme sulfurique (SB2S3) on peut le retrouver dans des applications pyrotechniques comme les feux de Bengale, explosifs, bombes fumigènes, balles traçantes, allumettes et les feux d'artifices (INERIS, 2007).
- Lubrifiants : pour ses propriétés antifriction, du trioxyde d'antimoine est appliqué sur les plaquettes et disques de freins dans l'automobile, ce qui est une source non négligeable de rejets d'antimoine dans l'atmosphère (Tian, et al., 2014).
- Agent de vulcanisation du caoutchouc rouge (Dupont, Arnout, Jones, & Binnemans, 2016).
Rejets dans l’environnement
Sources naturelles
FTE 2015 Importer
La teneur moyenne de l'écorce terrestre en nickel est de 75 ppm 49 . Cette teneur peut varier selon la localisation de 0,7 à 259 mg Ni/kg50 .
Le FOREGS51 construit des cartes montrant les concentrations en nickel dans 26 pays européens et dans différents milieux (sol couche profonde et de surface, humus, sédiments de cours d'eau et de plaines alluviales et l'eau). Ces cartes montrent de grandes différences entre les régions. Ainsi le sud de la Scandinavie, le nord de l'Allemagne, la Pologne et les pays baltes présentent des teneurs en nickel inférieures à 6 mg/kg, tandis que la Grèce, le nord de l'Italie, la Slovénie et la Croatie présentent des teneurs supérieures à 40 mg/kg (supérieure à 80 mg/kg dans le cas de la Grèce). La France présente des teneurs variant entre 10 et 40 mg/kg selon les régions et le type de sol.
Bennett (1981) a estimé (tous milieux confondus) les rejets naturels de nickel à l'échelle mondiale :
- poussières éoliennes: 4 800 t.an-1 ;
- volcans: 2.500 t.an-1 ;
- végétation: 800 t.an-1 ;
- incendies de forêts: 200 t.an-1 ;
- poussières de météorites: 200 t.an-1 ;
- projections d'eau de mer: 9 t.an-1 ;
Le total de ces rejets atteint 8,5.103 t.an-1 .
[49] Site internet de la société chimique de France : (consulté en décembre 2013). http://www.societechimiquedefrance.fr/extras/Donnees/acc.htm
[50] (consulté en décembre 2013). http://www.nickelinstitute.org/Sustainability/EnvironmentalQuality/Soil.aspx
[51] Forum of the European Geological Surveys : Atlas Géochimique de l'Europe : (consulté en décembre 2013). http://weppi.gtk.fi/publ/foregsatlas/
Sources non-intentionelles
FTE 2015 Importer
Sans objet
Émissions anthropiques totales
FTE 2015 Importer
Dans le cadre de l'étude « Source screening of priority substances under the WFD » (Directive Européenne « Water Framework Directive »ou Directive Cadre sur l'Eau établie en 2000) une évaluation datée de 2003 a été menée pour le nickel (cf. Tableau 9).
Selon le site internet de l'IREP52 (registre français des émissions polluantes), en France, pour l'année 2012, 248 établissements industriels étaient répertoriés en tant qu'émetteurs de nickel dans l'environnement (air, eau, sol). Parmi ces établissements, 64 rejetaient du nickel dans l'air, 126 dans l'eau directement, 20 dans l'eau indirectement et 72 dans les sols. Tous milieux confondus, les rejets industriels de nickel sont donc extrêmement diffus et disséminés à l'échelle du territoire national.
[52] Registre Français des Emissions Polluantes (consulté en janvier 2014). http://www.pollutionsindustrielles.ecologie.gouv.fr/IREP/index.php
Tableau 9. Source et importance des voies de contamination en nickel des eaux de surface, d'après WFD, 2003.

[53] L'Union européenne a une série de règles communes sur l'octroi d'autorisations aux installations industrielles. Ces règles sont exposées dans la directive IPPC de 1996.
Les rejets de nickel par les industries productrices ou utilisatrices de nickel sont estimés dans le Tableau 10.
Tableau 10. Estimation des rejets de nickel, d'après Danish EPA, 2008a.
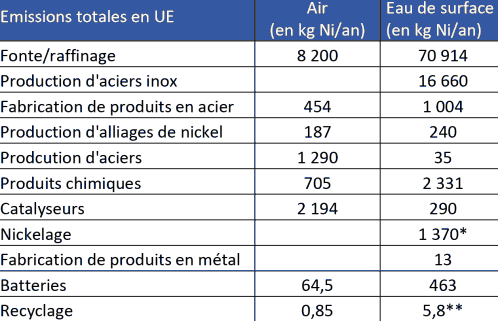
[*] vers les eaux de surface et les égouts
[**] vers les égouts
Émissions atmosphériques
FTE 2015 Importer
Emissions françaises
En France, selon l'INS54 , les émissions de nickel en 2007 étaient réparties sur le territoire comme le montre la figure ci-après.
[54] Inventaire National Spatialisé : (consulté en mars 2014). http://90.83.82.201/ins-webapp/

Figure 6. Répartition des émissions de nickel en France en 2007, d'après l'INS.
Les départements ayant émis le plus de nickel en 2007 étaient le Nord, l'Aisne, la Seine-Maritime, les Yvelines, la Seine-et-Marne, la Marne, le Bas-Rhin, la Loire-Atlantique, le Rhône et les Bouches-du-Rhône.
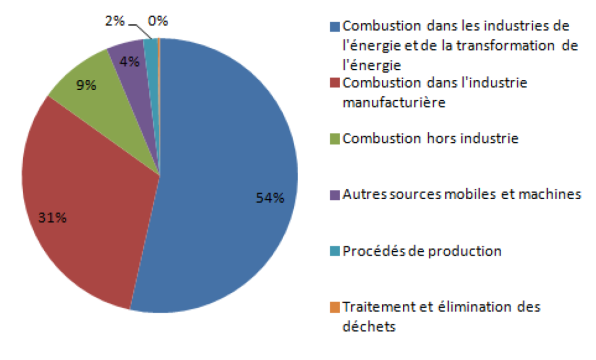
Figure 7. Secteurs émettant du nickel en France en 2007, d'après l'INS.
Les deux secteurs émettant le plus de nickel en France en 2007 étaient la combustion dans les industries de l'énergie et de la transformation d'énergie (53 %) et la combustion dans l'industrie manufacturière (32 %).
Selon le site internet du CITEPA55 , le nickel et ses composés sont principalement rejetés dans l'air par les sous-secteurs industriels suivants (sous-secteurs prépondérants en 2011 pour la France métropolitaine) :
Ces mêmes données peuvent être présentées sous forme graphique dans la Figure 8.
[55] Centre Interprofessionnel Technique d'Etudes de la Pollution Atmosphérique : (consulté en janvier 2014). http://www.citepa.org/fr/pollution-et-climat/polluants/metaux-lourds/nickel
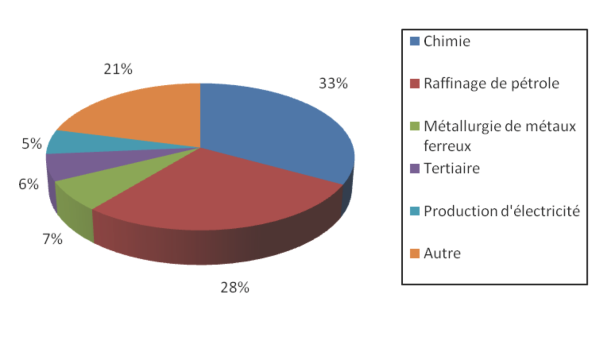
Figure 8. Secteurs industriels responsables des rejets atmosphériques de nickel et de ses composés, d'après les données du CITEPA, 2011.
Les rejets atmosphériques ont représenté 76 tonnes en 2011. Ce chiffre correspond au minimum des rejets jamais rapportés (rejets suivis depuis 1990). La diminution observée de 1990 à 2011 équivaut à – 75 % (Figure 9).
Selon les chiffres publiés par le CITEPA (2013), deux secteurs prédominent majoritairement dans les émissions de nickel : l'industrie manufacturière (consommation de fioul lourd et installations sidérurgiques) et la transformation d'énergie (en grande majorité le raffinage du pétrole) avec respectivement 50 % et 38 % des émissions totales en France métropolitaine en 2011. Les émissions de nickel sont essentiellement expliquées par de la présence de ce métal à l'état de traces dans le fioul lourd. La baisse des émissions de nickel est due à une diminution de la consommation de fioul lourd.
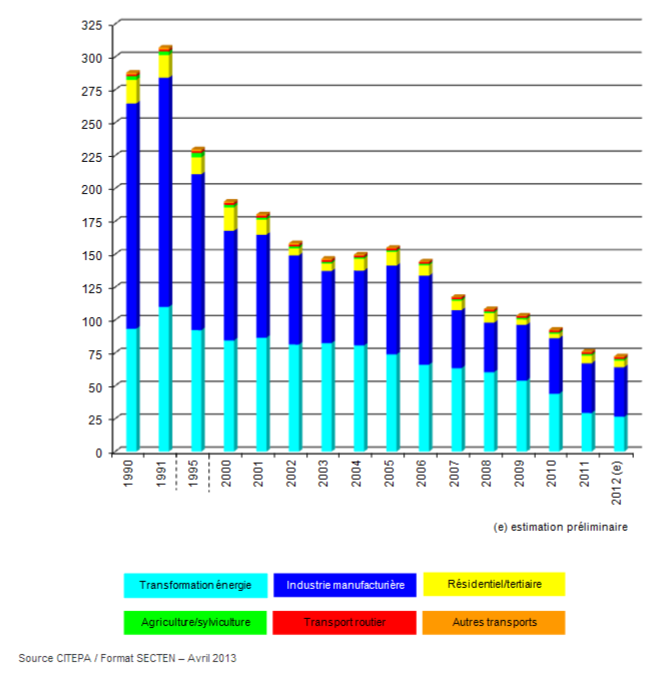
Figure 9. Émissions de nickel dans l'air en France métropolitaine, en tonnes, d'après CITEPA, 2013.
Selon INERIS (2006), le nickel émis dans l'atmosphère par des sources anthropiques l'est principalement sous forme d'aérosols, ce qui couvre une très large gamme de taille de
particules56 . Les émissions des centrales électriques sont associées à des particules de plus petite taille que celles émises par des fonderies. Les particules contenant du nickel peuvent atteindre des demi-vies de l'ordre d'une semaine à un mois (Hertel et al., 1991 ; ATSDR, 1997).
La nature du nickel présent dans des particules d'origine anthropique varie selon l'origine de ces particules (Hertel et al., 1991 ; ATSDR, 1997). Ainsi, les émissions de nickel issues de la combustion d'huiles se présentent principalement sous forme de sulfates. Les cendres volantes provenant de la combustion du charbon contiennent majoritairement du nickel sous forme d'oxydes complexes de fer. L'extraction minière et la fonte du minerai de latérite émettent dans l'atmosphère des silicates de nickel et des oxydes fer-nickel. Le raffinage des mattes conduit à des émissions de nickel métallique et de sulfure de nickel.
Le site européen E-PRTR regroupe les émissions des 27 Etats membres de l'Union européenne ainsi que l'Islande, le Liechtenstein, la Norvège, la Serbie et la Suisse. Selon le site internet E-PRTR57 , les émissions de nickel atmosphériques françaises représentent 17 % des émissions européennes totales en 2011.
Le site internet E-PRTR, pour la France, pour 205 établissements répertoriés, rapporte 58 établissements émettant du nickel vers l'atmosphère pour l'année 2011 et des émissions de nickel de 41,2 tonnes (soit environ 54 % des émissions rapportées par le CITEPA).
Émissions vers les eaux
FTE 2015 Importer
Rejets industriels dans les eaux européennes
Le nickel et ses composés peuvent atteindre les eaux de surface s'ils sont présents dans les eaux usées rejetées par des sites industriels.
Au niveau européen, le site internet E-PRTR présente les émissions directes (Figure 10) de nickel et de ses composés vers l'eau (année 2011) pour 1 125 installations industrielles.
[56] Selon l'ATSDR (1997) le diamètre moyen des particules d'origine anthropique contenant du nickel est de 5,4 μm.
[57] Registre européen des rejets et des transferts de polluants : (consulté en janvier 2014). http://prtr.ec.europa.eu/PollutantReleases.aspx
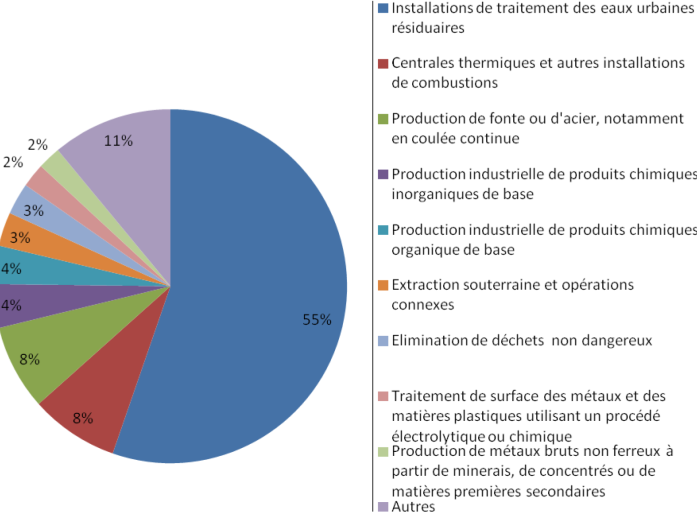
Figure 10. Emissions de nickel vers l'eau en Europe en 2011, d'après le site internet E-PRTR.
Selon le site internet E-PRTR, les émissions françaises de nickel vers les eaux de surface représentent 6 % des émissions européennes totales. Il convient de préciser que ces données d'émission n'incluent pas la Nouvelle-Calédonie58 .
Le BREF sur les installations de traitement des déchets dangereux indique que la concentration moyenne dans leurs effluents en Europe varie de <0,01 à 0,1 mg.L-1 (en 2002, pour 9 installations répertoriées) (European Commission, 2005c).
[58] De par son statut territorial particulier (Pays d'Outre Mer ou POM), la Nouvelle-Calédonie n'est pas soumise aux obligations liées à la Directive Cadre sur l'Eau.
D'après (European Commission, 2005), les valeurs typiques d'émissions de nickel par les aciéries (sites non équipés de système de traitement des effluents gazeux) sont 0,015 mg.Nm-3 (mg.m-3 à 0°C et sous une pression de 1.013 bar). D'autre part, lorsque des telles installations sont équipées de systèmes de "lavage" des effluents gazeux, les teneurs en nickel observées dans les rejets liquides atteignent 0,04 à 0,23 mg.L-1 .
Rejets industriels français
Parmi les 248 établissements industriels émetteurs de nickel répertoriés sur le site internet IREP (France métropolitaine, Guyane, Guadeloupe, Martinique et Réunion uniquement), seuls 146 établissements émettent ce métal vers l'eau (émissions directes et/ou indirectes). Ainsi, ces émissions sont estimées pour l'année 2012 à respectivement 16,1 tonnes et 2,4 tonnes pour les émissions directes et indirectes.
Les activités principales de ces établissements industriels sont reprises ci après en fonction de l'importance des rejets observés (Figure 11).
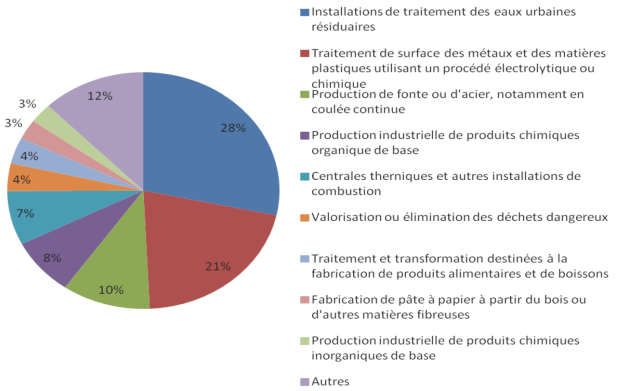
Figure 11. Activités rejetant du nickel vers les eaux en 2011, d'après le site internet E-PRTR.
Rejets dans les eaux du bassin Seine-Normandie
L'Agence de l'eau Seine-Normandie (2004) précise l'origine et l'importance des différents flux de nickel vers les eaux superficielles du bassin Seine-Normandie (le flux total moyen de nickel sur ce bassin est estimé à 75 t.an-1). Ces flux sont représentés de façon graphique dans la Figure 12.

Figure 12. Sources d'émission vers les eaux superficielles du bassin Seine-Normandie ; P : rejets ponctuels, D : rejets diffus, d'après les données de l'AESN, 2004.
Ce graphique souligne l'importance des rejets diffus (l'érosion et le drainage entraînent à eux-seuls plus de 40 % des rejets). De ce fait, même la suppression de tous les rejets ponctuels serait largement insuffisante pour respecter un objectif de « zéro rejets et pertes ».
Parmi les sources à l'origine des rejets diffus de nickel on peut citer :
- Certains procédés de production industriels de métaux utilisent des matières premières contenant des quantités importantes de nickel (en particulier pour l'extraction du fer et du cuivre). Bien qu'aucune information ne soit disponible sur le sujet, cette voie de production accidentelle ne peut-être totalement écartée (en particulier via des pollutions accidentelles historiques).
- Rejets de nickel liés à l'usage d'aciers inoxydables en tant que matériau de construction (toitures à Paris par exemple). A la suite d'expériences de vieillissement d'aciers inoxydables
en laboratoire Wallinder et al. (2006), ont démontré que les quantités de nickel relarguées par ce phénomène entraînent la présence de nickel dans l'environnement.
- Rejets diffus agricoles, du fait de la présence naturelle de nickel dans les sols, et aussi de la présence artificielle en provenance d'engrais phosphatés (la majorité du nickel présent dans les roches phosphorées se retrouve dans l'acide phosphorique, cf. Commission Européenne, 2004).
Émissions vers les sols
FTE 2015 Importer
Rejets industriels français
Pour les 248 établissements industriels émetteurs de nickel répertoriés sur le site internet IREP, seuls 72 sont répertoriés comme émetteurs de nickel vers les sols et les émissions sont estimées pour l'année 2012 à 23,4 tonnes.
Pour les 205 établissements répertoriés sur le site E-PRTR, seuls 28 émettaient du nickel vers les sols en 2011 et ses émissions étaient estimées à 3,20 tonnes.
Selon le site internet E-PRTR, en 2011, les rejets vers les sols concernent les secteurs suivant :
- Fabrication de pâte à papier à partir du bois ou d'autres matières fibreuses : 51,2 % ;
- Fabrication de papier et de carton et d'autres produits dérivés du bois : 20,6 % ;
- Traitement et transformation destinés à la fabrication de produits alimentaires et de boissons : 13,1 % ;
- Elimination des déchets non dangereux : 10,7 % ;
- Fabrication industrielle de produits pharmaceutiques de base : 2,2 % ;
- Traitement et transformation du lait : 1,5 % ;
- Abattoirs : 0,8 %.
Selon le site internet E-PRTR, 32 établissements rejettent du nickel vers les sols, dont 28 en France. Les émissions françaises de nickel vers les sols représentent 91 % des émissions européennes totales.
Rejets dans l'environnement
FTE 2015 Importer
Forme chimique dans l'environnement
Selon INERIS (2006), le nickel à l'état divalent peut former une large gamme de composés et constitue le seul état d'oxydation important du nickel (d'autres états d'oxydation comme le nickel(+4) peuvent être présents dans quelques complexes ou oxydes). Ainsi, le nickel reste très faiblement absorbé par la plupart des organismes vivants, mais est associé en grande partie à la matière particulaire (Kabata-Pendias et Pendias, 1992 ; ATSDR, 1997).
Comportement dans les eaux de surface
Dans les systèmes aquatiques, le nickel existe généralement (selon le pH) sous forme d'ions Ni2+ .
Selon INERIS (2006), les anions présents naturellement (OH -, SO4 2-ou Cl -) ne forment des complexes avec le nickel que dans une faible proportion : par exemple, le complexe Ni(OH)2 ne devient l'espèce dominante qu'au delà d'un pH égal à 9,5. En présence de soufre en milieu aqueux anaérobie, du sulfate de nickel se forme, ce qui limite la solubilité du nickel (ATSDR, 1997).
Le nickel est présent dans les eaux de surface en tant que sels solubles adsorbés ou associés avec des particules argileuses, de la matière organique ou d'autres substances. Le nickel forme des complexes solubles, forts avec OH-, SO4 2-et HCO3 -, cependant ces espèces sont en minorité par rapport à l'ion Ni2+ (Danish EPA, 2008a).
Le nickel est un des métaux les plus mobiles quand il est rejeté dans les eaux, particulièrement dans les eaux polluées, dans lesquelles des éléments organiques vont garder le nickel soluble (Danish EPA, 2008a).
Comportement dans le milieu marin côtier et estuarien
Selon le site internet de l'IFREMER, le transport du nickel vers le milieu marin s'effectue via les fleuves sous formes particulaire et via l'atmosphère, conséquence de l'utilisation des combustibles fossiles et la production de métaux non ferreux. Dans le milieu marin, l'affinité du nickel pour les oxyhydroxydes de fer ou de manganèse constitue la caractéristique essentielle de son comportement géochimique.
Dans les eaux interstitielles des sédiments anoxiques60 on observe des concentrations très faibles de nickel dissous, qui peuvent être attribuées à sa précipitation sous forme de sulfure : dans ce cas le nickel est piégé dans le sédiment. Par contre, dans les sédiments oxiques61 les eaux interstitielles sont fortement enrichies en nickel dissous.
Comportement dans les sols
Bien plus que la teneur totale, la spéciation et l'état physico-chimique du nickel sont des paramètres essentiels à considérer afin d'évaluer son comportement dans l'environnement et en particulier sa biodisponibilité. Ainsi, le nickel incorporé dans certains réseaux minéraux peut se révéler inerte. Dans les sols, les principales formes du nickel, et en particulier NiOH+ , sont adsorbées à la surface d'oxydes amorphes de fer, d'aluminium ou de manganèse (Kabata-Pendias et Pendias, 1992 ; McGrath, 1995 ; ATSDR, 1997) et dans une moindre mesure à la surface de minéraux argileux.
La mobilité du nickel augmente aux pH faibles, alors que l'adsorption sur certains composés adsorbants du sol peut devenir irréversible en milieu alcalin. Si le pH est le paramètre influençant le plus la mobilisation du nickel dans les sols, il faut également tenir compte de la concentration en sulfates (qui réduisent l'adsorption du nickel par complexation) et de la surface spécifique des oxydes de fer présents dans le sol (Hertel et al., 1991 ; McGrath, 1995 ; ATSDR, 1997). La présence de cations tels que Ca2+ ou Mg2+ entraîne également une diminution de l'adsorption du nickel sur les composés du sol, résultat de phénomènes de compétition.
Dans les sols alcalins, les composants majeurs sont Ni2+ et Ni(OH)-, dans les sols acides, les espèces majoritaires sont Ni2+ , NiSO4 et NiHPO4 (Danish EPA, 2008d).
Le nickel rejeté dans les sols va filtrer vers les eaux souterraines ou être lessivé dans les eaux de surface (Danish EPA, 2008d).
Comportement dans l'air
Selon Ontario (2001), le nickel présent dans l'air (dissous ou particules en suspension) peut avoir été rejeté par des activités humaines ou suite à des phénomènes naturels (éruptions volcaniques, incendies de forêts et combustion de météorites dans la haute atmosphère). Le Haut Comité de Santé Publique (2000) estime la participation anthropique aux émissions atmosphériques de nickel à 85 % des émissions totales : les principales sources d'émission
[60] Sédiments au sein desquels l'oxygène est absent et donc indisponible aux réactions physico-biochimiques.
[61] Sédiments au sein desquels l'oxygène est présent et donc disponible aux réactions physico-biochimiques.
humaines sont la métallurgie du nickel, la combustion de fiouls et charbons, l'incinération des déchets et la sidérurgie. On le trouve dans l'air sous différentes formes chimiques (sulfures, oxydes...).
Des données de terrain confirment que le nickel peut être transporté via le compartiment atmosphérique sur de moyennes à longues distances. Néanmoins, d'après le site internet d'Environnement Canada, dans l'atmosphère, le nickel est généralement présent en faibles concentrations dans les particules en suspension ; son temps de séjour est de 5 à 8 jours. D'autre part, d'après la même source, le seul composé gazeux notable du nickel, le tétracarbonylnickel, se décompose dans l'air avec une demi-vie de moins d'une minute.
FTE 2015 ImporterCAUSES NATURELLES DES EMISSIONS D'ANTIMOINE
L'antimoine est naturellement présent dans l'environnement sous différentes formes, principalement dans les sols où les particules sont adsorbées. Il s'agit d'un métalloïde très volatil qui a tendance s'évaporer en cas de combustion, ainsi on évaluerait à 41% des émissions totales dans l'air les émissions naturelles provenant des particules déplacées par le vent, des volcans, aérosols marins, feux de forêts, sources biogéniques (Nriagu, 1989).
Figure 10 : Répartition des émissions naturelles dans l'air

Source: (Nriagu, 1989)
CAUSES ANTHROPOGENIQUES DES EMISSIONS D'ANTIMOINE
REJETS DANS L'AIR
La forme la plus rejetée dans l'environnement serait le trioxyde d'antimoine (Sb2O3).
Les rejets anthropogéniques d'antimoine dans l'air sont liés aux activités suivantes principalement (Tian, et al., 2014) :
- L'industrie des métaux non ferreux (vapeurs et poussières émises par l'industrie minière et métallurgique lors des opérations d'extraction, de fonte et du raffinage des métaux).
- La combustion d'énergie fossile : du fait de la présence d'antimoine dans les sols et sa chalcophilie, on en retrouve des traces dans le charbon et les combustibles fossiles.
- L'incinération des déchets municipaux, du fait de la présence d'antimoine dans une gamme variée de produits plastiques en tant que retardateurs de flamme (gaines isolantes, tapis, vêtement, emballages…), céramiques, peintures, …
- Les produits lubrifiés avec du trisulfure d'antimoine (Sb2S3) : usure des plaquettes et disques de freins dans le domaine des transports avec des concentrations plus élevées autour des voies de circulation embouteillées (Varrica, Bardelli, Dongarra, & Tamburo, 2013).
- L'industrie de la fonte et de l'acier, avec des traces présentes dans la fonte, et en raison des opérations de brunissage de l'acier (procédé chimique visant à altérer la couleur et pouvant accroitre la résistance à la corrosion, et à l'abrasion).
Figure 11 : Répartition des émissions anthropogéniques atmosphériques en Europe par secteurs majeurs (t/Sb)

Figure 12 : Répartition des émissions anthropogéniques atmosphériques mondiales par secteurs majeurs (t/Sb)
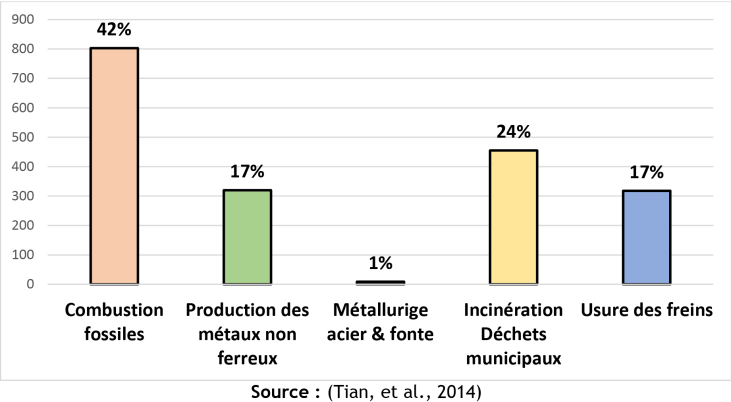
REJETS DANS LES SOLS
La concentration d'antimoine dans les sols serait bien plus élevée dans les sites autour des activités industrielles métallurgiques, minières (poussières, scories, boues) et dans une moindre mesure des décharges municipales (ATSDR, 2017). Une étude illustrant ce phénomène sur des sols pollués dans le nord de la France explique des niveaux importants d'antimoine par l'activité de deux fonderies (Metaleurop Nord et Umicore) ainsi que par la combustion passée de charbon à usage domestique (Douay, et al., 2008). En effet, les sols aux alentours de Metaleurop présentent une teneur moyenne d'antimoine de 28,89 mg.Kg-1 de sol sec (médiane à 13,85) et de 20,85 mg.Kg-1 (médiane à 11,30) pour Umicore soit entre 20 et 25 fois la teneur moyenne des sols agricoles régionaux.
REJETS DANS L'EAU
Les sources anthropogéniques de rejets d'antimoine dans l'eau seront les mêmes que pour les sols (INERIS, 2007). En effet, on retrouvera les facteurs « primaires « tels que les résidus issus des activités minières, métallurgiques ou encore l'utilisation de peintures, vernis et dans un second temps les rejets des stations de traitement des eaux usées (Choubert, et al., 2011). Ainsi, si la concentration moyenne d'antimoine dans les eaux non-polluées est inférieure à 1µg.l-1, elle peut atteindre des niveaux de concentration 100 fois supérieur aux abords des sites industriels qui sont des sources de pollution (Fillela et al, 2012).
L'antimoine, en tant qu'élément chimique, ne peut se dégrader dans la biosphère. On le retrouve sous différentes formes suivant les conditions auxquelles il est exposé (niveau d'oxygène, présence de métaux comme l'arsenic, le fer ou la manganèse…) et généralement sous ses formes oxydées Sb2O3 et Sb2O5 (INERIS, 2007).
COMPORTEMENT ET PRÉSENCE DANS L'AIR
L'antimoine étant très volatil, et suite à l'élévation de sa température, il va s'évaporer généralement sous forme d'oxyde et se déposer sur des microparticules, voyageant ainsi sur de plus ou moins longues distances avec une durée de demi-vie estimée de 1,9 à 3,2 jours dans l'atmosphère (INERIS, 2007). La concentration moyenne dans l'air de l'antimoine varie entre 1 et 170 ng.m-3 mais peut être jusqu'à 1000 fois supérieure à proximité des sources d'émission (ATSDR, 2017).
COMPORTEMENT ET PRESENCE DANS L'EAU
Le comportement de l'antimoine dans l'eau n'est pas bien connu. Sa forme élémentaire Sb est peu soluble (INERIS, 2007), et on peut avancer qu'il est généralement majoritairement présent dans les sédiments et les matières en suspension. Sa forme chimique dépend des conditions (Ph, température, présence de sulfure) et le plus souvent il apparait sous forme pentavalente Sb(V) (Sb(OH)6-et SbO3-) et dans une moindre mesure sous forme trivalente Sb(III) (Sb(OH)3 ou HSbO2). Il serait présent sous forme chloro-hydroxylée dans l'eau de mer (Fillela et al, 2012).
Généralement la présence d'antimoine dans l'eau douce n'excède pas 1 µg.l-1 (Filella et al, 2002) y compris dan les eaux sousterraines, avec une concentration estimée à 200 ng.l-1 dans les océans.
La base de données Naïade recense 10 522 prélèvements d'antimoine24 entre 2015 et 2017 en France dans les eaux de surface (eaux, biotes, sédiments, particules). Les données sont résumées dans le Tableau 6.
[24] 24008 prélèvements dont 10522 sont supérieurs au seuil de quantification et inférieur au seuil de saturation.
Tableau 6 : Présence d'antimoine dans l'eau de surface en France

MES : Matière en suspension
Source : NAIADE
Il n'existe pas de Norme de Qualité Environnementale pour l'antimoine, cependant on peut se référer aux valeurs guide environnementales proposées par l'INERIS avec une concentration maximale acceptable dans l'eau de 177µg.l-1 ou encore aux concentrations acceptables proposées aux Pays Bas pour les sédiments de l'ordre de 14 mg/Kg de matière sèche équivalente (RIVM, 2012). Aucun des prélèvements dans l'eau rapportés dans NAIADE entre 2015 et 2017 n'est supérieur à la concentration maximale acceptable proposée par l'INERIS. Environ 8,5% des prélèvements réalisés dans les sédiments sont supérieurs au seuil proposé de 14 mg/kg. Un tiers des prélèvements d'antimoine dans les biotes (12 sur 36) sont supérieurs à la Valeur Guide Environnementale de 24,3 µg/Kg proposée par l'INERIS (Tableau 2).
COMPORTEMENT ET PRESENCE DANS LES SOLS
L'antimoine présente une concentration moyenne de l'ordre de 0,2 ppm dans la croûte terrestre (BRGM, 2011). Le comportement de l'antimoine dans le sol fait débat et les avis divergent quant à sa mobilité (ATSDR, 2017). Il faut retenir que la sorption et transformation en Ca[Sb(OH)6]2 serait plus importante que la dissolution de trioxyde d'antimoine dans les sols. Celle-ci est régie de manière générale par des paramètres dont les principaux sont le PH, la durée et la présence d'hydroxydes de fer, manganèse ou d'aluminium (RIVM, 2012). Les bases de données ADES et CAPEX ne donnent pas d'informations sur la présence d'antimoine dans les eaux souterraines.
Pollutions historiques et accidentelles
FTE 2015 Importer
En France, le site internet BASOL59 du Ministère de l'Ecologie et du Développement Durable recense les sites pollués au nickel :
[59] Base de données BASOL sur les sites et sols pollués (ou potentiellement pollués) appelant une action des pouvoirs publics, à titre préventif ou curatif.
- 20 sites son mis en sécurité et/ou doivent faire l'objet d'un diagnostic ;
- 184 sites sont en cours d'évaluation ;
- 128 sites sont en cours de travaux ;
- 447 sites ont été traités avec surveillance et/ou restriction d'usage ;
- 27 sites ont été traités et sont libres de toute restriction.
Présence environnementale
Atmosphère
FTE 2015 Importer
Selon le site internet « Public Health » de la Commission européenne, des mesures sur les espèces de nickel présentes dans l'air ambiant (mesures moyennes journalières) ont été effectuées en deux sites à Dortmund (Allemagne) : cf. Tableau 12.
Tableau 12. Mesures des espèces de nickel présentes dans l'air ambiant, d'après le site internet Public Health.

Marlière et al. (2002), fournissent quelques indications quantitatives quant à la présence de nickel dans l'air de différents types de site (typologie définit par l'occupation des sols) :
- sites industriels et urbains : de 70 à 95 ng.m -3 ;
- sites industriels urbains et sub-urbains : de 4 à 140 ng.m -3 (moyenne de 33) ;
- sites urbains : de 3 à 100 ng.m-3 ;
- sites ruraux : 3 et 9 ng.m-3 (deux concentrations indiquées).
Dépôts atmosphériques
Motelay-Massei et al. (2005) ont mesuré les dépôts atmosphériques humides et solides de nickel (Fig. 3.2) sur cinq stations situées le long de la Seine.
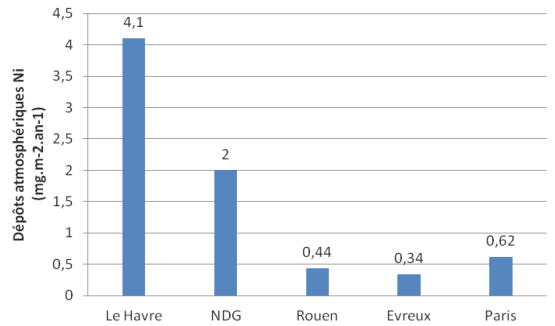
Figure 19. Dépôts atmosphériques de nickel pour cinq stations françaises ; NDG : Notre-Dame-de-Gravenchon, d'après Motelay-Massei et al., 2005.
En généralisant la valeur la plus basse de dépôt de nickel atmosphérique (0,34 mg.m -2 .an -1 à Evreux) à la surface totale de la France (550 000 km²) on peut estimer un minima de dépôts annuel de nickel par voie atmosphérique : 187 tonnes. Pour cette même année, les rejets vers les eaux étaient estimés à 61 tonnes.
Aquatique
FTE 2015 Importer
Dans les cours d'eau, les valeurs de nickel relevées sont comprises entre 0,03 et 24,6 µg.L-1, avec une médiane de 1,91 µg.L-1.
[62] (consulté en janvier 2014). http://weppi.gtk.fi/publ/foregsatlas/text/Ni.pdf
[63] Médiane: valeur correspondant à 50% des résultats.

Figure 13. Distribution géographique du nickel dans les milieux aquatiques, d'après le site internet du FOREGS.
Terrestre
FTE 2015 Importer
Selon le site internet du CNB (Comité National sur l'épandage des Boues d'épuration), les éléments-traces métalliques sont naturellement présents dans les roches à l'origine des différents types de sol (roches-mères). Les principales roches associées au nickel sont les roches magmatiques ultrabasiques.
Selon le site internet du CNB :
- « Les teneurs des sols en éléments métalliques dépendent donc directement de la nature des roches-mères sur lesquelles ils se sont formés. La concentration d'un élément, lorsqu'il n'y a pas eu d'apport extérieur (dû à l'activité humaine), constitue le fonds géochimique naturel de cet élément. Il varie d'une zone géographique à une autre en fonction de la roche-mère.
Pour un même lieu, il peut varier selon la nature des travaux agricoles : par exemple, un labour profond qui fait remonter en surface des éléments issus de la roche-mère. »
Ce même site présente des concentrations en nickel dans les sols issues de suivis mis en place dans le cadre des plans d'épandage des boues d'épuration. Pour le nickel ces valeurs atteignent :
- au minimum 0,1 g.t-1 de sol sec ;
- à la médiane 20,4 g.t-1 ;
- au 9ième décile64 41,8 g.t-1 .
En considérant une couche arable de 25 à 30 cm de sol (3 500 tonnes de terre par hectare), il est possible d'estimer les stocks en nickel pour un hectare de terre arable :
- au minimum 350 g.ha-1 ;
- à la médiane 71 400 g.ha-1 ;
- au 9ième décile 146 300 g.ha-1 .
La Nouvelle-Calédonie, la Réunion sont un cas particulier, avec des sols souvent particulièrement riches en nickel
Sédiments de cours d'eau
La valeur médiane en nickel total dans les sédiments est de 23 mg/kg, avec une gamme de 1 à 1 460 mg/kg.
[64] 9e décile : valeur maximale observée pour 90% des résultats.

Figure 14. Distribution géographique du nickel dans les sédiments des cours d'eau, d'après le site internet du FOREGS.
Sédiments de plaines alluviales
La valeur médiane en nickel total dans les sédiments varie en 2 et 1 080 mg/kg, avec une valeur médiane de 22 mg/kg.
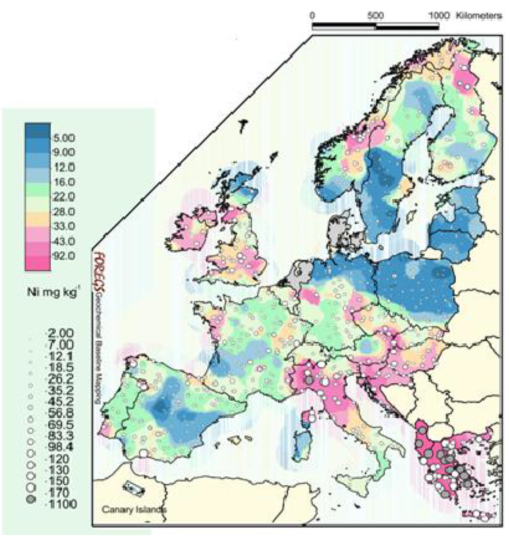
Figure 15. Distribution géographique du nickel dans les sédiments des plaines alluviales, d'après le site internet du FOREGS.
Sols
La valeur médiane en nickel est de 21,8 mg/kg dans les sous-sols, avec une gamme allant de < 2,0 mg/kg à 2 400 mg/kg. Dans la couche supérieure, la valeur médiane est de 18,0 mg/kg, avec des valeurs allant jusqu'à 2 690 mg/kg.

Figure 16. Distribution géographique du nickel dans les couches profondes des sols, d'après le site internet du FOREGS.
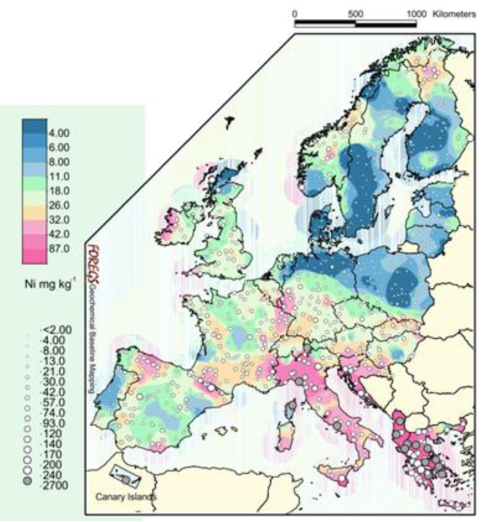
Figure 17. Distribution géographique du nickel dans les couches superficielles des sols, d'après le site internet du FOREGS.
Humus
La valeur médiane en nickel total est de 3,80 mg/kg, avec des valeurs comprises entre < 0,3 mg/kg et 74,9 mg/kg.
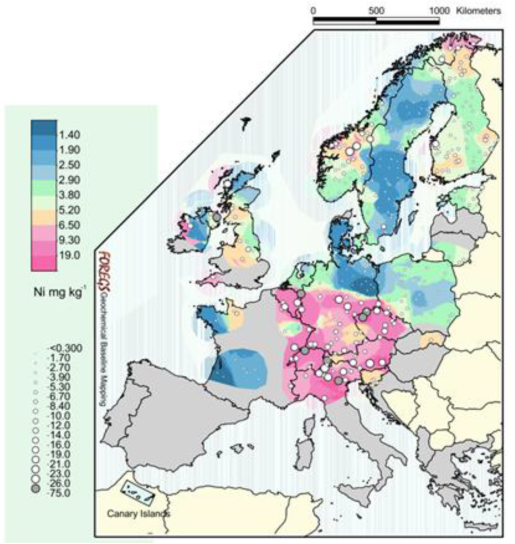
Figure 18. Distribution géographique du nickel dans l'humus, d'après le site internet du FOREGS.
Boues de stations d'épurations
Selon le site internet du CNB, les boues d'épuration concentrent les contaminants présents dans les eaux usées. Le taux de capture des contaminants (y compris le nickel) par les boues se situe entre 70 et 90 % des quantités entrantes dans la station d'épuration. Les teneurs des boues en contaminants varient selon la qualité des eaux entrantes et les traitements de stabilisation et/ou de déshydratation appliqués aux boues. Le chaulage, par exemple, diminue les valeurs observées par effet de dilution.
Le site internet du CNB (Comité National sur l'épandage des Boues d'épuration) reprend des données collectées à travers des enquêtes ou des campagnes de mesure menées par l'ADEME,
en 1995, l'Agence de l'eau Rhône-Méditerranée-Corse et Recyval en 1998 et SYPREA en 2000. En ce qui concerne le nickel, la valeur moyenne observée correspond à 40 g.t-1 (matière sèche). Ce chiffre est à mettre en parallèle avec la valeur limite réglementaire de 200 g.t-1 (matière sèche).
Selon le site internet du CNB, une analyse statistique plus approfondie permet d'identifier des situations à faible niveau de contamination et des situations comparativement moins bonnes. Néanmoins, les données les plus récentes (SYPREA, 2000 cité par le site internet du CNB) confirment la baisse continue des teneurs en éléments métalliques des boues d'épuration.
Perspectives de réduction
Réduction des rejets
Réduction des émissions industrielles
FTE 2015 Importer
Selon (European Commission, 2001a), l'industrie de la métallurgie du nickel peut respecter les performances environnementales suivantes :
- 10 à 300 g de poussière de nickel formés par tonnes de nickel produite ;
- 0,1 à 10 mg.L-1 de liquide de lavage des gaz (dont 10 à 60% de matière en suspension).
Après traitement de ces rejets, les émissions de nickel peuvent être abaissées à des valeurs non quantifiables pour les poussières et à moins de 0,1 mg.L-1 pour les rejets liquides.
Selon (European Commission, 2005), au sujet du traitement de surface des métaux et des plastiques, avant traitement, les émissions aqueuses de nickel sont estimées à moins de 2 mg.L-1 . Celles-ci peuvent être ramenées à des valeurs négligeables en appliquant les meilleures techniques de traitement des effluents disponibles.
Techniques de traitement pour les effluents aqueux
Le Tableau 13 présente un récapitulatif des différentes techniques de traitement des effluents contenant du nickel et/ou des ses composés. Ces techniques (décrites ci-après) sont dédiées au traitement des effluents liquides, spécialement dans le domaine de la chimie, mais aussi pour le traitement d'effluents de traitement de surface, ou encore l'effluents provenant du lavage de gaz contenant du nickel (industrie métallurgique, incinération de déchets,…).
Tableau 13. Récapitulatif des techniques et de leur efficacité vis à vis de la dénickelisation des
effluents aqueux ; * : élimination de 0 à 20% ; ** : de 20 à 50% ; *** : de 50 à 80% ; **** : de 80 à 100%, d'après Degrémont, 2005.

Clarification
La clarification regroupe les processus suivants : coagulation, floculation et décantation.
Le coagulant ajouté à l'eau a pour rôle de transformer les métaux lourds dissous dans l'eau en composés insolubles qui précipiteront. On utilisera alors un procédé de décantation ou de filtration pour finir le traitement.
Les taux de nickel peuvent être réduits de 0 à 20% (Degrémont, 2005). On doit veiller à séparer le nickel des composés cyanurés avec lesquels il forme des complexes stables qui ne pourront pas être traités (European Commission, 2005a).
Filtres à charbon actif
Le phénomène physique à l'œuvre au sein des filtres à charbon actif67 est l'adsorption, c'est à dire l'adhésion des matières à filtrer sur la surface d'un solide, sans réaction chimique. L'utilisation de la filtration par charbon actif en poudre permet une adsorption moyenne du nickel (Degrémont, 2005).
Ces procédés sont utilisés notamment dans le traitement des effluents des activités de traitement de surface (nickelage). Dans cette industrie, les émissions de nickel concernent les milieux aquatiques et les sols, mais très peu le compartiment atmosphérique (European Commission, 2005a)
Techniques spécifiques de réductions des émissions industrielles aqueuses dans le domaine de la chimie
Lorsqu'il est utilisé comme catalyseur, le nickel est récupéré et recyclé en grande partie. Une optimisation des taux de récupération est de recyclage pourrait parfois être envisageable.
Des procédés spécifiques sont utilisés dans le domaine de la chimie pour les effluents liquides fortement chargés en métaux et notamment en nickel (European Commission, 200368) :
- cristallisation pour des effluents provenant de la fabrication de dithiocarbamates métalliques (pour des concentrations dans l'effluent comprises entre 50 et 250 ppm) ;
[67] On dénomme également «filtres CAG » les filtres à charbon actif granulaire.
[68] Best Available Techniques Reference Documents: Common Waste Water and Waste Gas Treatment/ Management Systems in the Chemical Sector (consulté en janvier 2014). http://eippcb.jrc.ec.europa.eu/reference/cww.html
- cristallisation pour des effluents provenant de la fabrication de certains élastomères métalliques (pour des concentrations dans l'effluent comprises entre 50 et 400 ppm).
Dans ces deux cas, les concentrations en nickel après traitement pouvant être atteintes sont de 1 mg.L-1.
- précipitation suivie d'un procédé de séparation. La performance du procédé est très variable.
Réductions des émissions industrielles aqueuses dans le domaine du traitement de surface
Le secteur ayant fait l'objet d'une action prioritaire du Service des Installations Classées, les émissions ont été réduites dans ce secteur ces dernières années.
Les niveaux d'émissions atmosphériques suivants peuvent être atteints par certaines installations pour le nickel (d'après European Commission, 2005a) : 0,01 à 0,1 mg/Nm3
Un moyen important pour réduire les émissions est d'augmenter l'efficacité de l'emploi du nickel en minimisant les pertes de nickel lors des opérations de rinçage, en recyclant les eaux de rinçage :
- pour un fonctionnement en circuit « fermé », une efficacité de 95 % peut parfois être atteinte (on utilise alors des traitements de type membranaire) ;
- pour un fonctionnement sans circuit fermé, l'efficacité peut parfois être portée à 80-85 %.
Réductions des émissions industrielles lors des opérations minières
A tous les stades de l'extraction du minerai de nickel, des précautions doivent être prises pour protéger l'environnement69 :
- contrôle de la circulation des eaux de ruissellement pour éviter les entraînements de matériaux fins : réseau de drainage, bassins de décantation, barrages filtrants ;
- aucun rejet volontaire de matériaux dans la nature, ni au moment du traçage des pistes, ni au moment de l'exploitation (stockage des stériles en décharges contrôlées et stabilisées) ;
- revégétalisation des surfaces dénudées en fin d'exploitation, notamment le sommet des décharges de latérites ;
[69] Selon Eramet (2005), le principal polluant rejeté pour l'industrie minière du nickel est le SO2 (originaires des minerais sulfurés).
- contrôle des rejets de poussières, selon le site internet de la société Eramet, la mise en place de différents dispositifs de captage (électrofiltres, filtres à manche) permet de diminuer des trois quarts les émissions de poussières.
Réductions des émissions industrielles lors du traitement des minerais
Dans le domaine des minerais latéritiques, des essais menés en usine pilote sur le site futur de l'usine de Goro Nickel en Nouvelle-Calédonie permettent d'estimer les rejets de nickel potentiellement induits par cette future installation et d'apprécier sa performance environnementale (Goro Nickel, 2004b). Ces rejets concernent uniquement les effluents liquides :
- les valeurs attendues moyennes annoncées correspondent à 0,5 mg.L-1 de nickel ;
- les valeurs attendues maximales annoncées correspondent à 2 mg.L-1 de nickel ;
- le flux moyen au débit nominal de 1 500m3.h-1 annoncé correspond à 0,75 kg.h-1 .
Pour atteindre ces valeurs, il est envisagé de mettre en place un process de traitement des effluents à base de précipitation des métaux sous forme d'hydroxydes insolubles par neutralisation avec du calcaire et de la chaux à ph > 7.
Autres possibilités envisageables
FTE 2015 Importer
Accroissement du recyclage
Selon Eramet (2005), des perspectives s'ouvrent actuellement avec la valorisation de certains sous-produits tels que les poussières des aciéries électriques élaborant des aciers inoxydables. Néanmoins, à ce jour l'impact de ces mesures est difficilement chiffrable.
En ce qui concerne le recyclage des batteries, l'ADEME70 indique que, pour l'année 2012, 1 973 tonnes d'accumulateurs Ni-Cd et 2 904 tonnes des NiMH ont été mises en vente et 900 tonnes d'accumulateurs NiCd, et 250 tonnes de NiMH ont été traités.
Le taux de collecte pour les piles et accumulateurs portables a été, en 2012, de 35,4 %.
[70] Agence de l'Environnement et de la Maîtrise de l'Energie (consulté en janvier 2014). http://www2.ademe.fr/servlet/getBin?name=0114256509FEE2CF7274229C10450B92_tomcatlocal1386078272092.pdf
Exemple du traitement des sols
Une société chargée de traitement des sols indique qu'à ce jour, aucune problématique de nickel seul ne leur a été soumise, néanmoins, la problématique nickel se retrouve fréquemment associée à celle d'autres métaux (en particulier le chrome et le cuivre).
La principale difficulté technique réside dans la spéciation du nickel (certaines formes complexées du nickel sont solubles). La rémédiation consiste donc en la stabilisation de ces sols (fabrication de complexes de nickel insolubles par ajout d'un agent chimique et modification du pH des sols). Ce premier traitement chimique peut s'accompagner d'un traitement physique secondaire : emprisonnement des complexes dans une matrice cristalline étanche.
Le coût de ces techniques est évalué entre 50 et 500 €.t-1 de sol à traité en fonction de la complexité de la pollution (pollution simple ou multi-pollution).
L'efficacité de ce procédé permet d'atteindre des seuils de lixiviation des déchets inférieurs à 50 mg.kg-1 de matière sèche (valeur limite pour l'acceptation en centre de stockage des déchets ultime de classe 1).
Ce type de techniques a été mis en œuvre :
- en 1994, pour le traitement in-situ de terres polluées par des métaux lourds (chrome, nickel et cuivre) : 3 000 m 3 de sols situés à Clamecy (Nièvre) où étaient initialement situés des bassins de décantation d'effluents industriels ;
- en 1996, pour la stabilisation de boues de dragage polluées par des métaux lourds et des composés organiques (chrome, nickel, zinc et cuivre) : sédiments à teneurs métalliques trop importantes pour que l'épandage soit autorisé.
Exemple pour le secteur du traitement des déchets dangereux
Le site internet de la DRIRE d'Ile-de-France rapporte un exemple de traitement des effluents liquides industriels contenant du nickel en centre de traitement et de valorisation de déchets dangereux. Cette installation de valorisation de nickel par voie électrolytique permet d'extraire du nickel pur de déchets liquides provenant de l'industrie électronique (bains de sulfamate de nickel sans matière organique ni toxique contenant en moyenne 35 g.L-1 de nickel). Mis en servie en 2003 suite à un investissement de 220 k€, ce centre obtient, pour 1 tonne de déchet traité, 34 kg de nickel pur qui peut être recyclé. La quantité finale de déchets destinés à être stockés en centre d'enfouissement technique de classe 1 n'est plus que de 2,5 kg par tonne de déchet brut traité, alors qu'elle était de 140 kg en l'absence du traitement de valorisation.
RECYCLAGE
FTE 2015 Importer
La valeur de l'antimoine et une crainte de baisse de la production primaire font que le recyclage de l'antimoine présent dans les matériaux semble recevoir une attention croissante.
L'antimoine contenu dans les batteries au plomb antimonié (Pb-Sb) est souvent récupéré (>90%) et représentait jusqu'à 20% de la production totale d'antimoine en 2010 (Dupont, Arnout, Jones, & Binnemans, 2016). Dans cette filière on peut nommer les acteurs comme ECO BAT TECHNOLOGIES avec 2 sites en France ASPM (60) et STCM (35). Cependant il s'agit d'un usage en déclin au profit des batteries Plomb Calcium notamment (USGS, 2013), ainsi la production secondaire d'antimoine devrait baisser dans le futur.
[28] https://echa.europa.eu/documents/10162/53ff04a3-fc9b-4e53-94e0-a4ec6040ec3e
Pour ce qui est du reste des usages qui sont plus diffus, on ne dispose pas à l'heure actuelle de filière bien établie (European Commission, 2014), l'antimoine non-métallique n'est pas réutilisé. Une exception dans ce domaine est le recyclage de l'antimoine contenu dans le PET : en 2007, environ 25% du PET de bouteilles était recyclé, et autour de 72 % des flocons PET était réutilisé dans les textiles, et 10% dans de nouvelles bouteilles (Henckens, Driessen, & Worrel, 2016).
Cependant, un potentiel de recyclage existe : il est techniquement possible de récupérer l'antimoine des cendres issues de l'incinération de plastiques ou textiles des déchets municipaux ou des eaux de sites industriels. (Dupont, Arnout, Jones, & Binnemans, 2016).
La présence d'antimoine dans l'halophosphate utilisé dans les lampes fluorescentes pourrait donner lieu aussi à la mise en place d'un processus de recyclage via le réseau déjà existant de récupération des lampes classées comme déchets toxiques, mais qui ne valorise pas le contenu en antimoine actuellement. Les perspectives de recyclages concernent aussi les consommations intermédiaires (Catalyseurs) dans la production de polymère et notamment le polyéthylène téréphtalate (PET) utilisé dans les emballages alimentaires et les vêtements, en récupérant l'antimoine dans les résidus d'éthylène glycol issus de la fabrication du polymère (Dupont, Arnout, Jones, & Binnemans, 2016).
Alternatives aux usages
Produits de substitution
FTE 2015 Importer
Selon RPA (2000) et (European Commission, 2001a), il y a de nombreuses applications où aucune alternative à l'utilisation de nickel n'est disponible.
De plus, selon RPA (2000), le nickel est utilisé en remplacement de certaines applications de substances potentiellement dangereuses. Par exemple, les batteries Ni-MH65 ont été développées comme alternative aux batteries rechargeables Ni-Cd66 .
De plus, selon les producteurs de nickel, INSG (International Nickel Study Group) et Eramet (2005), le nickel possèderait des avantages au détriment de ses éventuelles alternatives :
- prolongation de la durée de vie des équipements de production et des articles dans lesquels il est présent (par le biais d'une augmentation de la résistance à la corrosion et à la chaleur des matériaux).
- facilité de nettoyage (en termes d'élimination de la prolifération bactérienne). (notamment dans le milieu médical et dans l'industrie agro-alimentaire).
- les propriétés magnétiques particulières conférées aux alliages contenant du nickel facilitent leur tri lors de la récupération d'anciens équipements.
Dans le cadre des travaux sur le nickel en cours dans le cadre de REACH, le Nickel Institute a réalisé des analyses des alternatives à certains composés du nickel (oxyde et sulfate de nickel) dans les secteurs industriels suivant : coatings décoratifs, industrie aérospatiale, industrie électronique. Une analyse socio-économique des conséquences d'une éventuelle interdiction du sulfate de nickel pour les coatings décoratifs a été réalisée.
L'oxyde de nickel est utilisé comme catalyseur dans le raffinage des hydrocarbures et le piégeage du soufre. Sa substitution impliquerait une augmentation de coûts, ainsi qu'une augmentation de l'utilisation d'énergie. De plus, l'élimination du soufre sera moins efficace, ce qui augmentera la quantité de soufre dans les carburants et donc les émissions vers l'atmosphère. Il n'existe pas pour le moment d'alternatives permettant de ne plus utiliser l'oxyde de nickel dans les pigments ou le verre.
[65] Ces batteries ont été développées pour des usages particuliers tels que l'usage dans des véhicules électriques et hybrides. Cet usage est encouragé par la Commission européenne (Anyadike, 1999).
[66] Cette technologie Ni-Cd sera interdite à partir du 1er juillet 2006 suivant la directive européenne 2002/95/CE du parlement européen et du conseil du 27 janvier 2003 relative à la limitation de l'utilisation de certaines substances dangereuses dans les équipements électriques et électroniques.
ALTERNATIVES AUX USAGES DE L'ANTIMOINE
FTE 2015 Importer
Les observations récentes (Roskill, 2018) 25 du marché montrent une diminution générale des usages d'antimoine dans les plastiques, textiles et alliages métalliques aux profits de substances comme l'étain, le calcium, le zinc… Un phénomène compensé par une augmentation constante des usages en tant que retardateurs de flamme et catalyseurs dans la plasturgie des polymères.
Plusieurs substituts à l'usage d'antimoine dans les retardateurs de flamme se développent (Posner, 2004). On citera des composés organiques de phosphores chlorés, l'oxyde de zinc et l'oxyde d'aluminium hydraté (BRGM, 2011). En effet, le marché des câbles et gaines retardatrices de flamme qui reste le marché principal de cet usage verrait les parts de marché du trioxyde d'antimoine chuter au profit du trioxyde d'aluminium (Al2O3) qui présente l'avantage d'émettre moins de fumée noire lors de la combustion (Morgan & Wilkie, 2014).
Pour des raisons d'efficacité, l'antimoine est remplacé par d'autre éléments comme le calcium dans les batteries en plomb ou l'étain voire des batteries uniquement en plomb (VRLA), elles-mêmes en concurrences avec les batteries lithium dans certains secteurs26 .
L'utilisation de l'antimoine dans les alliages métalliques afin d'augmenter la durabilité ou pour des d'usage antifrictions pourrait trouver des alternatives parmi d'autres éléments tels que le Baryum (Ba), le Cadmium (Cd), le Calcium (Ca), le Plomb (Pb) ou encore l'Etain (Sn) 27 . Ceci peut expliquer la tendance à la baisse des usages d'antimoine dans les plaquettes de freins notamment (Tian, et al., 2014).
[25] https://roskill.com/market-report.an-1timony/
[26] http://www.seenrgy.com/webservice/document/_getStream.asp?id=8B9CF4C1-F833-438D-82B7-E6652F2A0E4A
Il est aussi en concurrence avec d'autres métaux (Cd, Cr, Sn, Ti, Zn, Zr) dans la confection de pigments et d'émaux dans les céramiques, peintures et couches de vernis ignifugeants (BRGM, 2011). Il est estimé qu'il est aussi possible de substituer entièrement l'antimoine dans les verres et céramiques dans les années à venir (Henckens, Driessen, & Worrel, 2016).
Concernant les usages en plasturgie en guise de catalyseur pour polymères, l'antimoine rencontrera la même concurrence à laquelle il fait face dans la production de batteries, à savoir les alternatives suivantes : Ba, Cd, Ca, Pb, Sn, Zn (BRGM, 2011). Aussi, la plupart des alternatives commercialisées sont basées sur le Titane (Henckens, Driessen, & Worrel, 2016).
Dans les usages mineurs comme les couches conductrices (ATO) en électronique, allié à l'étain il rencontre la concurrence de produits alternatifs à base d'indium et d'étain (ITO), ou encore de zinc et d'aluminium (AZO) (BRGM, 2011).
A l'inverse des marchés précédant, l'hydrométallurgie du zinc emploie du trioxyde d'arsenic afin d'affiner le processus de purification du zinc. Le trioxyde d'antimoine représenterait une alternative techniquement crédible mais pas assez efficace économiquement et sans assurance de réduire les risques sanitaires et environnementaux28 .
L'antimoine représenterait aussi une alternative au Mercure (Hg) et au Bismuth (Bi) dans la composition des électrodes des points de vue technique et environnemental (Serrano, Diaz-Cruz, Ariño, & Esteban, 2016).
Conclusion
FTE 2015 Importer
La présence du nickel dans l'environnement résulte, pour plus de 84 % des émissions, de son utilisation dans la production d'acier et divers alliages, dans les batteries, les circuits électriques. Le nickel existe également naturellement dans l'environnement.
Malgré un déclin des rejets industriels lié à la mise en place de nouvelles technologies de contrôle des émissions de nickel, et un meilleur recyclage des effluents riches en nickel, les apports de cet élément aux milieux aquatiques vont perdurer longtemps. Ceci est lié à de multiples raisons :
- existence de sources naturelles de nickel ;
- difficulté et/ou impossibilité de supprimer le nickel dans certaines applications particulières (alliages, aciers inoxydables,…) ;
- durée de vie importante des produits contenant du nickel (à l'exception des batteries) ;
- recours à des produits contenant du nickel en remplacement à des produits présentant un fort impact pour l'environnement (remplacement des batteries au plomb, cadmium, … par des batteries Ni-MH) ;
- encouragement à l'usage de produits contenant du nickel dans une optique de préservation de l'environnement (du nickel est utilisé pour les batteries des véhicules électriques et hybrides, ...) ;
- croissance du marché de l'ensemble des produits contenant du nickel ;
- présence d'apports industriels diffus à l'échelle du territoire ;
- apport agricoles diffus via les engrais, difficilement contrôlables.
Malgré les progrès effectués dans le domaine de la dépollution des effluents industriels et le fort intérêt économique que représente la valorisation des déchets contenant du nickel, la disparition des rejets (d'origine anthropique) de cet élément à court terme semble hors de portée.
FTE 2015 ImporterL'antimoine, moins surveillé que d'autres métaux tels que l'arsenic, le plomb ou le nickel n'en reste pas moins toxique d'où l'existence de réglementation en matière d'usages professionnels et son inscription ainsi que certains de ses composés au Community Action Rolling Plan de l'ECHA en vue d'établir le niveau de dangerosité et les restrictions appropriées.
Bien que des substituts potentiels existent dans la plupart des applications de l'antimoine, la demande reste en constante augmentation à l'exception des batteries qui représente encore le second usage le plus élevé (≈30%). Le quasi-monopole chinois au niveau mondial de la production minière d'antimoine potentiellement soumise à des quotas, et l'incertitude entourant l'offre viennent alimenter les craintes de dépendance en Europe, qui l'a donc inclus dans la liste des matières critiques.
A ce contexte économique incertain vient s'ajouter la pollution issue des rejets d'antimoine. En effet l'accroissement faible mais stable de la consommation d'antimoine donne lieu à des rejets dans la biosphère qui devraient perdurer.
Les rejets dans l'air se font sous forme de trioxyde d'antimoine, et sont associés aux exploitations minières, métallurgiques, à la combustion de charbon dans le secteur de l'énergie, l'abrasion des plaquettes de freins lubrifiées à l'antimoine, l'incinération des déchets municipaux, et pouvant se déplacer sur de grandes distances puis se déposer et s'adsorber sur les sols, ou se déposer directement sur les milieux aquatiques.
A ces rejets dans les sols viennent s'ajouter les boues et les scories contenant de l'antimoine issue des mines, fonderies et autres sites industriels ou encore les dépôts de déchets plastiques, textiles ou alliages métalliques dans les décharges.
Des rejets d'antimoine directs dans les milieux aquatiques pourront provenir de l'usage de matériaux en milieu extérieur, ou de leur contact avec l'eau, ou encore de l'usage de peintures à l'eau en contenant. Une partie de l'antimoine rejeté dans les milieux aquatiques intégrera la matière en suspension, les sédiments ou encore les biotes.
Les perspectives en matière de recyclage de l'antimoine existent mais seule la filière du recyclage des batteries Pb-Sb est opérationnelle à grande échelle (≈90% recyclé). Les sources plus diffuses de la pollution de l'antimoine font l'objet de programmes de recherche impliquant la valorisation de l'antimoine dans les déchets municipaux, le filtrage de l'eau, la récupération de l'antimoine dans les procédés de plasturgie des polymères, dans les lampes halogènes mais rien ne laisse prévoir une réduction des émissions à court ou moyen terme.
Bibliographie
Archives
Dernière vérification le 29/03/2024
Documents
Exporter la substance
Choisissez le format de l'export :

