Configuration de votre affichage
Vous avez activé le mode de configuration de l'affichage qui permet de sélectionner les informations que vous souhaitez afficher sur la fiche substance. Une fois que vous aurez sélectionné les rubriques à afficher, vous pouvez revenir au mode de consultation de la fiche substance en cliquant à nouveau sur le bouton de filtrage.
Formaldéhyde (50-00-0)
Informations générales
Dernière vérification le 18/12/2025
Identification
Numero CAS
50-00-0
Nom scientifique (FR)
Formaldéhyde
Nom scientifique (EN)
Autres dénominations scientifiques (FR)
Autres dénominations scientifiques (Autre langues)
Code EC
200-001-8
Code SANDRE
1702
Numéro CIPAC
-
Formule chimique brute
\(\ce{ CH2O }\)
Code InChlKey
Code SMILES
O=C
Familles
Familles chimiques
Familles d'usages
Classification CLP
Type de classification
Harmonisée
ATP insertion
CLP00/ATP06
Description de la classification
Classification harmonisée selon réglement 1272/2008 ou CLP
| Mention du danger - Code | H314 |
|---|---|
| Mention du danger - Texte | Provoque de graves brûlures de la peau et de graves lésions des yeux. |
| Classe(s) de dangers | Corrosion / Irritation cutanée |
| Libellé UE du danger | - |
| Limites de concentration spécifique |
STOT SE 3;H335: C ≥ 5 % Skin Corr. 1B;H314: C ≥ 25 % Skin Irrit. 2;H315: 5 % ≤ C < 25 % Eye Irrit. 2;H319: 5 % ≤ C < 25 % Skin Sens. 1;H317: C ≥ 0,2 % |
| Facteur M | - |
| Estimation de toxicité aigüe | - |
| Mention du danger - Code | H301 |
|---|---|
| Mention du danger - Texte | Toxique en cas d'ingestion |
| Classe(s) de dangers | Toxicité aiguë |
| Libellé UE du danger | - |
| Mention du danger - Code | H311 |
|---|---|
| Mention du danger - Texte | Toxique par contact cutané |
| Classe(s) de dangers | Toxicité aiguë |
| Libellé UE du danger | - |
| Mention du danger - Code | H331 |
|---|---|
| Mention du danger - Texte | Toxique par inhalation |
| Classe(s) de dangers | Toxicité aiguë |
| Libellé UE du danger | - |
| Limites de concentration spécifique |
STOT SE 3;H335: C ≥ 5 % Skin Corr. 1B;H314: C ≥ 25 % Skin Irrit. 2;H315: 5 % ≤ C < 25 % Eye Irrit. 2;H319: 5 % ≤ C < 25 % Skin Sens. 1;H317: C ≥ 0,2 % |
| Facteur M | - |
| Estimation de toxicité aigüe | - |
| Mention du danger - Code | H317 |
|---|---|
| Mention du danger - Texte | Peut provoquer une allergie cutanée |
| Classe(s) de dangers | Sensibilisation respiratoire/cutanée |
| Libellé UE du danger | - |
| Limites de concentration spécifique |
STOT SE 3;H335: C ≥ 5 % Skin Corr. 1B;H314: C ≥ 25 % Skin Irrit. 2;H315: 5 % ≤ C < 25 % Eye Irrit. 2;H319: 5 % ≤ C < 25 % Skin Sens. 1;H317: C ≥ 0,2 % |
| Facteur M | - |
| Estimation de toxicité aigüe | - |
| Mention du danger - Code | H341 |
|---|---|
| Mention du danger - Texte | Susceptible d'induire des anomalies génétiques (indiquer la voie d'exposition s'il est formellement prouvé qu'aucune autre voie d'exposition ne conduit au même danger) |
| Classe(s) de dangers | Mutagénicité sur les cellules germinales |
| Libellé UE du danger | - |
| Mention du danger - Code | H350 |
|---|---|
| Mention du danger - Texte | Peut provoquer le cancer (indiquer la voie d'exposition s'il est formellement prouvé qu'aucune autre voie d'exposition ne conduit au même danger) |
| Classe(s) de dangers | Cancerogénicité |
| Libellé UE du danger | - |
| Limites de concentration spécifique |
STOT SE 3;H335: C ≥ 5 % Skin Corr. 1B;H314: C ≥ 25 % Skin Irrit. 2;H315: 5 % ≤ C < 25 % Eye Irrit. 2;H319: 5 % ≤ C < 25 % Skin Sens. 1;H317: C ≥ 0,2 % |
| Facteur M | - |
| Estimation de toxicité aigüe | - |
Physico-Chimie
Dernière vérification le 29/03/2024
Généralités
Poids moléculaire
30.03 g/mol
Tableau des paramètres
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Bibliographie
Dangers physiques
Dernière vérification le 29/03/2024
Explosivité
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Inflammabilité
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Bibliographie
Comportement et devenir dans les milieux
Dernière vérification le 30/06/2025
Matrices
Atmosphère
Compte tenu de son importante pression de vapeur (5,2.105 Pa à 25°C), le formaldéhyde est très volatil en tant que produit pur.
Milieu eau douce
Volatilisation :
La constante d'Henry indique que le formaldéhyde n'est pas volatil depuis un milieu aqueux, mais qu'il l'est depuis un sol sec puisqu'il est à l'état gazeux en conditions ambiantes. (HSDB, 2011)
Milieu sédiment eau douce
Adsorption :
Le faible Koc (37 L.kg-1) du formaldéhyde suggère que la substance ne s'adsorbera pas sur le sédiment et la matière en suspension dans l'eau. La substance aura également une mobilité importante dans le sol. (HSDB, 2011)
Milieu terrestre
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Persistance
Biodégradabilité
Biodégradabilité :
Le formaldéhyde est facilement biodégradable avec 90% de biodégradation observée dans un essai OECD 301D (essai en flacon fermé). (OECD, 2002; HSDB, 2011)
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Dégradabilité abiotique
Hydrolyse :
Le formaldéhyde n'est pas censé se dégrader par hydrolyse. Cela est dû à l'absence de groupe hydrolysable dans sa structure chimique. Par contre, le formaldéhyde dans l'eau est hydraté en méthylène glycol (CH2(OH)2) (OECD, 2002; FOOTPRINT, 2011; HSDB, 2011)
Photolyse :
Le formaldéhyde absorbe les UV aux longueurs d'ondes supérieures à 360 nm, il est donc susceptible d'être dégradé par photolyse. Un temps de demi-vie de 6 h a été mesuré en lumière naturelle simulée.
Calvert (1972) a également mesuré un temps de demi-vie en photolyse de 1.6 h en atmosphère basse à 40°C.
(HSDB, 2011)
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Bioaccumulation
Organismes aquatiques
Le formaldéhyde se retrouve naturellement chez les végétaux et les animaux. Il est facilement métabolisé par ces organismes. La faible valeur du coefficient de partage octanol–eau (logKow = 0,35 à 20°C) indique un faible potentiel de bioaccumulation du formaldéhyde. Ce constat est confirmé par les résultats obtenus lors d’essais réalisés sur poissons et sur crevettes, ne montrant aucune bioaccumulation du formaldéhyde (Hose et Lightner, 1980 ; Sills et Allen, 1979 ; IPCS, 2002).
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Conclusion sur la bioaccumulation
Bioaccumulation/ Biomagnification :
La faible valeur du logKow indique un faible potentiel de bioaccumulation de la substance.
Un BCF calculé de 3 suggère une faible tendance du formaldéhyde à se bioconcentrer dans les organismes aquatiques.
Ce BCF de 3 est utilisé dans la détermination des normes de qualité ce qui correspond à un BMF1 de 1 auquel s'ajoute pour les organismes marins un BMF2 de 1. (OECD, 2002 HSDB, 2011)
Bibliographie
Toxicologie
Dernière vérification le 30/06/2025
Introduction
L'ensemble des informations et des données toxicologiques provient de diverses monographies publiées par des organismes reconnus pour la qualité scientifique de leurs documents (IARC, 1982, 1987, 1995, 2004, 2006 ; OMS, 1996 ; US EPA (IRIS), 1998 ; ATSDR, 1999, 2010 ; Anses, 2008, 2011, 2018 ; INRS, 2008, 2022). Les références bibliographiques aux auteurs sont citées pour permettre un accès direct à l’information scientifique mais n’ont pas fait l’objet d’un nouvel examen critique par les rédacteurs de cette rubrique.
Toxicocinétique
Chez l'homme
Absorption
Le formaldéhyde est une substance endogène, intermédiaire du métabolisme cellulaire. Il est produit lors du métabolisme d’acides aminés tels que sérine, glycine, méthionine et choline et également lors de la déméthylation des composés N-, S- et O-méthyles. C’est un intermédiaire essentiel de la biosynthèse des purines, thymidines et certains acides aminés (Neuberger, 1981).
Bien qu’il existe d’autres voies d’exposition (digestive et cutanée), le formaldéhyde exogène peut affecter l’organisme humain par inhalation. Il manifeste des effets locorégionaux importants par une action toxique cellulaire au point de contact et d’autres effets peuvent résulter de l’absorption au niveau du tractus respiratoire. Quatre-vingt-dix-huit pourcents du formaldéhyde se déposent au niveau de la muqueuse nasale (Leikauf, 1992). Par ingestion, le formaldéhyde est très rapidement absorbé au niveau du tractus gastro-intestinal et subit les mêmes transformations métaboliques que celles impliquées suite à une exposition par inhalation. Chez l’homme, le taux d’absorption cutanée est faible : 319 µg.cm-2.h-1 in vitro après application d’une solution à 37 % sur de la peau (INRS, 2008).
Quelle que soit la voie, l’absorption semble limitée aux couches de cellules immédiatement adjacentes au point de contact. Ce qui limite son passage systémique et explique notamment que les concentrations sanguines varient très peu en cas d’exposition au formaldéhyde (ATSDR, 1999). Néanmoins, les lésions corrosives au site de contact peuvent favoriser le passage systémique (INRS, 2008).
Métabolisme
La concentration sanguine endogène en formaldéhyde chez l’homme est de l’ordre de 2,5 mg.L-1. Le métabolisme du formaldéhyde, rapide, est hépatique. La demi-vie du formaldéhyde dans le sang excède rarement 2 minutes chez l’homme (AFSSET, 2008). Le formaldéhyde est oxydé en acide formique métabolisé en dioxyde de carbone, qui est exhalé (les formiates sont aussi incorporés dans les synthèses organiques). Cette étape est chez les primates saturable et moins performante que celle des rongeurs1. L’acide formique peut être éliminé dans les urines où les concentrations restent inférieures à 100 mg.L-1 (Schweda 1985).
Le formaldéhyde peut également se lier de manière covalente avec des substances nucléophiles des protéines et des acides nucléiques (adduits et ponts ADN-protéines).
Du fait de sa forte réactivité et de sa métabolisation rapide en formiate, l’exposition humaine par inhalation au formaldéhyde, n’a pas mis en évidence de modifications de son taux sanguins. Ce dosage constitue donc un inutile marqueur d’exposition par inhalation (ATSDR 1999).
Chez l’homme, il a été estimé que plus de 50 000 mg de formaldéhyde endogène est métabolisé par jour, le foie d’un adulte transformant environ 1320 mg par heure (Owen et al., 1990).
1 Chez les primates on peut observer une augmentation des formiates lors de l’ingestion importante de méthanol qui est transformé en formaldéhyde dans l’organisme. La concentration moyenne en formiate urinaire des travailleurs exposés au formaldéhyde est de 12,5 mg.L-1. Cette valeur est soumise à de considérables variations intra- et interindividuelles
Chez l'animal
Absorption
Par inhalation :
Des études par inhalation de formaldéhyde radiomarqué ont permis de montrer chez le rat un taux absorption proche de 100 %. Cette absorption se situe préférentiellement au niveau des cavités nasales (Heck et al., 1985).
Des travaux antérieurs réalisés chez le chien avaient également permis d’observer une absorption du formaldéhyde proche de 100 % au niveau des voies aériennes supérieures (Egle, 1972).
Les concentrations de formaldéhyde sanguin ne subissent aucune variation liée à l’exposition des animaux (inhalation de 14 ppm de formaldéhyde pendant 2 heures chez le rat). Ces résultats ont depuis été confirmés chez le singe pour des expositions à 6 ppm de formaldéhyde 6 heures par jour, 5 jours par semaine, pendant 4 semaines (Casanova et al., 1988). La demi-vie est de 1 minute 30 après injection intraveineuse chez le rat (INRS, 2008).
Conolly et al. (2000) dans un modèle de dynamique des fluides en 3 dimensions montrent que la courbe dose-réponse prédictive des adduits protéine-ADN pour les 3 espèces (rat, singe et homme) était similaire en dépit des différences significatives d’anatomie nasale des 3 espèces et de leur fréquence respiratoire différente.
Par voie orale :
Des études de toxicocinétique réalisées chez le rat et la souris ont permis d’établir par voie orale un taux d’absorption à peu près constant et proche de 90 % (Galli et al., 1983). L’administration orale de
Une corrélation entre l’administration orale de formaldéhyde et sa présence dans le lait a été mise en évidence chez des vaches laitières et des chèvres (Buckley et al., 1988 ; Barry et Tome, 1991).
Par voie cutanée :
Le faible taux d’absorption du formaldéhyde par voie cutanée est lié à sa réaction spontanée avec les protéines cellulaires de
Par voies orale et cutanée, plusieurs études montrent l’absence de bioaccumulation du formaldéhyde au niveau du cœur, du foie, des reins et des tissus musculaires (Buckley et al., 1988 ; Jeffcoat et al., 1983).
Synthèse
Le formaldéhyde est une substance endogène, intermédiaire du métabolisme cellulaire humain et animal. La principale voie d’exposition au formaldéhyde exogène est l’inhalation. La concentration sérique physiologique en formaldéhyde chez l’homme est de l’ordre de 2,5 mg.L-1. Par ingestion, le formaldéhyde est très rapidement absorbé au niveau du tractus gastro-intestinal et subit les mêmes transformations métaboliques que par inhalation. Chez l’homme, le taux d’absorption cutanée n’a pas été déterminé. Cependant, il semble que le formaldéhyde soit très peu absorbé par cette voie.
Des études par inhalation de formaldéhyde radiomarqué ont permis de montrer chez le rat un taux d’absorption proche de 100 %. Cette absorption se situe préférentiellement au niveau des cavités nasales.
Toxicité aiguë
Chez l'homme
Inhalation
Le formaldéhyde présent dans l’air est très irritant pour les yeux, le nez et la gorge à de faibles concentrations de l’ordre de 0,2 à 1,6 ppm (0,25 à 2 mg.m-3).
L’irritation oculaire peut apparaître avant que l’odeur ne soit perçue.
Plusieurs études d’exposition contrôlée par inhalation ont montré chez l’homme le pouvoir irritant du formaldéhyde. Les symptômes pris en compte sont l’irritation des yeux accompagnée ou non de larmoiements, ainsi que l’irritation nez / gorge et la sécheresse buccale. Ces symptômes apparaissent, dans la plupart des études, dès 0,2 à 0,3 ppm (0,25 à 0,375 mg.m-3) ; le plus souvent, l’inconfort des patients augmente en même temps que la concentration d’exposition jusqu’à 2 ou 3 ppm (2,5 ou 3,75 mg.m-3) (Andersen et Molhave, 1983 ; Bender et al., 1983 ; Kulle, 1993 ; Day, 1984).
Des études complémentaires réalisées chez des sujets dits sensibles, asthmatiques ou répondant par une dermatite allergique de contact au formaldéhyde en solution, ont confirmé l’apparition de symptômes irritatifs consécutifs à l’exposition à 0,4 ppm (0,5 mg.m-3) de formaldéhyde pendant deux heures (Gorski et al., 1992 ; Pazdrak et al., 1993 ; Krakowiak et al., 1998).
L’exposition aiguë au formaldéhyde par inhalation, entraîne également une congestion nasale, à laquelle peuvent être associés des démangeaisons et des éternuements décrits notamment dans les études sur volontaires sains et sensibles de Pazdrak et al. (1993) et Krakowiak et al. (1998). Ces symptômes caractéristiques d’une rhinite sont accompagnés dans les populations sensibles ou normales, par une augmentation de la concentration des protéines totales et de l’albumine, ainsi que du nombre d’éosinophiles recueillis dans les liquides de lavage nasal. D’après Pazdrack et al. (1993), ces modifications inflammatoires non spécifiques apparaissent à partir de 500 µg.m-3.
En ce qui concerne les effets du formaldéhyde sur la fonction respiratoire, les résultats sont beaucoup moins clairs et parfois contradictoires.
Une dizaine d’études décrivent l’absence d’effets chez des volontaires sains, sensibilisés ou asthmatiques, exposés à des concentrations variant de 0 à 3 ppm sur des périodes allant de 10 minutes à 4 heures, et soumis ou non à des exercices physiques (Andersen et Molhave 1983 ; Kulle et al., 1987 ; Green et al., 1987 ; Schachter et al.,1987).
Seules quelques études, réalisées en milieu professionnel, ont permis d’observer une diminution du VEMS (Volume Expiratoire Maximum Seconde) pour des expositions courtes (20 et 30 minutes) à des concentrations de 2,4 mg.m-3 (1,9 ppm) et 6,4 mg.m-3 (5,2 ppm) (Nordman et al.,1985 ; Burge et al.,1985).
Voie orale
Plusieurs cas mortels sont rapportés dans la littérature. Des troubles respiratoires importants (cyanose, syndrome de détresse respiratoire aiguë), des lésions sévères au niveau de l'estomac, de l’intestin grêle, des reins et des collapsus circulatoires (Koppel et al., 1990 ; Eells et al., 1981 ; Gosselin et al., 1976) sont rapportés.
En cas d’ingestion, des effets corrosifs sévères peuvent être observés (Eells et al., 1981 ; Burkhart et al., 1990 ; Bartone et al., 1968).
Voie cutanée
L’application cutanée chez l’homme d’une solution à 1% de formaldéhyde est faiblement irritante, tandis que les solutions concentrées sont corrosives pour la peau humaine (INRS, 2008).
Synthèse
Chez l’homme, en cas d’exposition aiguë, le formaldéhyde est très irritant par inhalation pour les yeux, le nez et la gorge à de très faibles concentrations de l’ordre de 0,2 à 1,6 ppm (0,25 à 2 mg.m-3). Par voie orale, il peut être à l’origine de troubles respiratoires importants et de lésions viscérales sévères (estomac, intestin, reins). Le formaldéhyde est faiblement irritant pour la peau à des concentrations inférieures à 1 % et corrosif à concentration élevée.
Chez l'animal
Inhalation
Toutes les études aiguës par inhalation chez l'animal confirment les effets irritants du formaldéhyde au niveau des voies aériennes supérieures, à partir de 2 ppm (2,5 mg.m-3), qui se traduisent localement par des lésions de l'épithélium nasal (Monticello et al., 1991 ; Cassee et Feron, 1994 ; Monteiro-Riviere et Popp, 1986).
Pour des fortes expositions de 150 ppm (187,5 mg.m-3) pendant 6 heures chez le rat, le formaldéhyde atteint les poumons et entraîne des lésions sévères (œdèmes pulmonaires, épaississement de la paroi alvéolaire) (Kamata et al.,1996a, 1996b).
Les CL50 sont de 400 mg.m-3 (325 ppm) chez la souris et 203 mg.m-3 (165 ppm) chez le rat (RTECS, 1993).
Voie orale
Les études de mortalité réalisées chez l’animal par voie orale montrent des résultats différents. Cette disparité s’explique au moins en partie par le fait que le formaldéhyde est très volatil et réactif. La rigueur, que demandent la préparation et la conservation des solutions administrées aux animaux, n’est pas observée dans toutes les études. Par ailleurs, certains des résultats sont faussés par la présence de méthanol utilisé dans les solutions commerciales de formaldéhyde (10 à 15 % de méthanol dans le formalin) afin d’éviter la polymérisation du produit.
Les valeurs de DL50 calculées par voie orale chez le rat et le cobaye sont respectivement de 800 et 260 mg.kg-1 (Smyth et al., 1941).
Voie cutanée
Une DL50 par voie percutanée de 270 mg.kg-1 a été mise en évidence chez le lapin. Une application de 50 mg de formaldéhyde pendant 24 heures sur la peau du lapin peut entraîner une irritation cutanée modérée. De même, il est fortement caustique pour les muqueuses oculaires. Le formaldéhyde est un sensibilisant cutané chez l’animal induisant une réponse modérée à forte, à des concentrations non irritantes (INRS, 2008).
Synthèse
Chez l’animal, ces effets irritants par inhalation sont confirmés. A partir de 2 ppm, une irritation des voies respiratoires supérieures est observée. Il peut également entraîner une irritation cutanée modérée chez le lapin. Il est corrosif pour les muqueuses oculaires et est sensibilisant cutané.
Toxicité à doses répétées
Effets généraux
Chez l'homme
Inhalation
De nombreuses études réalisées dans la population générale exposée au formaldéhyde présent dans l’air intérieur des logements ont confirmé le pouvoir irritant du formaldéhyde au niveau des voies aériennes supérieures, initialement observé en milieu professionnel. Pour des expositions moyennes se situant entre 0,1 et 1 ppm, (0,125 et 1,25 mg.m-3) l'irritation des yeux, du nez et de la gorge est en moyenne ressentie par 75 % des adultes (Garry et al, 1980 ; Ritchie et Lehnen, 1987 ; Edling et al., 1988).
Des analyses histologiques de biopsies nasales ont été effectuées chez des travailleurs exposés au formaldéhyde sur une plus ou moins longue période (variant de 1 à 30 années).
Holmstrom et al. (1989), ont examiné les modifications histologiques sur des prélèvements de tissu nasal effectués sur un groupe de 70 travailleurs de l’industrie chimique (production de formaldéhyde et résines de formaldéhyde pour imprégnation de papier), un groupe de 100 travailleurs dans une usine de production de meubles (planches d’aggloméré et composants de colle), ainsi qu’un groupe témoin de 36 personnes non exposées professionnellement au formaldéhyde et travaillant dans un bureau. Les concentrations inhalées en formaldéhyde sont estimées entre 0,04 et 0,4 ppm (0,5 mg.m-3), pour les travailleurs de l’industrie chimique, entre 0,16 et 0,4 ppm pour les travailleurs de l’usine produisant des meubles et entre 0,07 et 0,13 ppm pour les témoins. Les signes cliniques observés chez les travailleurs exposés durant en moyenne 10,4 ans (de 1 à 36 ans) à des concentrations moyennes de formaldéhyde de 0,24 ppm (0,04 à 0,4 ppm) sont une irritation modérée des yeux et du tractus respiratoire supérieur, ainsi que des lésions modérées de l’épithélium nasal. La LOAEC retenue est de 0,24 ppm.
Ces différentes études mettent en évidence différents types d’anomalies de l'épithélium nasal, telle que la destruction des cellules ciliées, la prolifération de foyers de cellules hyperplasiques ou plus rarement dysplasiques (Edling et al., 1988 ; Boysen et al., 1990 ; Ballarin et al., 1992). Ces études ont contribué à établir, après un ajustement tenant compte de l’exposition en continue, des valeurs de NOAEC et LOAEC respectivement de 26 ppb (32 µg.m-3) et 75 ppb (92 µg.m-3).
Dans deux études plus récentes (Lang et al., 2008 et Mueller et al., 2013), des tests objectifs de mesure de l’irritation sensorielle tels que la fréquence de clignement oculaire, le flux et la résistance nasale ont été évalués.
L’étude de Lang et al. (2008) a été réalisée chez 21 volontaires (11 hommes et 10 femmes) exposés 4 heures à des concentrations de 0, 185, 369, 615 µg.m-3 incluant ou non des pics de concentration. Aucune modification significative n’a été rapportée suite à l’exposition au formaldéhyde pour la résistance et le flux nasal, la fonction pulmonaire ainsi que le temps de réaction. Une rougeur oculaire et l’augmentation de la fréquence de clignement oculaire, statistiquement significative, n’ont été mises en évidence qu’à l’exposition de la concentration la plus élevée de 615 µg.m-3 associé à 4 pics de 1 230 µg.m-3, de même qu’en présence d’un agent masquant (acétate d’éthyle). Concernant les effets subjectifs analysés (irritation oculaire, nasale, respiratoire, symptômes olfactifs, gêne), les premiers effets apparaissent généralement dès 369 µg.m-3 mais ne sont pas toujours significatifs avec l’agent masquant.
L’étude de Mueller et al. (2013) a été réalisée chez 41 hommes volontaires également exposés 4 heures à des concentrations de 0, 615, 861 µg.m-3 associés ou non à des pics d’exposition de 15 minutes. Il est à noter que cette étude a réparti les volontaires en « hypersensibles » et « hyposensibles » à l’aide d’un test de sensibilité au CO2. Aucune modification significative n’a été observée en ce qui concerne la rougeur conjonctivale et la fréquence de clignement oculaire par rapport aux témoins. Le temps de rupture du film lacrymal a été diminué chez les personnes « hyposensibles » exposées à 369 et 4 pics de 615 µg.m-3 et 861 µg.m-3 par rapport aux témoins. Cependant, aucune relation dose-réponse n’est apparue et les mêmes observations n’ont pas été réalisées chez les « hypersensibles ». De façon similaire pour le flux nasal, celui-ci était augmenté uniquement à 369 et 4 pics de 615 µg.m-3 chez les « hyposensibles ». Concernant les effets subjectifs, aucune différence statistiquement significative n’a été rapportée pour les tests d’irritation nasale et oculaire (ANSES, 2018).
Wilhelmsson et Holmstrom (1992) étudient les effets d’une exposition professionnelle chronique à une concentration moyenne de 0,21 ppm (0,26 mg.m-3) de formaldéhyde. Pour une durée de travail de 8 heures par jour, 5 jours par semaine, la durée moyenne d’exposition est de 10 ans (de 1 à 36 ans). Les effets observés chez les 66 travailleurs étaient des irritations oculaires et nasales et des lésions histologiques de l'épithélium nasal (rhinite, métaplasie squameuse, dysplasie). Cette étude a permis de dériver un NOAEC moyen de 0,09 mg.m-3 (groupe contrôle de travailleurs en bureau), pour une exposition discontinue et un LOAEC moyen de 0,26 mg.m-3 (de 0,05 à 0,6 mg.m-3).
La sensibilité exacerbée des enfants au formaldéhyde a été décrite une première fois dans une étude comparative, qui a observé une diminution de la fonction respiratoire d’enfants exposés à des concentrations faibles de 30 ppb (45 µg.m-3) de formaldéhyde, sans effet sur celle des adultes (Krzyzanowski et al., 1990). L’auteur fait également état, dans cette étude, d’une augmentation de la fréquence d'apparition de l'asthme et de la bronchite chez les enfants vivant dans des logements présentant des concentrations moyennes de formaldéhyde supérieures à 60 ppb (0,075 mg.m-3). Cette sensibilité des enfants au formaldéhyde a été confirmée par la présence au niveau sanguin, après exposition à de faibles concentrations de formaldéhyde, d’anticorps spécifiques (IgE) bien plus fréquente que chez les adultes, (Wantke et al., 1996). De plus, le transfert d’enfants d’une école à l’autre, correspondant à une exposition initiale comprise entre 43 et 75 ppm (soit 54 et 112 mg.m-3) et réduite à des valeurs comprises entre 23 et 29 ppm (34,5 et 43,5 mg.m-3), a pu être corrélé à une diminution du taux d’IgE et à la baisse des symptômes respiratoires.
Chez l’adulte, les études ne permettent pas aujourd'hui d'affirmer que le formaldéhyde est, de lui-même, une cause d’allergie respiratoire. En milieu professionnel, plusieurs travaux ont en effet permis de constater l’absence d’effet sur le système immunitaire, avec en particulier l’absence d’anticorps spécifiques (Dykewicz et al., 1991 ; Grammar et al., 1990 ; Kramps et al., 1989).
L’apparition de maladies respiratoires chroniques obstructives par expositions répétées au formaldéhyde, avec des retentissements sur la fonction respiratoire, reste très controversée. Il semblerait que la baisse du VEMS, faiblement significative dans la plupart des études, ne soit pas cohérente avec l’absence de signes cliniques. Les auteurs sont par ailleurs souvent confrontés à des problèmes d’interprétation dus à la co-exposition à d'autres produits ou à la présence de poussières de bois sur lesquelles s'adsorbe le formaldéhyde (Malaka et Kodama, 1990 ; Alexandersson et Hedenstierna, 1989 ; Neghab et al., 2011).
Une étude cas-témoin a été menée chez 162 patients asthmatiques dans des habitations du Bas-Rhin. Pour des niveaux de concentrations en formaldéhyde dans l’air ambiant similaires chez les patients asthmatiques et chez les témoins, cette étude a révélé une corrélation entre concentration en formaldéhyde dans l’air ambiant et la sévérité de l’asthme observé chez des sujets asthmatiques (AFSSET, 2008).
Le formaldéhyde a également été désigné comme responsable d’effets respiratoires à partir de 3 mg.m-3 chez des sujets présentant une hyperactivité respiratoire. Toutefois, ces résultats ne sont pas corroborés par l’étude de sensibilisation menée chez 12 sujets asthmatiques et allergiques au pollen par Ezratty et al. (2007). Plusieurs revues récentes de la littérature portant spécifiquement sur l’air intérieur de logements ou le milieu professionnel aboutissent à la conclusion qu’une sensibilisation respiratoire causée par le formaldéhyde est très peu probable, en particulier à de faibles concentrations (Golden, 2011 ; Schram-Bijkerk et al., 2013). En effet, les associations entre formaldéhyde et symptômes respiratoires pourraient s’expliquer par l’influence de co-expositions ou résulter de facteurs de confusion tels que des facteurs psychosociaux (ANSES, 2018).
Des troubles neurologiques (perte de la mémoire, manque de concentration) ont été décrits dans plusieurs études où la présence de formaldéhyde était concomitante à d'autres solvants neurotoxiques. Kilburn et al. (1985) ont pu établir une corrélation entre l'exposition au formaldéhyde et la baisse de performance à une batterie de tests alliant dextérité, mémoire et coordination. Cependant, en raison des co-expositions avec des solvants organiques, il n’est pas possible d’attribuer ces effets au seul formaldéhyde (INRS, 2022).
Voie orale
Les effets chroniques du formaldéhyde par voie orale chez l’homme ne sont pas documentés.
Voie cutanée
Le formaldéhyde est classé au niveau européen pour ses propriétés sensibilisantes cutanées. En solution, c’est un agent de sensibilisation cutanée induisant, lors d’expositions répétées, une dermatite allergique de contact (type IV, hypersensibilité retardée à médiation cellulaire) ou un urticaire de contact (type I, hypersensibilité immédiate, peut-être à médiation IgE) (Leikauf, 1992). Plusieurs études montrent l’augmentation de la fréquence de ces dermatites allergiques chez le personnel funéraire et hospitalier (Nethercott et Holness, 1988 ; Rudzki et al., 1989). Les réactions d’irritation cutanée n’apparaissent de façon certaine qu’au contact direct de solutions contenant du formaldéhyde (chez environ 5 % des sujets, d’après OMS IPCS, 1989).
Wilkinson et al. (2002) ont mis en évidence grâce à une étude multicentrique réalisée à travers 11 pays d’Europe (1991-2000), chez des patients consultants pour un eczéma de contact présumé, une prévalence de sensibilisation au formaldéhyde comprise entre 1,8 et 2,4 % (AFSSET, 2008).
Parmi les nombreux essais réalisés par « patch-test », l’étude de Flyvholm et al. (1997) a permis d’observer que les sujets sains ne développaient aucun signe d’irritation à la concentration de 1 % de formaldéhyde, et que les réactions allergiques étaient rares chez les sujets sensibilisés pour des expositions à des concentrations de 0,025 à 0,5 % en formaldéhyde.
Eberlein-Konig et al. (1998) ont montré, chez des personnes déclarant un urticaire de contact, que l'exposition à une concentration de 0,08 ppm (0,1 mg.m-3) de formaldéhyde pendant 4 heures était responsable, au niveau des bras, d’une déshydratation sans apparition de rougeurs.
Même si les seuils de sensibilisation chez l’homme sont difficiles à déterminer, Basketter et al. (2005), proposent une valeur de 37 µg.cm-2 obtenue à partir d’un test HRIPT (Human Repeated Insult Patch test), comparé à un LLNA (local lymph node assay) chez la souris (AFSSET, 2008).
Voie oculaire
Plusieurs études mentionnent également chez l’homme une forte irritation de contact au niveau des yeux (ACGIH, 1992 ; Krivanek et Imbus, 1992).
Synthèse
Chez l’homme, les principaux effets observés sont des effets locaux au niveau des voies aériennes supérieures avec une irritation des yeux, du nez et de la gorge, et des lésions de l’épithélium nasal. Le formaldéhyde possède également des propriétés de sensibilisation cutanée.
Chez l'animal
Inhalation
Des expositions répétées par inhalation à 40 ppm (50 mg.m-3) de formaldéhyde (6 heures par jour, 5 jours par semaine) pendant 13 semaines, ont entraîné une forte mortalité (80 %) des souris exposées. La mort des animaux, importante dans la cinquième et sixième semaine, a été attribuée au développement d’une rhinite purulente et à la formation de lésions occlusives dans la trachée (Maronpot et al., 1986). Les animaux avaient aussi des troubles de la coordination, une perte de poids très importante, et des foyers inflammatoires métaplasiques dans les cavités nasales, le larynx, la trachée et les poumons.
Rusch et al. (1983) ont mené une étude sur un groupe de 6 singes Cynomolgus mâles exposés par inhalation, à des concentrations en formaldéhyde de 0 - 0,19±0,02 – 0,98±0,08 ou 2,95±0,18 ppm, 22 heures par jour, 7 jours par semaine, et durant 26 semaines. Les singes du groupe exposé à la dose de 2,95 ppm montrent un enrouement, une congestion nasale et un écoulement nasal, en particulier durant les 13 dernières semaines de l’étude. Le poids des organes n’est pas modifié. Une augmentation significative de l’incidence de métaplasie/hyperplasie squameuse de l’épithélium nasal survient pour la concentration de 2,95 ppm. Ainsi, le NOAEC et le LOAEC pour l’irritation nasopharyngée sont respectivement 0,98 et 2,95 ppm.
Toujours par inhalation, mais pour des expositions chroniques supérieures à un an, de nombreuses études ont également montré un excès de mortalité chez la souris et le rat pour des expositions journalières comprises, selon les études, entre 5 et 15 ppm (6,25 et 18,75 mg.m-3) de formaldéhyde (Albert et al., 1982 ; Kerns et al., 1983 ; Swenberg et al., 1980 ; Kamata et al.,1997).
L’action inhibitrice des mouvements ciliaires, accompagnée d’une diminution de la clairance mucociliaire mise en évidence chez l’animal, existe aussi chez l’homme mais il n'a pas été établi de relation avec la dose ou la durée d'exposition (Leikauf, 1992 ; OMS IPCS, 1989).
À des doses non létales, aucune modification histologique des tissus lymphoïdes n'a été observée chez les différentes espèces étudiées (singe, rat, souris) (Monticello et al., 1989 ; Kamata et al., 1997 ; Kerns et al., 1983). Après 3 semaines d’exposition au formaldéhyde, il n’a a pas été observé, chez la souris, d’altérations du système immunitaire impliquant les lymphocytes T et B (AFSSET, 2008).
Des troubles du comportement sont décrits chez la souris et le rat pour une exposition à 20 ppm (25 mg.m-3) pendant 13 semaines (Maronpot et al., 1986 ; Appelman et al., 1988).
Voie orale
Lors de l’administration dans l’eau de boisson, l’excès de mortalité immédiat observé chez le rat, à la plus forte dose de 300 mg.kg-1.j-1, s’accentue au fil des mois pour atteindre 100 % après 21 mois d’exposition chez les femelles et 24 mois chez les mâles (Tobe et al., 1989). Les animaux ont présenté des lésions dégénératives sévères au niveau de l’estomac. Une valeur de NOAEL de 10 mg.kg-1.j-1 a été déterminée sur la base de cet effet.
A de plus faibles concentrations, aucun cas de mortalité n’a été décrit dans plusieurs études, aux concentrations de 10 et 50 mg.kg-1.j-1 (Vargova et al., 1993 ; Tobe et al., 1989).
Til et al. (1988b) ont étudié l’effet d’une absorption orale de formaldéhyde chez des rats de type Cpb:WU; Wistar random (10 mâles et 10 femelles). Ces animaux ont reçu 0, 5, 25, ou 125 mg.kg-1.j-1 de formaldéhyde dans l’eau de boisson durant 4 semaines. Les effets obtenus chez ces animaux ont été comparés à ceux observés au sein d’un groupe contrôle de 20 mâles et 20 femelles. Un NOAEL pour des effets gastro-intestinaux a été fixé à 25 mg.kg-1.j-1. A la dose de 125 mg.kg-1.j-1, un épaississement et une hyperkératose de la paroi du pré-estomac, une inflammation focale atrophique de la zone glandulaire de l’estomac, une hyperkératose légère à modérée du pré-estomac, une gastrite, une hyperplasie papillomateuse ont été observés.
Ceci a été confirmé chez le chien pour des expositions allant jusqu’à 100 mg.kg-1.j-1 pendant 3 mois (Johannsen et al., 1986). Les animaux (rats, chiens) présentent une perte de poids plus ou moins sévère selon les études (de 10 à 40 % par comparaison aux animaux témoins).
Les effets sur le tractus gastro-intestinal ne s’observent chez le rat qu’après plus d’une année de traitement et se traduisent par le développement de papillomes, associés à une hyperkératose, une légère atrophie gastrique et la présence d’ulcérations localisées. Les valeurs de NOEL associées à ces effets sont de 15 mg.kg-1.j-1 chez les mâles et 21 mg.kg-1.j-1 chez les femelles dans l’étude de Til et al. (1988b) et 10 mg.kg-1.j-1 tous sexes confondus dans l’étude de Tobe et al. (1989).
Ces études montrent par ailleurs que les systèmes respiratoire et cardiaque ne sont pas altérés par une exposition prolongée au formaldéhyde par voie orale.
Les atteintes hépatiques et rénales sont absentes de la plupart des études ou limitées à la diminution de protéines, d’albumine, de cholestérol total plasmatique ou l’augmentation d’urée dans le sang (Johannsen et al., 1986 ; Tobe et al., 1989).
Til et al. (1989) ont étudié les effets d’une administration orale (via l’eau de boisson) de concentrations de 5, 25, et 125 mg.kg-1.j-1 de formaldéhyde (95% de paraformaldéhyde), à des rats de type Cpb:WU; Wistar random, durant 2 ans. Les concentrations administrées, étaient : 0, 1,2, 15, ou 82 mg.kg-1.j-1 pour les mâles et 0, 1,8, 21, ou 109 mg.kg-1.j-1 pour les femelles. Un NOAEL de 15 mg.kg-1.j-1 est déterminé pour des effets gastro-intestinaux chez le mâle. A 82 mg.kg-1.j-1, les effets suivants ont été observés : modifications gastriques incluant hyperplasie épithéliale papillaire et hyperkératose, ulcération du pré-estomac, et gastrite chronique atrophique, occasionnellement accompagnée d’une ulcération et/ou une hyperplasie au niveau de l’estomac glandulaire et d’une nécrose rénale papillaire.
Voie cutanée
Le caractère irritant du formaldéhyde par voie cutanée, fortement suspecté chez l’homme, a été confirmé par deux études réalisées l’une chez le cobaye et l’autre chez la souris. Dans la première étude, l’application quotidienne de formaldéhyde (solution de 0,5 à 4 %) entraîne après 2 jours l’apparition d’un érythème qui précède une hyperkératose (Wahlberg, 1993). Dans la seconde étude, sur une période de deux ans, il a été observé la présence d’ulcérations et d’hyperplasie consécutives à l’application de solutions de 1 à 10 % de formaldéhyde chez la souris (Iversen, 1988).
Aucun NOAEL ou LOAEL n’a été déterminé dans ces deux études.
Synthèse
Les études menées chez l’animal confirment la sensibilité des voies aériennes supérieures à une exposition chronique de formaldéhyde. L’exposition chronique au formaldéhyde par voie orale chez l’animal a montré un excès de mortalité chez le rat, ainsi que des lésions dégénératives sévères de l’estomac.
Effets cancérigènes
Classifications
| Organisme | Classification | Année |
|---|---|---|
| UE | Catégorie 1B : substance dont le potentiel cancérogène pour l’homme est supposé en raison d’effets cancérogènes possibles | 2014 |
| IARC | Groupe 1 : le formaldéhyde est cancérigène pour l’homme | 2004 |
| US EPA | Classe B1 : le formaldéhyde est probablement cancérigène pour l'homme. Des données limitées chez l'homme sont disponibles | 1991 |
Chez l'homme
Inhalation
Les principaux cancers étudiés chez les sujets exposés au formaldéhyde par inhalation concernent les voies respiratoires supérieures et la cavité buccale, et plus marginalement le cerveau, ou l’apparition de leucémies et de maladies de Hodgkin. Les populations étudiées sont des professionnels utilisant le formaldéhyde pour la préservation des tissus biologiques (embaumeurs, anatomopathologistes) et les travailleurs de l’industrie intervenant dans la production ou l’utilisation de ce produit (industrie chimique, textile, du bois et des résines). Les niveaux et les durées d’exposition ne sont pas toujours connus avec précision.
- Cancer du nasopharynx
Parmi les données disponibles, les deux méta-analyses de Blair et al. (1990) et Partanen (1993) qui reprennent par des techniques d’analyses un peu différentes les données d’études épidémiologiques (cas-témoins pour l’essentiel), arrivent aux mêmes conclusions. Tous deux considèrent en effet, que c’est pour le cancer du nasopharynx, et dans une moindre mesure celui des cavités nasales, que l’on peut attribuer un rôle causal hautement probable au formaldéhyde, en raison d’une relation exposition-effet et de l’action directe du formaldéhyde sur ces sites (site de contact respiratoire). Dans ce sens, la méta-analyse de Collins et al. (1997) met en évidence un risque « méta –relatif » accru de développement de cancer du nasopharynx.
Le groupe de travail à l’origine de la monographie de l’IARC (2006) sur le formaldéhyde, considère qu’il est improbable que les nombreux résultats positifs pour le cancer du nasopharynx recensés dans différentes études épidémiologiques soient le fait de biais. Il conclut que les résultats des études menées aux USA chez des travailleurs de l’industrie (cohorte NCI (National Cancer Institute) regroupant 25 619 travailleurs de l’industrie exposés au formaldéhyde), ainsi que les nombreux autres résultats positifs tirés d’autres études, apportent une preuve épidémiologique suffisante pour démontrer que le formaldéhyde peut être à l’origine de cancers du nasopharynx chez l’homme.
La méta-analyse de Collins et al. (1997) était basée sur 11 études de cohortes, 3 études de mortalité proportionnelle et 15 études cas-contrôles publiées entre 1975 et 1995 (après 1992 pour la plupart). Le risque « méta-relatif » global pour le cancer nasal était de 1. Le risque méta-relatif pour le cancer du nasopharynx était de 1,3, chiffre basé sur 12 études portant sur 455 cas et de 1,6 pour les études de cohorte.
Les résultats des 3 méta-analyses, citées ci-dessus, sont présentés dans le tableau suivant (d’après IARC, 2006).
|
Niveau ou durée d’exposition |
Sites de cancer |
||||
|
Nez et sinus nasaux |
Nasopharynx |
||||
|
O/A* |
Risque méta-relatif (IC 95%) |
O/A* |
Risque méta-relatif (IC 95%) |
Références |
|
|
Toutes expositions confondues |
61/58 |
1,0 (0,8-1,3) |
35/27 |
1,3 (0,9-1,8) |
Blair et al. (1990) |
|
93/78 |
1,11 (0,81-1,53) |
36/21 |
2,00 (1,36-2,90) |
Partanen (1993) |
|
|
936/808 |
1,0 (1,0-1,1) |
455/412 |
1,3 (1,2-1,5) |
Collins et al. (1997) |
|
|
Faible à moyenne |
38/46 |
0,8 (0,6-1,1) |
30/27 |
1,1 (0,7-1,6) |
Blair et al. (1990) |
|
33/30 |
1,10 (0,67-1,79) |
23/16 |
1,59 (0,95-2,65) |
Partanen (1993) |
|
|
Elevée |
30/28 |
1,1 (0,7-1,5) |
13/6 |
2,1 (1,1-3,5) |
Blair et al. (1990) |
|
36/21 |
1,68 (1,00-2,82) |
11/4 |
2,74 (1,36-5,55) |
Partanen (1993) |
|
*Observés/Attendus
Dans une étude multicentrique cas-témoins issue de 5 banques de données sur les cancers aux USA, un rapprochement était effectué entre l’exposition professionnelle au formaldéhyde, les poussières de bois et les cancers du nasopharynx (Vaughan et al., 2000). Les sujets retenus étaient des hommes ou des femmes, entre 18 et 74 ans, ayant un cancer nasopharyngé. L’étude portait sur 294 sujets et 244 témoins. La proportion de sujets potentiellement exposés au formaldéhyde était de 40,3%, versus 32,4% chez les contrôles. Chez les sujets exposés professionnellement, l’odd-ratio pour les cancers nasopharyngés épithéliaux était de 1,3 (IC 95%, 0,8-2,1). Le risque avait tendance à augmenter avec la durée de l’exposition : l’odd-ratio chez des sujets professionnellement exposés au moins 18 ans était de 2,1 (IC 95%, 1-4,5).
Dans un avis du BFR (Bundesinstitut für Risikobewertung) paru en mars 2006, il est souligné que les travaux d’Hauptmann et al. (2004) ont mis en évidence une relation causale entre l’exposition au formaldéhyde et l’incidence de tumeurs de la région nasopharyngée chez l’homme. Cette incidence est d’autant plus élevée que le niveau d’exposition est important. Dans les études humaines, la relation dose réponse n’a été évaluée que sur l’intervalle de valeurs 1 à 5 ppm, il n’existe pas de données humaines aux concentrations supérieures à 6 ppm.
Les plus récentes mises à jour des études de cohortes industrielles, dont la cohorte NCI (Möhner et al., 2019), ainsi que l’analyse de deux autres cohortes finlandaise (1,2 millions d’hommes professionnellement actifs) (Siew et al., 2012) et italienne (3 126 employés d’une usine de plastique stratifié) (Pira et al., 2014), ne montrent pas d’excès de risque de cancer nasopharyngé (INRS, 2022).
- Cancers pulmonaires
Bien que le faible excès de risque noté pour les cancers pulmonaires ne soit pas associé aux différentes mesures d’exposition (latence, durée, niveau ou cumul), le rôle du formaldéhyde a été envisagé (Blair et al., 1986 ; Bond et al., 1986 ; Chiazze et al., 1993). Ces données ont été revues et complétées par Blair et al. en 1990 et 1994, les auteurs ont conclu à l’absence de lien entre exposition au formaldéhyde et cancer du poumon.
Ces études ont été successivement réinterprétées, et la divergence des conclusions, selon le type d’analyse, contribue à alimenter les discussions quant à l’occurrence du cancer pulmonaire chez les personnes exposées au formaldéhyde.
- Cancers cérébraux
Le risque augmenté de mortalité par cancers cérébraux n’a généralement pas été trouvé parmi les travailleurs de l’industrie, mais il semble exister pour les embaumeurs et anatomopathologistes, suggérant que d’autres facteurs que le formaldéhyde entrent en jeu (Harrington et Oakes, 1984 ; Stroup et al., 1986 ; Walrath et Fraumeni 1984).
- Leucémies
Une mortalité excessive par leucémie est apparue de façon assez constante dans 6 des 7 études menées chez des travailleurs exposés au formaldéhyde (embaumeurs, employés des pompes funèbres et anatomopathologistes). Une méta-analyse récemment publiée (Collins et Lineker, 2004), étudiant le risque de leucémie chez les professionnels exposés au formaldéhyde montre des résultats relativement homogènes entre les études et rapporte un risque accru chez les professionnels type embaumeurs (risque méta-relatif 1,6 ; 95% IC, 1,2-2,0) et anatomopathologistes (risque « méta-relatif » 1,4 ; 95% IC, 1,0-1,9). La majorité des leucémies observées dans ces études sont de type myéloïde. Plus récemment, un excès de risque de décès par leucémie myéloïde (34 cas dont 20 de leucémie myéloïde aiguë) (OR 11,2, IC 95 % 1,3-95,6) a été corrélée avec la durée de travail chez les embaumeurs dans une étude cas-témoins nichée dans une cohorte de 6 808 travailleurs exposés au formaldéhyde (embaumeurs, employés des pompes funèbres) (Mundt et al., 2018).
Jusqu’à récemment, les résultats de ces études n’étaient pas corroborés par ceux obtenus lors d’études menées chez les professionnels de l’industrie, exposés au formaldéhyde (risque « méta-relatif » 0,9 ; 95% IC, 0,8-1,0). Cependant, une récente mise à jour de ces études a mis en évidence une incidence élevée de leucémies dans deux des trois cohortes de professionnels de l’industrie étudiées (Marsh et Youk, 2004 ; Pinkerton et al., 2004). Une réserve peut être émise sur certains de ces résultats car dans l’une des cohortes (Stayner et al., 1985, 1988), le faible nombre relatif de décès n’était pas statistiquement significatif. L’étude portait sur environ 11000 femmes employées de 3 usines produisant des chemises traitées au formaldéhyde. Les niveaux d’exposition étaient compris entre 0,09 et 0,2 ppm au début de l’étude et ne sont pas connus pour la suite de l’étude, mais ils sont présumés être inférieurs. Un faible excès de mortalité par leucémie a été rapporté : 24 décès, SMR 1,09 (95% IC, 0,70-1,62). Et celui-ci était supérieur pour les leucémies myéloïdes : 15 décès, SMR 1,44 (95% IC, 0,80-2,37).
L’étude de Coggon et al. (2003), menée chez des travailleurs de l’industrie britannique, n’a pas révélé une mortalité accrue par leucémies chez ces travailleurs exposés au formaldéhyde. Cette étude a été menée dans une cohorte de 14014 travailleurs industriels masculins (industrie chimique produisant du formaldéhyde), les données collectées couvraient la période de 1941 à 2000. Quatre niveaux d’exposition sont évalués : < 0,1 ppm - 0,1 à 0,5 ppm - 0,6 à 2 ppm et > 2 ppm. 31 décès par leucémies sont rapportés, l’excès de risque ne dépassant pas 0,91 (95% IC 0,47-1,59). Cette étude, de bonne qualité, porte sur un large échantillon de travailleurs et couvre une durée suffisante d’exposition pour présenter des résultats fiables.
Voie orale
Le formaldéhyde par voie digestive ne conduit pas au développement de tumeur cancéreuse (OMS, 2022). Il n’existe pas de données montrant une relation entre exposition cutanée au formaldéhyde et augmentation de l’incidence de tumeurs (AFSSET, 2008). Seules les propriétés cancérigènes du formaldéhyde par inhalation sont donc présentées ci-dessus.
Synthèse
Il existe des informations robustes pour établir une présomption de lien de causalité entre l’exposition professionnelle au formaldéhyde et l’apparition de cancer nasopharyngé et de leucémies notamment de type myéloïde. Les données concernant les autres types de cancers sont très limitées. L’IARC considère qu’il existe une preuve épidémiologique suffisante pour démontrer que le formaldéhyde peut être à l’origine de cancers du nasopharynx chez l’homme. Il existe également une forte présomption, mais non suffisante, pour établir un lien de causalité entre l’exposition professionnelle au formaldéhyde et l’apparition de leucémies. Bien que l’excès de risque noté pour les cancers pulmonaires soit faible, le rôle du formaldéhyde ne peut être exclu définitivement.
Effets génotoxiques
Classifications
| Organisme | Classification | Année |
|---|---|---|
| UE | Le formaldéhyde est classé mutagène catégorie 2 | 2014 |
Chez l'animal
Toutes voies
In vivo, le formaldéhyde est génotoxique sur les cellules somatiques au site de contact. En particulier, des adduits ADN-protéine (DPX) ont été induits dans la muqueuse nasale des rats et dans les cornets nasaux des singes exposés par inhalation. La réparation incomplète des adduits peut alors conduire à des mutations (Barker et al., 2005) ou des effets clastogènes (Anses, 2011). Cependant, les études in vivo n’ont pas montré de potentiel génotoxique du formaldéhyde sur les cellules somatiques à distance du site de contact (ECHA, 2012).
Synthèse
les études in vivo montrent que le formaldéhyde semble être un composé génotoxique direct dont les effets sont principalement observés au niveau du site de contact et pour des concentrations élevées. La formation d’adduits ADN-protéines dans la muqueuse nasale serait déterminante dans le mécanisme d’action cancérogène du formaldéhyde au niveau du nasopharynx.
In vitro
Organismes eucaryotes
Données humaines :
Les résultats des tests du micronoyau sur lymphocytes circulants issus de différentes études chez des travailleurs exposés au formaldéhyde indiquent une corrélation entre le niveau et la durée d’exposition au formaldéhyde et la présence d’une instabilité génétique dans les lymphocytes circulants sous la forme de micronoyaux lorsque les lymphocytes sont mis en culture ex-vivo (Wang et al., 2009 ; Fenech et al., 2016). Cependant, ce test ne permet pas de distinguer si les micronoyaux observés proviennent de l’effet du formaldéhyde sur les lymphocytes circulants lorsque ceux-ci sont dans la circulation sanguine, ce qui serait plutôt un marqueur d’exposition au formaldéhyde, ou d’un effet sur les progéniteurs lymphoïdes localisés dans la moelle osseuse, qui en accumulant des mutations généreraient des lymphocytes circulants pourvus d’une plus grande instabilité génétique.
Dans une autre étude conduite chez 46 travailleurs d’une fabrique de meubles exposés au formaldéhyde (moyenne par prélèvements pendant 8 heures sur 7 sites : 37 à 111 µg.m-3) versus 45 sujets non exposés, les résultats du test des comètes ont montré un index et une fréquence de dommages de l’ADN plus élevés chez les sujets exposés (cellules de sang périphérique), ainsi qu’une fréquence augmentée de cellules binucléées micronucléées par le test du micronoyau (cellules de la muqueuse buccale) (Peteffi et al., 2016). En revanche, aucune corrélation n’a été mise en évidence entre les marqueurs de génotoxicité et le taux d’acide formique urinaire, ce dernier étant considéré comme trop peu spécifique.
En conclusion, il n’y a pas de preuves suffisantes pour conclure à la génotoxicité systémique du formaldéhyde chez l’Homme (ANSES, 2018).
Etudes chez l’animal :
Différentes études de génotoxicité ont montré des résultats positifs tant sur bactéries que sur cellules de mammifères in vitro. Ces tests ont également mis en évidence la capacité du formaldéhyde à induire des lésions primaires de l’ADN et des adduits ADN-protéine pouvant, en cas de réparation incomplète, produire des mutations. Il peut donc être considéré comme un mutagène in vitro avec un mode d’action clastogénique (Speit et al., 2011).
Synthèse
En conclusion, il n’y a pas de preuves suffisantes pour conclure à la génotoxicité systémique du formaldéhyde chez l’Homme (ANSES, 2018).
Chez l'animal, les études in vitro montrent que le formaldéhyde semble être un composé génotoxique direct dont les effets sont principalement observés au niveau du site de contact et pour des concentrations élevées. La formation d’adduits ADN-protéines dans la muqueuse nasale serait déterminante dans le mécanisme d’action cancérogène du formaldéhyde au niveau du nasopharynx.
Effets sur la reproduction
Chez l'homme
Inhalation
Ward et al. (1984) ont étudié la qualité du sperme de 11 hommes exposés par inhalation au formaldéhyde dans le cadre de leur emploi dans un service hospitalier de médecine légale. Ils ont été comparés à 11 sujets témoins. Dix des sujets étaient employés dans le service depuis 4,3 mois en moyenne (de 1 à 11 mois) et un depuis plusieurs années. Les expositions au formaldéhyde étaient ponctuelles et comprises en moyenne entre 0,61 et 1,32 ppm (soit 0,76 et 1,65 mg.m-3) (exposition par semaine de 3 à 40 ppm.h-1 soit 3,75 à 50 mg.m-3). Les auteurs n’ont pas mis en évidence de différences significatives de qualité du sperme entre les sujets professionnellement exposés et les témoins. Chez la femme (275 sujets) un taux d'avortements spontanés de 11,6 % a été jugé compatible avec le taux basal d'avortements (Garry et al., 1980).
Le nombre limité des sujets de la première étude et le manque de données sur l'exposition dans la seconde restreignent les conclusions relatives à ces études.
Des effets sur la reproduction (cycles menstruels perturbés, grossesses difficiles, fausses couches) ont été observés chez des femmes professionnellement exposées au formaldéhyde (Grazuleviciene et al., 1998). L’exposition maternelle au formaldéhyde a été associée à un excès de risque d’avortement spontané dans une méta-analyse de 18 études (RR 1,76 ; IC 95 % 1,2-2,59) (données de 7 études) (Duong et al., 2011).
De plus, une diminution du poids des nouveau-nés en rapport avec l’exposition des mères au formaldéhyde (>2,8 ppb) a été notée (Grazuleviciene et al., 1998).
Du fait de la biodisponibilité systémique extrêmement faible du formaldéhyde dans les conditions d’exposition professionnelle, des effets reprotoxiques ne sont pas attendus (INRS, 2022).
Voie orale
Cette voie d’exposition n' est pas documentée chez l’homme.
Voie cutanée
Cette voie d’exposition n'est pas documentée chez l’homme.
Chez l'animal
Inhalation
Deux études menées chez des rats Wistar Albino mâles et femelles par Woutersen et al. (1987) et Appelman et al. (1988) ont montré que des expositions au formaldéhyde aux concentrations de 0,1, 1, 10 et 20 ppm (6 heures par jour, 5 jours par semaine, 13 et 52 semaines) n’entraînent aucune altération morphologique des testicules et des ovaires.
Maronpot et al. (1986) ont étudié chez 10 souris B6C3F1 mâles et 10 femelles, les effets d’une exposition à des concentrations en vapeur de formaldéhyde de 2, 4, 10, 20 ou 40 ppm (soit 3, 6, 15, 30 ou 60 mg.m-3) (6 heures par jour, 5 jours par semaine durant 13 semaines). Les lésions ovariennes observées pour une exposition à 40 ppm (50 mg.m-3) sont, d'après les auteurs, plutôt la conséquence de l'affaiblissement général de la souris qu'un effet ciblé du formaldéhyde.
Voie orale
Des effets non précisés sur la spermatogenèse ont été mis en évidence chez le rat pour une exposition de 200 mg.kg-1 pendant un jour dans une étude de qualité incertaine (AFSSET, 2008).
Ward et al. (1984) ont évalué la qualité du sperme chez des souris B6C3F1 après l’administration orale pendant 5 jours de doses de 100 mg.kg-1 de formaldéhyde. Aucune anomalie morphologique n’a été détectée chez les animaux traités.
Voie cutanée
Des hamsters Syriens femelles en gestation, ont été traités par applications topiques de 0,5 mL de solution de formaldéhyde à 37 %, aux jours 8, 9, 10 et 11 de leur gestation. Les fœtus ont été prélevés à J15 chez 4 hamsters sur 6 par lot, ont été pesés, mesurés et observés. Le taux d’avortement était supérieur dans le groupe traité, mais aucun effet tératogène n’a été mis en évidence. Les effets observés semblent davantage liés au stress inhérent à l’application cutanée du traitement plutôt qu’au formaldéhyde lui-même (Overman, 1985).
Synthèse
La qualité des données disponibles dans la littérature ne permet pas de classer le formaldéhyde comme reprotoxique.
Effets sur le développement
Chez l'animal
Inhalation
Pour des expositions à des concentrations de 2, 5 ou 10 ppm (2,5, 6,2 ou 12,3 mg.m-3), 6 heures par jour du 6ème au 15ème jour de gestation, aucune toxicité maternelle ou fœtale n'a été observée chez 25 rates Sprague–Dawley gestantes (Martin, 1990). Par contre, Saillenfait et al. (1989) considèrent que le formaldéhyde présente une légère fœtotoxicité à partir d’une exposition de 20 ppm (25 mg.m-3)(du 6ème au 20éme jour de gestation), mais n’a retrouvé à la plus forte concentration de 40 ppm (60 mg.m-3) aucun effet tératogène.
L’IARC (2006) a conclu qu’aucun effet tératogène n’a pu être mis en évidence chez des femelles gestantes, à des niveaux de concentration en formaldéhyde inférieurs aux concentrations toxiques maternelles.
Voie orale
Les études réalisées chez la souris, le rat et le chien n’ont pas permis de déceler d’éventuels effets tératogènes ou fœto-toxiques du formaldéhyde (Hurni et Ohder, 1973 ; Seidenberg et Becker, 1987 ; Til et al., 1988b ; Tobe, 1989 ; Johannsen et al., 1986). Concernant le rat, les valeurs de NOAEL sont, selon les différentes études, de 125 mg.kg-1.j-1 (exposition de 4 semaines, Til et al., 1988b), 150 mg.kg-1.j-1 (exposition de 3 mois, Johannsen et al., 1986) et 300 mg.kg-1.j-1 (exposition de 12 mois, Tobe et al., 1989).
Chez le chien, un NOAEL de 9,4 mg.kg-1.j -1a été déterminé pour une exposition des femelles du 4ème au 56ème jour de gestation.
Chez le rat, des anomalies du développement fœtal ont été mises en évidence pour une exposition du 1er au 21ème jour de gestation (atteinte du système hépatobiliaire, altérations biochimiques chez les fœtus) avec un LOAEL de 8 mg.kg-1.j-1.
Voie cutanée
Synthèse
La qualité des données disponibles dans la littérature ne permet pas de classer le formaldéhyde comme reprotoxique ou embryotoxique.
Valeurs accidentelles
Valeurs seuils de toxicité aigüe françaises
Le rapport de valeurs seuils de toxicité aiguë françaises est accessible dans la rubrique « Archives ». L’intégralité des rapports de valeurs seuils de toxicité aiguë françaises actuellement en vigueur est consultable dans le tableau des VSTAF.
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Autres seuils accidentels
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Valeurs réglementaires
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Valeurs guides
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Valeurs de référence
Introduction
Une Valeur Toxicologique de Référence (VTR) est un indice qui est établi à partir de la relation entre une dose externe d'exposition à une substance dangereuse et la survenue d'un effet néfaste. Les valeurs toxicologiques de référence proviennent de différents organismes. Pour accéder à une information actualisée, nous conseillons au lecteur de se reporter directement sur les sites internet des organismes qui les élaborent.
Dans la mesure, où il a été démontré que le formaldéhyde présente un mécanisme de genèse de cancer à seuil, il n’est pas retenu de valeur sans seuil. Par ailleurs, d’après les données disponibles, l’OMS considère dans le formaldéhyde n’est pas cancérigène par voie orale (OMS, guide eau de boisson, 2022).
Valeurs de l'ANSES et/ou de l'INERIS
Description
Effets à seuil - Exposition aiguë par inhalation:
L’ANSES propose une VTR de 123 µg.m-3 (0,1 ppm) pour une exposition aiguë par inhalation au formaldéhyde (ANSES, 2018)
Cette valeur a été construite à partir d’une étude chez le volontaire sain exposé en continu pendant 4 h au formaldéhyde avec ou sans pic d’exposition de 15 minutes (Lang et al., 2008). Dans cette étude les concentrations varient entre 185 et 615 µg.m-3. L’effet critique retenu est l’irritation oculaire qui est un effet précoce des irritation nasale et respiratoire. Dans cette étude, une augmentation de la fréquence de clignement oculaire et de rougeur oculaire sont observés à partir de 615 µg.m-3 avec 4 pics d’exposition de 1 230 µg.m-3. Aucun effet n’a été observé à la concentration inférieure de 369 µg.m-3 qui est retenue comme une NOAEC. Aucun ajustement temporel ou allométrique n’a été appliqué.
Facteurs d’incertitude : un facteur d’incertitude 3 a été utilisé pour tenir compte de variabilité de sensibilité au sein de la population.
Calcul : 369 µg.m-3 x 1/3 = 123 µg.m-3
Indice de confiance : L’ANSES accorde un indice de confiance fort dans sa valeur correspondant à un indice fort pour la nature et la qualité des données, pour le choix de l’effet critique et le mode d’action, le choix de l’étude clé et un indice moyen pour le choix de la concentration critique.
Effets à seuil - Exposition sub-chronique par inhalation:
L’ATSDR propose un MRL de 40 µg.m-3 (0,03 ppm) pour une exposition subchronique par inhalation (ATSDR, 2010)
Cette valeur est établie à partir d’une étude expérimentale chez le singe exposé aux concentrations de 0 – 0,19 – 0,98 – 2,95 ppm de formaldéhyde 22 h/j, 7 j/7 pendant 26 semaines. Le MRL est dérivé d’un NOAEL de 0,98 ppm (1,2 mg.m-3) défini sur la base de l’augmentation de lésions métaplasiques et hyperplasiques au niveau des cavités nasales (Rusch et al., 1983).
Facteurs d’incertitude : un facteur de 30 a été appliqué (3 pour l’extrapolation de l’animal à l’homme, 10 pour la variabilité au sein de la population)
Calcul : 0,98 x 1/30 = 0,03 ppm
Indice de confiance : cet organisme ne propose pas d’indice de confiance.
Effets à seuil - Exposition chronique par inhalation:
L’ANSES propose une VTR de 123 µg.m-3 (0,1 ppm) pour une exposition chronique par inhalation au formaldéhyde (ANSES, 2018).
Cette valeur est la même que celle développée pour des expositions aigües. En effet, l’ANSES considère « L’effet critique retenu suite à une exposition chronique au formaldéhyde est le cancer du nasopharynx. En effet, il s’agit de l’effet cancérogène du formaldéhyde le mieux décrit, pour lequel une relation causale est établie à partir de nombreuses données humaines, animales et mécanistiques. Le développement de cancers du nasopharynx est lié à une altération répétée et prolongée de l’épithélium nasal, donc à des expositions suffisamment importantes et prolongées causant préalablement une irritation. Les données sur le mécanisme d’action permettent de déterminer une relation dose-réponse à seuil, inscrivant une succession d’évènements clés conduisant à la formation de tumeurs au niveau du nasopharynx dont le premier est l’irritation oculaire et nasale. »
Ainsi, l’ANSES retient l’irritation oculaire pour protéger de la survenue de cancer du nasopharynx.
Facteurs d’incertitude : un facteur d’incertitude 3 a été utilisé pour tenir compte de variabilité de sensibilité au sein de la population.
Calcul : 369 µg.m-3 x 1/3 = 123 µg.m-3
Indice de confiance : L’ANSES accorde un indice de confiance moyen dans sa valeur correspondant à un indice fort pour le choix de l’effet critique et le mode d’action et un indice moyen pour la nature et la qualité des données, le choix de l’étude clé et le choix de la concentration critique.
Effets à seuil - Exposition sub-chronique par voie orale:
L’ATSDR propose un MRL par voie orale de 0,3 mg.kg-1.j-1 pour une exposition subchronique par voie orale au formaldéhyde (ATSDR, 2010)
Cette valeur est basée sur une étude chez le rat exposé à 0 – 5 – 25 – 125 mg.kg-1.j-1 de formaldéhyde via l’eau de boisson pendant 4 semaines (Til et al., 1988b). L’existence d’effets gastro-intestinaux a été observée à 125 mg.kg-1.j-1 mais n’est pas retrouvée à la plus faible dose (25 mg.kg-1.j-1) qui est retenue comme un NOAEL.
Facteurs d’incertitude : un facteur de 100 a été appliqué (10 pour la variabilité au sein de la population et 10 pour l’extrapolation de données animales vers l’homme).
Calcul : NOAEL x 1/100 = 25 mg.kg-1.j-1 x 1/100 = 0,25 mg.kg-1.j-1 (arrondi à 0,3 mg.kg-1.j-1)
Indice de confiance : cet organisme ne propose pas d’indice de confiance.
Effets à seuil - Exposition chronique par voie orale:
L’ATSDR propose un MRL par voie orale de 0,2 mg.kg-1.j-1 pour une exposition chronique par voie orale au formaldéhyde (ATSDR, 2010)
Cette valeur est basée sur une étude chez le rat exposé à 0 – 5 – 25 – 125 mg.kg-1.j-1 de formaldéhyde via l’eau de boisson pendant 2 ans (Til et al., 1988b) correspondant à des doses de 0 – 1,2 – 15 – 82 mg.kg-1.j-1 chez le mâle. Des effets gastrointestinaux correspondant à des hyperplasies épithéliales papillaires associées à une hyperkératose et une altération locale du préestomac et une atrophie gastrique chronique localisée occasionnellement accompagnée d’une ulcération et/ou d’une hyperplasie glandulaire (au niveau de l’estomac glandulaire) et d’une nécrose rénale papillaire. En l’absence d’effet à la dose la plus faible, celle-ci est retenue comme NOAEL de 15 mg.kg-1.j-1.
Facteurs d’incertitude : un facteur de 100 a été appliqué (10 pour l’extrapolation de l’animal à l’homme, 10 pour la variabilité au sein de la population).
Calcul : NOAEL x 1/100 = 15 mg.kg-1.j-1 x 1/100 = 0,15 mg.kg-1.j-1 (arrondie à 0,2 mg.kg-1.j-1)
Indice de confiance : cet organisme ne propose pas d’indice de confiance.
L’US EPA (IRIS) propose une RfD par voie orale de 0,2 mg.kg-1.j-1 pour une exposition chronique par voie orale au formaldéhyde (US EPA, 1990)
Cette valeur est construite de manière identique à celle de l’ATSDR pour des expositions chroniques par voie orale. Elle a été calculée en appliquant un facteur d’incertitude de 100 au NOAEL de 15 mg.kg-1.j-1 établi lors d’une étude de deux ans chez le rat au cours de laquelle des irritations de l’estomac ont pu être observées (Til et al., 1989). La valeur calculée de 0,15 mg.kg-1.j-1 a été arrondie à 0,2 mg.kg-1.j-1.
Facteurs d’incertitude : un facteur de 100 a été appliqué (10 pour l’extrapolation de l’animal à l’homme, 10 pour la variabilité au sein de la population).
Calcul : NOAEL x 1/100 = 15 mg.kg-1.j-1 x 1/100 = 0,15 mg.kg-1.j-1 (arrondie à 0,2 mg.kg-1.j-1)
Indice de confiance : L’US EPA accorde un indice de confiance élevé dans l’étude retenue, moyen dans la base de données et moyen dans la valeur qui a été construite.
A noter que l’US EPA travaille sur une révision de cette valeur (US EPA, 2022).
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Synthèse
Effets à seuil - Exposition aiguë par inhalation:
L’ANSES retient pour une exposition aiguë au formaldéhyde par inhalation la VTR de 123 µg.m-3 (Anses, 2018).
Cinq valeurs sont disponibles dont deux de l’OEHHA : ATSDR, 2010 ; OEHHA, 2014 ; TCEQ, 2015 ; ANSES, 2018.
La valeur de l’OEHHA pour 8 heures est construite à partir d’une étude chez le travailleur exposé pendant 10 ans. Cette durée d’exposition n’est pas compatible avec la construction d’une valeur pour des expositions aiguës.
Les quatre autres valeurs sont construites sur des études sur le volontaire sain respectivement Pazdrak et al. (1993), Krakoviac et al. (1998), Kulle et al., 1987 et Lang et al., (2008) pour l’ATSDR, le TCEQ, l’OEHHA et l’ANSES. L’étude retenue par l’ANSES correspond à des niveaux d’exposition plus bas. Cette démarche est retenue.
Indice de confiance : l’ANSES accorde un indice de confiance fort dans sa valeur.
Effets à seuil - Exposition sub-chronique par inhalation:
L’INERIS propose de retenir pour une exposition sub-chronique au formaldéhyde par inhalation la VTR de 123 µg.m-3 développée par l’ANSES pour des expositions chroniques.
Une seule VTR est proposée par l’ATSDR (2010). Cette valeur de 4.10-2 mg.m-3 est établie à partir d’une étude chez le singe (Rusch et al., 1983). Toutefois pour des raisons de cohérence avec les valeurs développées par l’ANSES pour des expositions aiguées et chroniques cette valeur ne sera pas retenue. La valeur qui sera retenue est la proposition de l’ANSES pour des expositions chroniques.
Indice de confiance : l’ANSES accorde un indice de confiance moyen dans sa valeur.
Effets à seuil - Exposition chronique par inhalation:
L’ANSES retient pour une exposition chronique au formaldéhyde par inhalation la VTR de 123 µg.m-3 (Anses, 2018).
Quatre valeurs sont disponibles (ATSDR, 2010 ; OEHHA, 2008 ; TCEQ, 2023 et ANSES, 2018).
Les valeurs de l’ATSDR, de l’OEHHA et du TCEQ sont construites à partir d’études épidémiologique chez le travailleur.
La valeur de l’ANSES est élaborée à partir d’une étude chez le volontaire sain en considérant que le développement de cancers du nasopharynx est lié à une altération répétée et prolongée de l’épithélium nasal causant une irritation par un mécanisme à seuil de dose et que l’irritation oculaire protège de la survenue de cancer du nasopharynx. La valeur proposée est celle construite pour une exposition aiguë au formaldéhyde. Cette démarche est retenue.
Indice de confiance : l’ANSES accorde un indice de confiance moyen dans sa valeur.
Effets à seuil - Exposition sub-chronique par voie orale
L’INERIS propose de retenir pour une exposition sub-chronique au formaldéhyde par voie orale la VTR de 0,3 mg.kg-1.j-1 (ATSDR, 2010).
Une seule VTR est proposée par l’ATSDR. Elle est basée sur l’existence d’effets gastro-intestinaux chez des rats exposés 4 semaines au formaldéhyde par l’eau de boisson pour lesquels un NOAEL de 25 mg.kg-1.j-1 a été établi (Til et al., 1988b). Cette étude est de bonne qualité et de durée adaptée quoiqu’un peu courte pour l’établissement d’une valeur pour des expositions sub-chroniques. Un facteur 100 a été appliqué (10 pour la variabilité au sein de la population et 10 pour l’extrapolation de données animales vers l’homme) et est adapté au regard des données disponibles.
Indice de confiance : La valeur est établie à partir d’une étude de qualité et de durée d’exposition adaptée mais non parfaitement contrôlée (pas de cage métabolique), la construction de la valeur est cohérente : l’indice de confiance est moyen.
Effets à seuil - Exposition chronique par voie orale:
L’INERIS propose de retenir pour une exposition chronique au formaldéhyde par voie orale la VTR de 0,2 mg.kg-1.j-1 (ATSDR, 2010 ; US EPA 1990).
Deux VTR sont proposées, basées sur la même étude de Til et al. (1989) et toutes deux identiques.
Cette étude de deux ans chez le rat est de bonne qualité. Les effets de type gastrointestinaux correspondant à un effet local. Les valeurs de l’ATSDR et de l’US EPA ont été calculée en appliquant un même facteur d’incertitude 100 (pour les variations inter et intra-spécifiques) au NOAEL de 15 mg.kg-1.j-1.
La construction de cette valeur est recevable. L’INERIS propose de retenir la valeur de l’ATSDR et de l’US EPA.
Indice de confiance : L’étude est de bonne qualité et de durée adaptée, le choix de l’effet critique est cohérent avec le profil toxicologique de la substance et le choix des facteurs d’incertitude est adapté. Deux organismes ont dérivé la même valeur sur la base du même jeu de données : indice de confiance élevé.
Effets sans seuil - Exposition chronique par inhalation:
L’ANSES retient une approche à seuil de dose, aucune valeur sans seuil n’est donc à retenir.
Autres valeurs des organismes reconnus
Description
Effets à seuil - Exposition aiguë par inhalation:
L’ATSDR propose un MRL de 50 µg.m-3 (0,04 ppm) pour une exposition aiguë par inhalation au formaldéhyde (ATSDR, 2010)
Cette valeur est établie à partir d’une étude chez le volontaire, deux groupes distincts ont été évalué des non-fumeurs et des fumeurs (Pazdrak et al., 1993). Une LOAEC de 0,4 ppm (0,5 mg.m-3) tient compte des effets irritants et inflammatoires du formaldéhyde sur les muqueuses nasales et des effets irritants sur les yeux chez l’homme.
Facteurs d’incertitude : un facteur de 9 arrondi à 10 a été appliqué (3 pour l’utilisation d’un LOAEC et 3 pour tenir compte de la variabilité de sensibilité au sein de la population).
Calcul : LOAEC x 1/10 = 0,4 ppm x 1/10 = 0,04 ppm (soit 50 µg.m-3).
Indice de confiance : cet organisme ne propose pas d’indice de confiance.
L’OEHHA propose un REL de 55 µg.m-3 (0,044 ppm) pour une exposition aiguë par inhalation au formaldéhyde (OEHHA, 2014)
Cette valeur est établie à partir d’une étude chez l’homme non asthmatique et non-fumeur (Kulle et al., 1987) soumis à une exposition unique de formaldéhyde à des concentrations de 0,5 à 3,0 ppm pendant 3 heures. Une irritation oculaire moyenne à modérée est observée à 1 ppm mais n’est pas retrouvée à 0,5 ppm. Une benchmark concentration de 0,44 ppm a été calculée. Aucun ajustement temporel n’a été pratiqué.
Facteurs d’incertitude : un facteur de 10 a été appliqué pour tenir compte de la variabilité de sensibilité au sein de la population en particulier de l’exacerbation de la sensibilité à l’asthme chez les enfants.
Calcul : 0,44 ppm x 1/10 = 0,044 ppm (soit 55 µg.m-3).
Indice de confiance : cet organisme ne propose pas d’indice de confiance.
L’OEHHA propose un REL de 9 µg.m-3 (0,007 ppm) pour une exposition aiguë (8 h) par inhalation au formaldéhyde (OEHHA, 2014)
Cette valeur est établie à partir d’une étude épidémiologique chez travailleurs exposé 8 h/j, 5 j/7 en moyenne pendant 10 ans (Wihelmsson et Holmstrom, 1992). L’effet retenu est l’obstruction et l’inconfort nasal, l’inconfort au niveau des voies aériennes supérieures et l’irritation oculaire. Cet effet est observé à 0,26 mg.m-3 (LOAEC) mais n’est pas retrouvé à 0,09 mg.m-3 (NOAEC). Aucun ajustement temporel n’a été pratiqué.
Facteurs d’incertitude : un facteur de 10 a été appliqué pour tenir compte de la variabilité de sensibilité au sein de la population en particulier de l’exacerbation de la sensibilité à l’asthme chez les enfants.
Calcul : 0,09 mg.m-3 x 1/10 = 9 µg.m-3 (soit 0,007 ppm).
Indice de confiance : cet organisme ne propose pas d’indice de confiance.
Le TCEQ propose un ReV de 50 µg.m-3 (41 ppm) pour une exposition aiguë de 1 heure ou 24 heures au formaldéhyde par inhalation (TCEQ, 2015).
Cette valeur a été établie à partir des étude de Pazdrak et al. (1993) et de Krakowiak et al. (1998), réalisées sur des volontaires sains ou sensibles exposés à 0,5 mg.m-3 (0,4 ppm) pendant 2 heures. Le TCEQ a retenu comme effet critique des sensations transitoires de brûlures oculaires et les symptômes associés à une rhinite au niveau des voies aériennes supérieures. Une LOAEC de 0,5 mg.m-3 (0,4 ppm), seule dose testée dans ces études, a été retenue comme dose critique.
Aucun ajustement sur la durée d’exposition n’a été réalisé en raison de l’absence d’éléments permettant de considérer que l’effet critique observé était dépendant de la concentration et de la durée d’exposition. Le TCEQ a construit ses deux valeurs pour 1 et 24 heures, selon le même calcul.
Facteurs d'incertitude : un facteur 9 arrondi à 10 a été appliqué : 3 pour tenir compte de la variabilité de sensibilité au sein de la population et 3 pour l’utilisation d’une LOAEC.
Calcul : ReVaiguë 1h. = 0,5 mg.m-3/ 10 = 0,05 mg.m-3 (41 ppb)
Indice de confiance : cet organisme n’accorde pas d’indice
Effets à seuil - Exposition chronique par inhalation:
L’ATSDR propose un MRL de 10 µg.m-3 (0,008 ppm) pour une exposition chronique par inhalation au formaldéhyde (ATSDR, 2010)
Cette valeur est construite à partir d’une étude chez le travailleur exposé au formaldéhyde et aux résines de formaldéhyde (Holmstrom et al., 1989). la valeur est dérivé d’une LOAEC de 0,24 ppm (0,3 mg.m-3) défini à partir de l’augmentation de lésions de l’épithélium nasal en atmosphère professionnelle.
Facteurs d’incertitude : un facteur 30 est retenu : 10 pour la variabilité au sein de la population et 3 pour l’utilisation d’un LOAEC.
Calcul : 0,24 ppm x 1/30 = 0,008 ppm soit 10 µg.m-3
Indice de confiance : cet organisme ne propose pas d’indice de confiance.
L'OEHHA propose un REL de 9 µg.m-3 pour une exposition chronique par inhalation au formaldéhyde (OEHHA, 2014).
Cette valeur a été calculée à partir d'une étude épidémiologique réalisée chez 66 travailleurs exposés durant 1 à 36 ans (moyenne 10 ans) à une concentration moyenne de 0,21 ppm (0,26 mg.m-3) de formaldéhyde (Wilhelmsson et Holmstrom, 1992). Un groupe témoin était constitué de 36 personnes travaillant dans une agence gouvernementale et exposés à une concentration moyenne de 0,07 ppm (0,09 mg.m-3). Les effets observés chez les 66 travailleurs étaient des irritations oculaires et nasales et des lésions histologiques de l'épithélium nasal (rhinite, métaplasie squameuse, dysplasie). La concentration moyenne de 0,26 mg.m-3 est considérée comme un LOAEC tandis que la concentration moyenne de 0,09 mg.m-3 est considérée comme un NOAEC. Ce NOAEC est donné pour une exposition discontinue.
Facteurs d’incertitude : un facteur de 10 a été appliqué pour les variations intra-spécifiques.
Calcul : 0,09 mg.m-3 x 1/10 = 9 µg.m-3 (soit 0,007 ppm).
Indice de confiance : cet organisme ne propose pas d’indice de confiance.
Le TCEQ propose un ReV de 11 mg.m-3 (8,9 ppb) pour une exposition chronique par inhalation au formaldéhyde (TCEQ, 2023).
Cette valeur a été établie à partir de l’étude de Wilhelmsson et Holmstrom, (1992), également retenue par l’OEHHA, réalisée en milieu professionnel (durée de travail de 8 heures par jour, 5 jours par semaine). Le TCEQ a retenu le même effet critique, à savoir les symptômes associés à des irritations au niveau des yeux et des voies respiratoires supérieures (nez et irritation de la gorge). Le TCEQ a également retenue la concentration sans effet de 0,09 mg.m-3 (0,07ppm) (NOAEC), comme dose critique.
Un ajustement pour tenir compte de l’exposition discontinue a été réalisé à partir du calcul suivant :
PODHEC = POD x (VEtravail/VEhumain) X (5 jours/7 jours)
= 0,09 mg.m-3 X (10/20) X (5/7) = 0,032 mg.m-3 ou 32 µg.m-3 (26 ppb)
VEtravailleur : volume par défaut de 10 m3 respiré pendant une journée de travail
VEhumain : volume par défaut de 20 m3 respiré chez un homme exposé pendant 1 journée entière.
Facteurs d'incertitude : un facteur d'incertitude 3 est appliqué pour la variabilité au sein de la population humaine.
Calcul : ReVchronique = 32 µg.m-3 / 3 = 11 µg.m-3 (8,9 ppb)
Indice de confiance : cet organisme n’accorde pas d’indice
A noter que le TCEQ a également construit en 2015 une VTR chronique de 18 mg.m-3 fondée sur des effets cancérogènes, non retenue dans la mise à jour de 2023 car moins protectrice que la VTR construite pour les effets non cancérigènes.
Effets sans seuil - Exposition chronique par inhalation:
L’US EPA (IRIS) propose une valeur d’excès de risque unitaire par inhalation (ERUi) de 1,3.10-5 (µg.m-3) -1 soit 1,1.10-5 ppm-1 (1991)
Cette valeur a été calculée à partir de l'étude de Kerns et al. (1983), qui avait pour but de déterminer l’incidence de tumeurs nasales malignes chez des rats Fischer 344 mâles, exposés par inhalation à des concentrations de 0 - 2 - 5,6 - 14,3 ppm de formaldéhyde pendant deux ans. Les auteurs ont observé à la fin de l’étude (sur une période de 6 à 30 mois suivant l’arrêt de l’exposition) la présence de carcinomes au niveau des cavités nasales chez 51 mâles sur 117 et 52 femelles sur 115 dans le lot de rats exposés à 14,3 ppm. Ce type de tumeur n’a été observé que chez deux rats (1 mâle et 1 femelle) dans le groupe exposé à 5,6 ppm.
Méthode d’extrapolation : modèle multi-étapes linéarisé.
Selon les recommandations de l’US EPA, le risque unitaire ne devrait pas être utilisé si la concentration dans l’air dépasse 8.102 µg.m-3 soit 0,65 ppm (non approprié).
L'OEHHA propose un ERUi de 6.10-6 (µg.m-3)-1 pour une exposition par inhalation (2008).
Cette valeur est issue de la même étude que celle utilisée par l'US EPA pour son ERUi (voir ci-dessus). La méthode employée est un modèle multi-étapes linéarisé, avec une extrapolation pharmacocinétique des données de dosimétrie moléculaire aux données d'incidence de tumeurs.
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Bibliographie
Ecotoxicologie
Dernière vérification le 30/06/2025
Introduction
Evaluations existantes :
US-EPA, 2008: Reregistration Eligibility Decision (RED) for Formaldehyde and Paraformaldehyde. Washington DC, 20460, United States Environmental Protection Agency, Office of Prevention, Pesticides and Toxic Substances.
ATSDR, 1999: Toxicological profile for Formaldehyde. Reregistration Eligibility Decision for Formaldehyde and Paraformaldehyde
OECD, 2002: Formaldehyde. SIDS Initial assessment report For SIAM 14. Paris, France, March 2002.
Robert Chénier, 2003: An ecological Risk Assessment of Formaldehyde.
Critères PBT / POP :
La substance ne remplit pas les critères PBT/vPvB1 (C.E., 2006) ou POP2 (PNUE, 2001).
Normes de qualité existantes :
-
Substance(s) associée(s) :
-
[1] Les PBT sont des substances persistantes, bioaccumulables et toxiques et les vPvB sont des substances très persistantes et très bioaccumulables. Les critères utilisés pour la classification des PBT sont ceux fixés par l'Annexe XIII du règlement n°1907/2006 (REACH).
[2] Les Polluants Organiques Persistants (POP) sont des substances persistantes (aux dégradations biotiques et abiotiques), fortement liposolubles (et donc fortement bioaccumulables), et volatiles (et peuvent donc être transportées sur de longues distances et être retrouvée de façon ubiquitaire dans l'environnement). Les critères utilisés pour la classification POP sont ceux fixés par l'Annexe 5 de la Convention de Stockholm placée sous l'égide du PNUE (Programme des Nations Unies pour l'Environnement).
Dangers
Description
ORGANISMES AQUATIQUES
Dans les tableaux ci-dessous, sont reportés pour chaque taxon uniquement les résultats des tests d'écotoxicité montrant la plus forte sensibilité à la substance.
Ces résultats d'écotoxicité sont principalement exprimés sous forme de NOEC (No Observed Effect Concentration), concentration sans effet observé, d'EC10 concentration produisant 10% d'effets et équivalente à la NOEC, ou de EC50, concentration produisant 50% d'effets. Les NOEC sont principalement rattachées à des tests chroniques, qui mesurent l'apparition d'effets sub-létaux à long terme, alors que les EC50 sont plutôt utilisées pour caractériser les effets à court terme.
ECOTOXICITE
ECOTOXICITE AQUATIQUE AIGUË
Plusieurs essais référencés dans la base de données américaine des pesticides (IPMCenter2) n'ont pas pu être utilisés. En effet, ceux-ci n'ont pas été suffisamment renseignés, notamment en ce qui concerne la composition des solutions utilisées (dans ces tests, les solutions indiquent des concentrations de formaldéhyde de 18 à 37% mais n'indiquent pas la nature du diluant). Le tableau ci-dessous répertorie les données d'écotoxicité aiguë jugées pertinentes pour notre étude.
|
Organisme |
Espèce |
Critère d'effet |
Valeur [mg/L] |
Validité |
Source |
|
|---|---|---|---|---|---|---|
|
Algues & plantes aquatiques |
Eau douce |
Scenedesmus quadricauda |
EC50 (24 h) |
14.7 |
Valide |
Tisler et J., 1997 cité dans OECD, 2002 |
|
Milieu marin |
Phyllospora comosa |
LC50 (96 h) |
1 |
Non valide |
Burridge et al., 1995b |
|
|
Invertébrés |
Eau douce |
Cypridopsis sp. |
LC50 (96h) |
(1.051) 0.42 |
Non valide |
Bills et al., 1977 cité dans OECD, 2002 |
|
Daphnia pulex |
EC50 (48 h) |
5.8 |
Valide |
Tisler et J., 1997 cité dans OECD, 2002 |
||
|
EC50 (48 h) |
14.8 |
Valide |
Cooney et Bourgoin, 2001 cité dans Hohreiter et Rigg, 2001 |
|||
|
EC50 (48 h) |
12.2 |
Valide |
Cooney et Bourgoin, 2001 cité dans Hohreiter et Rigg, 2001 |
|||
|
EC50 (48 h) |
10.2 |
Moyenne géométrique |
||||
|
Daphnia magna |
EC50 (24 h) |
18.2 |
Valide |
Bringmann et Kühn, 1977 cité dans OECD, 2002 |
||
|
EC50 (24 h) |
14.7 |
Valide |
Bringmann et Kühn, 1982 cité dans OECD, 2002 |
|||
|
EC50 (48 h) |
29 |
Valide |
Janssen et Persoone, 1993 cité dans Hohreiter et Rigg, 2001 |
|||
|
|
|
|
EC50 (48 h) |
7.6 |
Valide |
Nazarenko, 1960 cité dans Hohreiter et Rigg, 2001 |
|
|
|
|
EC50 (96 h) |
20 |
Valide |
Prasad, 1980 cité dans Hohreiter et Rigg, 2001 |
|
|
|
|
EC50 (96 h) |
16.4 |
Moyenne géométrique |
|
|
|
Ceriodaphnia dubia |
EC50 (48 h) |
11.9 |
Valide |
Vasu, 1990 cité dans Hohreiter et Rigg, 2001 |
|
|
EC50 (48 h) |
11.4 |
Valide |
Vasu, 1990 cité dans Hohreiter et Rigg, 2001 |
|||
|
EC50 (48 h) |
12.9 |
Valide |
Vasu, 1990 cité dans Hohreiter et Rigg, 2001 |
|||
|
EC50 (48 h) |
9.5 |
Valide |
Cooney et Bourgoin, 2001 cité dans Hohreiter et Rigg, 2001 |
|||
|
EC50 (48 h) |
9.6 |
Valide |
Cooney et Bourgoin, 2001 cité dans Hohreiter et Rigg, 2001 |
|||
|
EC50 (48 h) |
11 |
Moyenne géométrique |
||||
|
Organisme |
Espèce |
Critère d'effet |
Valeur [mg/L] |
Validité |
Source |
|
|---|---|---|---|---|---|---|
|
Invertébrés |
Eau douce |
Cypridopsis vidua |
LC50 (96 h) |
68.6 |
Valide |
Cooney et Bourgoin, 2001 cité dans Hohreiter et Rigg, 2001 |
|
LC50 (96 h) |
54.4 |
Valide |
Cooney et Bourgoin, 2001 cité dans Hohreiter et Rigg, 2001 |
|||
|
LC50 (96 h) |
68.2 |
Valide |
Cooney et Bourgoin, 2001 cité dans Hohreiter et Rigg, 2001 |
|||
|
LC50 (96 h) |
63.4 |
Moyenne géométrique |
||||
|
Palaemonetes kadiakensis |
LC50 (96 h) |
(4651)187.6 |
Valide |
Bills et al., 1977 cité dans Hohreiter et Rigg, 2001 |
||
|
Corbicula sp. |
LC50 (96 h) |
(1261) 50.8 |
Valide |
Bills et al., 1977 cité dans Hohreiter et Rigg, 2001 |
||
|
|
LC50 (96 h) |
35.2 |
Valide |
Chandler et Marking, 1979 cité dans Hohreiter et Rigg, 2001 |
||
|
|
LC50 (96 h) |
46.7 |
Valide |
Chandler et Marking, 1979 cité dans Hohreiter et Rigg, 2001 |
||
|
Helisoma sp. |
LC50 (96 h) |
(931) 37.5 |
Valide |
Bills et al., 1977 cité dans Hohreiter et Rigg, 2001 |
||
|
Notonecta sp. |
LC50 (96 h) |
(8351) 336.8 |
Valide |
Bills et al., 1977 cité dans Hohreiter et Rigg, 2001 |
||
|
Milieu marin |
Pas d’information disponible |
|||||
|
Sédiment |
Chironomus sp. |
LC50 (96 h) |
450 |
Valide |
Prasad, 1980 cité dans Hohreiter et Rigg, 2001 |
|
|
Organisme |
Espèce |
Critère d'effet |
Valeur [mg/L] |
Validité |
Source |
|
|---|---|---|---|---|---|---|
|
Poissons |
Eau douce |
Ameiurus melas |
LC50 (96 h) |
(62.11) 24.8 |
Valide |
Bills et al., 1977 |
|
Lepomis macrochirus |
LC50 (96 h) |
(1001) 40.25 |
Valide |
Bills et al., 1977 cité dans Hohreiter et Rigg, 2001 |
||
|
Salmo salar |
LC50 (96 h) |
(1731) 69.2 |
Valide |
Bills et al., 1977 cité dans Hohreiter et Rigg, 2001 |
||
|
Micropterus dolomieui |
LC50 (96 h) |
(1361) 54.74 |
Valide |
Bills et al., 1977 |
||
|
Oncorhynchus mykiss |
LC50 (48 h) |
50 |
Valide |
Tisler et J., 1997 cité dans OECD, 2002 |
||
|
LC50 (96 h) |
(117.261) 47.2 |
Valide |
Bills et al., 1977 |
|||
|
LC50 (96 h) |
1020 |
Valide |
McKim et al., 1976 |
|||
|
Micropterus salmoides |
LC50 (96 h) |
(1431) 57.56 |
Valide |
Bills et al., 1977 |
||
|
Pimephales promelas |
LC50 (96 h) |
24.1 |
Valide |
Geiger et al., 1990 cité dans Hohreiter et Rigg, 2001 |
||
|
Ictalurus punctatus |
LC50 (96 h) |
(65.81) 26.48 |
Valide |
Bills et al., 1977 cité dans Hohreiter et Rigg, 2001 |
||
|
Ictarus melas |
LC50 (96 h) |
(62.11) 24.99 |
Valide |
Bills et al., 1977 |
||
|
Lepomis cyanellus |
LC50 (96 h) |
(1731) 69.64 |
Valide |
Bills et al., 1977 |
||
|
Salmo gairdneri |
LC50 (96 h) |
(1181) 47.50 |
Valide |
Bills et al., 1977 |
||
|
Salvelinus namaycush |
LC50 (96 h) |
(1001) 40.25 |
Valide |
Bills et al., 1977 |
||
|
Milieu marin |
Morone saxatilis |
LC50 (96 h.) |
6.7 |
Valide |
Wellborn, 1969 |
|
(1) Valeur en µl/L de formaline (solution à 37% de formaldéhyde) indiquée pour information. Celle-ci a ensuite été rapportée en concentration (µg.L-1) pour une solution de formaldéhyde pure.
(2) (US-EPA. (2011). "Pesticide Ecotoxicity Database, Environmental Fate and Effects Division of the Office of Pesticide Programs." from http://www.ipmcenters.org/Ecotox/DataAccess.cfm.)
ECOTOXICITE AQUATIQUE CHRONIQUE
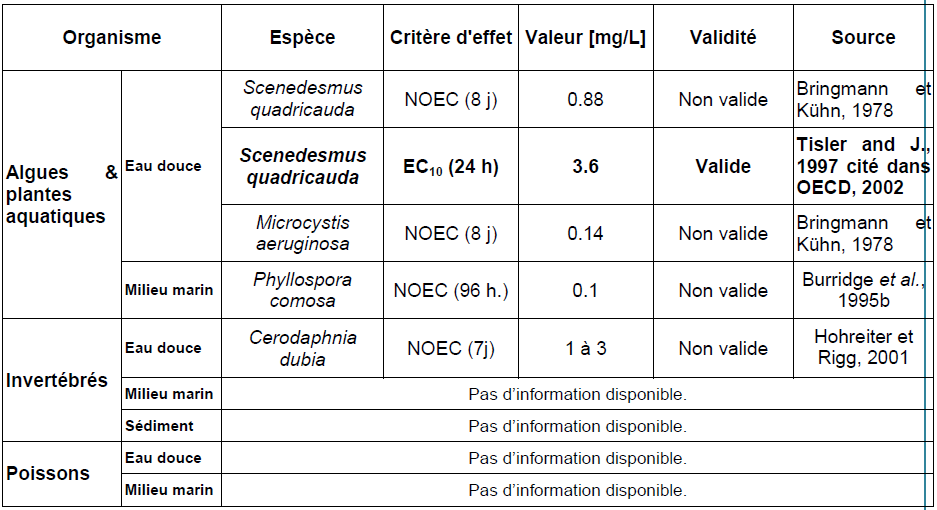
ECOTOXICITE POUR LES VERTÉBRÉS TERRESTRES
Ce chapitre traite de la toxicité chronique induite par la substance sur les prédateurs via la consommation d'organismes aquatiques contaminés (appelés biota, i.e. poissons ou invertébrés vivant dans la colonne d'eau ou dans les sédiments). Il s'agit donc d'évaluer la toxicité chronique de la substance par la voie d'exposition orale uniquement.
Dans les tableaux ci-dessous, ne sont reportés pour chaque type de test que les résultats permettant d'obtenir les NOEC ou la valeur toxicologique de référence (VTR) les plus protectrices. N'ont été recherchés que des tests sur mammifères ou oiseaux exposés par voie orale (exposition par l'alimentation ou par gavage). Toutes les données présentées ont été validées puisqu'elles sont issues de sources fiables.
Les résultats de toxicité sont principalement donnés sous forme de doses journalières : NOAEL (No Observed Adverse Effect Level), ou LOAEL (Lowest Observed Adverse Effect Level). NOAEL et LOAEL sont exprimées en termes de quantité de substance administrée par unité de masse corporelle de l'animal testé, et par jour.
Pour calculer la norme de qualité liée à l'empoisonnement secondaire des prédateurs, il est nécessaire de connaître la concentration de substance dans le biote n'induisant pas d'effets observés pour les prédateurs (exprimée sous forme de NOEC). Il est possible de déduire une NOEC à partir d'une NOAEL grâce à des facteurs de conversion empiriques variables selon les espèces testées. Les facteurs utilisés ici sont ceux recommandés par le projet de guide technique européen pour la détermination de normes de qualité (E.C., 2010). Les valeurs de ces facteurs de conversion dépendent de la masse corporelle des animaux et de leur consommation journalière de nourriture. Celles-ci peuvent donc varier d'une façon importante selon le niveau d'activité et le métabolisme de l'animal, la valeur nutritive de sa nourriture, etc. En particulier elles peuvent être très différentes entre un animal élevé en laboratoire et un animal sauvage.
Afin de couvrir ces sources de variabilité, mais aussi pour tenir compte des autres sources de variabilité ou d'incertitude (variabilité inter et intra-espèces, extrapolation du court terme au longterme, etc.) des facteurs d'extrapolation sont nécessaires pour le calcul de la QSbiota sec pois. Les valeurs recommandées pour ces facteurs d'extrapolation sont données dans le guide technique européen (E.C., 2010). Un facteur d'extrapolation supplémentaire (AFdose-réponse) est utilisé dans le cas où la toxicité a été établie à partir d'une LOAEL plutôt que d'une NOAEL.
Les données obtenues sur les mammifères terrestres et les oiseaux, utilisées pour la détermination des valeurs guides pour la protection des prédateurs vis-à-vis de l’empoisonnement secondaire, sont répertoriées dans les tableaux ci-dessous.
TOXICITE ORALE POUR LES MAMMIFERES
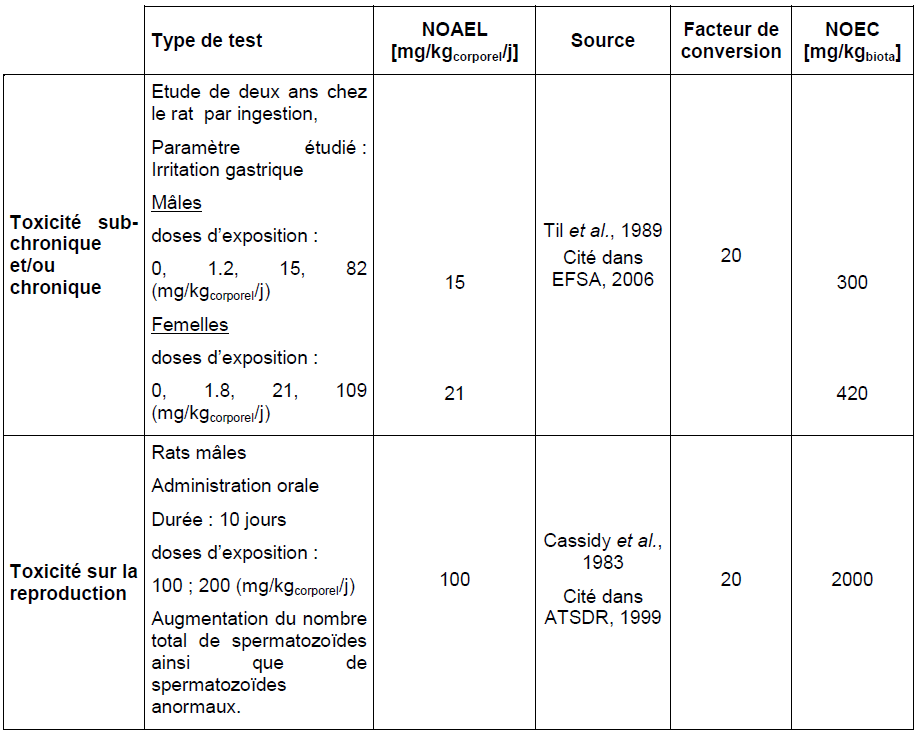
Valeurs de danger
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Valeurs écotoxicologiques
Introduction
Dans cette rubrique, sont reportées des valeurs de référence pour la protection des écosystèmes aquatiques et de la santé humaine via l’environnement.
Elles peuvent avoir un statut de « Valeur réglementaire » si elles sont issues
- de réglementations européennes et issues par exemple de dossiers d’évaluation des risques dans le cadre de processus d’autorisation de mise sur le marché des substances chimiques (c’est le cas des Concentrations Prédites Sans Effet pour l’environnement (PNEC) issues des dossiers réglementaires sous REACh ou dans le cas de la réglementation des produits biocides) ou issues de « Normes de Qualité Environnementale » (NQE) de la Directive Cadre européenne sur l’Eau (DCE) ;
- de réglementations françaises telles que les arrêtés de mise en application de la DCE à l’échelle nationale.
Elles peuvent être des « Valeurs guides » lorsque ce sont des propositions scientifiques de l’INERIS qui ne sont pas reportées dans des textes réglementaires. C’est le cas de toutes les valeurs établies par l’INERIS pour guider l’évaluation de la qualité des milieux aquatiques pour les substances qui n’ont pas, ou pas encore, un statut réglementaire dans le contexte de la DCE.
Les « Valeurs Guides Environnementales » (VGE) et les « Normes de Qualité Environnementale » (NQE) sont les outils consacrés pour l’évaluation de la qualité des eaux de surface, dont l’établissement est basé sur une même méthodologie européenne dédiée (E.C., 2018).
Leur construction, d’un point de vue méthodologique, est donc similaire.
Valeurs guides
Description
NORMES DE QUALITÉ POUR LA COLONNE D'EAU
Les normes de qualité pour les organismes de la colonne d'eau sont calculées conformément aux recommandations du guide technique européen la détermination des normes de qualité environnementale (E.C., 2010). Elles sont obtenues en divisant la plus faible valeur de NOEC ou d'EC50 valide par un facteur d'extrapolation (AF, Assessment Factor).
La valeur de ce facteur d'extrapolation dépend du nombre et du type de tests pour lesquels des résultats valides sont disponibles. Les règles détaillées pour le choix des facteurs sont données dans le guide technique européen (E.C., 2010).
En ce qui concerne les organismes marins, selon le projet de document guide technique pour la détermination de normes de qualité environnementale (E.C., 2010), la sensibilité des espèces marines à la toxicité des substances organiques peut être considérée comme équivalente à celle des espèces dulçaquicoles, à moins qu'une différence ne soit montrée.
Néanmoins, le facteur d'extrapolation appliqué pour déterminer la AA-QSmarine_eco doit prendre en compte les incertitudes additionnelles telles que la sous-représentation de taxons clefs et une diversité d'espèces plus complexe en milieu marin.
- Moyenne annuelle (AA-QSwater_eco) :
Une concentration annuelle moyenne est déterminée pour protéger les organismes de la colonne d'eau d'une possible exposition prolongée.
Pour le formaldéhyde, seules des données valides chroniques sont disponibles pour les algues marines. En revanche, des données valides aigües sont disponibles pour trois niveaux trophiques. La donnée issue du test aigu sur Cypridopsis sp., est jugé non valide car cet essai n'est pas reproductible (Hohreiter et Rigg, 2001, OECD, 2002). Les essais sur Daphnia pulex seront préférés en utilisant comme EC50 la moyenne géométrique de toutes les EC50 valides disponibles sur cette espèce. La donnée sélectionnée pour le calcul de l'AA-QSwater_eco est donc une EC50 (48 h) d'une valeur de 10.2 mg.L-1, un facteur de sécurité de 1000 lui sera appliqué :
AA-QSwater_eco = 10.2 μg/L
En ce qui concerne les organismes marins, un essai est disponible pour un seul niveau trophique en aigu. Le jeu de données disponible ne permet pas de montrer une différence de sensibilité. Conformément au guide technique (E.C., 2010), un facteur de sécurité de 10000 sera appliqué à la moyenne géométrique des EC50 (10.2 mg.L-1) obtenues sur un test sur Daphnia pulex afin de déterminer l'AA-QSmarine_eco :
AA-QSmarine_eco = 1.02 μg/L
Concentration Maximum Acceptable (MAC et MACmarine)
La concentration maximale acceptable est calculée afin de protéger les organismes de la colonne d'eau de possibles effets de pics de concentrations de courtes durées (E.C., 2010).
On dispose de données aiguës pour trois niveaux trophiques (plantes, invertébrés et poissons), la plus faible étant celle sur Daphnia pulex EC50 (48 h) = 10.2 mg.L-1 (moyenne géométrique). Par défaut, un facteur d'extrapolation de 100 s'applique pour calculer la MAC. Pour le formaldéhyde :
MAC =10.2 /100 soit 0.102 mg.L-1
MAC = 102 μg/L
De la même manière, un facteur d'extrapolation de 1000 s'applique pour calculer la MACmarine. Pour le formaldéhyde on a donc :
MACmarine = 10.2/1000 soit 0.0102 mg.L-1
MACmarine= 10.2 µg.L-1
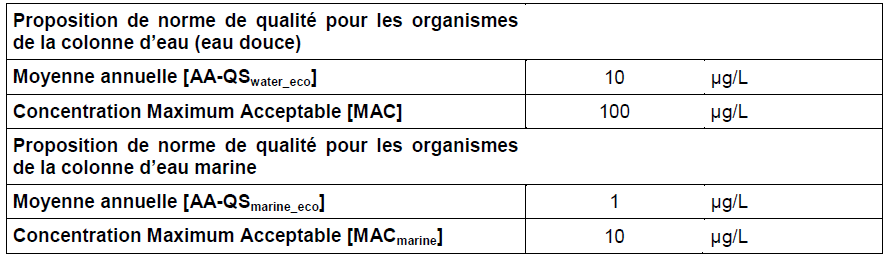
VALEUR GUIDE DE QUALITÉ POUR LE SÉDIMENT (QSSED ET QSSED-MARIN)
Un seuil de qualité dans le sédiment est nécessaire (i) pour protéger les espèces benthiques et (ii) protéger les autres organismes d'un risque d'empoisonnement secondaire résultant de la consommation de proies provenant du benthos. Les principaux rôles des normes de qualité pour les sédiments sont de :
- Identifier les sites soumis à un risque de détérioration chimique (la norme sédiment est dépassée)
- Déclencher des études pour l'évaluation qui peuvent conduire à des études plus poussées et potentiellement à des programmes de mesures
- Identifier des tendances à long terme de la qualité environnementale (Art. 4 Directive 2000/60/CE).
Aucune information d'écotoxicité pertinente pour les organismes benthiques n'a été trouvée dans la littérature.
A défaut, une valeur guide pour le sédiment peut être calculée à partir du modèle de l'équilibre de partage.
Ce modèle suppose que :
- il existe un équilibre entre la fraction de substances adsorbées sur les particules sédimentaires et la fraction de substances dissoutes dans l'eau interstitielle du sédiment,
- la fraction de substances adsorbées sur les particules sédimentaires n'est pas biodisponible pour les organismes et que seule la fraction de substances dissoutes dans l'eau interstitielle est susceptible d'impacter les organismes,
- la sensibilité intrinsèque des organismes benthiques aux toxiques est équivalente à celle des organismes vivant dans la colonne d'eau. Ainsi, la norme de qualité pour la colonne d'eau peut être utilisée pour définir la concentration à ne pas dépasser dans l'eau interstitielle.
Une valeur guide de qualité pour le sédiment peut être alors calculée selon l'équation suivante (E.C., 2010) :
![]()
Avec :
RHOsed : masse volumique du sédiment en [Kgsed.m-3sed]. En l'absence d'une valeur exacte, la valeur générique proposée par le guide technique européen (E.C., 2010) est utilisée : 1300 kg.m-3.
Ksed-eau : coefficient de partage sédiment/eau en m3/m3 . En l'absence d'une valeur exacte, les valeurs génériques proposées par le guide technique européen (E.C., 2010) sont utilisées. Le coefficient est alors calculé selon la formule suivante :
0.8 + 0.025 * Koc soit Ksed-eau = 1.725 m3/m3 .
Ainsi, on obtient:
QSsed wet weight = 13.5 μg/kg (poids humide)
La concentration correspondante en poids sec peut être estimée en tenant compte du facteur de conversion suivant :
![]()
Avec : Fsolidesed : fraction volumique en solide dans le sédiment en [m3solide/m3sed]. En l'absence d'une valeur exacte, la valeur générique proposée par le guide technique européen (E.C., 2010) est utilisée : 0.2 m3/m3 .
RHOsolide : masse volumique de la partie sèche en [kgsolide/m3solide]. En l'absence d'une valeur exacte, la valeur générique proposée par le guide technique européen (E.C., 2010) est utilisée : 2500 kg.m-3 .
Pour le formaldéhyde, la concentration correspondante en poids sec est :
QSsed dry_weight = 7.69* 2.6 = 35.2 μg/kgsed poids sec
Selon la même approche que pour le sédiment d'eau douce, une valeur guide de qualité pour le sédiment marin peut être calculée selon la formule suivante :
![]()
QSsed-marin wet weight = 1.3 μg/kg (poids humide)
La concentration correspondante en poids sec est alors la suivante :
QSsed-marin dry_weight= 3.5 μg/kgsed poids sec
Le logKow de la substance étant inférieur à 5, un facteur additionnel de 10 n'est pas jugé nécessaire.
Il faut rappeler que les incertitudes liées à l'application du modèle de l'équilibre de partage sont importantes. Les sédiments naturels peuvent avoir des propriétés très variables en termes de composition (nature et quantité de matières organiques, composition minéralogique), de granulométrie, de conditions physico-chimiques, de conditions dynamiques (taux de déposition/taux de resuspension). Par ailleurs ces propriétés peuvent évoluer dans le temps en fonction notamment des conditions météorologiques et de la morphologie de la masse d'eau. Si bien que le partage entre la fraction de toxique adsorbé et la fraction de toxique dissous peut être extrêmement variable d'un sédiment à un autre et l'hypothèse d'un équilibre entre ces deux fractions ne semble pas très réaliste pour des conditions naturelles.
Par ailleurs, certains organismes benthiques peuvent ingérer les particules sédimentaires, et donc être contaminés par la fraction de substance adsorbée sur ces particules, ce qui n'est pas pris en compte par la méthode.
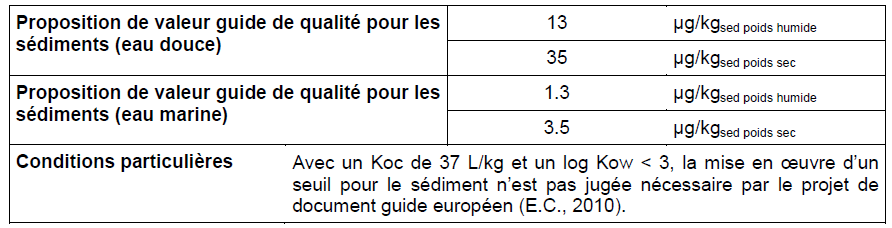
NORME DE QUALITÉ EMPOISONNEMENT SECONDAIRE (QSBIOTA_SEC POIS)
La norme de qualité pour l'empoisonnement secondaire (QSbiota sec pois) est calculée conformément aux recommandations du projet de guide technique européen pour la détermination de normes de qualité (E.C., 2010). Elle est obtenue en divisant la plus faible valeur de NOEC valide par les facteurs d'extrapolation recommandés( E.C., 2010).
Pour le formaldéhyde, un facteur de 30 est appliqué sur la NOEC la plus faible de 300 mg.kg-1biota. On obtient donc :
![]()
Cette valeur de norme de qualité pour l'empoisonnement secondaire peut être ramenée :
- à une concentration dans l'eau douce selon la formule suivante :
- à une concentration dans l'eau marine selon la formule suivante :
![]()
Avec :
BCF : facteur de bioconcentration,
BMF1: facteur de biomagnification,
BMF2: facteur de biomagnification additionnel pour les organismes marins.
Ce calcul tient compte du fait que la substance présente dans l'eau du milieu peut se bioaccumuler dans le biota. Il donne la concentration à ne pas dépasser dans l'eau afin de respecter la valeur de la norme de qualité pour l'empoisonnement secondaire déterminée dans le biota.
La bioaccumulation tient compte à la fois du facteur de bioconcentration (BCF, ratio entre la concentration dans le biota et la concentration dans l'eau) et du facteur de biomagnification (BMF, ratio entre la concentration dans l'organisme du prédateur en bout de chaîne alimentaire, et la concentration dans l'organisme de la proie au début de la chaîne alimentaire). En l'absence de valeurs mesurées pour le BMF1 et BMF2, celles-ci peuvent être estimées à partir du BCF selon le guide technique européen (E.C., 2010).
Ce calcul n'est donné qu'à titre indicatif. Il fait en effet l'hypothèse qu'un équilibre a été atteint entre l'eau et le biote, ce qui n'est pas véritablement réaliste dans les conditions du milieu naturel. Par ailleurs il repose sur un facteur de bioaccumulation qui peut varier de façon importante entre les espèces considérées.
Pour le formaldéhyde, un BCF de 3 et un BMF1 = BMF2 de 1 (E.C., 2010) ont été retenus. On a donc :
![]()
![]()
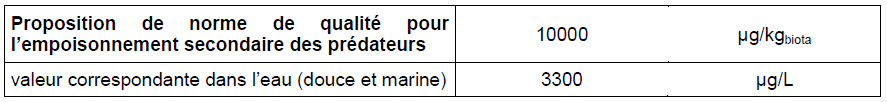
NORME DE QUALITE POUR LA SANTE HUMAINE VIA LA CONSOMMATION DES PRODUITS DE LA PECHE (QSBIOTA_HH)
La norme de qualité pour la santé humaine est calculée de la façon suivante (E.C., 2010) :
![]()
Ce calcul tient compte de :
- la valeur toxicologique de référence (VTR), correspondant à une dose totale admissible par jour.
- un facteur correctif de 10% (soit 0.1) : la VTR donnée ne tient compte en effet que d'une exposition par voie orale, et pour la consommation de produits de la pêche uniquement. Mais la contamination peut aussi se faire par la consommation d'autres sources de nourriture, par la consommation d'eau, et d'autres voies d'exposition sont possibles (inhalation ou contact cutané). Le facteur correctif de 10% (soit 0.1) permet de rendre l'objectif de qualité plus sévère d'un facteur 10 afin de tenir compte de ces autres sources de contamination possibles.
- un poids corporel moyen de 70 kg,
- Fsécurité : facteur de sécurité supplémentaire de 10 pour tenir compte de l'effet cancérogène de la substance.
- Cons. Journ. Moy : une consommation journalière moyenne de produits de la pêche (poissons, mollusques, crustacés) égale à 115 g par jour.
Ce calcul n'est donné qu'à titre indicatif. Il peut être inadapté pour couvrir les risques pour les individus plus sensibles ou plus vulnérables (masse corporelle plus faible, forte consommation de produits de la pêche, voies d'exposition individuelles particulières). Le facteur correctif de 10% n'est donné que par défaut, car la contribution des différentes voies d'exposition varie selon les propriétés de la substance (et en particulier sa distribution entre les différents compartiments de l'environnement), ainsi que selon les populations considérées (travailleurs exposés, exposition pour les consommateurs/utilisateurs, exposition via l'environnement uniquement). L'hypothèse cependant que la consommation des produits de la pêche ne représente pas plus de 10% des apports journalier contribuant à la dose journalière tolérable apporte une certaine marge de sécurité (E.C., 2010).
Pour le formaldéhyde, le calcul aboutit à :
![]()
Comme pour l'empoisonnement secondaire, la concentration correspondante :
- dans l'eau douce du milieu peut être estimée en tenant compte de la bioaccumulation de la substance :
- dans l'eau marine du milieu peut être estimée en tenant compte de la bioaccumulation de la substance :
![]()
Pour le formaldéhyde, on obtient donc :
![]()
![]()
NORME DE QUALITE POUR LA SANTE HUMAINE VIA L'EAU DE BOISSON (QSdw_hh)
La norme de qualité pour l'eau de boisson est calculée de la façon suivante (E.C., 2010) :
![]()
Ce calcul tient compte de :
- la valeur toxicologique de référence (VTR), correspondant à une dose totale admissible par jour ; pour cette substance elle sera considérée égale à 150 µg/kgcorporel/j (Cf. tableau ci-dessus),
- Cons.moy.eau [L.j-1] : une consommation d'eau moyenne de 2 L par jour,
- un poids corporel moyen de 70 kg,
- Fsécurité : facteur de sécurité supplémentaire de 10 pour tenir compte de l'effet cancérogène de la substance.
- un facteur correctif de 10% (soit 0.1) afin de tenir compte de ces autres sources de contamination possibles.
L'eau de boisson est obtenue à partir de l'eau brute du milieu après traitement pour la rendre potable. La fraction éliminée lors du traitement dépend de la technologie utilisée ainsi que des propriétés de la substance.
![]()
En l'absence d'information, on considèrera que la fraction éliminée est nulle et le critère pour l'eau de boisson s'appliquera alors à l'eau brute du milieu. Par ailleurs, on rappellera que ce calcul n'est donné qu'à titre indicatif et peut s'avérer inadéquat pour certaines substances et certaines populations.
Pour le formaldéhyde, on obtient :
![]()

Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Synthèse
PROPOSITION DE NORME DE QUALITE ENVIRONNEMENTALE (NQE)
La NQE est définie à partir de la valeur de la norme de qualité la plus protectrice parmi tous les compartiments étudiés.
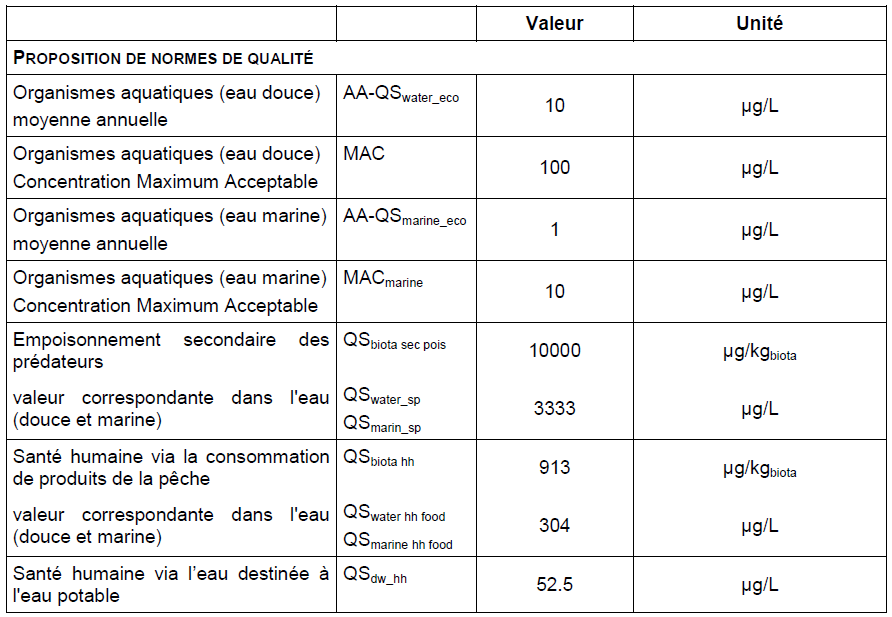
Pour le formaldéhyde, la norme de qualité pour l'eau douce et celle pour l'eau marine sont les valeurs les plus faibles pour l'ensemble des approches considérées et pour les compartiments considérés. La proposition de NQE pour le formaldéhyde est donc la suivante :

VALEURS GUIDES POUR LE SÉDIMENT
Avec un Koc de 37 L.kg-1 et un log Kow < 3, la mise en œuvre d'un seuil pour le sédiment n'est pas jugée nécessaire par le projet de document guide européen (E.C., 2010).
Bibliographie
Activité endocrine
Dernière vérification le 29/03/2024
Généralités sur les activités endocrines
Le formaldéhyde n'est pas citée dans la stratégie communautaire concernant les perturbateurs endocriniens (E.C., 2004) et dans le rapport d'étude de la DG ENV sur la mise à jour de la liste prioritaire des perturbateurs endocriniens à faible tonnage (Petersen et al., 2007).
Données technico-économiques
Dernière vérification le 29/03/2024
Introduction
FTE 2020 Importer
Le formaldéhyde ou aldéhyde formique, de formule brute HCHO, est le plus simple des aldéhydes. À température ambiante, il est présent sous forme de gaz.
Il n'existe pas de norme de qualité environnementale (NQE) réglementaire associée au formaldéhyde au niveau communautaire et au niveau national. L'Ineris a néanmoins établi en 2011 une valeur guide environnementale (VGE) de 10 µg.L-1 dans l'eau pour cette substance.
La production mondiale et européenne de formaldéhyde est en augmentation sur les dix dernières années et pourrait poursuivre sa croissance. En Europe, les principales capacités de production de cette substance se trouvent en Allemagne.
Le formaldéhyde est principalement utilisé dans la synthèse de nombreuses substances chimiques employées dans de très nombreux secteurs d'activités. C'est une substance qui est moins directement utilisée sauf pour divers usages biocides (pisciculture, élevage, médical…). Selon l'ECHA, à l'heure actuelle, 98% du formaldéhyde produit ou importé en Union Europe serait utilisé comme intermédiaire de réaction pour la production de résines, de thermoplastiques et d'autres substances chimiques (ECHA, 2019). En UE, la majeure partie de ces résines est utilisée pour la production de résines condensées : résines phénoliques (PF), résines aminoplastes (MF, UF, MUF) et résorcinols. Ces résines sont en premier lieu utilisées dans le cadre de la production de panneaux de bois.
Pour limiter les émissions de formaldéhyde, une des solutions est de réaliser une substitution par des résines à base de formaldéhyde moins émettrices. Par exemple il est possible pour certains usages de substituer les résines UF, résines les plus émettrices et les plus utilisées, par d'autres résines à base de formaldéhyde (PF, MF, MUF, RF et PRF), ou d'opter pour des résines ou des matériaux alternatifs ne nécessitant pas le recours au formaldéhyde. Une autre solution pour réduire les émissions consiste à utiliser des capteurs de formaldéhyde.
Il est également possible de substituer l'utilisation directe du formaldéhyde par d'autres substances ou par des procédés techniques (utilisation de chambres froides en thanatopraxie, cuisson des aliments dans l'élevage par exemple).
Néanmoins la substituabilité du formaldéhyde varie en fonction des utilisations. Ainsi par exemple elle semble avancée pour les peintures et les vernis contrairement à d'autres secteurs comme celui de la thanatopraxie. Divers facteurs conditionnent pour chaque usage la possibilité de substitution d'une substance par exemple : l'efficacité, la disponibilité, la faisabilité de l'utilisation (intégration dans le procédé technique, capacité des travailleurs à utiliser le substitut), la toxicité, l'écotoxicité, le coût du substitut. C'est pourquoi la substitution doit être réfléchie et mise en place au cas par cas, notamment s'il s'agit de remplacer un matériau par un autre.
On retrouve du formaldéhyde dans l'atmosphère, les eaux de surfaces et souterraines et dans l'air intérieur de bâtiments. Sa présence dans l'environnement peut provenir de plusieurs sources ; des sources naturelles d'émissions (combustion de matières organiques, oxydation dans l'air de composés organiques volatils, décomposition de résidus de végétaux ou de déchets d'animaux), des sources d'émissions non intentionnelles de formaldéhyde vers l'air issues de combustions d'origine anthropique, de la décomposition de résines à base de formaldéhyde, des sources d'émissions d'origine industrielle. Ces dernières seraient, en France sur la période 2008-2018, en baisse pour le milieu aquatique, et stables pour le milieu atmosphérique. Des émissions mineures ont aussi lieu du fait de certains usages intentionnels (agro-alimentaire, pisciculture, médical, thanatopraxie…).
Abstract
Formaldehyde, with the raw formula HCHO, is the simplest of the aldehydes. At room temperature, it is present as a gas.
There are no regulatory Environmental Quality Standards (EQS) associated with formaldehyde at EU and national level. Nevertheless, Ineris has established in 2011 an environmental guideline value (EGV) of 10 µg.L-1 in water for this substance.
Global and European production of formaldehyde has been increasing over the last ten years and should continue to grow. In Europe, the main production capacities for this substance are located in Germany.
Formaldehyde is used in the synthesis of many chemical substances used for numerous industrial sectors. In its own form few uses are reported, excepted biocidal uses for various sectors (fish farming, animal husbandry, medical, etc.). According to ECHA, 98% of formaldehyde produced or imported into the European Union is currently used as a reaction intermediate in the production of resins, thermoplastics and other chemical substances (ECHA, 2019). In the EU, most of these resins are used for the production of condensed resins as for instance phenolic resins (PF), aminoplast resins (MF, UF, MUF) and resorcinols. These resins are primarily used in the production of wood panels.
One way to limit formaldehyde emissions is to substitute formaldehyde-based resins with resins which emit less. For example, for certain uses it is possible to substitute UF resins, the most emitting and widely used resins, with other formaldehyde-based resins (PF, MF, MUF, RF and PRF), or to opt for alternative resins or materials that do not require the use of formaldehyde. Another solution for reducing emissions is to use formaldehyde sensors.
It is also possible to substitute the direct use of formaldehyde with other substances or technical processes (e.g. use of cold rooms in thanatopraxy, cooking of food in animal husbandry).
Nevertheless, the substitutability of formaldehyde varies according to the use. For example, substitution seems to be advanced for paints and varnishes in contrast to other sectors such as thanatopraxy. For each use, various factors condition the substitution of the substance, as for example: efficiency, availability, feasibility of use (integration into the technical process, ability of workers to use the substitute), toxicity, ecotoxicity, cost of the substitute. For this reason, substitution must be considered and implemented on a case-by-case basis, especially if it involves replacing one material with another. In the environment formaldehyde is found in the atmosphere, surface water, groundwater compartments and indoor air in buildings. Multiple emission sources explain this presence. There are natural sources of emissions to air from the combustion of organic materials, air oxidation of volatile organic compounds or the decomposition of plant residues or animal waste. There are also sources of unintentional emissions of formaldehyde to the air from combustion of anthropogenic origin, decomposition of formaldehyde-based resins, etc. Finally, there are emissions of formaldehyde from the industrial sector. In France over the period 2008-2018, these emissions are expected to have decreased for the aquatic compartment and stabilized for the atmospheric compartment.
Tableaux de synthèse
Généralités
| CAS | 50-00-0 |
|---|---|
| SANDRE | 1702 |
| Usages principaux |
FTE 2020 Importer Production de résines condensées utilisées dans les panneaux de bois, peintures colles et vernis, textiles, de polyols, MDI et résines POM et comme intermédiaires dans la synthèse de nombreux produits chimiques |
| Autres informations d'usage |
FTE 2020 Importer Biocide, conservateur en taxidermie, bactéricide pisciculture et agroalimentaire |
| Substance prioritaire dans le domaine de l’eau (DCE) | non |
| Substance soumise à autorisation dans Reach | non |
| Substance soumise à restriction dans Reach | non |
| Substance extrêmement préoccupante (SVHC) | non |
| Réglementations |
FTE 2020 Importer Les paragraphes ci-après présentent les principaux textes en vigueur à la date de la rédaction de cette rubrique. Cet inventaire n’est pas exhaustif. Textes générauxClassification CMREn juin 2004, l'IARC a modifié la classification du formaldéhyde le faisant passer de la catégorie « substance probablement cancérogène pour l'homme » (groupe 2A) à « substance cancérogène avérée pour l'homme » (groupe 1) pour les cancers du nasopharynx par inhalation, sur la base d'études épidémiologiques en milieu du travail. Au niveau européen, le règlement (UE) n°605/2014 de la Commission du 5 juin 2014 classe le formaldéhyde cancérogène de catégorie 1B et mutagène de catégorie 2. Cette décision fait suite à un avis de l'ECHA de novembre 2012 et à la proposition de révision de la classification du formaldéhyde déposé en 2011 par l'Anses (Anses 2011). ReachRestrictions d'usageDans le cadre du règlement REACH concernant la mise sur le marché des substances chimiques (Règlement (CE) n° 1907/2006 du 18/12/06), le formaldéhyde fait partie de la liste des substances soumises à restrictions quant à leurs fabrication, mise sur le marché et utilisations (Annexe XVII). La limite de concentration en poids dans des matières homogènes pour le formaldéhyde est fixée à 75 mg.kg-1 par le règlement (UE) 2018/1513 de la Commission du 10 octobre 2018. Par dérogation, pour la mise sur le marché de formaldéhyde dans les vêtements, les accessoires connexes, les textiles autres que les vêtements qui entrent en contact avec la peau humaine (par exemple tissus d'ameublement) et les chaussures, la concentration applicable est de 300 mg. kg-1 du 1er novembre 2020 au 1er novembre 2023. Ensuite la concentration de 75 mg. kg-1 sera appliquée. Ne sont pas concernés par cette restriction :
En mars 2019, l'ECHA a rendu son rapport concernant sa proposition de restreindre la mise sur le marché d'articles libérant du formaldéhyde à des concentrations supérieures à 0,124 mg.m-3 (valeur limite d'émission) et de ne pas dépasser une concentration de formaldéhyde de 0,1 mg.m-3 dans l'habitacle des véhicules routiers et des avions (ECHA 2019). Cette proposition vise des articles pour lesquels le formaldéhyde ou des substances pouvant libérer du formaldéhyde ont été utilisés au cours de leur fabrication. Sont exclus de la proposition de restriction :
Le SEAC (Committee for Socio-economic Analysis) et RAC (Committee for Risk Assessment) soutiennent la proposition de l'ECHA, mais le RAC a proposé une valeur limite d'émission de 0,05 mg.m-3 pour les articles libérant du formaldéhyde et de limiter la concentration de formaldéhyde à l'intérieur des véhicules routiers à 0,05 mg.m-3 . Le RAC a recommandé d'inclure les articles à usage extérieur exclusif dans le champ d'application de la restriction, mais a estimé que les habitacles des avions devaient être exclus du champ d'application. En raison des valeurs limites de concentration inférieures, le RAC propose une période de transition de 24 mois après l'entrée en vigueur de la restriction (ECHA 2020). Actuellement, ce projet de règlementation n'a pas encore été adopté par la Commission Européenne. Directive cadre eau (DCE)Le formaldéhyde ne fait pas partie des substances prioritaires listées au niveau européen pour la politique dans le domaine de l'eau citées dans la directive 2013/39/UE du 12/08/2013 modifiant les directives 2000/60/CE et 2008/105/CE. Règlementations sectoriellesProduits phytopharmaceutiquesLe formaldéhyde n'est plus autorisé comme pesticide au niveau européen (European Commission, 2016) et (Commission Européenne, 2009). Il était utilisé comme fongicide notamment pour le traitement du mildiou. Aucun usage n'est référencé dans la base de données Ephy (Anses). BiocidesAu niveau européen le formaldéhyde est autorisé comme biocide2 pour les utilisations suivantes :
Néanmoins, l'utilisation du formaldéhyde en tant que biocide est actuellement cours de réévaluation au niveau européen. [2] « Le « produit biocide » est défini comme toute substance ou tout mélange, sous la forme dans laquelle il est livré à l'utilisateur, constitué d'une ou plusieurs substances actives, en contenant ou en générant destiné à détruire, repousser ou rendre inoffensifs les organismes nuisibles, à en prévenir l'action ou à les combattre de toute autre manière, par une action autre qu'une simple action physique ou mécanique » (Anses, 2020). [3] Le formaldéhyde en tant que TP 22 (type de produits biocides concernant les fluides utilisés dans la taxidermie et la thanatopraxie) est en cours d'évaluation par l'Allemagne. Les conclusions de cette évaluation pourront être mises à disposition au plus tard le 31/12/2022 (Anses, 2020). CosmétiquesLe formaldéhyde fait partie des substances interdites dans les produits cosmétiques commercialisés pour un usage en Union Européenne (Règlementation 1223/2009/EC sur les Produits Cosmétiques, amendé par la règlementation 2019/1966/EU datant de novembre 2019) (ECHA). TextilesComme mentionné ci avant dans cette fiche, le formaldéhyde est inclus dans l'appendice 12 de l'annexe XVII de Reach (Restrictions applicables à la fabrication, à la mise sur le marché et à l'utilisation de certaines substances dangereuses et de certains mélanges et articles dangereux). Cette restriction interdit la mise sur le marché de vêtements contenant du formaldéhyde à plus 75 mg/kg à partir du 1er novembre 2020 sauf pour certains articles comme les vestes manteaux ou tissus d'ameublement, les vêtements entièrement en cuir naturel, dans les vêtements ou chaussures de seconde main, les textiles jetables (utilisation unique), les tapis et revêtements de sol textile (ECHA, 2020). Panneaux de boisLe Règlement Produits de Construction (RPC) (No 305/2011abrogeant la Directive des Produits de Construction (n° 89/106/CEE) impose des normes européennes avant la mise sur le marché de produits utilisés dans la construction. En 2004 les normes d'émissions (EN 13986 et en France NF EN 717) définissent les classes E1 et E2 en fonction des émissions de formaldéhyde des panneaux de bois agglomérés (panneaux de fibres) non revêtus contenant des résines à base de formaldéhyde. La classe E1 est définie par des rejets dans l'air inférieurs à 0.124 mg par m3 d'air (émissions estimées dans une chambre test en suivant les conditions prescrites dans les standards européens EN 717-1). La classe E2 quant à elle est définie par des rejets supérieurs à 0.124 mg par m3 d'air. Concernant la qualité des panneaux contreplaqués, en termes d'émission en formaldéhyde, celle-ci est définie par la norme européenne NF EN 1084. Les classes de dégagement de formaldéhyde sont définies comme suit : Classe A ≤ 3,5 mg/m2/h, Classe B ≤ 8 mg/m2/h, Classe C > 8 mg/m2/h. Les panneaux de bois à base de résines phénoplastes appartiennent généralement à la classe A (ATMO ALSACE, 2007). Agro-alimentaire« L'arrêté du 19 octobre 2006 (modifié par arrêté du 22 avril 2020) autorise l'utilisation de formaldéhyde, en tant qu'auxiliaire technologique dans le procédé d'extraction du sucre de betterave, sous la forme d'une solution aqueuse de formaldéhyde à 30 % dans les conditions d'emploi de 120 g par tonne de betteraves » (Anses, 2020). Le formaldéhyde est autorisé par le règlement (CE) n° 68/2013 pour le tannage des protéines dans les tourteaux. La teneur en aldéhyde libre est fixée à 0,12%. L'utilisation en tant que conservateur d'ensilages, pour le lait écrémé destiné aux porcs de moins de 6 mois ainsi qu'en tant qu'agent anti-salmonelle, n'est plus autorisé en France en alimentation animale depuis le 1 juillet 2015 conformément à la décision de la Commission n°2013/204/UE. Autres textesEaux de rejetLe formaldéhyde n'est pas concerné par l'action nationale de recherche et de réduction des rejets de substances dangereuses dans les eaux (RSDE), qui a pour objectif l'amélioration de l'état des milieux aquatiques, via la réduction progressive des émissions, rejets et pertes de substances dangereuses. Eaux souterrainesLe formaldéhyde fait partie de l'annexe I (listes des substances dangereuse) de l'arrêté du 17 juillet 2009 relatif aux mesures de prévention ou de limitation des introductions de polluants dans les eaux souterraines. Eaux de surfaceLes annexes II et III de l'arrêté du 25 janvier 2010 établissant le programme de surveillance de l'état des eaux en application de l'article R. 212-22 du code de l'environnement, ne définissent pas le formaldéhyde ni comme une substance pertinente à surveiller ni comme polluant spécifique de l'état écologique. Produits phytosanitaires dans l'alimentationIl n'existe pas de Limite Maximale de Résidus concernant le formaldéhyde dans les aliments au niveau de l'Union Européenne (Union Européenne, 2011). Néanmoins il existe une limite à la présence de formaldéhyde pour certains types de tourteaux destinés à la consommation animale. Comme précédemment expliqué dans cette fiche, le formaldéhyde n'est plus autorisé comme pesticide. Il est en revanche toujours utilisé en agriculture dans certains engrais. Contact alimentaireSelon le règlement (UE) N°10/2011 concernant les matériaux et objets en matière plastique destinés à entrer en contact avec des denrées alimentaires, le formaldéhyde peut être utilisé comme additif ou auxiliaire de production de polymères et comme monomère ou autre substance de départ ou macromolécule obtenue par fermentation microbienne. |
| Classification CLP | Voir la classification CLP |
| Valeurs et normes appliquées en France |
FTE 2020 Importer Les paragraphes ci-après présentent les principales valeurs et normes en vigueur à la date de la rédaction de cette rubrique. Cet inventaire n’est pas exhaustif. Seuils de rejets pour les installations classées et les stations de traitement des eaux uséesL'Arrêté du 31/01/08 relatif au registre et à la déclaration annuelle des émissions et des transferts de polluants et des déchets modifié par l'arrêté du 11 décembre 2014 indique que les seuils de déclaration pour le formaldéhyde sont de :
Le formaldéhyde n'est pas visé par l'AM du 2/02/98 modifié fixant des VLE pour les rejets dans l'eau. Valeurs appliquées en milieu professionnelLe décret n° 2020-1546 du 9 décembre 2020 fixe les valeurs limites d'exposition professionnelles qui entrent en vigueur le 1er février 2021 : VLEP 8H = 0,37 mg.m-3 (0,3 ppm) VLCT (15 min) = 0,74 mg.m-3 (0,6 ppm) Ces VLEP sont assorties de l'observation ‟sensibilisation cutanée”. Pour les secteurs des soins de santé, des pompes funèbres et de l'embaumement, la valeur limite est de 0,62 mg.m-3 (0,5 ppm) jusqu'au 11 juillet 2024. Valeurs appliquées pour la qualité des eaux de consommationL'arrêté du 11 janvier 2007 relatif aux limites et références de qualité des eaux brutes et des eaux destinées à la consommation humaine mentionnées aux articles R. 1321-2, R. 1321-3, R. 1321-7 et R. 1321-38 du code de la santé publique ne fixe pas de teneur maximale (annexe I), de valeur limite de qualité (annexe II), ni de valeur guide ou impérative (annexe III) pour le formaldéhyde. Le formaldéhyde ne figure pas dans la directive européenne sur l'eau potable mise en vigueur à partir du 12 janvier 2021 (directive (UE) 2020/2184 du 16 décembre 2020, refonte de la directive 98/83/CE) Valeurs appliquées dans l'airAir ambiantLe formaldéhyde est un précurseur d'ozone et il est cité à l'annexe 1 « liste des polluants réglementés » de l'arrêté du 19/04/17 relatif au dispositif de surveillance de la qualité de l'air. Le formaldéhyde fait partie du programme de mesure concerté de surveillance continue et d'évaluation du transport à longue distance des polluants atmosphériques en Europe (EMEP), dont la composante française est l'observatoire « MERA ». Air intérieurLa loi du 1er août 2008 portant engagement national pour l'environnement a rendu obligatoire la surveillance de la qualité de l'air intérieur dans certains établissements recevant un public sensible (articles L. 221-8 et R. 221-30 et suivants du code de l'environnement) et oblige à définir des ‟valeurs guides”. Les établissements concernés sont notamment ceux accueillant des enfants :
Le décret n2011-1727 du 2 décembre 2011 relatif aux valeurs-guides pour l'air intérieur pour le formaldéhyde et le benzène, fixe pour le formaldéhyde une valeur-guide pour l'air intérieur pour une exposition de longue durée à 30 µg/m³ au 1er janvier 2015 et à 10 µg/m³ au 1er janvier 2023. Ces « valeurs-guides » ont été déterminés sur la base des expertises de l'Agence nationale de sécurité sanitaire de l'alimentation, de l'environnement et du travail (Anses) et du Haut Conseil de la Santé publique (HCSP). Le décret n° 2015-1926 du 30 décembre 2015 relatif à l'évaluation des moyens d'aération et à la mesure des polluants effectuées au titre de la surveillance de la qualité de l'air intérieur de certains établissements recevant du public fixe pour le formaldéhyde une concentration > 100 µg.m-3 , valeur pour laquelle des investigations complémentaires doivent être menées et pour laquelle le préfet du lieu d'implantation de l'établissement doit être informé. En 2018, l'Anses a proposé des valeurs guides de la qualité de l'air intérieur (VGAI) non réglementaire pour le formaldéhyde (Anses 2018): Le Haut Conseil de Santé Publique (HCSP) a mis en jour en 2019 ses recommandations en termes de« valeurs repères d'aide à la gestion » pour le formaldéhyde (HCSP 2019). Le HCSP recommande de retenir deux valeurs repères d'aide à la gestion pour prévenir des effets liés à une exposition au formaldéhyde :
|
| Informations complémentaires |
Le formaldéhyde ou aldéhyde formique, de formule brute HCHO, est le plus simple des aldéhydes. À température ambiante, c’est un gaz incolore, d’odeur piquante et suffocante. Le formaldéhyde pur, sous forme de gaz anhydre, est difficile à produire et à conserver car il a tendance à se polymériser. Il n’est donc pas commercialisé sous forme gazeuse mais disponible en solutions aqueuses ou sous ses formes polymérisées : le paraformaldéhyde et le trioxane. • Réactivité : le formaldéhyde est un composé très réactif avec les oxydants forts, les acides, les bases et il est très hygroscopique. Il se polymérise facilement en particulier à froid ou en présence de traces d’impuretés polaires (acides, alcalins) ou d’eau. En solution diluée il peut réagir avec l’hydroxyde de sodium en libérant de l’hydrogène. Les solutions d’aldéhyde formique sont légèrement corrosives vis-à-vis de la plupart des métaux. Dans l’air, le formaldéhyde s’oxyde lentement avec formation d’acide formique ; l’oxydation complète donne du dioxyde de carbone et de l’eau. C'est un réactif très inflammable qui peut former des mélanges explosifs avec l’air (en fonction de la température, de la concentration et du milieu). La réaction de condensation du phénol avec l’aldéhyde formique peut être violente, voire explosive. |
Volume de production
| France |
FTE 2020 Importer 44 000 t.an-1 |
|---|---|
| UE |
FTE 2020 Importer 3 200 000 t.an-1 |
| Monde |
FTE 2020 Importer 41 000 000 t.an-1 |
Consommation
| Volume de consommation en France |
FTE 2020 Importer 185 000 t.an-1 |
|---|---|
| Part de la consommation dédiée à l’usage principal en France |
FTE 2020 Importer 80% utilisé pour la production de résines en 2005 |
Présence dans l'environnement
| Eaux de surface |
FTE 2020 Importer La base de données Naïades recense 6 226 mesures de formaldéhyde dans les eaux de surface en France entre 2017 et 2019. Parmi ces mesures, 1 004 (soit 16%) présentent des concentrations de formaldéhyde supérieures à la limite de quantification comprise entre 0,05 et 50 µg.L-1. La concentration médiane en formaldéhyde des échantillons dont la concentration est quantifiable s'élève à 2 µg.L-1 et est inférieure à la Valeur Guide Environnementale (VGE) de 10 µg.l-1 dans l'eau douce établie par l'Ineris en 2011. La concentration maximale en formaldéhyde observée s'élève à 1 242 µg.L-1 et correspond à un prélèvement effectué dans un cours d'eau de la région Normandie (BRGM). |
|---|---|
| Eaux souterraines |
FTE 2020 Importer En 2011, le BRGM a mené une campagne exceptionnelle (CAMPEX) d'analyses des substances présentes dans les eaux souterraines en métropole. Le formaldéhyde a fait l'objet de 943 mesures dont 9 présentent une concentration de formaldéhyde supérieure à la limite de quantification de 5 µg.l-1, la concentration maximale est de 34 µg.L-1. La base de données ADES répertorie 4 375 mesures de formaldéhyde dans les eaux souterraines en France entre 2017 et 2019. Parmi ces mesures, 146 (soit 3 % de la totalité des mesures) présentent une concentration supérieure à la limite de quantification comprise entre 1 et 50 µg.l-1, une médiane de 7,2 µg.l-1 et une concentration maximale de 493 µg.l-1. |
| Air |
FTE 2020 Importer Il existe en France une station de mesure du formaldéhyde dans l'air, celui-ci se situe en zone urbaine et à distance de sites industriels, les mesures étant effectuées sur une année complète au moyen de tubes à diffusion par l'association de surveillance de la qualité de l'air Atmo Auvergne Rhône Alpes. La base nationale de données de qualité de l'air appelée GEOD'AIR indique qu'en 2018 et 2019, la concentration atmosphérique annuelle moyenne de formaldéhyde s'élevait pour ce site respectivement à 1,72 et 1,9 µg.m-3. |
| Sols |
FTE 2020 Importer Compte tenu de la valeur du Koc (37 L.kg-1), une adsorption du formaldéhyde au niveau des sols n'est pas attendue et sa mobilité devrait être élevée. Par conséquent, il peut être facilement mobilisé par ruissellement ou par lixiviation vers les eaux de surface ou des eaux souterraines. |
Production et utilisation
Production et ventes
Données économiques
FTE 2020 Importer
Le formaldéhyde a été produit pour la première fois en Allemagne à la fin du XIXème siècle. Sa production industrielle a débuté après la première guerre mondiale (ICIS). Durant la fin du XXème siècle, comme le montre le tableau 4, sa production a été en constante augmentation jusqu'à aujourd'hui. Sa production entre 1983 et 1999 en Europe de l'Ouest et aux Etats Unis (IARC, 2006) selon IARC aurait augmenté de 180%. Au vu des données consultées dans la littérature il semblerait également que les quantités produites aient augmenté au début du XXIème siècle avec le développement des capacités de production en Asie.
Tableau 4 : Production de formaldéhyde pur par région en millions de tonnes

En 2008, 48% du formaldéhyde était produit en Asie, 23% en Europe et 17% en Amérique du Nord (Hunt, et al., 2018). En Asie, la Chine est le principal producteur de formaldéhyde, avec en 2007 34% de la production mondiale. Le développement de ses capacités de production s'est déroulé entre 1990 et 2005, avec une multiplication de sa production par 16 (Tang, et al., 2009).
En Europe, le formaldéhyde est majoritairement commercialisé sous la forme de solution aqueuse, formaline ou formol. Les principales capacités de production de cette solution se trouvent en Allemagne avec une capacité de 2,2 millions de tonnes de formaline (formaldéhyde à 37%) en 2010. Les capacités de la France étaient de 0,5 millions de tonnes de formaline (formaldéhyde à 37%).
La répartition géographique de la consommation de formaldéhyde est proche de la répartition de sa production ; 47% est consommée en Asie, 29% en Europe et 14% en Amérique du Nord. Une des raisons expliquant cette similitude est que cette substance est peu stable, ce qui génère des coûts de transports élevés (IHS Markit, 2019).
En France les sources consultées montrent que la production a été en augmentation jusqu'à 2005 à minima. L'absence de données concernant la production actuelle ne nous permet pas de conclure sur la tendance de ces dernières années jusqu'à aujourd'hui. Néanmoins il semblerait que la consommation du formaldéhyde soit elle, en augmentation avec une très large utilisation de cette substance pour la production de résine utilisée dans le secteur du bois.
Tableau 5 : Evolution de la production et de la consommation de formaldéhyde pur en France (en tonnes)

Selon l'OCDE le formaldéhyde a généré en 2011, 11 milliards de recettes au niveau mondial. La Chine représentait 50% de ce marché en 2011, l'Europe 23% et l'Amérique du Nord 17% (Hunt, et al., 2018). Au regard des données disponibles consultées et malgré la mise en place de mesures de restrictions de certains usages en Europe, il semblerait que le marché de cette substance sera en augmentation au cours des 10 prochaines années. Cette tendance s'explique par la demande croissante en produits à base de bois (panneaux de bois reconstitués) dans lesquels le formaldéhyde est utilisé pour la fabrication de résines utilisées comme liant (Transparency Market Research) (Acumen Research and Consulting).
[7] Europe de l'ouest
[8] UE +28
Procédés de production
FTE 2020 Importer
La majorité du formaldéhyde est utilisée pour la production de résines phénoliques, aminoplastes et acétals. Etant donné l'importante utilisation de formaldéhyde pour la production de résines, la production de formaldéhyde et la production des résines produites à partir de cette substance sont détaillées distinctement.
Production du formaldéhyde
Deux procédés sont utilisés pour la production de formaldéhyde :
- Par une réaction d'oxydation-déshydrogénation en utilisant de l'argent comme catalyseur. Durant cette réaction du méthanol est vaporisé avec de l'air chauffé à 650 °C, engendrant sa déshydrogénation et ainsi la formation de formaldéhyde. La chaleur de cette réaction endothermique est produite par la combustion de l'hydrogène produit par la réaction de déshydrogénation. (ICIS)
- En oxydant du méthanol (procédé Formox) avec comme catalyseurs le molybdène et fer oxydé. La réaction se fait autour de 350 °C et est fortement exothermique
Dans les deux processus, le formaldéhyde formé est isolé par absorption dans l'eau. L'augmentation de la concentration du formaldéhyde en solution (formaline) est possible par distillation (Braun, et al., 1989). Les rendements de ces deux procédés se situent autour de 90%. Bien que la seconde réaction se fasse à une température plus basse et avec des catalyseurs moins chers, il semblerait que ce soit la première qui soit la plus utilisée.
Production de résines à base de formaldéhyde
Résines phénoliques
Les résines phénoliques (ou résines phénoplastes (PF) sont des résines synthétiques obtenues par polycondensation d'un phénol et d'un aldéhyde, généralement le formaldéhyde. Le phénol peut être substitué par d'autres substances et conduire à la formation d'autres résines : exemple crésol, résorcinol (voir ci-après). Lorsque la réaction se fait en présence d'un excès de phénol sur le formaldéhyde, et d'un catalyseur de type acide fort, on obtient des résines thermoplastiques (résines novolaques phénol-formol (PF), alors qu'en présence d'un excès de formaldéhyde sur le phénol, et d'un catalyseur de type basique, on obtient des résines thermodurcissables appelées résols ou résitols (phénol-résorcinol-
formol (PRF), phénol-formol (PF). Les novolaques peuvent également être transformés en matières thermodurcissables par l'ajout d'hexaméthylènetétramine. Les résines phénoliques sont particulièrement intéressantes pour leur très bonne résistance au feu et leur excellente tenue thermique (Ineris, 2013), (CHEVALIER, 1991). Les premières résines PF ont été synthétisées par Bayer en 1872. Leur commercialisation se fera un peu plus tard à la fin du XIXème siècle, une fois leur fabrication industrielle réalisable à un prix permettant de concurrencer les résines présentes sur le marché. La bakélite (nom commercial) est une des résines de type PF les plus connues.
Résines aminoplastes
Les résines aminoplastes sont des résines thermodurcissables. Ce sont des résines synthétiques produites par la réaction du formaldéhyde avec l'urée ou la mélamine : soit respectivement les résines mélamine-formol (MF), urée-formol (UF), ou encore mélamine-urée-formol (MUF) en cas d'utilisation d'un mélange urée/mélamine.
La production industrielle de résines UF est réalisée en deux phases : une étape alcaline de méthylation suivie d'une étape acide de condensation.
Résines acétals ou polyacétals
Ce sont des résines thermoplastiques. Les résines acétals sont généralement des polyoxyméthylènes (POM) obtenus par polymérisation du formaldéhyde ou des copolymères du formaldéhyde, avec l'oxyde d'éthylène. Ces acétals de polyvinylalcool et d'aldéhydes peuvent également utiliser l'aldéhyde acétique (éthanal) ou l'aldéhyde butyrique (butanal) (Ineris, 2013) et (AFFSET, 2009).
Noms commerciaux
FTE 2020 Importer
Les noms commerciaux figurant dans le Tableau 6 sont issus de la page de l'Echa relative au formaldehyde (ECHA). Par cohérence avec ces données européennes nous avons laissé les noms sont en anglais.
Tableau 6 : Synonymes et noms commerciaux extraits du site de l'Echa (ECHA)

Utilisations
Introduction (varitétés d'utilisations)
FTE 2020 Importer
Le formaldéhyde est une des substances les plus utilisées par l'industrie chimique au monde, il s'agit de l'aldéhyde le plus commercialisé étant donné le large spectre des usages que la substance permet. Selon l'ECHA, aujourd'hui, 98% du formaldéhyde produit ou importé en Union Européenne est utilisé comme intermédiaire réaction pour la production de résines (majoritairement utilisées pour leurs propriétés liantes pour la fabrication de panneaux de bois) de thermoplastiques, de mousses de polyuréthane et d'autre substances chimiques (ECHA, 2019). Selon une enquête initiée en 2005 par la Direction Générale des entreprises auprès des industriels français, la production de résines constituerait 84% des usages du formol (Ineris, 2007).
En dehors de son emploi pour produire des résines ou d'autres substances, le formaldéhyde peut être utilisé en tant que tel ou comme adjuvant à un produit, et dans ce cas il remplit généralement une fonction de conservateur, ou de biocide notamment dans les secteurs de l'élevage, de la pisciculture, de la taxidermie et de la médecine. Cette substance est également utilisée dans la synthèse de nombreuses substances chimiques (sel tétrasodique d'EDTA, hexaméthylènetétramine, pyridine…).
En UE, parmi les résines produites à partir de formaldéhyde la majeure partie du formaldéhyde est utilisé pour la production de résines condensées (figure 1), c'est-à-dire les résines phénoliques (PF), les résines aminoplastes (MF, UF, MUF) et les résorcinols.
Dans les années 1990 l'utilisation de ces résines se concentrait majoritairement aux Etats Unis et en Europe. Aujourd'hui la Chine est le pays qui utilise le plus de résines à base de formaldéhyde (Tang, et al., 2009). Quelques soient les marchés, ces résines sont en premier lieu utilisées dans le cadre de la production de panneaux de bois.

Figure 1 : Utilisations industrielles du formaldéhyde selon ECHA 2019 citant « Formacare » 2015 (ECHA, 2019)
Dans la figue 1, la catégorie « autres usages » correspond à l'utilisation de formaldéhyde comme intermédiaire de synthèse, bactéricide utilisé dans le secteur médical, agent de conservation utilisé en taxidermie, agent biocide et conservateur dans l'agroalimentaire, ingrédient pour la production d'engrais agricole.
Production de résines condensées
FTE 2020 Importer
Comme expliqué ci-avant la production de résines constitue la première utilisation du formaldéhyde. Parmi les résines produites à base de formaldéhyde, les résines condensées sont les plus produites et parmi celles-ci les plus produites sont les résines UF puis les résines PF et MF (Ineris, 2007).
Les résines aminoplastes (UF, MF, MUF) sont utilisées à différentes concentrations, en solution ou en poudre, dans des secteurs variés. Avec des propriétés identiques aux résines phénoliques, leurs teintes très claires leur permettent de surcroit d'être faciles à colorer (Ineris, 2013) et (AFFSET, 2009). Les résines UF représentent 42% de la consommation de formaldéhyde en 2015 et sont utilisées (à 80%) comme adhésif (liant) dans l'industrie du bois notamment pour la production de panneaux contreplaqué à usage intérieur (dans des conditions sèches) (ECHA, 2019).
Ces résines sont utilisées comme agent liant dans de nombreux matériaux et produits, principalement les panneaux de particules, les matériaux isolants, les produits de revêtement (protection, vernis…), et des colles.
Production de produits à base de bois (panneaux de bois contreplaqué et aggloméré)
Dans le secteur du bois parmi les résines condensées ce sont les résines aminoplastes UF qui sont les plus utilisées en tant qu'adhésif (liant) pour la production de contreplaqué notamment.
Tableau 7 : Répartition des types de résines condensées utilisées comme adhésif dans le secteur du bois en 1999 en Europe de l'ouest (DUNKY, et al., no date)

Dans les produits à base de bois les résines condensées sont présentes en tant que liant, et composants des colles. Leur fonction est aussi de libérer du formaldéhyde qui aura une action fongicide et bactéricide et donc de conservation pour le produit. Les produits-bois concernés sont les panneaux de contreplaqué / stratifié (collage du contreplaqué), les panneaux de fibres de bois, les panneaux de lamelles minces, longues et orientées (OSB), les panneaux de particules bruts ou revêtus de placage, les portes planes, les parquets contrecollés, les charpentes lamellées-collées. D'après www.egger.com citant une étude du Fraunhofer Institut WKI, 80 à 85% de panneaux bois seraient collés avec une résine au formol dans le monde. Les quantités de formol employées en France en 2006 dans ce domaine étaient de 190 000 t (AFFSET, 2009).
La distinction entre colles à base de résine, et résines n'est pas toujours faite par les professionnels, et les deux termes parfois utilisés indifféremment. Néanmoins dans ce rapport le terme résine sera utilisé pour les produits permettant la production de panneaux à bois et le terme colle sera utilisés pour les produits d'ameublement.
Les panneaux en contreplaqués sont plus ou moins résistants à l'humidité, en fonction de la résine utilisée pour lier les différentes feuilles de plaquage. Les panneaux utilisés en environnement sec intérieur sont liés avec de la résine urée-formaldéhyde (UF). Les panneaux destinés aux cuisines et salles de bains sont liés avec une résine mélamine-urée-formol (MUF), car ils doivent être résistants à l'humidité. Les panneaux fabriqués pour être totalement exposés aux intempéries et à l'eau bouillante sont assemblés avec un adhésif de couleur rouge foncé, la résorcine-formaldéhyde ou la phénol-résorcine formaldéhyde. Les contreplaqués de feuillus (bois dur) contiennent des résines à base d'urée-formaldéhyde (UF) alors que les contreplaqués de résineux contiennent des résines à base de phénol-formaldéhyde (PF), plus stables chimiquement que les résines UF et donc moins sensibles aux fluctuations de température et d'humidité. D'après l'UIPP, cette solution est la plus utilisée pour les contreplaqués (ATMO ALSACE, 2007).
D'après une enquête du Ministère de l'Industrie exploitée par l'Ineris en 2007, du formaldéhyde pur est également incorporé aux panneaux en contreplaqué (Ineris, 2007).
Les panneaux de particules agglomérées sont constitués de particules de bois (grands copeaux, particules, copeaux de rabotage, sciures) et/ou autre matériau lignocellulosique en forme de particules (amas de chanvre, amas de lin, fragments de bagasse). Ces copeaux de bois ou de résidus sont le plus fréquemment agglomérés à l'aide de résine d'urée-formaldéhyde, mais la résine mélamine-urée-formol (MUF) peut également être employée.
Les panneaux de particules orientées (OSB) sont liés avec des résines phénolformaldéhyde (PF), mélamine-urée-formol (MUF) et diisocyanate de diphénylméthane (pMDI), ou une combinaison de ces liants (ATMO ALSACE, 2007).
Les panneaux de fibres à moyenne densité (MDF), sont constitués de fibres lignocellulosiques liées à l'aide d'une résine à base de formaldéhyde (résine urée-formol ou UF). Cette résine représentant jusqu'à 9 % du poids de ces panneaux, ils dégagent plus de formaldéhyde que les panneaux de particules. Ils sont généralement reconnus comme étant les produits en bois pressé ayant l'émission de formaldéhyde la plus élevée (ATMO ALSACE, 2007). Cette information est confirmée par l'US EPA. (US EPA 2012)
Dans l'industrie de l'ameublement les colles sont utilisées pour les emplois suivants :
- Le collage de placage fin (feuille de bois noble) sur bois ou panneaux : des colles urée-formol9 (ou phénol-formol10) peuvent être utilisées pour le collage des chants
- L'habillage : colles à base de résines urée-formol, phénol-formol entre autres
- L'assemblage du meuble : les colles néoprènes11 sont les plus utilisées
[9] Également appelé colle aminoplaste
[10] Également appelé colle phénoplaste
[11] Plus d'information partie « production de matériaux de construction dont colles »
Production de revêtements de type peintures, vernis, encres, couleurs
Les revêtements de matériaux de construction et décoration utilisent des produits à base de formaldéhyde comme des peintures, des produits de protection du bois, et des vernis. Les matériaux
de support concernés sont variés : ensemble des supports pour peinture, également certains plastiques, et le caoutchouc (pour certains vernis).
Vernis :
Selon le rapport de l'AFSSET (AFFSET, 2009), la majorité des vernis et laques pour meubles en bois sont sans formaldéhyde, et seule une famille d'aminoplastes, dite à catalyse acide, appelés parfois «vernis précatalysés » peuvent en émettre. Les vernis en phase aqueuse ou les poudres n'en contiennent pas. Les résines formoliques sont aussi employées dans des vernis pour l'émaillage des métaux.
On note également l'utilisation de vernis contenant du formaldéhyde pour isoler des câbles émaillés (Ineris, 2007).
Peintures :
Les peintures sont constituées d'un liant, de pigments, de solvants et d'additifs. Les liants utilisés peuvent contenir du formaldéhyde (résines urée-formol ou mélamineformol, phénol-formol), mais ce ne sont pas les liants les plus courants pour cette application (ATMO ALSACE, 2007). Les liants à base de formaldéhyde sont utilisés pour leurs propriétés d'adhérence sur supports difficiles (peintures pour métal, verre, faïences…), de résistances mécanique et chimique. Ils permettent de moduler la souplesse des revêtements (AFFSET, 2009). Sont également concernés par le formaldéhyde les additifs pour des peintures de revêtement de façades. Dans ce domaine, on dispose de données partielles concernant les volumes employés en France (AFFSET, 2009) :
- 4t.an-1 pour les colorants et pigments
- 0,8 t.an-1 pour les peintures et vernis (ce qui confirme une utilisation très restreinte mentionnée par les professionnels)
Les résines aminoplastes sont également utilisées dans la production d'encre.
Production de papier
Les résines phénoliques et les résines aminoplastes sont utilisées dans l'industrie papetière pour la production de papier spéciaux : papiers couchés12 , papiers résistants à l'humidité, papier kraft. Du formaldéhyde est également utilisé dans les serviettes en papier jetable pour leur apporter des propriétés de résistance à l'humidité notamment.
Environ 2000 tonnes de formaldéhyde seraient utilisées par an13 en France dans ce secteur pour la production des résines (Ineris, 2007).
[12] Le papier ou carton couché est un papier ou carton dont la surface est recouverte d'une ou plusieurs couches généralement constituées de produits minéraux en mélange avec des liants et des produits d'addition divers (source Wikipédia).
[13] Valeur estimée en 2005
Production de textile
Les résines UF sont utilisée dans l'industrie du textile14 , ces résines conférant notamment des propriétés comme la stabilité, l'infroissabilité, l'apprêt, le durcissement et comme liant des impressions pigmentaires…
Des résines dites « Résorcine Formol Latex » sont utilisées pour des textiles destinés au renfort de caoutchoucs (Ineris, 2013).
[14] Environ 1300 tonnes sont utilisées annuellement en France pour cet usage selon (Ineris, 2007).
Production du plastique
Les résines phénoliques et aminoplaste sont utilisées en tant que polymère dans la production de plastiques thermodurcissables. Les plastiques obtenus sont infusibles et insolubles. Ces plastiques résistent à la chaleur et sont donc utilisés pour produire des articles comme par exemple les poignées de casseroles, fer à lisser, composants électroniques, interrupteurs électriques…
Production de matériaux de construction dont colles
Les Résines phénoliques sont utilisées comme liant dans des isolants en laine minérale (laine de verre et laine de roche), dans la composition de revêtements de matériaux de construction (peintures, vernis)
Les résines aminoplastes (MF et MUF) sont utilisées dans l'industrie du béton, ces résines servant à retarder ou accélérer la prise du béton. Environ 3400 tonnes seraient utilisées annuellement en France pour cet usage selon le ministère de l'industrie (Ineris, 2007).
Dans les produits divers pour le bâtiment ou le bricolage, sont concernés les colles néoprène, des colles à bois, des colles pour canalisations en plastique, des mastics, des produits d'étanchéité, et des enduits de ragréage. En dehors des applications pour les panneaux de bois, les colles formoliques sont globalement assez peu utilisées dans le bâtiment.
D'après (Techniques de l'Ingénieur, 2006) les colles basées sur les résines formoliques sont utilisées uniquement pour coller les couples de matériaux suivants :
- Bois/Bois,
- Bois/Plâtre,
- Bois/Ciment-Béton-Mortier-Brique,
- Bois/Mousses isolantes PU,
- Bois/Polystyrène expansé,
- Bois/Stratifiés,
- Mousses isolantes rigides PU/Mousses isolantes rigides PU,
- Mousses isolantes rigides PU/Polystyrène expansé
- Stratifiés/Mousses isolantes rigides PU
- Plastiques thermodurcissables/ Polystyrène expansé
Les colles néoprènes dites « de contact », sont composées généralement d'un élastomère synthétique type résine formo-phénolique (PF) dissous dans un solvant organique. La résine PF utilisée est une résine novolaque (produite par un excès de phénol sur le formaldéhyde) ou resole (produite par un excès de formaldéhyde sur le phénol). Ces colles sont utilisées dans le domaine de la décoration ou pour le bricolage, mais aussi pour les petites réparations avec différents matériaux (cuir, matériaux poreux, bois…).
Les colles en phase aqueuse (colles vinyliques, acryliques), qui sont par exemple utilisées pour coller des moquettes ou du parquet, peuvent contenir du formaldéhyde comme agent biocide.
Production de caoutchouc
Des résines phénoliques sont utilisées dans l'industrie du caoutchouc15 pour la production de pneumatiques et pièces techniques en caoutchouc (courroie, tuyaux, cylindres, bandes transporteuse…), la résine servant au collage ou au renforcement du caoutchouc.
Environ 1300 tonnes sont utilisées annuellement en France pour cet usage selon (Ineris, 2007).
[15] Environ 1300 tonnes sont utilisées annuellement en France pour cet usage selon (Ineris, 2007).
Fonderie
Les résines phénoliques (PF), résines urée-formaldéhyde (UF), résorcinol- formaldéhyde (RF), mélamine formaldéhyde (MF) sont utilisées comme liants pour la fabrication de moules et de noyaux. s (AFFSET, 2009). Les quantités de formaldéhyde utilisées par ce secteur seraient négligeables en France selon (Ineris, 2007).
Production d'abrasifs
Les Résines phénoliques sont utilisées pour la production d'abrasifs appliqués pour les « meules minces » et « les meules abrasives » (Ineris, 2007).
Traitement de l'eau
Des résines cationiques utilisées pour le traitement de l'eau sont fabriquées à partir de résine mélanine-formaldéhyde (MF). En France 7000 tonnes de formaldéhyde auraient été utilisées en 2005 pour cet usage (Ineris, 2007).
Production de Polyols
FTE 2020 Importer
Le formaldéhyde est utilisé pour la production des polyols16 suivants à minima 17:
- Le 1,4-Butanediol (BDO) produit à partir de la réaction de deux molécules de formaldéhyde et une molécule d'acétylène est utilisé comme intermédiaire de production des résines : tétrahydrofurane (THF) et polybutylène (PBT). La production de cette substance représente environ 4% de la consommation de formaldéhyde au niveau européen. Sa production est majoritairement située en Norvège. Les résines THF et PBT sont utilisées pour la production de fibres notamment dans l'industrie du textile, de l'automobile et de l'électronique. (ECHA, 2019) Le 1,4-butanediol peut aussi être utilisé comme solvant.
- Le pentaérythritol ; ce polyol est utilisé pour la production de résines thermodurcissables alkydes utilisées dans les peintures de voitures et pour la production d'esters de polyol utilisé dans les lubrifiants automobiles et aéronautiques. La production de pentaérythriol représente 3% de la consommation européenne de formaldéhyde. Cette substance est également utilisée pour la production de tétranitrate de pentaérythriol entrant dans la fabrication d'explosif (l'élémentarium, 2015).
- Le trimethylol propane (TMP) également précurseur des résines alkydes (voir tiret précédent) et utilisé dans des revêtements et peintures
- Le triméthyloléthane (TME) également utilisé pour la production de résines alkydes
- Le neopentylglycol (NPG) ; utilisé pour la synthèse de polyesters, de peintures, de lubrifiants et de plastifiants ainsi que dans les cosmétiques pour ses propriétés émollientes.
[16] Un polyol, ou polyalcool ou « glycol » est un composé organique caractérisé par un certain nombre de groupes (-OH)
[17] Il se peut que d'autres polyols soient produits à partir de formaldéhyde, ceux présents dans cette liste sont ceux qui ont été le plus retrouvés dans la revue de littérature
Production de résines polyoxyméthylènes (POM)
FTE 2020 Importer
Les résines acétals et notamment les polyoxyméthylènes (POM) sont utilisées pour la production de thermoplastiques. Cette matière détient la propriété de pouvoir se ramollir lorsqu'elle est chauffée mais de redurcir lorsqu'elle refroidit. Les thermoplastiques produits à partir de POM sont très solides, ont une forte résilience ainsi qu'une résistance à l'eau et aux produits chimiques et sont recyclables. On peut retrouver ces plastiques dans le domaine du transport (pièces de moteur de voiture), de la construction, de l'agriculture (machinerie, pompes…), dans des équipements domestiques (montres, mixeurs, appareils de cuisine…), dans des équipements sanitaires et médicaux ainsi que dans des bateaux et planches à voiles et équipement de ski (l'élémentarium, 2015) (Anses, 2016).
Production de 4,4'-diisocyanate de diphénylméthylène (MDI)
FTE 2020 Importer
Le 4,4'-diisocyanate de diphénylméthylène (MDI) produit à partir de formaldéhyde est utilisé pour la production de mousses de polyuréthane utilisées pour l'isolation dans le secteur du bâtiment et de l'automobile et de certains appareils électroniques comme les réfrigérateurs, congélateurs et les appareils à air conditionné. Ces mousses sont également utilisées pour la confection de chaussures. La production de cette substance représente 6% de la consommation de formaldéhyde en Europe (Anses, 2016).
Intermédiaire dans la synthèse de produits chimiques
FTE 2020 Importer
Le formaldéhyde est utilisé comme intermédiaire de synthèse pour les substances suivantes à minima (ECHA, 2019) (liste de substances présentées ci-après n'est pas exhaustive) :
- Urée formaldéhyde pour la production d'engrais à libération prolongée (d'azote), qui permet un contrôle de l'apport nutritif aux plantes et une diminution du lessivage d'éléments nutritif
- L'hexaméthylènetétramine (HMTA)18 obtenue par une réaction de condensation entre le formaldéhyde et l'ammoniac est notamment utilisée comme antibiotique pour les infections urinaires et en tant qu'additif alimentaire comme conservateur, sous le code E239 . Cette substance est aussi utilisée comme composant pour la production d'explosifs (C-4), dans des pastilles de combustible pour campeurs ou militaires (l'élémentarium, 2015)
- Le formaldéhyde est également utilisé comme intermédiaire de synthèse de composés organiques, notamment: comme le sel tétrasodique d'EDTA19 (Ineris, 2011)
- des pyridines ; précurseur pour la productions de nombreux produits comme des insecticides, des explosifs, des médicaments, des arômes alimentaires…
- Substances entrant dans la production de teintures, de parfums et vitamines…
[18] Ou méthénamine, ou hexamine ou urotropine
[19] éthylènediaminetétraacétate de sodium
Autres usages
FTE 2020 Importer
Elevage
Le formaldéhyde est actuellement utilisé dans ce secteur quasi exclusivement pour le tannage des protéines des aliments pour ruminants, notamment des tourteaux d'oléagineux. Le tannage permet de limiter la dégradation microbienne ruminale des protéines végétales et de préserver leurs propriétés nutritives. « Le procédé consiste à faire réagir le formaldéhyde avec les protéines contenues dans un aliment pour que celles-ci ne soient pas dégradées par les micro-organismes du rumen en établissant une liaison stable au pH neutre du rumen mais soient dégradées au niveau intestinal. Le tannage permet d'accroitre pour une même quantité d'aliment ingérée, la fraction de protéines effectivement disponible dans l'intestin dans le but d'augmenter les performances zootechniques de l'animal (production laitière, production de viande) ». (AFSSA, 2004) et (Anses, 2019)
Le formol est également utilisé dans l'élevage pour la désinfection des bâtiments, du matériel et des équipements de transports. La base de données Simmbad référence de nombreux produits utilisés pour l'hygiènes vétérinaire.
Agroalimentaire
Selon l'Echa le formaldéhyde est utilisé dans le secteur de l'agroalimentaire comme conservateur (utilisé pour la production d'additif (voir ci avant 3.2.6) et biocide (pour nettoyer certaines surfaces au contact avec des aliments, utilisé pour la production d'emballage).
Dans l'industrie sucrière il est utilisé comme bactéricide pour stabiliser les infestions microbiennes lors de la production de sucre de canne et betterave pour les étapes d'extraction et de stockage. Le formaldéhyde permet de préserver la qualité du produit et réduire les pertes de production. Selon une étude de l'INRS, 2600 tonnes auraient été utilisées pour cet usage en 2007 (Ineris, 2007). Selon le Syndicat National des Fabricants de Sucre la consommation annuelle de formaldéhyde s'élèverait à environ 80 tonnes/an par usine produisant du sucre à partir de betterave. Aucune estimation à ce jour n'a été réalisée au niveau national (Anses, 2020).
Traitement du cuir
Il existe des résines à base de formaldéhyde consommées par les tanneries, mégisseries, chamoiseries et pelleteries comme conservateur ainsi que pour la transformation du cuir et d'autres applications. Selon plusieurs sources, environ 15 tonnes étaient utilisées en France, pour ces usages (AFFSET, 2009).
Pisciculture
Le formol (formaldéhyde en solution aqueuse) est utilisé en pisciculture afin de lutter contre certaines parasitoses20 . L'utilisation du formol permet de maintenir la population parasitaire a un niveau d'équilibre favorable au développement des poissons.
L'utilisation du formol a diminué entre 1997 et 2007 passant de 77% à 55%. L'utilisation est plus importante en pisciculture marine qu'en eau douce. Selon une enquête menée par le ministère des
finances sur la période 2005 et 2015, 300 tonnes de formaldéhyde seraient utilisées dans ce secteur par an avec un formol contré en formaldéhyde à 23% (Anses, 2019).
[20] Exemple : Ichthyobodo sp, responsable de la costiase ou ichthyobodose
Secteur médical
Dans le secteur médical le formaldéhyde est utilisé en tant que biocide pour désinfecter les salles d'opérations, les salles d'autopsies, les laboratoires de recherche, les instruments utilisés dans les cabinets dentaires… 1000 tonnes de formaldéhyde auraient été utilisées en 2005 en France pour la désinfection des milieux hospitaliers.
Du paraformaldéhyde (formaldéhyde dilué) peut être utilisé en chirurgie dentaire dans certains mastics.
Le formaldéhyde est également utilisé dans la confection de vaccins, comme agent de conservation21 (Ineris, 2007).
Le formaldéhyde est utilisé comme réactif dans les laboratoires de contrôle (contrôle des matières premières, contrôle microbiologique). Il est également utilisé pour fixer les échantillons en anatomie et cytologie médicale ; spécialité médicinale qui a pour objectif d'établir le diagnostic de maladies ou d'y contribuer, par l'interprétation morphologique, macroscopique, microscopique ou moléculaire d'organes, de tissus ou de cellules analysés (cette spécialité contribue à la gestion de la totalité des diagnostics des tumeurs bénignes et malignes). Comme fixateur, le formaldéhyde possède les atouts suivants : il permet de durcir les tissus sans les rétracter, il n'hydrolyse pas les protéines comme par exemple les acides nucléiques (ADN, ARN), il peut fixer les lipides sans les solubiliser contrairement aux fixateurs alcooliques et enfin c'est un biocide qui permet une décontamination tissulaire pendant la phase de fixation (Anses, 2019).
Il est également utilisé pour la production de spécialités pharmaceutiques (VIDAL, 2013). Comme par exemple la production de gélules (capsules) de médicaments à dissolution lente, permettant une meilleure absorption de la substance active par l'organisme (ECHA, 2019). Il est également utilisé lors de la production d'antibiotiques.
Des solutions à base de formaldéhyde sont utilisées pour la conservation d'organes en recherche médicale.
[21] Vaccins à usage vétérinaire également
Taxidermie
Des injections de solutions chimiques à base de formaldéhyde sont utilisées en taxidermie pour désinfecter et préserver la totalité ou certaines parties de cadavres d'animaux (Anses, 2020).
Thanatopraxie
Des solutions à base de formaldéhyde sont également réalisées en thanatopraxie22 pour retarder le processus de décomposition naturelle du corps. En France en 2019, l'essentiel des fluides de conservation étaient à base de formaldéhyde. Selon un professionnel enquêté, les alternatives au formaldéhyde utilisées pour réaliser des soins mortuaires seraient plus compliquées à doser. Il est nécessaire d'adapter les techniques d'injection du produit (Anses, 2020).
[22] soins mortuaires
Nucléaire
Le formaldéhyde peut être utilisé lors du traitement des déchets nucléaires. 2300 tonnes auraient été utilisées en 2005 (Ineris, 2007).
Rejets dans l’environnement
Sources naturelles
FTE 2020 Importer
Divers phénomènes naturels peuvent induire la présence de formaldéhyde dans l'atmosphère : la combustion de matières organiques, l'oxydation dans l'air de composés organiques volatils (COV) ou la décomposition de résidus de végétaux ou de déchets d'animaux (Anses 2009, Salthammer 2010).
La combustion de biomasse lors de feux de forêt ou de broussailles peut générer des émissions de formaldéhyde dans l'atmosphère avec des niveaux d'émission variant en fonction de l'activité du feu et de l'essence de bois.
A titre d'exemple, Hedberg et al. et Schauer et al. ont étudié la combustion de diverses essences de bois et rapportent des facteurs d'émissions de formaldéhyde du bouleau, du chêne, du pin et de l'eucalyptus respectivement de 180-710 mg/kg, 759 mg/kg, 1165 mg/kg et 599 mg/kg (Hedberg 2002 ;
Schauer 2001). De même, Lutes et al., Hays et al. et Andreae et al. ont évalué les facteurs d'émission du formaldéhyde lors du brûlage à l'air libre de déchets verts, de pâturage et de forêt respectivement à 453, 193 et 1210 mg/kg sur brut (Ineris 2012).
Le formaldéhyde peut être formé dans l'atmosphère par oxydation de COV d'origine naturelle : par oxydation photochimique de terpènes, du méthane, de l'isoprène ; par ozonolyse de la carvone, du carvéol, du géraniol et du citral.
En tant qu'intermédiaire métabolique, le formaldéhyde est présent à de faibles niveaux dans la plupart des organismes vivants. A titre d'exemple le niveau de concentration du formaldéhyde peut atteindre 200 mg/kg chez certaines espèces de poissons (EFSA 2014).
Le formaldéhyde est également produit par la décomposition végétale ou de déchets d'animaux. Plusieurs études ont mis en évidence la présence de formaldéhyde dans des milieux forestiers : à l'intérieur et au-dessus d'une forêt de conifères en Allemagne, dans un site forestier isolé en Amazonie centrale (ConcentrationFormaldéhyde de l'ordre de plusieurs ppb), dans des forêts des Alpes autrichiennes (0,24 ppb < ConcentrationFormaldéhyde < 0,52 ppb).
Sources non-intentionelles
FTE 2020 Importer
Les combustions d'origine anthropique, la décomposition de résines, les formations secondaires à partir de substances d'origine anthropique peuvent mener à la formation puis à la présence de formaldéhyde dans l'atmosphère. Lors de conditions météorologiques pluvieuses, le formaldéhyde peut être « lessivé » et gagner les eaux de surface ou les sols.
- La décomposition des résines et colles urée-formaldéhyde et phénol-formaldéhyde employées principalement pour fabriquer des panneaux de bois aggloméré, des produits isolants thermiques (laines minérales), des revêtements (peintures…) et de façon moindre dans les industries papetière4 et textile5 (cf. paragraphe 3.2) peut émettre du formaldéhyde dans l'air (Atmo Alsace 2007).
- La combustion incomplète des carburants ainsi que toutes les formes de combustion qu'elles aient pour origine les incinérateurs de déchets, les centrales thermiques, le chauffage des bâtiments, la cuisson des aliments, l'utilisation d'encens ou de bougies (Ineris 2017), le tabagisme représentent des sources non-intentionnelles de formaldéhyde dans l'atmosphère.
- La présence de formaldéhyde dans l'air peut provenir de réactions chimiques secondaires telles que la réaction d'oxydation des terpènes (substances présentes notamment dans les produits d'entretien et les désodorisants non-combustibles) avec l'ozone. Selon une étude de l'Ineris, les facteurs d'émission massique du formaldéhyde de divers détergents6 sont compris entre 0 et 220 µg.g-1/h durant les trente premières minutes (Ineris 2013). Une étude menée par l'Ineris sur l'utilisation de désodorisants non-combustibles a permis d'identifier le formaldéhyde parmi les substances contribuant le plus aux risques (Ineris 2020).
[4] les résines sont utilisées afin d'augmenter la résistance du papier à l'humidité ou pour la plastification et l'imprégnation du papier « voir détails section suivante 3.2 ? »
[5] les résines aminoplastes (urée-formaldéhyde et mélamine-formaldéhyde) et phénoplastes (phénol-formaldéhyde) à base de formaldéhyde utilisées dans l'industrie de la finition textile (impression, traitement anti-froissage, ignifugation…) « voir détails section suivante 3.2 ? »
[6] Produits vaisselle, nettoyants WC, nettoyants vitres, dépoussiérants, nettoyants multi-usages… « voir détails section suivante 3.2 ? »
Émissions anthropiques totales
FTE 2020 Importer
Le formaldéhyde ne fait pas partie des substances déclarées dans E-PRTR (European Pollutant Release and Transport Register, registre européen des rejets et transferts de polluants à partir de sites industriels), qui selon le Règlement 166/2006/CE, impose aux exploitants de sites industriels visés par ce règlement de déclarer leurs rejets, en fonction de seuils prédéfinis. Les émissions de formaldéhyde dans l'eau, le sol et l'air ne sont donc pas répertoriées au niveau européen.
En France, le formaldéhyde fait partie des substances dont les rejets dans l'air et l'eau doivent être déclarés lorsqu'ils dépassent un certain seuil23 (cf. paragraphe 2.4.1 Seuils de rejets pour les installations classées et les stations de traitement des eaux usées). Cette déclaration annuelle se fait sur le Registre des Emissions Polluantes, via le logiciel de saisie GEREP (Gestion électronique du registre des émissions polluantes) et est gérée dans la base de données nationale du registre des émissions polluantes (BDREP, IREP24).La Figure 2 et le Tableau 8 ci-dessous compilent les données d'émission industrielles du formaldéhyde vers les compartiments « Eau » et « Air » entre 2008 et 2018, notons que cette compilation n'est pas exhaustive car les données BDREP correspondent à des déclarations qui ne concernent que les installations classées pour la protection de l'environnement (ICPE) soumises aux régimes d'autorisation et d'enregistrement, ainsi que les stations de traitement des eaux usées (STEU).

Figure 2. Evolution des émissions industrielles de formaldéhyde entre 2008 et 2018 (Source : BDREP)
Tableau 8. Emissions industrielles totales de formaldéhyde entre 2008 et 2018 (Source : BDREP)

Les émissions atmosphériques de formaldéhyde déclarées entre 2008 et 2018 représentent la quasi-totalité des émissions industrielles totales de cette substance et sont relativement stables au cours de cette période.
Les émissions industrielles de formaldéhyde vers les eaux ont diminué de façon constante entre 2008 et 2018, hormis un pic en 2009 correspondant aux émissions d'un site de collecte et traitement des eaux usées (cf. paragraphe 4.3).
[23] Arrêté du 31/01/08 relatif au registre et à la déclaration annuelle des émissions et des transferts de polluants et des déchets modifié par l'arrêté du 11 décembre 2014
[24] https://www.georisques.gouv.fr/risques/registre-des-emissions-polluantes
Émissions atmosphériques
FTE 2020 Importer
Les flux de formaldéhyde émis dans l'atmosphère et déclarés entre 2008 et 2018 via le logiciel GEREP ainsi que le nombre de déclarants sont présentés dans le Tableau 9 et la Figure 3 ci-dessous.
Tableau 9. Emissions atmosphériques de formaldéhyde entre 2008 et 2018 (Source : BDREP)


Figure 3. Evolution des émissions atmosphériques de formaldéhyde entre 2008 et 2018 (Source : BDREP)
Les flux de formaldéhyde émis dans l'atmosphère entre 2008 et 2018 sont relativement stables (compris entre approximativement 150 000 et 300 000 kg.an-1).
Le nombre de déclarations (compris entre 68 et 98) et le nombre de déclarations avec un niveau de rejet supérieur au seuil (compris entre 12 et 27) évoluent de façon similaire : ils augmentent régulièrement depuis 2008.
Le Tableau 10, ci-après, compile les dix secteurs d'activité les plus émetteurs de formaldéhyde dans l'atmosphère en 2018 selon les données issues de la base de données BDREP, ces données sont aussi illustrées par la Figure 4 ci-dessous. Notons que ces secteurs d'activité sont dans l'ensemble cohérents vis à vis des secteurs d'utilisation du formaldéhyde identifiés précédemment (cf. paragraphe 3.2).
Tableau 10. Dix secteurs d'activité les plus émetteurs de formaldéhyde dans l'atmosphère en 2018 (Source : BDREP)


Figure 4. Répartition sectorielle des émissions atmosphériques de formaldéhyde en 2018 (Source : BDREP)
Avec une part de 74%, la fabrication de placage et de panneaux de bois représentait en 2018 près des ¾ des émissions atmosphériques de formaldéhyde.
La Figure 5, ci-après, illustre la répartition géographique des émissions de formaldéhyde déclarées en 2016 et consignées dans la base nationale BDREP.

Figure 5. Répartition géographique des émissions moyennes de formaldéhyde déclarées dans l'air en France entre 2016 et 2018
Selon les flux d'émission disponibles sur la base de données BDREP, huit établissements concentraient en 2018 les ¾ des émissions de formaldéhyde dans l'atmosphère. Parmi ces huit établissements, sept ont une activité de fabrication de placage et de panneaux de bois et un établissement correspond à une usine de méthanisation. Le site le plus émetteur est un site de production de panneaux mélaminés et
de particules bruts, il représente un peu plus du quart des émissions atmosphériques de formaldéhyde en 2018 (27%).
L'Inventaire National Spatialisé des émissions de polluants dans l'air (INS) concerne les émissions d'une quarantaine de polluants émis par toutes les sources recensées (activités anthropiques ou émissions naturelles).
D'après l'INS, les 5 principales sources d'émissions atmosphériques de formaldéhyde en 2007 étaient classées comme suit (Ineris 2020) :
- Combustion hors industrie : Résidentiel (chaudières, cheminées…) avec 2255 tonnes
- Autres sources mobiles et machines : Engins spéciaux - Agriculture avec 1174 tonnes
- Combustion dans l'industrie manufacturière : Chaudières, turbine à gaz, moteurs fixes avec 450 tonnes
- Autres sources mobiles et machines : Engins spéciaux – Industrie avec 372 tonnes
- Combustion hors industrie : Commercial et institutionnel avec 300 tonnes
Notons que les émissions atmosphériques de formaldéhyde liées au transport routier, à l'agriculture, à la sylviculture, aux émissions naturelles (forêts, animaux, volcans…) et à l'extraction et la distribution de combustibles fossiles/énergie géothermique n'ont pas été recensées en 2007.
D'après l'INS, les émissions atmosphériques de formaldéhyde liées uniquement aux procédés de production industrielle (donc hors combustion) s'élevaient en 2007 à 241 tonnes, il apparait donc que cette source d'émission ne représente qu'une minorité des quantités de formaldéhyde émises dans l'atmosphère.
[25] Seuil2008-2014 = 1500 kg.an-1 / Seuil2015-2018 = 1000 kg.an-1
Émissions vers les eaux
FTE 2020 Importer
La base de données BDREP compte deux types d'émissions vers les eaux : les émissions directes et les émissions indirectes. Un rejet direct est défini comme un rejet isolé dans le milieu naturel avec ou sans passage par une station de traitement propre au site industriel, alors qu'un rejet indirect est défini comme un rejet raccordé à une station d'épuration extérieure au site émetteur. L'évolution des rejets de formaldéhyde industriels totaux, directs et indirects vers les eaux est présentée dans le Tableau 11 et la Figure 6.
Tableau 11. Evolution des émissions de formaldéhyde vers les eaux (Source : BDREP)

Figure 6. Evolution des émissions totales (rejets directs et indirects) de formaldéhyde vers les eaux entre 2008 et 2018 (Source : BDREP)
Le nombre de déclarants peu élevé, tend lui aussi à baisser entre 2008 et 2018 : on dénombrait 8 déclarants d'émissions de formaldéhyde vers les eaux en 2018 contre 15 en 2008. En 2009 la valeur des rejets est de 70 230 kg dont 95% correspondent aux émissions d'un seul site dont l'activité est la collecte et le traitement des eaux usées
Notons que le seuil de rejet pour le formaldéhyde a été établi en 2014, c'est pourquoi la courbe du nombre de déclarants avec des émissions supérieures au seuil ne débute qu'en 2015.
Depuis 2009, les émissions « directes » représentent la quasi-totalité des effluents aqueux formaldéhyde.
Le Tableau 12, ci-après, classe, selon les données issues de la base de données BDREP, les secteurs d'activité émetteurs de formaldéhyde vers les eaux en 2018, ces données sont aussi illustrées par la Figure 7 ci-dessous.
Tableau 12. Secteurs d'activité émetteurs de formaldéhyde vers les eaux en 2018 (Source : BDREP)


Figure 7. Répartition sectorielle des émissions de formaldéhyde vers les eaux en 2018 (Source : BDREP)
Pour rappel en 2018, le nombre de déclarants d'émissions de formaldéhyde vers les eaux s'élevait à 8, par conséquent hormis pour le secteur d'activité « Fabrication de matières plastiques de base », à chaque secteur d'activité correspond un site déclarant.
Les Figure 7 et Figure 8 représentent respectivement les répartitions géographiques des émissions moyennes des rejets directs et des rejets indirects de formaldéhyde vers les eaux entre 2016 et 2018.

Figure 8. Répartition géographique des émissions moyennes de formaldéhyde déclarées dans l'eau (rejet direct) en France entre 2016 et 2018

Figure 9. Répartition géographique des émissions moyennes de formaldéhyde déclarées dans l'eau (rejet indirect) en France entre 2016 et 2018
En 2018, un seul établissement représentait plus des ¾ (78% - 950 kg.an-1 – Rejet direct) des émissions de formaldéhyde vers les eaux, il s'agit d'un site de production de résines échangeuses d'ions, de résines adsorbantes et de catalyseurs.
[26] Pas de seuil jusqu'en 2014 / Seuil2015-2018 = 300 kg.an-1
Émissions vers les sols
FTE 2020 Importer
Le registre français des émissions polluantes pour les installations soumises à déclaration (BDREP) ne répertorie pas d'émission de formaldéhyde vers les sols entre 2008 et 2018.
Pollutions historiques et accidentelles
FTE 2020 Importer
BASOL27 est une base de données française qui recense les sites et sols pollués ou potentiellement pollués suivis par les services de la DREAL.
La base recense au moins 3 sites contaminés par du formaldéhyde :
- un site de fabrication de papiers imprégnés de résines synthétiques pour lequel des analyses de sol ont révélé la présence de formaldéhyde (2.6 mg/kg MS) au niveau de la zone extérieure de stockage de déchets ;
- un site de blanchiment, teinture, impression dont l'analyse des sols en 2007 a mis en évidence une contamination par du formaldéhyde au niveau des bassins de décantation ;
- un site de fabrication de panneaux contreplaqués pour lequel un diagnostic de la pollution des sols a révélé en 2012 la présence de formaldéhyde au niveau de certaines zones.
D'après les données BDREP, trois émissions accidentelles ont été déclarées depuis 2010 :
- deux émissions atmosphériques émises par le même site de fabrication de plaques, feuilles, tubes et profilés en matières plastiques en 2010 et 2011 s'élevant respectivement à 1098 kg et 1509 kg ;
- une émission de 82kg de formaldéhyde vers les eaux en 2011 par une entreprise de fabrication de matières plastiques de base.
[27] (consulté en novembre 2020) https://basol.developpement-durable.gouv.fr/
Présence environnementale
Atmosphère
FTE 2020 Importer
Présence dans l'atmosphère
Il existe en France un site de mesure du formaldéhyde dans l'air, celui-ci se situe en zone urbaine et à distance de sites industriels, les mesures étant effectuées sur une année complète au moyen de tubes à diffusion par l'association de surveillance de la qualité de l'air Atmo Auvergne Rhône Alpes. La base nationale de données de qualité de l'air appelée GEOD'AIR indique qu'en 2018 et 2019, la concentration atmosphérique moyenne de formaldéhyde s'élevait pour ce site respectivement à 1,72 et 1,9 µg.m-3 (LCSQA 2020).
En 2015, des mesures de formaldéhyde ont été mises en œuvre par l'association de surveillance de la qualité de l'air Airparif sur un site de fond urbain et sur deux sites dits « de trafic ». Les concentrations moyennes annuelles de formaldéhyde ainsi obtenues étaient légèrement plus élevées en situation de proximité du trafic routier (2,4 et 2,7 µg.m-3) qu'en fond urbain (1,9 µg.m-3) (AIRPARIF 2016).
Pour mémoire, le formaldéhyde peut être produit lors de phénomènes de combustion, dont celle des carburants de véhicules.
Présence dans l'air intérieur
Les sources potentielles de formaldéhyde dans l’air intérieur sont exclusivement non-intentionnelles et ont été décrites dans le paragraphe 2.8, citons :
- Les produits de construction, de décoration et d’ameublement (panneaux bois aggloméré, isolants thermiques, revêtements, …) ;
- Les combustions (fumée de tabac, bougies, cheminées à foyer ouvert, cuisinières à gaz, …) ;
- Les produits d’usage courant (produits d’entretien, …)
En 2003-2005, la « Campagne nationale Logements 1 » menée par l’Observatoire de la qualité de l’air intérieur dans 567 résidences principales françaises sur une durée d’une semaine avait permis d’effectuer 554 mesures de formaldéhyde (Observatoire de la qualité de l'air 2007).
Les données recueillies lors de cette campagne ont mis en évidence que :
- Le formaldéhyde était présent dans tous les logements avec des concentrations comprises entre 1,3 et 86,3 µg/m3
- L’air intérieur de 50% des logements présentaient des concentrations de formaldéhyde supérieures à 19,6µg/m3
Une « Campagne nationale Logements 2 » visant entre autres à déterminer l’évolution de la qualité de l’air dans les logements en France depuis la première campagne nationale se déroulera en 2020-2022.
Aquatique
FTE 2020 Importer
La base de données Naïades28 recense 6 226 mesures de formaldéhyde dans les eaux de surface en France entre 2017 et 2019. Parmi ces mesures, 1 004 (soit 16%) présentent des concentrations de formaldéhyde supérieures à la limite de quantification comprise entre 0,05 et 50 µg.L-1. La concentration médiane en formaldéhyde des échantillons dont la concentration est quantifiable s'élève à 2 µg.L-1 et est inférieure à la Valeur Guide Environnementale (VGE) de 10 µg.l-1 dans l'eau douce établie par l'Ineris en 2011. La concentration maximale en formaldéhyde s'élève à 1 242 µg.L-1 et correspond à un prélèvement effectué dans un cours d'eau de la région Normandie (BRGM).
Notons que les mesures ne sont pas réparties de façon uniforme sur tout le territoire (cf. Figure 10). Une carte similaire est obtenue pour des valeurs datant de 2009 à 2019.

Figure 10. Répartition géographique des mesures de formaldéhyde issues de la base de données Naïades entre 2017 et 2019
Aucune mesure de formaldéhyde sur matrice solide n'a été effectuée entre 2017 et 2019.
Terrestre
FTE 2020 Importer
La base de données ADES répertorie 4 375 mesures de formaldéhyde dans les eaux souterraines en France entre 2017 et 2019. Parmi ces mesures, 146 (soit 3 % de la totalité des mesures) présentent une concentration supérieure à la limite de quantification comprise entre 1 et 50 µg.l-1, une médiane de 7,2 µg.l-1 et une concentration maximale de 493 µg.l-1, cette dernière correspond à un prélèvement effectué en Picardie (BRGM).
En 2011, le BRGM a mené une campagne exceptionnelle (CAMPEX) d'analyses des substances présentes dans les eaux souterraines en métropole. Le formaldéhyde a fait l'objet de 943 mesures dont 9 présentent une concentration de formaldéhyde supérieure à la limite de quantification de 5 µg.l-1, la concentration maximale s'élève à 34 µg.L-1 et correspond à un prélèvement issu d'un forage effectué en Picardie (EAUFRANCE 2013).
Perspectives de réduction
Réduction des rejets
Réduction des émissions de formaldéhyde
FTE 2020 Importer
Substitution par des résines à base de formaldéhyde moins émettrices
Pour limiter les émissions de formaldéhyde, une des solutions est de réaliser une substitution par des résines à base de formaldéhyde moins émettrices. Par exemple il est possible en fonction des usages de substituer les résines UF, résines les plus émettrices et les plus utilisées, par d'autres résines à base de formaldéhyde (PF, MF, MUF, RF et PRF). Parmi ces résines les moins émettrices sont les résines phénoplaste (RF et PRF) dont les liaisons C-C sont plus solides et s'hydrolysent moins facilement que celles des résines aminoplastes (Nwaogu , et al., 2013).
Les capteurs de formaldéhyde
Les capteurs de formaldéhyde dans les résines aminoplastes représentent une solution de réduction d'émission déjà utilisée aujourd'hui au niveau industriel, mais qui d'après l'UIPP ne semble pas permettre une disponibilité des panneaux en quantités suffisamment importantes pour couvrir le marché. Le capteur réagit avec le formaldéhyde libre lors de la réticulation de la résine, et peut également réagir avec le formaldéhyde émis ultérieurement (AFFSET 2009). Selon une autre source (Francis G, 2011), il existerait plus de 150 substances différentes pour jouer le rôle de capteur, comme par exemple : l'urée, la mélanine, le Kaurit®
L'UIPP ajoute qu'on n'a que de peu de recul quant aux émissions à long terme de ces panneaux, car une fois que la totalité du capteur a été "consommée", le formaldéhyde est à nouveau susceptible d'être émis. Pour cette raison, ce type de solution ne nous semble pas prioritaire en termes de substitution.
Alternatives aux usages
Introduction
FTE 2020 Importer
« En France, l'arrêté du 13 juillet 2006 a ajouté « les travaux exposant au formaldéhyde » à la liste des substances, mélanges et procédés cancérogènes au sens de l'article R. 4412-60 du code du travail. La recherche de substitution des agents cancérogènes, mutagènes ou toxiques pour la reproduction (CMR) de catégorie 1A ou 1B est une obligation qui s'impose à l'employeur. Elle est énoncée dans les principes généraux de prévention à l'article L. 4121-2 du code du travail et est renforcée à l'article R. 4412-66. (Anses, 2019) » Ainsi pour certains articles comme les vernis ont déjà été développés des produits sans formaldéhyde, pour protéger les travailleurs et les consommateurs. Néanmoins le formaldéhyde est toujours utilisé dans de nombreux secteurs (cf partie 2 sur les usages du formaldéhyde) et le développement de solutions de substitution est toujours une question d'actualité, dont nous présentons ci-après l'état d'avancement.
Substitution de l'utilisation des résines à base de formaldéhyde
FTE 2020 Importer
Production de produits à base de bois (panneaux de bois contreplaqués et agglomérés)
Des études sur la substitution de l'utilisation des résines UF et MUF dans les panneaux de bois, ont été réalisées dans le cadre de la proposition de restriction REACH (annexe XV) (ECHA, 2019) (Anses, 2016). Les substituts sont présentés dans le tableau ci-après :
Tableau 13 : Substituts aux résines aminoplastes et phénoliques dans le secteur du bois (source Anses (Anses, 2016), (ECHA, 2019) et (Nwaogu , et al., 2013)

Production de revêtements de type peintures et vernis
Lors de l'étude réalisée par l'Ineris en 2013 sur la substitution du formaldéhyde, il avait été conclu à la suite d'une enquête auprès d'industriels que ; les résines à base de formol disposaient de substituts pour l'ensemble des applications, au moins pour les applications grand public et que l'utilisation de résines aminoplastes dans les peintures domestiques était très marginale (Ineris, 2013).
Le rapport de l'Anses de 2016 présente comme substituts aux peintures à base de résines aminoplastes
:
- époxy ; faible résistance à la lumière, utilisation en couche primaire.
- alkyde (peintures glycerophtalique) ; peintures durables pouvant être biosourcées
- acrylique ; moins durable sur le bois, plus cher que les peinture aminoplaste
- polyester ; moins cher que les peintures aminoplastes
Les peintures alkydes, peuvent être considérées comme des alternatives aux résines basées sur le formaldéhyde. Toutefois, leur synthèse implique des polyols (de type pentaérytritol) qui comportent du formaldéhyde à l'état de trace, présent en tant que résidu de synthèse (Ineris, 2013).
Selon l'enquête réalisée par l'Ineris en 2013 auprès de producteurs français de peintures et vernis, les résines urée-formol ne seraient presque plus utilisées en France pour la fabrication de produits vitrificateurs pour parquets (Ineris, 2013). En effet, l'arrêté du 13 juillet 2006 29 impose aux employeurs d'utiliser une alternative aux produits entraînant l'exposition des employés utilisant ces produits au formaldéhyde. Ils ont été principalement remplacés par d'autres produits en phase solvantée (résine alkyde ou glycérophtalique, résine polyuréthane mono ou bi composants, résines photoréticulables), ou en phase aqueuse (acrylique, polyuréthane en émulsion). Selon les résultats de l'enquête cette substitution a peu d'impact économique car la majeure partie du prix de la vitrification d'un parquet provient du coût de la main d'œuvre (plusieurs phases de ponçage), c'est pourquoi l'augmentation du prix du produit vitrificateur joue un rôle mineur dans le devis global de la vitrification d'un parquet. Enfin les vernis à base de polyuréthane présentent des performances supérieures à ceux à base de résine aminoplaste. Par contre, ils peuvent contenir des isocyanates qui sont nocifs par inhalation, ainsi que des solvants. Les produits mono composant en émulsion permettent de s'affranchir de ces inconvénients, car l'isocyanate a déjà réagi avec la résine et les émissions en sont fortement diminuées. Les résines polyuréthanes étaient en 2010 les produits les plus utilisés en France. On trouve également de nombreux produits hybrides en phase aqueuse ou solvantée produits à partir d'un mélange de plusieurs résines.
[29] L'arrêté du 13 juillet 2006 classe les travaux professionnels exposant au formaldéhyde dans la catégorie des procédés cancérogènes de catégorie 1 soumis aux prescriptions du décret «CMR» daté de février 2001. Cet arrêté est entré en vigueur en France depuis le 1er janvier 2007, rendant ainsi obligatoire par l'employeur le remplacement du formaldéhyde dans la mesure où cela est techniquement possible, par une substance, une préparation ou un procédé qui n'est pas ou moins dangereux pour la santé des travailleurs
Industrie du papier
L'Anses indique que les résines PAE (Polyamideamine epichlorohydrine) pourraient substituer l'utilisation des résines UF pour la production de certains papiers spéciaux. Cependant aucun substitut n'est identifié pour les résines MF et les résines phénoliques (Anses, 2016)..
Industrie du textile
Dans le rapport de l'Anses de 2016, le chitosan et l'urée dimethyle glyoxale sont présentés comme des substituts à la résine UF mais sans information concernant leurs efficacités, faisabilités et coûts (Anses, 2016).
D'après les rapports de l'AFSSET (AFFSET, 2009) et l'Ineris (Ineris, 2007) il semblait en 2009 que les principales alternatives aux résines à base de formaldéhyde étaient dans ce secteur :
- Technologie basée sur la mémoire de forme (les résines ayant un effet « repassage permanent » et résistance sur les textiles
- Les acides polycarboxyliques (PCAs) - en particulier, l'acide butane-1,2,3,4-tétracarboxylique
- (BTCA) -Différents types de silicones
Selon l'Union des Industries Textiles qui avait été interrogée dans le cadre de ces études, ces alternatives posaient encore des problèmes de coût et de faisabilité technique.
Industrie du plastique
Plusieurs matériaux plastiques pourraient substituer certains usages des plastiques thermodurcissables produits à partir de résines formiques. L'Anses mentionne différents thermoplastiques comme l'ABS (Acrylonitrile Butadiène Styrène) et le polypropylène, des polyesters thermodurcissables, des résines en époxy et l'utilisation de silicone. Peu d'information est disponible concernant la faisabilité économique et technique de ces substituts sauf pour le polyester qui pour ces deux critères semble présenter les propriétés adéquates (Anses, 2016).
Production de matériaux de construction
La consultation du site Internet www.batiproduits.com 30 avec les mots clefs « colle bois » montre la disponibilité de colles sans formaldéhyde (colles à base de polyuréthane généralement) pour les parquets et d'autres besoins de bricolage. La substitution des résines phénoplastes et aminoplastes dans les colles semble possible techniquement et économiquement.
L'entreprise « URSA » commercialise des laines de roche garanties sans formaldéhyde, tout comme l'entreprise « ROCKWOOL » qui commercialise un produit garanti sans formaldéhyde (« AFB evo »). Néanmoins aucune information n'est donnée sur le liant substituant le formaldéhyde. La comparaison des prix entre un produit standard de la marque « ROCKWOOL » contenant du formaldéhyde et un produit de la marque « URSA » sur le site « l'entrepôt du bricolage » ne montre pas de différence de prix importante (rockwool) (ursa). Il semblerait au regard des sites de ces deux marques que la production de laine de roche sans formaldéhyde soit possible. Néanmoins une simple consultation des sites de ces entreprises ne permet pas de conclure quant à l'efficacité de ces produits.
[30] Consultation le 17/09/2020
Fonderie
L'Anses de 2016 présente comme substituts aux résines formiques des silicates, des isocyanates et l'acrylique et le furane. Aucune information n'est indiquée concernant la faisabilité de ces substitutions (Anses, 2016).
Autres usages des résines à base de formaldéhyde
Nous n'avons pas trouvé de solution alternative à l'utilisation résines à base de formaldéhyde pour la production d'abrasif et de caoutchouc, ou pour le traitement de l'eau dans la littérature consultée dans le cadre de cette fiche.
Production de Polyols
FTE 2020 Importer
BDO
Très peu d'informations sont présentes dans la littérature concernant les substituts du BDO. Le rapport de l'Anses réalisés dans le cadre de la proposition de restriction REACH (annexe XV) (Anses, 2016) mentionne néanmoins l'oxyde de propylène, l'alcool allylique ainsi qu'un isomère du butane (n-butane) comme substitut au BDO. Il est à noter que l'oxyde de propylène est une substance cancérigène et mutagène, classée substance « SVHC » et soumise à autorisation par REACH.
Pentaérythritol
La littérature consultée présente un certain nombre de substituts du pentaérythriol variant en fonction des usages, parmi lesquels on trouve la glycérine, les polyépoxydes, l'uréthane et des huiles minérales... Cependant au vu de la littérature consultée il n'y a pas assez d'information disponible
permettant de conclure à un substitut disponible et compétitif avec le pentaérythriol pour la production de résines alkydes, d'explosifs, de lubrifiants et de colophane.
Substitution des résines polyoxyméthylènes (POM)
FTE 2020 Importer
Le tableau 14 extrait du rapport de l'Anses présente différents substituts aux thermoplastiques produits à partir de POM.
Tableau 14 : Substituts au POM (source Anses (Anses, 2016)

Des métaux peuvent également substituer les thermoplastiques produits à partir de POM utilisés dans le secteur automobile, industriel et dans certains articles de consommation. Les métaux identifiés par l'Anses sont : le cuivre, l'argent et le zinc moulé sous pression. La sélection de substituts variera en fonction des usages, et plus d'éléments devraient être réunis pour comparer l'impact sanitaire environnemental global de ces différents matériaux avec le POM avant une décision de substitution. Ces substituts métalliques sont les seuls substituts identifiés par l'Anses pour les articles de plomberie.
Production de MDI
FTE 2020 Importer
Le rapport de l'Anses de 2016 présente d'autres isocyanates et notamment le toluène diisocyanate (TDI) comme substituts au MDI pour son usage dans les mousses rigides et souples. Ces substances sont disponibles et apportent les propriétés recherchées aux mousses. De plus le TDI dispose d'un coût plus bas par rapport au MDI (Anses, 2016).
HTMA
FTE 2020 Importer
La littérature consultée ne permet pas de conclure à un substitut disponible et techniquement et économiquement compétitif à l'hexaméthylènetétramine (HTMA) pour ces utilisations dans le caoutchouc, comme conservateur et dans les résines époxy.
Fertilisants
FTE 2020 Importer
Concernant les fertilisants à libération prolongée, il existe notamment comme substituts chimiques les fertilisants à l'urée enrobée de soufre (mais qui sont plus chers), les fertilisants à l'urée-isobutylraldehyde, et à l'urée crotonylidène diurée (CDU). Aucune comparaison de prix n'a pu être effectuée dans cette fiche compte tenu des données disponibles. Il existe également des engrais organiques qui permettent une diffusion lente de l'azote comme par exemple la corne broyée. Cette dernière solution serait moins coûteuse que les solutions chimiques proposées ci avant mais son efficacité à court terme devrait être approfondie (Anses, 2016).
Autres usages
FTE 2020 Importer
Elevage
(Anses, 2019) a étudié la substitution du formaldéhyde dans différents secteurs dont l'élevage, où cette substance est utilisée pour le tannage des protéines dans des aliments pour ruminants.
Tableau 15 : Substituts au formaldéhyde identifiés pour le tannage des protéines utilisées en alimentation animale tiré de (Anses, 2019)

Les autres usages du formaldéhyde dans le secteur de l'élevage n'ont pas été étudiés dans ce rapport. Le rapport ne conclut pas précisément à une alternative, parmi les 3 principales identifiées (procédé cuisson extrusion, hydroxyde de sodium, et traitement thermique avec ajout de lignosulfates de calcium). En revanche il recommandé de cesser l'utilisation de formaldéhyde pour le tannage des protéines jugeant les alternatives présentées comme crédibles et disponibles pour substituer cet usage.
Agroalimentaire
(Anses, 2020) a recensé et a étudié les alternatives disponibles dans le secteur sucrier. Dans ce secteur le formaldéhyde est utilisé lors de la production de sucre (lors de l'opération de diffusion) puis lors du stockage. Pour le premier usage, 7 alternatives chimiques et 1 alternative faisant varier la température lors de l'extraction ont été identifiées comme disponibles et pouvant substituer le formaldéhyde. Les alternatives chimiques évoquées sont les suivantes ; acide peracétique en solution à 5%, acide peracétique en solution à 15%, betaStab® 10A, betastab® A, émulsion contenant 15% d'acides-β, betastab® A combiné à l'hydroxyde de sodium, solution de monochloramine. Ces alternatives sont présentées dans le tableau 15. Pour l'utilisation de formaldéhyde lors du stockage, aucun substitut n'a pu être étudié faute de donnée disponible mais (Anses, 2020) recommande tout de même de substituer le formaldéhyde par un autre bactériostatique lorsque l'utilisation d'un bactéricide est indispensable.
Tableau 15 : Comparaison des substituts au formaldéhyde identifiés pour le secteur sucrier tiré de (Anses, 2020)

Aucun document traitant précisément de substituts au formaldéhyde utilisé comme biocide dans le secteur agroalimentaire n'était disponible à notre connaissance lors de la rédaction de cette fiche. Néanmoins il semblerait que l'acide peracétique en solution à 2 ou 5% soit un bon substitut au formaldéhyde utilisé pour désinfecter les surfaces potentiellement en contact avec des produits alimentaires. Les points négatifs de cette alternative sont : son instabilité à la chaleur et sa dégradation en présence de matière organique (INRS, 2015).
[31] Evaluer par l'outil « GreenScreen »
Pisciculture
(Anses, 2019) a étudié et recensé les alternatives disponibles dans le secteur de la pisciculture. Pour réduire l'utilisation de formaldéhyde, utilisé pour le traitement de parasitose, le rapport recommande dans un premier temps de modifier les pratiques d'élevage en diminuant la densité des poissons dans les bassins et d'améliorer le contrôle de la qualité de l'eau en travaillant en « circuit recirculé ». Il recommande enfin, lorsqu'il y a infection des bassins, de traiter avec une des 5 substances alternatives identifiées ; le chlorure de sodium, le percarbonate de sodium, le produit INCIMAXX Aquatic®, le peroxyde d'hydrogène et le sulfate de cuivre pentahydraté. Seules les 3 dernières substances disposent d'une efficacité similaire au formaldéhyde pour lutter contre la parasitose.
Tableau 16 : Comparaison des substituts au formaldéhyde identifiés pour la pisciculture tiré de (Anses, 2019)

[32] Evaluer par l'outil « GreenScreen »
Médecine
Concernant la substitution des biocides à base de formaldéhyde utilisés pour la désinfection des locaux, de salles d'opération et d'instruments plusieurs substituts ont été identifiés mais il existe peu ou pas d'information concernant leur efficacité et leurs coûts. Les substances identifiées sont les suivantes : le peroxyde d'hydrogène, l'ortho-phthalaldehyde, l'acide peracétique, le dioxyde de chlore et l'ammonium quaternaire.
Pour substituer le formaldéhyde utilisé comme agent de conservation, deux substances ont été identifiées par l'Anses : le glutaraldéhyde, le bêta-propiolactone. L'utilisation de la chaleur ne permettrait pas substituer la conservation chimique.
Concernant l'usage comme fixateur des échantillons en anatomie et cytologie médicale, (Anses, 2019) a étudié les potentiels substituts au formaldéhyde en fonction des étapes de vie d'un échantillon. Finalement le rapport n'a pas conclu avec précision sur un substitut ou plusieurs substituts au formaldéhyde pour cet usage néanmoins il propose différentes solutions en fonction des spécificités de échantillons et des analyses. Pour la phase de préanalyse, si le temps d'ischémie33 ne dépasse pas 72h basées, des alternatives au formaldéhyde basées sur la conservation par le froid peuvent être envisagées. En ce qui concerne la phase analytique l' (Anses, 2019) il est conseillé de substituer le formaldéhyde par d'autres fixateurs (une liste de 46 fixateurs est proposée dans le rapport) en fonction de la technique analytique pour laquelle le formaldéhyde doit être substitué. Nous invitons le lecteur intéressé à se référer au rapport (Anses, 2019) pour plus d'informations et de précisions. Les éléments consultés dans le cadre de la réalisation de cette fiche, ne permettent pas de présenter des alternatives pour les autres usages médicaux du formaldéhyde.
[33] temps pendant lequel les organes ou les tissus à transplanter sont privés de sang et d'oxygène
Taxidermie
Le document réalisé par l'Anses en 2020 présente un certain nombre d'alternatives pouvant substituer l'utilisation du formaldéhyde utilisé dans les liquides d'embaumement utilisés en taxidermie et en thanatopraxie (Anses, 2016). Ces substituts n'étant pas spécifiques à la taxidermie mais aux liquides d'embaumement en général, nous invitons le lecteur intéressé à consulter ce document pour plus de renseignement.
Thanatopraxie
(Anses, 2020) a étudié les possibilités de substitution au formaldéhyde pour les actes de thanatopraxie. Ce travail a conclu que pour limiter l'utilisation du formaldéhyde comme conservateur lors des soins mortuaires, les alternatives ou pratiques disponibles sont de limiter les soins de conservation (non obligatoires dans certains cas) en éclairant les familles sur les situations où des soins doivent être réalisés, de développer les toilettes thermiques permettant de conserver les corps dans certains cas ou d'utiliser des substituts chimiques au formaldéhyde. Parmi les substituts identifiés, 4 sont étudiés en détail dans cette étude parmi la trentaine de mélanges et substances identifiées, il s'agit des mélanges : « Thanadès » (à base d'acide peracétique), « Tanato-Safebalm », « Art Cav Secure » et d'un mélange à base de polyvinylpyrrolidone iodé. Néanmoins seul le mélange « Art Cav Secure » est actuellement présent sur le marché, mais nécessite une formation des thanatopracteurs (Anses, 2020). Au vu de l'état de ces alternatives (Anses, 2020) recommande aux pouvoirs publics d'interdire le formaldéhyde en thanatopraxie.
Tableau 17 : Comparaison des substituts au formaldéhyde identifiés pour la taxidermie tiré de (Anses, 2020)

[34] Evaluer par l'outil « GreenScreen »
Coûts de la substitution
FTE 2020 Importer
Concernant le secteur du bois, un rapport de l'Ineris réalisé en 2013 (Ineris, 2013) a estimé le coût de substitution des résines formoliques utilisées pour la production de panneaux de bois. L'estimation s'appuie sur de fortes hypothèses considérant une substitution totale et immédiate du formaldéhyde par une résine synthétique type MDI à 70% et une résine biosourcée à 30%. Au total cette estimation prend en compte la substitution de 350 000 tonnes de résines UF, 71 500 tonnes de résines MUF et 21 500 tonnes de résines PF. Le montant de cette substitution a été estimé à 160 000 millions d'euros en 2013. Des estimations de coûts de substitution de l'usage du formaldéhyde pour d'autres secteurs d'activité n'ont pas été rencontrés dans la littérature consultée.
Le rapport de (ECHA, 2020) a considéré pour son avis sur la proposition de règlementation que le cout de production des panneaux de classe E1 était 10% supérieur aux panneaux de classe E2. Pour cela ce rapport s'est appuyé sur des données fournies par la « European Panel Federation » pour des panneaux répondant aux exigences E1. Les panneaux de classe E1 sont des panneaux contenant moins de résines à base de formaldéhyde, ce qui contraint les producteurs à un temps de « durcissement » de la résine plus long et donc une augmentation des couts de production.
Aucune estimation économique complète de la substitution du formaldéhyde pour un secteur donné, incluant les impacts économiques, sanitaires et environnementaux ne semble disponible dans la littérature. Néanmoins des informations sur le coût de certains substituts au formaldéhyde lorsque celles-ci étaient disponibles, ont été recensées dans les paragraphes précédents.
Conclusion
FTE 2020 Importer
Le règlement (UE) n°605/2014 de la Commission Européenne du 5 juin 2014 classe le formaldéhyde comme cancérogène de catégorie 1B et mutagène de catégorie 2. Une restriction dans le cadre du règlement chimique REACH est en cours d'instruction par l'UE, qui pourrait conduire à réduire les limites d'émissions de formaldéhyde par des matériaux, en particulier les matériaux en bois aggloméré ou stratifié.
On retrouve du formaldéhyde dans l'atmosphère, les eaux de surfaces et souterraines et dans l'air intérieur de bâtiments. Sa présence dans l'environnement peut provenir de plusieurs sources ; des sources naturelles d'émissions (combustion de matières organiques, oxydation dans l'air de composés organiques volatils, décomposition de résidus de végétaux ou de déchets d'animaux), des sources d'émissions non intentionnelles de formaldéhyde vers l'air issues de combustions d'origine anthropique, de la décomposition de résines à base de formaldéhyde, des sources d'émissions d'origine industrielle. Ces dernières seraient, en France sur la période 2008-2018, en baisse pour le milieu aquatique, et stables pour le milieu atmosphérique. Des émissions mineures ont aussi lieu du fait de certains usages intentionnels (agro-alimentaire, pisciculture, médical, thanatopraxie…).
Sur les 10 dernières années, la production mondiale et européenne de formaldéhyde est en augmentation et pourrait continuer à croitre au cours des prochaines années. En Europe, les principales capacités de production se trouvent en Allemagne.
Le formaldéhyde est une substance qui intervient dans la synthèse de nombreuses substances chimiques utilisées dans de très nombreux secteurs d'activités. En UE, la majeure partie de ces résines est utilisés pour la production de résines condensées, c'est-à-dire les résines phénoliques (PF), les résines aminoplastes (MF, UF, MUF) et les résorcinols. Ces résines sont en premier lieu utilisées dans le cadre de la production de panneaux de bois. Le formaldéhyde est également utilisé pour la production de polyols, de thermoplastiques et de mousses de polyuréthane. Cette substance est également utilisée dans la synthèse de nombreuses substances chimiques : sel tétrasodique d'EDTA, hexaméthylènetétramine, pyridine… Sous sa propre forme, c'est une substance qui est peu utilisée sauf pour divers usages biocides notamment dans les secteurs de l'élevage, de la pisciculture, de la thanatopraxie et de la médecine.
Pour limiter les émissions de formaldéhyde, une des solutions est de réaliser une substitution par des résines à base de formaldéhyde moins émettrices. Par exemple il est possible pour certains usages de substituer les résines UF, résines les plus émettrices et les plus utilisées, par d'autres résines à base de formaldéhyde (PF, MF, MUF, RF et PRF), ou d'opter pour des résines ou des matériaux alternatifs ne nécessitant pas le recours au formaldéhyde. Une autre solution pour réduire les émissions consiste à utiliser des capteurs de formaldéhyde.
Il est également possible de substituer l'utilisation directe du formaldéhyde par d'autres substances ou par des procédés techniques (utilisation de chambres froides en thanatopraxie, cuisson des aliments dans l'élevage par exemple).
Néanmoins la substituabilité du formaldéhyde varie en fonction des utilisations. Ainsi par exemple elle semble avancée pour les peintures et les vernis contrairement à d'autres secteurs comme celui de la thanatopraxie. Divers facteurs conditionnent pour chaque usage la possibilité de substitution d'une substance par exemple : l'efficacité, la disponibilité, la faisabilité de l'utilisation (intégration dans le procédé technique, capacité des travailleurs à utiliser le substitut), la toxicité, l'écotoxicité, le coût du substitut. C'est pourquoi la substitution doit être réfléchie et mise en place au cas par cas, notamment s'il s'agit de remplacer un matériau par un autre.
Bibliographie
Archives
Dernière vérification le 29/03/2024
Documents
Exporter la substance
Choisissez le format de l'export :











