Configuration de votre affichage
Vous avez activé le mode de configuration de l'affichage qui permet de sélectionner les informations que vous souhaitez afficher sur la fiche substance. Une fois que vous aurez sélectionné les rubriques à afficher, vous pouvez revenir au mode de consultation de la fiche substance en cliquant à nouveau sur le bouton de filtrage.
Acetochlore (34256-82-1)
Informations générales
Dernière vérification le 18/12/2025
Identification
Numero CAS
34256-82-1
Nom scientifique (FR)
Acétochlore
Nom scientifique (EN)
Autres dénominations scientifiques (Autre langues)
Code EC
251-899-3
Code SANDRE
1903
Numéro CIPAC
-
Formule chimique brute
\(\ce{ C14H20NO2Cl }\)
Code InChlKey
Code SMILES
Cc1cccc(CC)c1N(C(=O)CCl)COCC
Familles
Familles d'usages
Classification CLP
Type de classification
Harmonisée
ATP insertion
CLP00/ATP09
Description de la classification
Classification harmonisée selon réglement 1272/2008 ou CLP
| Mention du danger - Code | H315 |
|---|---|
| Mention du danger - Texte | Provoque une irritation cutanée |
| Classe(s) de dangers | Corrosion / Irritation cutanée |
| Libellé UE du danger | - |
| Mention du danger - Code | H317 |
|---|---|
| Mention du danger - Texte | Peut provoquer une allergie cutanée |
| Classe(s) de dangers | Sensibilisation respiratoire/cutanée |
| Libellé UE du danger | - |
| Mention du danger - Code | H332 |
|---|---|
| Mention du danger - Texte | Nocif par inhalation |
| Classe(s) de dangers | Toxicité aiguë |
| Libellé UE du danger | - |
| Mention du danger - Code | H335 |
|---|---|
| Mention du danger - Texte | Peut irriter les voies respiratoires |
| Classe(s) de dangers | Toxicité spécifique pour certains organes cibles (exposition unique) |
| Libellé UE du danger | - |
| Limites de concentration spécifique | - |
| Facteur M |
M=1000 M=100 |
| Estimation de toxicité aigüe | - |
| Mention du danger - Code | H351 |
|---|---|
| Mention du danger - Texte | Susceptible de provoquer le cancer (indiquer la voie d'exposition s'il est formellement prouvé qu'aucune autre voie d'exposition ne conduit au même danger) |
| Classe(s) de dangers | Cancerogénicité |
| Libellé UE du danger | - |
| Mention du danger - Code | H361f |
|---|---|
| Mention du danger - Texte | Susceptible de nuire à la Fertilité. |
| Classe(s) de dangers | Toxicité pour la reproduction |
| Libellé UE du danger | - |
| Mention du danger - Code | H373 |
|---|---|
| Mention du danger - Texte | Risque présumé d'effets graves pour les organes (indiquer tous les organes affectés, s'ils sont connus) à la suite d'expositions répétées ou d'une exposition prolongée (indiquer la voie d'exposition s'il est formellement prouvé qu'aucune autre voie d'exposition ne conduit au même danger) |
| Classe(s) de dangers | Toxicité spécifique pour certains organes cibles (exposition répétée) |
| Libellé UE du danger | - |
| Limites de concentration spécifique | - |
| Facteur M |
M=1000 M=100 |
| Estimation de toxicité aigüe | - |
| Mention du danger - Code | H400 |
|---|---|
| Mention du danger - Texte | Très toxique pour les organismes aquatiques |
| Classe(s) de dangers | Danger pour le milieu aquatique |
| Libellé UE du danger | - |
| Mention du danger - Code | H410 |
|---|---|
| Mention du danger - Texte | Très toxique pour les organismes aquatiques, entraîne des effets à long terme |
| Classe(s) de dangers | Danger pour le milieu aquatique |
| Libellé UE du danger | - |
| Limites de concentration spécifique | - |
| Facteur M |
M=1000 M=100 |
| Estimation de toxicité aigüe | - |
Physico-Chimie
Dernière vérification le 29/03/2024
Généralités
Poids moléculaire
269.77 g/mol
Tableau des paramètres
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Bibliographie
Comportement et devenir dans les milieux
Dernière vérification le 29/03/2024
Matrices
Milieu eau douce
VGE/NQE Importer
Volatilisation :
-3 -1
Avec une constante de Henry de 2,1.10 Pa.m3.mol
(EFSA, 2011), l'acétochlore est peu susceptible de se volatiliser à partir de la colonne d'eau.
Milieu sédiment eau douce
VGE/NQE Importer
Adsorption :
Avec un Koc compris entre 28 et 377 (EFSA, 2011), l'acétochlore n'est pas susceptible de s'adsorber de façon significative sur les particules solides et les sédiments.
Milieu terrestre
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Persistance
Biodégradabilité
VGE/NQE Importer
Biodégradabilité :
L'acétochlore est considéré comme une substance non facilement biodégradable. En système eau-sédiments :
- Valeur mesurée : DT50 = 17-22 j (DT90 = 56-75 j) mesurée lors d'une étude eau-sédiments en laboratoire à 20°C.
- Valeur calculée :
- DT50 • eau = 26-55 j (moyenne géométrique = 40,5 j)
- DT50 • sédiments = 9,6-7,5 j (moyenne géométrique = 8,6 j).
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Dégradabilité abiotique
VGE/NQE Importer
Hydrolyse :
Dans des conditions stériles de laboratoire, les essais d'hydrolyse à des pH allant de 5 à 9 montrent que l'acétochlore est une substance stable à des températures environnementales pertinentes. (EFSA, 2011)
Photolyse :
Dans des conditions stériles de laboratoire, les essais de photolyse en milieu aqueux montrent que l'acétochlore se dégrade peu. Ainsi, la photolyse directe ne peut être considérée comme une voie majeure de dégradation dans les systèmes aquatiques naturels. (EFSA, 2011)
Bioaccumulation
Organismes aquatiques
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Conclusion sur la bioaccumulation
VGE/NQE Importer
Bioaccumulation :
Une étude du potentiel de bioconcentration du poisson a permis de mesurer un BCF de 20, démontrant ainsi un faible risque de bioconcentration dans le poisson. (EFSA, 2011)
Bibliographie
Toxicologie
Dernière vérification le 29/03/2024
Toxicité à doses répétées
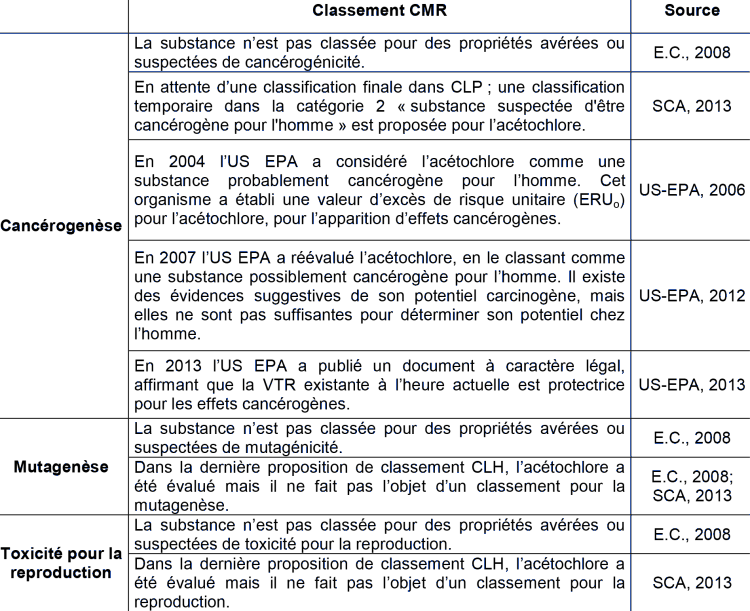
Effets cancérigènes
Classifications
| Organisme | Classification | Année |
|---|---|---|
| UE | FDTE/VTR Importer La substance est classée dans la catégorie 2 « substance suspectée d'être cancérogène pour l'homme » (H351). | 2016 |
| US EPA | FDTE/VTR Importer La substance est classée comme présentant des « Preuves suggestives d’un potentiel cancérogène » | 2014 |
Effets génotoxiques
Classifications
| Organisme | Classification | Année |
|---|---|---|
| UE | FDTE/VTR Importer La substance n’est pas classée pour des propriétés avérées ou suspectées de mutagénicité. | 2016 |
Effets sur la reproduction
Classifications
| Organisme | Classification | Année |
|---|---|---|
| UE | FDTE/VTR Importer La substance est classée dans la catégorie 2 des substances suspectées de toxicité pour la reproduction (H361f, susceptible de nuire à la fertilité). |
2016 |
Valeurs de référence
Introduction
VGE/NQE Importer
SANTE HUMAINE
Ce chapitre traite de la toxicité chronique induite par la substance sur l'homme soit via la consommation d'organismes aquatiques contaminés, soit via l'eau de boisson.
Pour l'évaluation des effets sur la santé humaine, seuls les résultats sur mammifères sont considérés comme pertinents. Contrairement à l'évaluation des effets pour les prédateurs, les effets de type cancérigène ou mutagène sont également pris en compte.
Dans les tableaux ci-dessous, ne sont reportés pour chaque type de test que les résultats permettant d'obtenir les NOEC ou la valeur toxicologique de référence (VTR) les plus protectrices. Compte tenu du mode d'exposition envisagée, seuls les tests sur mammifères exposés par voie orale (dans l'alimentation ou par gavage) ont été recherchés.
Toutes les données présentées ont été validées.
Les résultats de toxicité sont principalement donnés sous forme de doses journalières : NOAEL (No Observed Adverse Effect Level), ou LOAEL (Lowest Observed Adverse Effect Level). NOAEL et LOAEL sont exprimées en termes de quantité de substance administrée par unité de masse corporelle de l'animal testé, et par jour.
TOXICITE
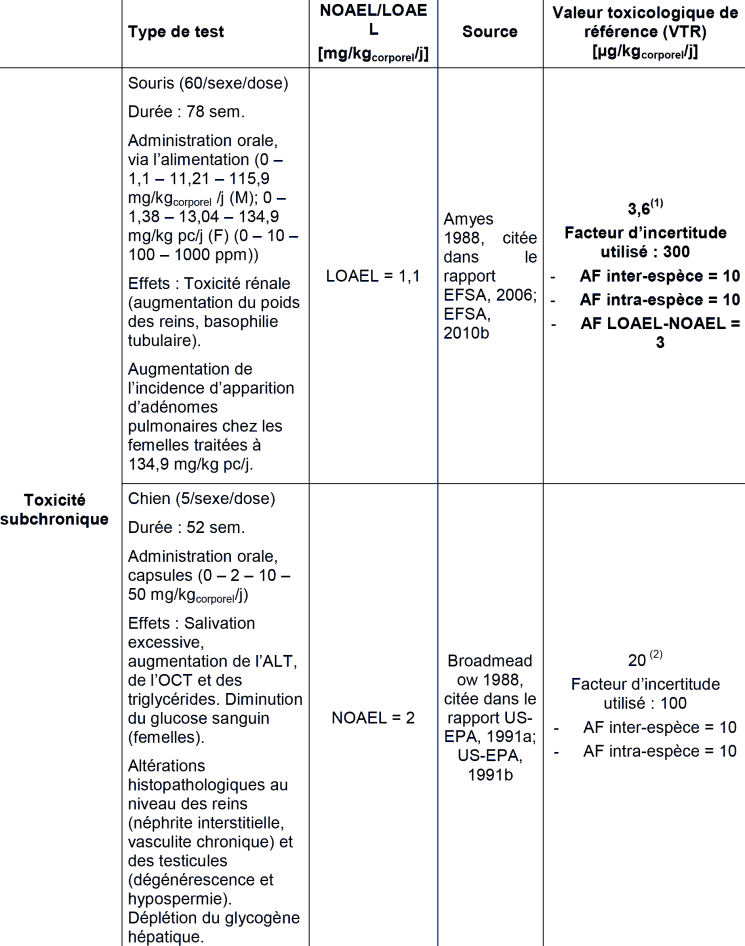
(1) Cette VTR a été déterminée par l'EFSA, et retenue par l'INERIS.
(2) Cette VTR a été déterminée par l'US EPA.
Choix de la VTR
Deux VTR pour l'acétochlore sont disponibles, fondées sur deux études différentes : l'EFSA retient une étude chez la souris (Amyes 1988, citée dans le rapport EFSA, 2006; EFSA, 2010b) alors que l'US EPA retient une étude chez le chien (Broadmeadow 1988, citée dans le rapport US-EPA, 1991a; US-EPA, 1991b). Ces deux études ont été évaluées et jugées de qualité acceptable.
L'US EPA retient comme effets critiques les modifications des paramètres biochimiques, l'excès de salivation chez les femelles et les altérations au niveau des reins et des testicules. Ces effets ont été observés à 10 mg/kg pc/j d'acétochlore (LOAEL). La NOAEL pour ces effets est de 2 mg/kg pc/j.
L'EFSA retient comme effet critique la survenue d'effets rénaux chez la souris mâle. En effet, l'acétochlore administré à des faibles doses (1,1 mg/kgcorporel/j) provoque des effets au niveau du rein, notamment une augmentation du poids absolu de cet organe et une augmentation statistiquement significative de l'incidence de basophilie tubulaire. Cette lésion, observée uniquement chez les mâles, présentait une incidence d'apparition plus élevée à 10 mg/kgcorporel/j qu'à 100 mg/kgcorporel/j. Toutefois, cette incidence était supérieure à celle observée chez les témoins historiques pour cette souche de souris, dans le même laboratoire. La basophilie tubulaire a été donc considérée comme un signe de toxicité précoce, pour lequel aucun NOAEL n'a pas été déterminé, le LOAEL étant de 1,1 mg/kgcorporel/j.
L'acétochlore provoquant une toxicité hépatique et rénale chez d'autres espèces animales, le choix de l'effet critique rénal semble adapté. La méthode de construction de la VTR de l'EFSA est recevable.
En ce qui concerne le potentiel cancérogène de l'acétochlore, différents types de tumeurs ont été rapportés lors des études chez l'animal. Une augmentation statistiquement significative de l'incidence d'apparition des tumeurs bénignes pulmonaires et des sarcomes histiocytaires de l'utérus a été observée chez la souris. Chez le rat, il a été décrit une augmentation statistiquement significative des tumeurs nasales.
En s'appuyant sur l'apparition de ces effets, l'US EPA a déterminé un ERUo pour l'acétochlore. Dans une réévaluation postérieure, cet organisme a considéré les preuves relatives aux tumeurs chez la souris comme faibles. Par ailleurs, l'US EPA a déterminé que le mécanisme d'action de l'acétochlore n'est pas mutagénique, l'utilisation d'un ERUo pour cette substance n'est pas justifiée. Lors de la réévaluation du classement CLH de l'acétochlore, les résultats des différents test réalisés in vivo et in vitro ont permis de conclure qu'un classement pour la mutagenèse n'est pas nécessaire (SCA, 2013). Enfin, l'US EPA considère sa RfD comme protectrice pour des effets non cancérogènes et cancérogènes (US-EPA, 2009b; US-EPA, 2013).
L'INERIS retient la valeur 3,6 µg/kgcorporel/j de l'EFSA calculée à partir des premiers signes de toxicité observés au niveau des reins.
FDTE/VTR Importer Une Valeur Toxicologique de Référence (VTR) est un indice qui est établi à partir de la relation entre une dose externe d'exposition à une substance et la survenue d'un effet néfaste. Les valeurs toxicologiques de référence proviennent de différents organismes.
Pour accéder à une information actualisée, nous conseillons au lecteur de se reporter directement sur les sites internet des organismes qui les élaborent.
PRINCIPALES ÉTUDES
Cette section rapporte les études sur lesquelles s’appuient les Valeurs Toxicologiques de Référence (VTR).
Effets à seuil - Exposition aiguë par voie orale
Kilgour, (2001), citée dans les rapportsi EFSA, 2011 ; US EPA, 2015
Espèce étudiée : Rat Alpk :ApfSD (Wistar-derived)
Sexe et nombre d’animaux par lot : 10 animaux/sexe/lot.
Voie d’exposition : orale (pas d’information complémentaire).
Substance - forme chimique : Acétochlore, (pureté 94,7 %).
Temps et fréquence d’exposition : dose unique.
Doses d’exposition / formes chimiques : dose unique de 150 - 500 - 1 500 mg.(kg pc)-1 d’acétochlore administré dans l’huile de maïs.
Lot témoin : oui (0 mg.(kg pc)-1)
Protocole : les animaux mâles et femelles ont subi une série d’essais d’observation fonctionnelle et de tests de l’activité motrice avant le début de l’étude, puis aux jours 1 (pic d’effet), 8 et 15 après l’exposition. Les signes cliniques, le poids, la consommation d’eau et de nourriture ont été suivis à intervalles réguliers pendant toute la durée de l’étude. A la fin de l’étude, les animaux ont été euthanasiés et perfusés in situ pour un examen neuro-pathologique. Les résultats de l’étude ont fait l’objet d’une analyse statistique (analyse de variance).
Résultats / effets observés : le traitement administré à la plus forte dose de 1 500 mg.(kg pc)-1.j-1 a entraîné la mort d’un mâle, ainsi qu’une baisse significative du poids des femelles (1, 8 et 15 jours) et des mâles (8 jours), la consommation alimentaire étant également significativement réduite au cours de la première semaine ayant suivi le traitement aussi bien chez les mâles que chez les femelles. Plusieurs signes cliniques attribuables au traitement (hypothermie, salivation, piloérection, respiration bruyante, etc) ont été décrits uniquement dans les premiers jours qui ont suivi le traitement administré à la plus forte dose, ces effets n’étant plus visibles au bout de huit jours chez la plupart des animaux. Dans le groupe exposé à la dose intermédiaire, les signes cliniques se sont limités le jour d’administration à une piloérection et une coloration du museau.
Les effets rapportés au cours des tests d’observation fonctionnelle et d’activité motrice sont, d’après les auteurs, plus le fait d’une toxicité générale que spécifique de l’atteinte du système nerveux. Des différences statistiquement significatives de l’activité motrice ont été décrites à J1 uniquement chez les femelles exposées aux deux plus fortes doses (augmentation à 500 mg.(kg pc)-1 et diminution à 1 500 mg.(kg pc)-1), et limitées à J8 au groupe exposé à la plus forte dose.
Dose critique : Sur la base des effets cliniques et de la modification de l’activité motrice observés dans le groupe exposé à 500 mg.(kg pc)-1, un NOAEL de 150 mg.(kg pc)-1 a été établi à partir de cette étude (EFSA , 2011). A noter que l’US EPA a retenu pour cette même étude un NOAEL de 500 mg.(kg pc)-1 (toxicité systémique), sans tenir compte des effets cliniques considérés comme mineurs et de l’augmentation de l’activité motrice dans les groupes exposés à 500 mg.(kg pc)-1. En absence d’effet direct ou spécifique sur le système nerveux, un NOAEL de 1 500 mg.(kg pc)-1 pour la neurotoxicité a été retenu.
Qualité de l’étude : La validité des données est considérée de qualité recevable, cotation 2, selon les critères de Klimisch et al., 1997. Il s’agit d’une étude qui n’a pas été réalisée sous BPL, mais qui répond aux principaux critères de la ligne directrice de l’OCDE 401 avec des limites concernant notamment les informations relatives aux conditions d’exposition.
Brooker, Stubbs et John, (1989, citée dans le rapport US EPA, 2015)
Espèce étudiée : Lapin New Zealand.
Sexe et nombre d’animaux par lot : 16 femelles gestantes/lot.
Voie d’exposition : orale via gavage.
Substance - forme chimique : Acétochlore, (pureté 90,5 %).
Temps et fréquence d’exposition : du 6ème au 18ème jour de gestation.
Doses d’exposition / formes chimiques : 0 – 30 – 100 - 300 mg.(kg pc)-1.j-1 d’acétochlore administré dans l’huile de maïs.
Lot témoin : oui (0 mg.(kg pc)-1.j-1)
Protocole : les signes cliniques des mères, le poids, la consommation d’eau et de nourriture ont été suivis à intervalles réguliers pendant toute la durée de la gestation. Des césariennes ont été réalisées sur toutes les femelles au 29ème jour de gestation. Le contenu de l’utérus a été examiné pour déterminer le nombre d’implants, de fœtus vivants et morts. Les fœtus ont été pesés, leur sexe déterminé et d’éventuelles anomalies morphologiques et viscérales ont été recherchées. Les résultats de l’étude ont fait l’objet d’une analyse statistique.
Résultats / effets observés : le traitement administré à la plus forte dose de 300 mg.(kg pc)-1.j-1 a entraîné de fortes difficultés de déplacement chez une femelle (pattes postérieures) nécessitant son euthanasie au 11ème jour de gestation, ainsi que la mort spontanée prématurée d’une seconde femelles au 19ème jour de gestation consécutif à un avortement spontané. Dans ce même groupe, les auteurs ont observé une baisse significative de la croissance pondérale des mères entre les 6 et 8èmes jours de gestation (baisse de -30, -21, -20 et -83 g, dans les groupes exposés respectivement à 0 – 30 - 100 et 300 mg.(kg pc)-1.j-1 d’acétochlore), de même que du 6 au 7ème jour une baisse significative de leur consommation alimentaire (moyenne de 125, 126, 120 et 86 g par lapine et par jour dans les groupes exposés respectivement à 0 – 30 - 100 et 300 mg.(kg pc)-1.j-1 d’acétochlore). Après ajustement du poids des femelles corrigé du poids de l’utérus gravide, aucune différence entre la croissance pondérale des femelles traitées ou non n’a été observée. L’examen post-mortem des femelles n’a mis en évidence aucun effet lié au traitement.
Le traitement n’a pas eu d’incidence sur la taille ou le poids des portées, le sex ratio, les pertes pré- ou post-implantatoires et le poids des fœtus, ni sur la présence de malformations ou d’anomalies des viscères et du squelette.
Dose critique : En s’appuyant sur la mortalité de deux femelles, ainsi que sur la baisse de croissance pondérale et consommation alimentaire dans le groupe exposé à 300 (kg pc)-1.j-1, un NOAEL de 100 mg.(kg pc)-1.j-1 pour la toxicité maternelle a été établi. En absence d’effet sur le développement, le NOAEL est de 300 mg.(kg pc)-1.j-1.
Qualité de l’étude : Les données sont considérées de qualité recevable, et validées avec une cotation 2, selon les critères de Klimisch et al., 1997. Il s’agit d’une étude qui n’a pas été réalisée sous BPL, mais qui répond aux principaux critères de la ligne directrice de l’OCDE 414 avec des limites concernant notamment la durée de l’exposition qui ne couvre pas la totalité du développement.
Effets à seuil - Exposition chronique par voie orale :
Amyes (1989, citée dans le rapport EFSA, (2006, 2010)
Espèce étudiée : Souris CD-1
Sexe et nombre d’animaux par lot : 60 animaux/sexe/lot
Voie d’exposition : voie orale via l’alimentation
Substance - forme chimique : Acétochlore, SC-5676, (pureté 90,8 %)
Temps et fréquence d’exposition : 78 semaines, quotidienne.
Doses d’exposition / formes chimiques : Doses de 10 - 100 - 1000 ppm ce qui correspond chez les mâles (M) à 1,1 – 11,21 – 115,9 mg.(kg pc)-1.j-1 et chez les femelles (F) à 1,38 – 13,04 - 134,9 mg.(kg pc)-1.j-1.
Lot témoin : oui (0 mg.(kg pc)-1.j-1)
Protocole : Cette étude a été conduite sous BPL et selon la ligne directrice de l’OCDE 453: « Etude combinée de toxicité chronique et de cancérogenèse ». Les animaux ont fait l’objet d’un examen clinique quotidien. Le poids et la consommation de nourriture ont été mesurés à intervalles réguliers. Des examens hématologiques ont également été réalisés régulièrement à partir de prélèvements sanguins. Un lot intermédiaire de 10 animaux a été sacrifié et autopsié après 52 semaines de traitement, les autres animaux ont été sacrifiés à la fin des 78 semaines de l’étude. A l’autopsie, les animaux ont été pesés, de même que les différents organes qui ont fait l’objet d’un examen anatomo-pathologique, tant macroscopique que microscopique. A noter dans cette étude, l’absence d’examen biochimique au niveau sanguin ou d’analyse d’urine.
Résultats / effets observés : A la fin de l’étude, une augmentation dose-dépendante et statistiquement significative du poids absolu et relatif des reins a été observée chez les mâles traités aux doses de 100 et 1000 ppm d’acétochlore (11,21 et 115,9 mg.(kg pc)-1.j-1).
Chez les mâles exposés à 1000 ppm (115,9 mg.(kg pc)-1.j-1) il a été observé une augmentation statistiquement significative de l’incidence des lésions compatibles avec une néphropathie chronique, notamment une basophilie tubulaire (observée également à 10 et 100 ppm, équivalents à 1,1 et 11,21 mg.(kg pc)-1./j-1 respectivement), une fibrose interstitielle, une minéralisation corticale et la présence d’agrégats hyalins.
Chez les femelles exposées à 1000 ppm d’acétochlore (134,9 mg.(kg pc)-1.j-1), la seule altération rénale décrite est la dilation des tubes corticaux, lésion augmentée de façon statistiquement significative par rapport au lot témoin. A cette dose, une augmentation statistiquement significative de l’incidence de vacuoles de la région polaire antérieure du cristallin a été observée chez les femelles.
Au niveau des poumons, l’incidence d’apparition d’une hyperplasie broncholaire a été statistiquement augmentée chez les mâles des lots 100 et 1000 ppm (11,21 et 115,9 mg.(kg pc)-1.j-1) et chez les femelles du lot 10 ppm (1,38 mg.(kg pc)-1.j-1). Cependant, pour cet effet, aucune relation dose-réponse n’a pu être établie.
A la fin de l’étude, des altérations de certains paramètres hématologiques, indicatifs d’une anémie, ont été décrits chez les mâles traités avec 100 et 1000 ppm (11,21 et 115,9 mg.(kg pc)-1.j-1). En effet, dans ces deux lots il a été observé une diminution statistiquement significative du nombre d’érythrocytes ainsi que de l’hématocrite.
Une augmentation de l’incidence d’adénomes pulmonaires a été mise en évidence chez les femelles à 1000 ppm (134,9 mg.(kg pc)-1.j-1).
Dose critique : En s’appuyant sur l’augmentation du poids des reins et la présence d’une basophilie rénale, le LOAEL pour des effets non cancérigènes est 10 ppm (1,1 mg.(kg pc)-1.j-1) chez les mâles. Dans cette étude, le NOAEL pour cet effet n’a pas pu être établi.
Concernant les effets cancérogènes, le LOAEL est 1 000 ppm (115,9 mg.(kg pc)-1.j-1) pour l’apparition d’adénomes pulmonaires et le NOAEL pour des effets cancérigènes correspondant au même effet, 100 ppm (11,21 mg.(kg pc)-1.j-1).
Qualité de l’étude : La validité des données est considérée acceptable, cotation 1, selon les critères de Klimisch et al., 1997.
Broadmeadow (1988), citée dans le rapport USEPA (1991b,a)
Espèce étudiée : Chien Beagle
Sexe et nombre d’animaux par lot : 5 animaux/sexe/lot.
Voie d’exposition : voie orale sous forme de capsule
Substance - forme chimique : Acétochlore, SC-5676 (pureté 91%)
Temps et fréquence d’exposition : 52 semaines; 1 capsule/jour
Doses d’exposition / formes chimiques : Mâles (M) et femelles (F) : 0 – 2 – 10 – 50 mg.(kg pc)-1.j-1
Lot témoin : oui, capsule vide (0 mg mg.(kg pc)-1.j-1 ).
Protocole : Les signes cliniques, le poids et la consommation de nourriture ont été mesurés à intervalles réguliers tout au long de l’étude. Des prélèvements sanguins ont régulièrement permis de réaliser des analyses hématologiques et biochimiques, des analyses d’urine ont également été pratiquées. Les animaux ont été sacrifiés et autopsiés à la fin des 52 semaines de traitement. Les différents organes (cerveau, foie, reins, rate, thyroïde, glandes surrénales et testicules) ont été pesés et ont fait l’objet d’une analyse histo-pathologique.
Résultats / effets observés : L’administration des capsules à l’acétochlore a entraîné une salivation excessive des mâles exposés à 50 mg.(kg pc)-1.j-1 et des femelles à partir des doses ≥ 10 mg.(kg pc)-1.j-1.
A la semaine 24, différents signes de toxicité rénale (tels qu’une augmentation statistiquement significative du volume urinaire ainsi que des niveaux d’urée et de créatinine sanguins) ont été observés chez les mâles et les femelles traités à 50 mg.(kg pc)-1.j-1.
Des signes de toxicité sévère au niveau du système nerveux, notamment des altérations des réflexes, de la posture et de la marche ainsi que de l’incoordination de mouvements, ont été observés chez 2/5 des mâles et chez 3/5 des femelles du lot exposé à 50 mg.(kg pc)-1.j-1.
Chez les mâles du lot exposé à 50 mg.(kg pc)-1.j-1, une diminution statistiquement significative du poids des testicules ainsi qu’une dégénérescence des tubes testiculaires chez 5/5 mâles ont été observées. A cette dose, au cours de la semaine 39 chez les mâles et lors des semaines 26 et 39 chez les femelles, il a été observé une diminution statistiquement significative du poids corporel.
Le traitement à l’acétochlore a provoqué des altérations hépatiques, mises en évidence par des augmentations statistiquement significatives de l’alanine aminotransférase (ALT) (à des doses de 50 mg.(kg pc)-1.j-1 chez les mâles et ≥ 10 mg .(kg pc)-1.j-1 chez les femelles), de la gamma glutamyl transférase (GGT) (à des doses de 50 mg.(kg pc)-1.j-1 chez les mâles), de l’ornithine transcarbamylase (OCT) (à des doses de 50 mg.(kg pc)-1.j-1 chez les mâles et ≥ 10 mg.(kg pc)-1.j-1 chez les femelles) et des triglycérides (à des doses de 50 mg.(kg pc)-1.j-1 chez les mâles). A la semaine 50, une diminution statistiquement significative du glucose sanguin a été mise en évidence à 10 mg.(kg pc)-1.j-1 chez les femelles.
A 50 mg.(kg pc)-1.j-1, une diminution du contenu en glycogène du foie a été observée chez 4/5 des mâles et chez 4/5 des femelles.
Une néphrite interstitielle chez 2/5 des mâles et une dégénérescence tubulaire des testicules chez 4/5 des mâles ont été observés dans le lot traités à 10 mg.(kg pc)-1.j-1 d’acétochlore.
Dose critique : un NOAEL de 2 mg.(kg pc)-1.j-1 et un LOAEL de 10 mg.(kg pc)-1.j-1 ont été déterminés pour les effets hématologiques et la salivation excessive chez les femelles, ainsi que les effets hépatiques et testiculaires chez les mâles.
Qualité de l’étude : La validité des données de cette étude est acceptable, cotation 1, selon les critères de Klimish (1997) pour l’évaluation des études de toxicologie. Il s’agit d’une étude qui n’a pas été réalisée sous BPL et qui ne suis aucune ligne directrice de l’OCDE. Cependant, cette étude satisfait les critères requis par d’autres guides et critères nationaux des Etats Unis, notamment le guide 83-1 pour les études de toxicité chronique chez non rongeurs par voie orale et les critères de 40 CFR 158.34 pour la neurotoxicité à 50 mg.(kg pc)-1.j-1 (HDT) (USEPA, 1991a).
Effest sans seuil:
L’IARC n’a procédé à aucun examen de l’acétochlore.
En 2014, l’ECHA a considéré l’acétochlore comme susceptible de provoquer le cancer chez l’animal (Carc. 2 – H351), en particulier sur la base de l’observation de tumeurs de l’épithélium olfactif chez le rat, de tumeurs pulmonaires bénignes chez la souris ainsi que des tumeurs histiocytaires de l’utérus chez la souris.
Les études mécanistiques sont en faveur d’un mode d’action non génotoxique pour l’induction tumorale. Certaines hypothèses ont été envisagée (déplétion du glutathion hépatique, génération d’espèces réactives de l’oxygène, etc.), mais font toujours l’objet de discussions (ECHA, 2014).
Dans l’état actuel des connaissances, les données disponibles concernant les effets cancérogènes de l’acétochlore ne sont pas suffisantes pour la construction de VTR sans seuil. Par ailleurs, dans sa dernière évaluation, l’US EPA a considéré que les preuves relatives aux tumeurs chez la souris étaient faibles et que le mécanisme d’action de l’acétochlore n’est pas mutagénique et donc que la construction d’une valeur pour les effets sans seuil pour des expositions par voie orale n’était pas justifiée pour cette substance. Ainsi, l’US-EPA considère que la VTR à seuil (RfD) est suffisamment protectrice pour couvrir les effets cancérogènes qui surviennent à des niveaux de doses plus élevés que les effets non cancérogènes (US-EPA, 2009b; US-EPA, 2013).
Sur la base d’effets testiculaires observés chez le chien, l’ECHA a proposé de classer l’acétochlore pour les effets sur la reproduction comme susceptible de nuire à la fertilité (Repr. 2 ; H361f) (ECHA, 2014).
Valeurs de l'ANSES et/ou de l'INERIS
Description
FDTE/VTR Importer Effets à seuil - Exposition chronique par voie orale :
L’EFSA (2011) propose une DJA de 3,6 µg.(kg pc)-1.j-1 pour une exposition chronique à l’acétochlore par voie orale.
Cette valeur est issue de l’étude combinée de toxicité chronique et de cancérogénèse de Amyes, 1989 (citée dans le rapport de l’EFSA 2006 et 2010) dans laquelle des souris (60 animaux par sexe et par lot) ont été exposées via l’alimentation à des doses de 0 – 10 – 100 et 1000 ppm d’acétochlore (soit à 0 - 1,1 - 11,21 - 115,9 mg.(kg pc)-1.j-1 pour les femelles (F) et 0 - 1,38 - 13,04 - 134,9 mg.(kg pc)-1.j-1 chez les mâles (M)) pendant 78 semaines.
Des lésions pulmonaires ont été observées aux deux plus fortes doses testées de 100 et 1 000 ppm chez les mâles (hyperplasie bronchiolaire) et à la plus forte de dose de 1 000 ppm chez les femelles (adénomes pulmonaires. Un LOAEL de 10 ppm a été établi à partir de l’augmentation du poids des reins et la présence d’une basophilie rénale à toutes les doses testées chez les mâles. Chez les femelles, une augmentation significative de la dilatation des tubes corticaux a été observée uniquement dans le lot exposé à 1 000 ppm. Une anémie est observée chez les souris mâles exposées à 100 et 1000 ppm.
Sur la base de la toxicité rénale observée chez les souris mâles (augmentation du poids des reins et la présence d’une basophilie rénale à toutes les doses testées), l’EFSA a retenu pour cette étude un LOAEL de 10 ppm, soit 1,1 mg.(kg pc) pc)-1.j-1.
Facteurs d’incertitude : Un facteur d’incertitude de 100 et un facteur supplémentaire de 3 ont été retenus. Le facteur 100 n’est pas détaillé mais semble avoir été utilisé pour tenir compte des variations inter- et intra-espèces. Un facteur supplémentaire 3 a été ajouté du fait de l’utilisation d’un LOAEL.
Calcul : 1,1 mg. (kg pc)-1.j-1 x 1 / 300 = 0,0036 mg.(kg pc)-1.j-1
Il est à noter que cette valeur prend en compte le potentiel cancérigène de l’acétochlore.
Indice de confiance : l’organisme ne propose pas d’indice de confiance
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Synthèse
FDTE/VTR Importer Effets à seuil - Exposition aiguë par voie orale :
En 2017, l’INERIS ne propose pas de choix de VTR.
En effet, l’analyse menée en 2013 n’avait pas porté sur les expositions aiguës. Les valeurs recueillies en 2017 se sont avérées sensiblement équivalentes dans ces conditions, il nous est apparu plus pertinent de mettre à disposition l’information le plus rapidement possible.
Effets à seuil - Exposition chronique par voie orale :
L’INERIS propose de retenir pour une exposition chronique à l’acétochlore par voie orale la VTR chronique de 3,6 μg.(kg pc)-1.j-1 de l’EFSA.
Deux VTR pour l’acétochlore sont disponibles, fondées sur deux études différentes : l’EFSA retient une étude chez la souris (Amyes 1989, citée dans le rapport EFSA, 2006; EFSA, 2010) alors que l’US EPA retient une étude chez le chien (Broadmeadow 1988, citée dans le rapport US-EPA, 1991a;US-EPA, 1991b). Ces deux études ont été évaluées et jugées de qualité acceptable.
L’EFSA retient comme effet critique la survenue d’effets rénaux chez la souris mâle. En effet, l’acétochlore administré à des faibles doses (1,1 mg.(kg pc)-1.j-1) provoque des effets au niveau du rein, notamment une augmentation du poids absolu de cet organe et une augmentation statistiquement significative de l’incidence de basophilie tubulaire. Cette lésion, observée uniquement chez les mâles, présentait une incidence d’apparition plus élevée à 10 mg.(kg pc)-1.j-1 qu’à 100 mg.(kg pc)-1.j-1. Toutefois, cette incidence était supérieure à celle observée chez les témoins historiques pour cette souche de souris, dans le même laboratoire. La basophilie tubulaire a donc été considérée comme un signe de toxicité précoce, pour lequel aucun NOAEL n’a été déterminé, le LOAEL étant de 1,1 mg.(kg pc)-1.j-1.
L’US EPA retient comme effets critiques les modifications des paramètres biochimiques, l’excès de salivation chez les femelles et les altérations au niveau des reins et des testicules. Ces effets ont été observés à 10 mg/kg pc/j d’acétochlore (LOAEL). La NOAEL pour ces effets est de 2 mg.(kg pc)-1.j-1.
L’acétochlore provoquant une toxicité hépatique et rénale chez plusieurs espèces animales, le choix de l’effet critique rénal semble adapté. L’apparition des effets aux doses les plus faibles est observée dans l’étude retenues par l’EFSA. La méthode de construction de la VTR de l’EFSA est recevable et sa VTR est retenue par l’INERIS.
Autres valeurs des organismes reconnus
Description
FDTE/VTR Importer Effets à seuil - Exposition aiguë par voie orale :
L’EFSA propose une RfD de 1,5 mg.(kg pc)-1 pour une exposition aiguë par voie orale à l’acétochlore (2011).
Cette valeur est établie à partir d’une étude de neurotoxicité aiguë chez le rat exposé à une dose unique de 0- 150 – 500 ou 1 500 mg.(kg pc)-1. (Kilgour, 2001). Un NOAEL de 150 mg.(kg pc)-1 a été retenu par l’EFSA à partir des signes cliniques (piloérection, coloration du museau) et modification de l’activité motrice décrits dans le groupe exposé à la dose intermédiaire de 500 mg.(kg pc)-1, les effets étant bien plus sévères à la dose supérieure de 1 500 mg.(kg pc)-1.
Facteurs d’incertitude : Un facteur d’incertitude de 100 a été retenu. Bien que cette valeur ne soit pas détaillée, elle semble avoir été utilisée pour tenir compte des variations inter- et intra-espèces.
Calcul : 150 mg.(kg pc)-1 x 1 / 100 = 1,5 mg.(kg pc)-1
Indice de confiance : l’organisme ne propose pas d’indice de confiance
L’US EPA propose une RfD de 1 mg.(kg pc)-1 pour une exposition aiguë par voie orale à l’acétochlore (2015).
Cette valeur est établie à partir d’une étude expérimentale chez la lapine gestante exposée par gavage du 6ème au 18ème jour de gestation à 0 – 10 – 100 – 300 mg.(kg pc)-1.j-1 (Brooker et al.,1989). Un NOAEL a été dérivé à partir des effets sur la toxicité maternelle (mortalité, baisse de croissance pondérale et diminution de la consommation alimentaire) observés à la plus forte doses testée de 300 mg.(kg pc)-1.j-1. La dose juste en dessous de 100 mg.(kg pc)-1.j-1 a été retenue comme étant le NOAEL pour le calcul de la VTR.
Facteurs d’incertitude : Un facteur d’incertitude de 100 a été retenu. Bien que cette valeur ne soit pas détaillée, elle semble avoir été utilisée pour tenir compte des variations inter- et intra-espèces.
Calcul : 100 mg.(kg pc)-1.j-1 x 1 / 100 = 1 mg.(kg pc)-1.j-1
Indice de confiance : l’organisme ne propose pas d’indice de confiance
Effets à seuil - Exposition chronique par voie orale :
L’US EPA (1991) propose un RfD de 20 µg.(kg pc)-1.j-1 pour une exposition chronique à l’acétochlore par voie orale.
Cette valeur repose sur une étude expérimentale de 52 semaines chez le chien Beagle (5/sexe/dose) exposé par voie orale à l’acétochlore (pureté 91%), sous forme de capsule, à des doses de 0 – 2 – 10 – 50 mg.(kg pc)-1.j-1 (Broadmeadow, 1988).
Un LOAEL de 10 mg.(kg pc)-1.j-1 a été établi dans cette étude à partir de l’observation de la modification des paramètres biochimiques (l’ornithine transcarbamylase) et à l’excès de salivation observés chez les femelles, ainsi qu’aux altérations rénales et testiculaires (dégénérescence tubulaire) chez les mâles.
Sur la base de ces effets, l’US EPA a retenu un NOAEL de 2 mg.(kg pc)-1.j-1.
Facteurs d’incertitude : Un facteur d’incertitude de 100 retenu pour tenir compte des variations inter- et intra-espèces
Calcul : 2 mg.(kg pc)-1.j-1 x 1 / 100 = 0,02 mg.(kg pc)-1.j-1
Indice de confiance : Le niveau de confiance de l’US EPA dans sa valeur est élevé.
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Bibliographie
Ecotoxicologie
Dernière vérification le 29/03/2024
Introduction
VGE/NQE Importer
Evaluations existantes :
Evalué dans le cadre de la Dir. 91/414/CEE.
- rapport d'évaluation proposé par l'Etat membre rapporteur (Espagne) publiquement disponible auprès de l'EFSA (EFSA, 2010a ; EFSA, 2011)
Effets endocriniens :
L'acétochlore est listé dans le rapport d'étude de la DG ENV établissant la mise à jour de la liste prioritaire des perturbateurs endocriniens à faible tonnage (Petersen et al., 2007), comme « substance pour laquelle des effets endocriniens sur organisme sain dans au moins une étude in vivo ont été mis en évidence » (catégorie 1) pour la santé humaine et comme « substance pour lesquelles il n'existe pas de preuve d'une activité de perturbation endocrine » (catégorie 3) pour la faune sauvage.
Critères PBT / POP :
La substance n'est pas citée dans les listes PBT/vPvB1 (C.E., 2006) ou POP2 (PNUE, 2001).
Normes de qualité existantes :
- Pas de norme référencée sur ETOX (ETOX, 20133)
- Directive 98/83/CE : norme de qualité pour les eaux destinées à la production d'eau potable : 0,1 µg.L-1
Substance(s) associée(s) :
Métabolites d'origine végétale :
- 2-éthyl-6-méthylaniline (EMA)
- 2-(1-hydroxyéthyl)-6-méthylaniline (HEMA) Métabolites d'origine animale :
- Acide tert-mercapturique Substances de dégradation de l'acétochlore dans les matrices environnementales :
- Acide t-oxanilique
- Acide t-sulfinylacétique
- Acétochlore t-norchloro
- Acide t-sulfonique
- Acide s-sulfonique
(EFSA, 2011)
[1] Les PBT sont des substances persistantes, bioaccumulables et toxiques et les vPvB sont des substances très persistantes et très bioaccumulables. Les critères utilisés pour la classification des PBT sont ceux fixés par l'Annexe XIII du règlement n° 1907/2006 (REACH).
[2] Les Polluants Organiques Persistants (POP) sont des substances persistantes (aux dégradations biotiques et abiotiques), fortement liposolubles (et donc fortement bioaccumulables), et volatiles (et peuvent donc être transportées sur de longues distances et être retrouvée de façon ubiquitaire dans l'environnement). Les critères utilisés pour la classification POP sont ceux fixés par l'Annexe 5 de la Convention de Stockholm placée sous l'égide du PNUE (Programme des Nations Unies pour l'Environnement).
[3] Les données issues de cette source (http://webetox.uba.de/webETOX/index.do) ne sont données qu'à titre indicatif ; elles n'ont donc pas fait l'objet d'une validation par l'INERIS.
Dangers
Description
VGE/NQE Importer
ORGANISMES AQUATIQUES
Dans les tableaux ci-dessous, sont reportés pour chaque taxon, essentiellement les résultats des tests d'écotoxicité pour les espèces montrant la plus forte sensibilité à la substance. Les données présentées sont issues du rapport européen d'évaluation des risques dans le cadre de la Directive 91/414/CE (EFSA, 2010a ; EFSA, 2011) ou de la base de données Pesticides Ecotox Database de l'US-EPA (US-EPA, 2005).
Ces résultats d'écotoxicité sont principalement exprimés sous forme de NOEC (No Observed Effect Concentration), concentration sans effet observé, d'EC10 concentration produisant 10% d'effets et équivalente à la NOEC, ou de EC50, concentration produisant 50% d'effets. Les NOEC sont principalement rattachées à des tests chroniques, qui mesurent l'apparition d'effets sub-létaux à long terme, alors que les EC50 sont plutôt utilisées pour caractériser les effets à court terme.
ECOTOXICITE
D'après les informations disponibles dans la littérature, les produits de dégradation de l'acétochlore potentiellement présents dans l'environnement sont tous moins toxiques pour les organismes aquatiques que le composé parent lui-même. Aussi, seules les données d'écotoxicité de l'acétochlore sont présentées ci-dessous.
ECOTOXICITE AQUATIQUE AIGUË
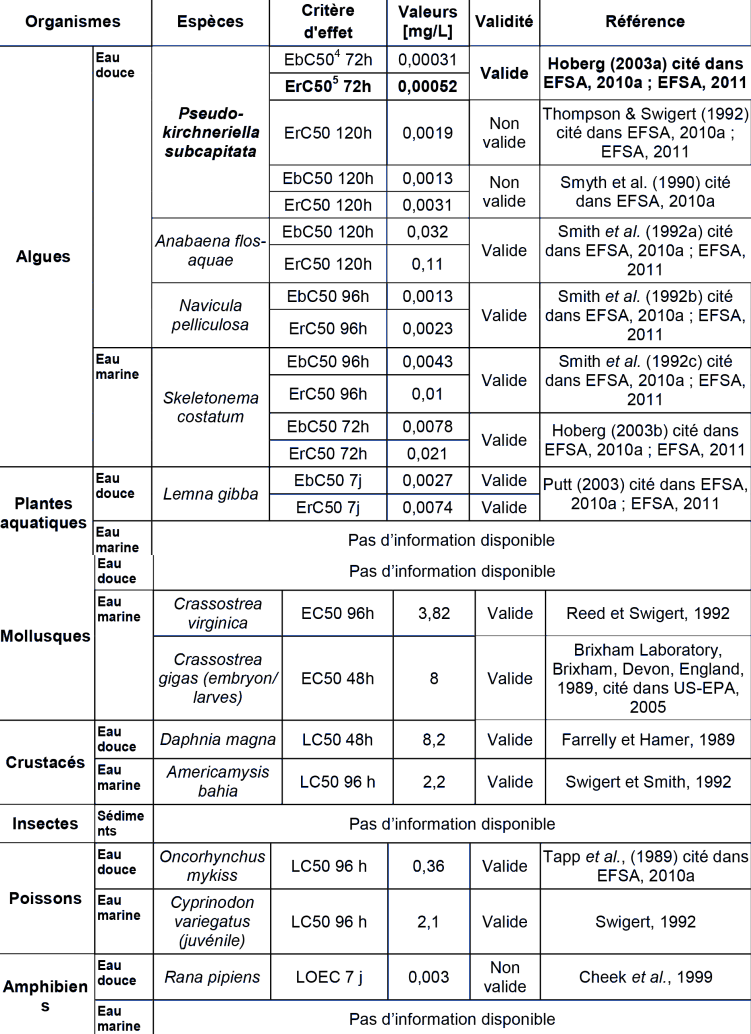
[4] EC50 biomasse
[5] EC50 croissance (growth rate)
ECOTOXICITE AQUATIQUE CHRONIQUE
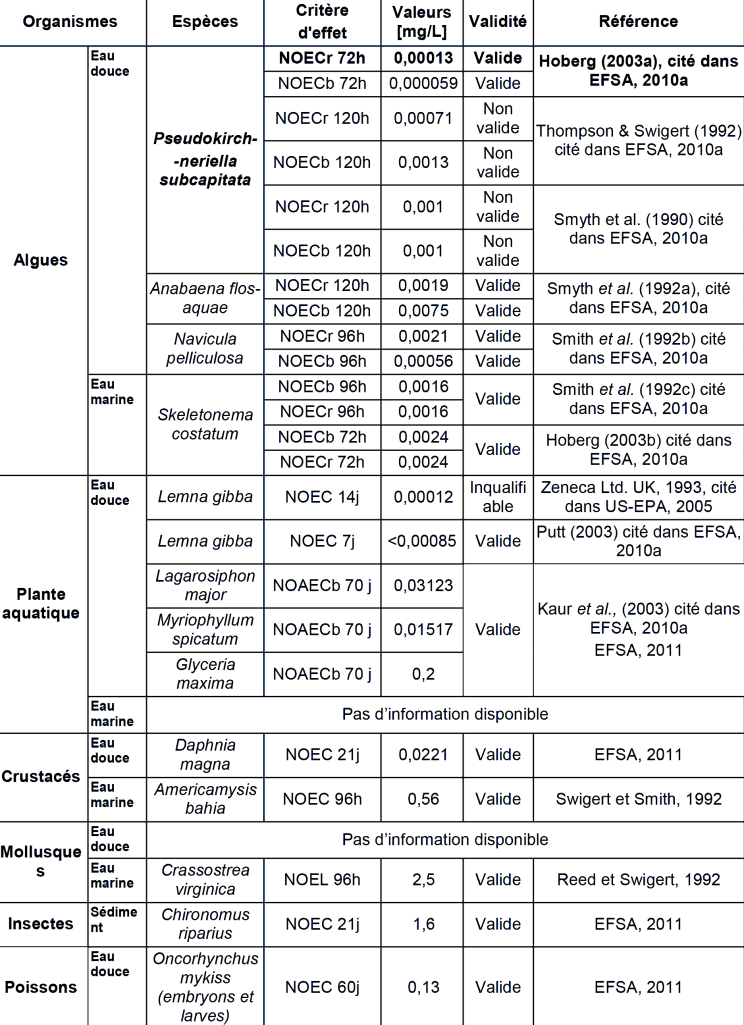
Valeurs de danger
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Synthèse
Biote
VGE/NQE Importer
EMPOISONNEMENT SECONDAIRE
Ce chapitre traite de la toxicité chronique induite par la substance sur les prédateurs via la consommation d'organismes aquatiques contaminés (appelés biote, i.e. poissons ou invertébrés vivant dans la colonne d'eau ou dans les sédiments). Il s'agit donc d'évaluer la toxicité chronique de la substance par la voie d'exposition orale uniquement.
Dans les tableaux ci-dessous, ne sont reportés pour chaque type de test que les résultats permettant d'obtenir les NOEC ou la valeur toxicologique de référence (VTR) les plus protectrices. N'ont été recherchés que des tests sur mammifères ou oiseaux exposés par voie orale (exposition par l'alimentation ou par gavage). Toutes les données présentées ont été validées.
Les résultats de toxicité sont principalement donnés sous forme de doses journalières : NOAEL (No Observed Adverse Effect Level), ou LOAEL (Lowest Observed Adverse Effect Level). NOAEL et LOAEL sont exprimées en termes de quantité de substance administrée par unité de masse corporelle de l'animal testé, et par jour.
Pour calculer la norme de qualité liée à l'empoisonnement secondaire des prédateurs, il est nécessaire de connaître la concentration de substance dans le biote n'induisant pas d'effets observés pour les prédateurs (exprimée sous forme de NOEC). Il est possible de déduire une NOEC à partir d'une NOAEL grâce à des facteurs de conversion empiriques variables selon les espèces testées. Les facteurs utilisés ici sont ceux recommandés par le guide technique européen pour la détermination de normes de qualité (E.C., 2011). Les valeurs de ces facteurs de conversion dépendent de la masse corporelle des animaux et de leur consommation journalière de nourriture. Celles-ci peuvent donc varier d'une façon importante selon le niveau d'activité et le métabolisme de l'animal, la valeur nutritive de sa nourriture, etc. En particulier elles peuvent être très différentes entre un animal élevé en laboratoire et un animal sauvage.
Afin de couvrir ces sources de variabilité, mais aussi pour tenir compte des autres sources de variabilité ou d'incertitude (variabilité inter et intra-espèces, extrapolation du court terme au long terme, etc.) des facteurs d'extrapolation sont nécessaires pour le calcul de la QSbiota sec pois. Les valeurs recommandées pour ces facteurs d'extrapolation sont données dans le guide technique européen (E.C., 2011). Un facteur d'extrapolation supplémentaire (AFdose-réponse) est utilisé dans le cas où la toxicité a été établie à partir d'une LOAEL plutôt que d'une NOAEL.
Les données obtenues sur les mammifères terrestres et les oiseaux, utilisées pour la détermination des valeurs guides pour la protection des prédateurs vis-à-vis de l’empoisonnement secondaire, sont répertoriées dans les tableaux ci-dessous.
ECOTOXICITE POUR LES VERTEBRES TERRESTRES
TOXICITE ORALE POUR LES MAMMIFERES
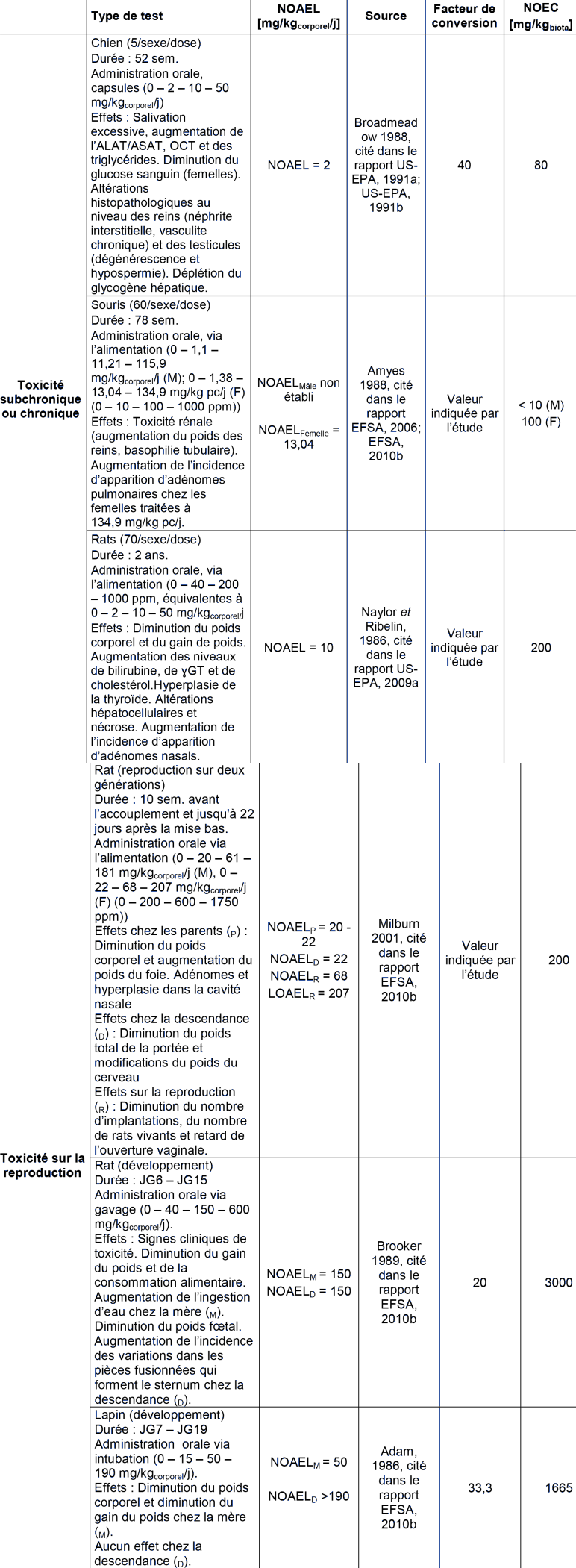
Concernant la toxicité subchronique, deux études de bonne qualité sont disponibles, une de Broadmeadow (1988, citée dans le rapport US-EPA, 1991a; US-EPA, 1991b) et une d'Amyes (1989, citée dans le rapport EFSA, 2006; EFSA, 2010b). L'atteinte des testicules chez le mâle est jugée pertinente pour les populations de prédateurs.
Pour les études sur la reproduction, le tableau ci-dessus présente les 3 études les plus pertinentes, considérées de bonne qualité. Il s'agit d'une étude sur 2 générations chez le rat et de deux études de reproduction l'une chez le rat et l'autre chez le lapin.
L'étude qui présente les niveaux d'effets les plus bas est celle sur 2 générations chez le rat (Milburn 2001, citée dans le rapport EFSA, 2010b).
Chez les parents, les effets qui se sont révélés les plus critiques sont l'augmentation du poids du foie observée chez les deux parents et la diminution du poids corporel ainsi que l'augmentation de l'incidence d'adénomes et d'hyperplasie dans la cavité nasale, décrits uniquement chez les femelles. Ces effets sont observés à des doses de 61 mg/kgcorporel/j chez les mâles et de 68 mg/kgcorporel/j chez les femelles.
Les effets les plus sensibles sur le développement sont la diminution du poids total de la portée et les altérations du poids du cerveau des nouveaux nés, observés à 68 mg/kgcorporel/j d'acétochlore.
Les effets sur la reproduction correspondent à une diminution du nombre d'implantations et du nombre de nouveaux nés vivants et un retard de l'ouverture vaginale. Ces effets ont été décrits à 207 mg/kgcorporel/j.
Ces effets sur la reproduction et le développement surviennent à des niveaux de doses supérieurs à ceux retenu pour la VTR, ils sont donc couverts par la valeur retenue.
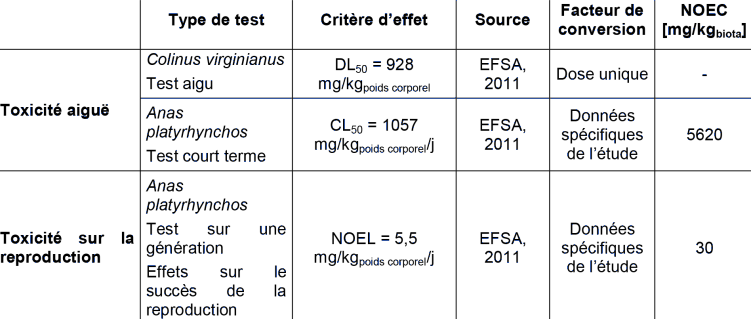
TOXICITE ORALE POUR LES OISEAUX
Valeurs écotoxicologiques
Introduction
Dans cette rubrique, sont reportées des valeurs de référence pour la protection des écosystèmes aquatiques et de la santé humaine via l’environnement.
Dans cette rubrique, sont reportées des valeurs de référence pour la protection des écosystèmes aquatiques et de la santé humaine via l’environnement.
Elles peuvent avoir un statut de « Valeur réglementaire » si elles sont issues
- de réglementations européennes et issues par exemple de dossiers d’évaluation des risques dans le cadre de processus d’autorisation de mise sur le marché des substances chimiques (c’est le cas des Concentrations Prédites Sans Effet pour l’environnement (PNEC) issues des dossiers réglementaires sous REACh ou dans le cas de la réglementation des produits biocides) ou issues de « Normes de Qualité Environnementale » (NQE) de la Directive Cadre européenne sur l’Eau (DCE) ;
- de réglementations françaises telles que les arrêtés de mise en application de la DCE à l’échelle nationale.
Elles peuvent être des « Valeurs guides » lorsque ce sont des propositions scientifiques de l’INERIS qui ne sont pas reportées dans des textes réglementaires. C’est le cas de toutes les valeurs établies par l’INERIS pour guider l’évaluation de la qualité des milieux aquatiques pour les substances qui n’ont pas, ou pas encore, un statut réglementaire dans le contexte de la DCE.
Les « Valeurs Guides Environnementales » (VGE) et les « Normes de Qualité Environnementale » (NQE) sont les outils consacrés pour l’évaluation de la qualité des eaux de surface, dont l’établissement est basé sur une même méthodologie européenne dédiée (E.C., 2018).
Leur construction, d’un point de vue méthodologique, est donc similaire.
Valeurs guides
Description
VGE/NQE Importer
NORMES DE QUALITE POUR LA COLONNE D'EAU
Les normes de qualité pour les organismes de la colonne d'eau sont calculées conformément aux recommandations du guide technique européen pour la détermination des normes de qualité environnementale (E.C., 2011). Elles sont obtenues en divisant la plus faible valeur de NOEC ou d'EC50 valide par un facteur d'extrapolation (AF, Assessment Factor).
La valeur de ce facteur d'extrapolation dépend du nombre et du type de tests pour lesquels des résultats valides sont disponibles. Les règles détaillées pour le choix des facteurs sont données dans le guide technique européen (E.C., 2011).
En ce qui concerne les organismes marins, selon le guide technique pour la détermination de normes de qualité environnementales (E.C., 2011), la sensibilité des espèces marines à la toxicité des substances organiques peut être considérée comme équivalente à celle des espèces dulçaquicoles, à moins qu'une différence ne soit montrée.
- Moyenne annuelle (AA-QSwater_eco et AA-QSmarine_eco) :
Une concentration annuelle moyenne est déterminée pour protéger les organismes de la colonne d'eau d'une possible exposition prolongée.
Pour l'acétochlore, on dispose de données aigues et de données chroniques pour au moins 3 niveaux trophiques (algues, crustacés, poissons), justifiant un facteur d'extrapolation de 10 pour la détermination de l'AA-QSwater_eco, conformément au guide technique européen pour la détermination des normes de qualité environnementale (E.C., 2011). En outre, les produits de dégradation de l'acétochlore potentiellement présents dans l'environnement sont tous moins toxiques pour les organismes aquatiques que le composé parent lui-même.
En chronique comme en aigu, les algues et plantes aquatiques représentent le taxon le plus sensible et l'espèce algale la plus sensible parmi celles représentées dans le jeu de données est Pseudokirchneriella subcapitata, avec une NOEC de 1,3 10-4 mg.L-1. Un facteur d'extrapolation de 10 à appliquer sur la plus faible NOEC obtenue sur P. subcapitata est proposé pour la détermination de l'AA-QSwater_eco.
L'INERIS propose donc la valeur suivante :
![]()
En ce qui concerne les organismes marins, le jeu de données disponibles pour l'acétochlore ne permet pas de mettre en évidence une différence de sensibilité entre les espèces marines et dulçaquicoles. Pour le milieu marin, le facteur d'extrapolation appliqué doit prendre en compte les incertitudes additionnelles telles que la sous-représentation des taxons spécifiques du milieu marin et une diversité d'espèces plus importante. Pour l'acétochlore, un test d'écotoxicité chronique valide existe sur un mollusque (Crassostrea) qui représente un taxon spécifique du milieu marin. Par conséquent et conformément au guide technique européen pour la détermination des normes de qualité environnementale (E.C., 2011), pour déterminer l'AA-QSmarine_eco, en tenant compte des mêmes arguments que pour le choix du facteur d'extrapolation pour la détermination de l'AA-QSwater_eco (mode d'action spécifique et bonne représentativité du taxon le plus sensible dans le jeu de données) ainsi que de la représentation d'un taxon spécifique du milieu marin, un facteur d'extrapolation de 50 s'applique sur la donnée chronique la plus faible, soit la même NOEC que précédemment (1,3 10-4 mg.L-1). L'INERIS propose donc la valeur suivante :
![]()
Concentration Maximum Acceptable (MAC et MACmarine)
La concentration maximale acceptable est calculée afin de protéger les organismes de la colonne d'eau de possibles effets de pics de concentrations de courtes durées (E.C., 2011).
Pour l'acétochlore, on dispose de données aigues pour au moins 3 niveaux trophiques (algues, crustacés, poissons), justifiant un facteur d'extrapolation de 100 pour la détermination de la MAC, conformément au guide technique européen pour la détermination des normes de qualité environnementale (E.C., 2011). En aigu, les algues représentent le taxon le plus sensible et la donnée la plus faible est obtenue pour l'espèce P. subcapitata, avec une ErC50 de 5,2 10-4 mg.L-1. Cette valeur est plus faible que les ErC50 des autres espèces végétales testées (les algues Anabaena flos-aquae, Navicula pelliculosa et Skeletonema costatum, ainsi que la plante Lemna gibba). Aussi, c'est sur cette concentration d'effets que se base la détermination de la MAC. Compte tenu du mode d'action spécifique et du fait que, d'après le jeu de données disponibles, les espèces végétales sont nettement plus sensibles à l'acétochlore que les espèces animales et que la diversité des espèces végétales testées est relativement large (4 espèces de plantes et 4 espèces algales), un facteur d'extrapolation de 10 est proposé pour déterminer la MAC. L'INERIS propose donc la valeur suivante :
![]()
![]()
En ce qui concerne les organismes marins, le jeu de données disponibles pour l'acétochlore ne permet pas de mettre en évidence une différence de sensibilité entre les espèces marines et dulçaquicoles. Pour le milieu marin, le facteur d'extrapolation appliqué doit prendre en compte les incertitudes additionnelles telles que la sous-représentation des taxons spécifiques du milieu marin et une diversité d'espèces plus importante. Pour l'acétochlore, un test d'écotoxicité aigu valide existe sur un mollusque (Crassostrea) qui représente un taxon spécifique du milieu marin. Par conséquent et conformément au guide technique européen pour la détermination des normes de qualité environnementale (E.C., 2011), pour déterminer la MACmarine, en tenant compte des mêmes arguments que pour le choix du facteur d'extrapolation pour la détermination de la MAC (mode d'action spécifique et bonne représentativité du taxon le plus sensible dans le jeu de données) ainsi que de la représentation d'un taxon spécifique du milieu marin, un facteur d'extrapolation de 50 s'applique sur la même donnée algue que pour la MAC (5,2 10-4 mg.L-1). L'INERIS propose donc la valeur suivante :
![]()
![]()
NORME DE QUALITE EMPOISONNEMENT SECONDAIRE (QSBIOTA_SEC POIS)
La norme de qualité pour l'empoisonnement secondaire (QSbiota sec pois) est calculée conformément aux recommandations du guide technique européen (E.C., 2011). Elle est obtenue en divisant la plus faible valeur de NOEC valide par les facteurs d'extrapolation recommandés (E.C., 2011).
Pour l'acétochlore, plusieurs études de toxicologie sont disponibles pour la détermination de la QSbiota sec pois. La plus faible NOEC est obtenue chez les oiseaux, avec une étude sur les effets de l'acétochlore sur le succès de la reproduction (NOEC de 30 mg/kgbiote). Les données d'études chez les oiseaux sont associées à un facteur d'extrapolation de 30 d'après le guide technique européen de détermination des normes de qualité environnementale (E.C., 2011). En outre, d'après le rapport d'étude de la DG ENV établissant la mise à jour de la liste prioritaire des perturbateurs endocriniens à faible tonnage (Petersen et al., 2007), l'acétochlore est considéré comme une « substance pour laquelle il n'existe pas de preuve d'une activité de perturbation endocrine » (catégorie 3) pour la faune sauvage. L'application d'un facteur additionnel pour la prise en compte des perturbations endocrines n'est donc pas nécessaire, d'autant plus que les potentielles perturbations endocrines sur la reproduction sont couvertes par cette étude sur oiseau une génération, une étude chez le rat sur 2 générations, ainsi que 2 études sur le développement du rat et du lapin dans lesquelles les effets ont été observés à des doses supérieures. On obtient donc :
![]()
Cette valeur de norme de qualité pour l'empoisonnement secondaire peut être ramenée :
- à une concentration dans l'eau douce selon la formule suivante :
- à une concentration dans l'eau marine selon la formule suivante :
![]()
Avec :
BCF : facteur de bioconcentration,
1 BMF: facteur de biomagnification,
2 BMF: facteur de biomagnification additionnel pour les organismes marins.
Ce calcul tient compte du fait que la substance présente dans l'eau du milieu peut se bioaccumuler dans le biote. Il donne la concentration à ne pas dépasser dans l'eau afin de respecter la valeur de la norme de qualité pour l'empoisonnement secondaire déterminée dans le biote.
La bioaccumulation tient compte à la fois du facteur de bioconcentration (BCF, ratio entre la concentration dans le biote et la concentration dans l'eau) et du facteur de biomagnification (BMF, ratio entre la concentration dans l'organisme du prédateur en bout de chaîne alimentaire, et la concentration dans l'organisme de la proie au début de la chaîne alimentaire). En l'absence de valeurs mesurées pour le BMF, celles-ci peuvent être estimées à partir du BCF selon le tableau 4-6, page 123, du guide technique européen (E.C., 2011).
Ce calcul n'est donné qu'à titre indicatif. Il fait en effet l'hypothèse qu'un équilibre a été atteint entre l'eau et le biote, ce qui n'est pas véritablement réaliste dans les conditions du milieu naturel. Par ailleurs il repose sur un facteur de bioaccumulation qui peut varier de façon importante entre les espèces considérées.
Pour l'acétochlore, un BCF de 20 et un BMF1 = BMF2 de 1 (cf. E.C., 2011) ont été retenus. On a donc :
![]()
![]()
![]()
NORME DE QUALITE POUR LA SANTE HUMAINE VIA LA CONSOMMATION DES PRODUITS DE LA PECHE (QSBIOTA_HH)
La norme de qualité pour la santé humaine est calculée de la façon suivante (E.C., 2011) :
![]()
Ce calcul tient compte de :
- un facteur correctif de 10% (soit 0.1) : la VTR donnée ne tient compte en effet que d'une exposition par voie orale, et pour la consommation de produits de la pêche uniquement. Mais la contamination peut aussi se faire par la consommation d'autres sources de nourriture, par la consommation d'eau, et d'autres voies d'exposition sont possibles (inhalation ou contact cutané). Le facteur correctif de 10% (soit 0,1) permet de rendre l'objectif de qualité plus sévère d'un facteur 10 afin de tenir compte de ces autres sources de contamination possibles.
- la valeur toxicologique de référence (VTR), correspondant à une dose totale admissible par jour ; pour cette substance elle sera considérée égale à 3,6 µg/kgcorporel/j (cf. tableau ci-dessus),
- un poids corporel moyen de 70 kg,
- Cons. Journ. Moy : une consommation journalière moyenne de produits de la pêche (poissons, mollusques, crustacés) égale à 115 g par jour.
- Fsécurité : facteur de sécurité supplémentaire pour tenir compte des potentiels effets CMR ou de perturbation endocrine de la substance. Il est considéré que la potentialité de perturbation endocrine et d'effets cancérogènes sont prises en compte dans l'étude retenue pour le choix de VTR. Aussi, aucun facteur supplémentaire n'est ajouté.
Ce calcul n'est donné qu'à titre indicatif. Il peut être inadapté pour couvrir les risques pour les individus plus sensibles ou plus vulnérables (masse corporelle plus faible, forte consommation de produits de la pêche, voies d'exposition individuelles particulières). Le facteur correctif de 10% n'est donné que par défaut, car la contribution des différentes voies d'exposition varie selon les propriétés de la substance (et en particulier sa distribution entre les différents compartiments de l'environnement), ainsi que selon les populations considérées (travailleurs exposés, exposition pour les consommateurs/utilisateurs, exposition via l'environnement uniquement). L'hypothèse cependant que la consommation des produits de la pêche ne représente pas plus de 10% des apports journalier contribuant à la dose journalière tolérable apporte une certaine marge de sécurité (E.C., 2011).
Pour l'acétochlore, le calcul aboutit à :
![]()
Comme pour l'empoisonnement secondaire, la concentration correspondante dans l'eau du milieu peut être estimée en tenant compte de la bioaccumulation de la substance :
- à une concentration dans l'eau douce selon la formule suivante :
- à une concentration dans l'eau marine selon la formule suivante :
![]()
Pour l'acétochlore, on obtient donc :
![]()
![]()
![]()
NORME DE QUALITE POUR LA SANTE HUMAINE VIA L'EAU DE BOISSON (QSdw_hh)
En principe, lorsque des normes de qualité dans l'eau de boisson existent, soit dans la Directive 98/83/CE (C.E., 1998), soit déterminées par l'OMS, elles peuvent être adoptées. Les valeurs réglementaires de la Directive 98/83/CE doivent être privilégiées par rapport aux valeurs de l'OMS qui ne sont que de simples recommandations.
Il faut signaler que ces normes réglementaires ne sont pas nécessairement établies sur la base de critères (éco)toxicologiques (par exemple les normes pour les pesticides avaient été établies par rapport à la limite de quantification analytique de l'époque pour ce type de substance, soit 0.1 µg.L-1). Pour l'acétochlore, la Directive 98/83/CE fixe une valeur de 0.1 µg.L-1.
A titre de comparaison, la valeur seuil provisoire pour l'eau de boisson est calculée de la façon suivante (E.C., 2011):
![]()
Ce calcul tient compte de :
- la valeur toxicologique de référence (VTR), correspondant à une dose totale admissible par jour ; pour cette substance elle sera considérée égale à 3,6 µg/kgcorporel/j µg/kgcorporel/j (cf. tableau ci-dessus),
- Cons.moy.eau [L.j-1] : une consommation d'eau moyenne de 2 L par jour,
- un poids corporel moyen de 70 kg,
- un facteur correctif de 10% (soit 0.1) afin de tenir compte de ces autres sources de contamination possibles.
- Fsécurité : facteur de sécurité supplémentaire pour tenir compte des potentiels effets CMR ou de perturbation endocrine de la substance. Il est considéré que la potentialité de perturbation endocrine est prise en compte dans l'étude retenue pour le choix de VTR. De plus, les potentiels effets cancérogènes sont également pris en compte dans l'étude retenue pour le choix de VTR. Aussi, aucun facteur supplémentaire n'est ajouté.
L'eau de boisson est obtenue à partir de l'eau brute du milieu après traitement pour la rendre potable. La fraction éliminée lors du traitement dépend de la technologie utilisée ainsi que des propriétés de la substance.
Ainsi, la norme de qualité correspondante dans l'eau brute se calcule de la manière suivante :
![]()
En l'absence d'information, on considèrera que la fraction éliminée est nulle et le critère pour l'eau de boisson s'appliquera alors à l'eau brute du milieu. Par ailleurs, on rappellera que ce calcul n'est donné qu'à titre indicatif et peut s'avérer inadéquat pour certaines substances et certaines populations.
Pour l'acétochlore, on obtient :
![]()
La valeur la plus protectrice, fixée par la directive 98/83/CE est proposée comme norme de qualité pour l'eau destinée à la production d'eau potable.
![]()
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Synthèse
VGE/NQE Importer
VALEUR GUIDE POUR LES ORGANISMES BENTHIQUES (QSSED ET QSSED-MARIN)
Un seuil de qualité dans le sédiment est nécessaire (i) pour protéger les espèces benthiques et (ii) protéger les autres organismes d'un risque d'empoisonnement secondaire résultant de la consommation de proies provenant du benthos. Les principaux rôles des normes de qualité pour les sédiments sont de :
- Identifier les sites soumis à un risque de détérioration chimique (la norme sédiment est dépassée)
- Déclencher des études pour l'évaluation qui peuvent conduire à des études plus poussées et potentiellement à des programmes de mesures
- Identifier des tendances à long terme de la qualité environnementale (Art. 4 Directive 2000/60/CE).
Les valeurs guides de qualité pour les organismes benthiques (QSsed et QSsed marin) sont calculées conformément aux recommandations du guide technique européen pour la détermination des normes de qualité environnementale (E.C., 2011). Elles sont obtenues en divisant la plus faible valeur de NOEC ou d'EC50 valide par un facteur d'extrapolation (AF, Assessment Factor).
La valeur de ce facteur d'extrapolation dépend du nombre et du type de tests sur les organismes benthiques pour lesquels des résultats valides sont disponibles. Les règles détaillées pour le choix des facteurs sont données dans le guide technique européen (E.C., 2011).
Un essai chronique réalisé sur Chironomus riparius est disponible. Ce test utilise l'eau comme voie de contamination et est validé dans le rapport de l'EFSA (EFSA, 2011). La NOEC obtenue est de 1,6 mg.L-1. Aucune valeur correspondante dans le sédiment n'est disponible dans le rapport de l'étude et cette valeur est très inférieure à la NOEC la plus basse de 1,3 10-4 mg.L-1 obtenue pour P. subcapitata, c'est pourquoi les valeurs guides pour le sédiment doivent être calculées à partir de l'AA-QSwater_eco et de l'AA-QSmarine_eco via le modèle de l'équilibre de partage.
Ce modèle suppose que :
- il existe un équilibre entre la fraction de substances adsorbées sur les particules sédimentaires et la fraction de substances dissoutes dans l'eau interstitielle du sédiment,
- la fraction de substances adsorbées sur les particules sédimentaires n'est pas biodisponible pour les organismes et que seule la fraction de substances dissoutes dans l'eau interstitielle est susceptible d'impacter les organismes,
- la sensibilité intrinsèque des organismes benthiques aux toxiques est équivalente à celle des organismes vivant dans la colonne d'eau. Ainsi, la norme de qualité pour la colonne d'eau peut être utilisée pour définir la concentration à ne pas dépasser dans l'eau interstitielle.
Une valeur guide de qualité pour le sédiment peut être alors calculée selon l'équation suivante (E.C., 2011) :
![]()
RHOsed : masse volumique du sédiment en [Kgsed.m-3sed]. En l'absence d'une valeur exacte, la valeur générique proposée par le document guide technique européen (E.C., 2011) est utilisée : 1300 kg.m-3 .
Ksed-eau : coefficient de partage sédiment/eau en m3/m3 . En l'absence d'une valeur exacte, les valeurs génériques proposées par le guide technique européen (E.C., 2011) sont utilisées. Le coefficient est alors calculé selon la formule suivante : 0,8 + 0,025 * Koc soit Ksed-eau = 4,7 m3/m3
Pour l'acétochlore, on obtient :
![]()
QSsed wet weight = 0,047 µg.kg-1poids humide
La concentration correspondante en poids sec peut être estimée en tenant compte du facteur de conversion suivant :
![]()
Avec :
Fsolidesed : fraction volumique en solide dans les sédiments en [m3solide/m3susp]. En l'absence d'une valeur exacte, la valeur générique proposée par le document guide technique européen (E.C., 2011) est utilisée : 0,2 m3/m3 .
RHOsolide : masse volumique de la partie sèche en [kgsolide/m3solide]. En l'absence d'une valeur exacte, la valeur générique proposée par le document guide technique européen (E.C., 2011) est utilisée : 2500 kg.m-3 .
Pour l'acétochlore, la concentration correspondante en poids sec est :
![]()
Selon la même approche que pour le sédiment d'eau douce, une valeur guide de qualité pour le sédiment marin peut être calculée selon la formule suivante :
![]()
Pour l'acétochlore, on obtient :
![]()
QSsed-marin wet weight = 0,0094 µg.kg-1poids humide
La concentration correspondante en poids sec est alors la suivante:
QSsed-marin dry weight = 0,0244 µg.kg-1sed poids sec
Le log Kow de la substance étant inférieur à 5, un facteur additionnel de 10 n'est pas jugé nécessaire.
Il faut rappeler que les incertitudes liées à l'application du modèle de l'équilibre de partage sont importantes. Les sédiments naturels peuvent avoir des propriétés très variables en termes de composition (nature et quantité de matières organiques, composition minéralogique), de granulométrie, de conditions physico-chimiques, de conditions dynamiques (taux de déposition/taux de resuspension). Par ailleurs ces propriétés peuvent évoluer dans le temps en fonction notamment des conditions météorologiques et de la morphologie de la masse d'eau. Si bien que le partage entre la fraction de substance adsorbée et la fraction de substance dissoute peut être extrêmement variable
d'un sédiment à un autre et l'hypothèse d'un équilibre entre ces deux fractions ne semble pas très réaliste pour des conditions naturelles.
Par ailleurs, certains organismes benthiques peuvent ingérer les particules sédimentaires, et donc être contaminés par la fraction de substance adsorbée sur ces particules, ce qui n'est pas pris en compte par la méthode.
![]()
PROPOSITION DE VALEUR GUIDE ENVIRONNEMENTALE (VGE)
Elle est définie à partir de la valeur la plus protectrice parmi tous les compartiments étudiés.
![]()
Pour l'acétochlore, la norme de qualité pour les organismes aquatiques est la valeur la plus faible pour l'ensemble des approches considérées.
VALEURS GUIDES POUR LES ORGANISMES BENTHIQUES
Avec un Koc moyen de 156 L.kg-1, la mise en œuvre d'un seuil pour le sédiment n'est pas recommandée par le document guide technique européen (E.C., 2011).
Valeurs réglementaires
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Bibliographie
Données technico-économiques
Dernière vérification le 29/03/2024
Introduction
FTE 2015 Importer 
A l'échelle mondiale, l'acétochlore est une substance organique exclusivement utilisée dans le domaine agricole pour ses usages herbicide.
Avant son interdiction en 2013, cette substance était utilisée en France pour le désherbage pré-levée du maïs : plusieurs dizaines de tonnes par an étaient ainsi vendues en France et qui représentaient plusieurs pourcents des quantités d'herbicides vendues.
Suite à cette interdiction, l'emploi d'autres substances herbicides s'est substitué à l'usage de l'acétochlore. Pour ce faire, les producteurs et/ou distributeurs de ce produit phytosanitaire ont mené des études et ont communiqué leurs résultats aux agriculteurs. Les ventes d'acétochlore ont ainsi chuté à plusieurs centaines de kilogrammes par an (ce qui représente moins d'un centième de pourcent des quantités d'herbicides vendues). Avant son interdiction la présence d'acétochlore a été caractérisée dans les compartiments aériens et aquatiques de l'environnement. A ce jour, nous ne disposons que de peu d'information permettant d'estimer le recul de l'imprégnation du milieu suite à son interdiction. On note toutefois que, malgré son interdiction, les métabolites de ce produit phytosanitaire restent encore significativement présents dans les eaux souterraines de certaines régions de l'Ouest de la France.
Viewed globally, acetochlor is an organic substance used exclusively in the agricultural sector for its herbicidal uses.
In France, before its ban in 2013, it was used for the pre-emergence weed control of maize: several tens of tons per year were sold in France and represented several percent of the quantities of herbicides sold.
Following this ban, the use of other herbicidal substances replaced the use of acetochlor. To do this, the producers and/or distributors of this phytosanitary product carried out studies and communicated their results to the farmers. Sales of acetochlor have thus fallen to several hundred kilograms per year (less than one hundredth of a percent of the quantities of herbicides sold).
Before its ban the presence of acetochlor was characterized in the air and aquatic compartments of the environment. To date, we only have few information allowing us to estimate the decrease of the impregnation of the environment following its prohibition.
However, despite its ban, the metabolites of this phytosanitary product are still significantly present in the groundwater of certain western regions of France.
Tableaux de synthèse
Généralités
| CAS | 34256-82-1 |
|---|---|
| SANDRE | 1903 |
| Substance prioritaire dans le domaine de l’eau (DCE) | non |
| Substance soumise à autorisation dans Reach | non |
| Substance soumise à restriction dans Reach | non |
| Substance extrêmement préoccupante (SVHC) | non |
| Réglementations |
FTE 2015 Importer TEXTES GENERAUX |
| Classification CLP | Voir la classification CLP |
| Valeurs et normes appliquées en France |
FTE 2015 Importer Lors de la rédaction de cette fiche, aucune limite d'exposition professionnelle dans l'air des lieux de travail n'a été identifiée pour la France. AUTRES TEXTESACTION DE RECHERCHE RSDEL'acétochlore n'est pas concerné par l'Action Nationale de Recherche et de Réduction des Rejets de Substances Dangereuses dans les Eaux (RSDE), ni pour l'action dédiée aux sites industrielles, ni pour l'action dédiée aux stations de traitement des eaux usées. AUTRES TEXTESL'acétochlore est cité par la circulaire du 13 juillet 2006 relative à la constitution et la mise en œuvre du programme de surveillance pour les eaux douces de surface en application de la directive 2000/60/CE du 23 octobre 2000 du Parlement et du Conseil établissant un cadre pour une politique communautaire dans le domaine de l'eau. Ce texte précise que cette substance doit être suivie sur 25 % des sites du contrôle de surveillance et sur 100 % des plans d'eau. REGLEMENTATION EXTRA EUROPEENNEL'acétochlore est, ou a été largement employé dans le domaine agricole au niveau mondial, notamment en Chine, aux Etats-Unis, en Argentine, … (USEPA, 2004). Il existe ainsi beaucoup de réglementations au niveau de ces pays régissant l'usage de ce pesticide. CLASSIFICATION ET ETIQUETAGEL'acétochlore est cité dans l'annexe VI du règlement 1272/20089 dit règlement CLP, qui lui associe les classifications et étiquetage ci-après.  Le tableau ci-après détaille les codes de danger associé à l'acétochlore. [9] Règlement (CE) n°1272/2008 du Parlement Européen et du Conseil du 16 décembre 2008 relatif à la classification, à l'étiquetage et à l'emballage des substances et des mélanges. Tableau 3. Codes de danger de l'aétochlore, d'après le site interenet de l'ECHA10 (annexe VI du règlement 1272/200811). 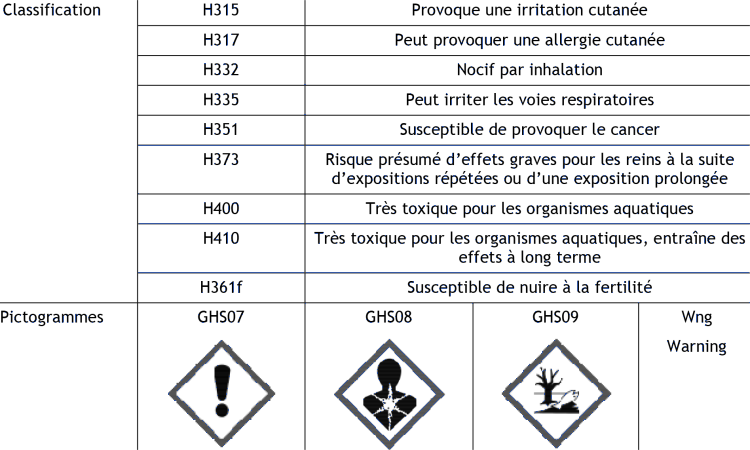 SOURCES NATURELLES D'ACETOCHLOREL'acétochlore est une substance d'origine anthropique : il n'y a donc pas de source naturelle pour ce produit phytosanitaire. [10] https://echa.europa.eu/fr/substance-information/-/substanceinfo/100.047.166 site consulté en décembre 2016. [11] https://echa.europa.eu/fr/information-on-chemicals/cl-inventory-database/-/discli/details/104340 site consulté en décembre 2016. SOURCES NON-INTENTIONNELLES D'ACETOCHLOREL'acétochlore n'est (ou n'a été) employé que pour ses propriétés phytosanitaires : il n'y a donc pas de source non-intentionnelle de cette substance dans l'environnement. |
Volume de production
| France |
FTE 2015 Importer inconnu |
|---|---|
| UE |
FTE 2015 Importer inconnu |
| Monde |
FTE 2015 Importer inconnu |
Consommation
| Volume de consommation en France |
FTE 2015 Importer qq. centaines de kilogrammes par an |
|---|
Production et utilisation
Production et ventes
Données économiques
FTE 2015 Importer
Très peu de données économiques sont disponibles quant à l'acétochlore. Néanmoins, BASF12 indique un coût moyen de traitement phytosanitaire avec cette molécule en France de 48 à 55 € par hectare traité entre 2010 et 2012.
Un article de Assani Bin Lukangila et al. (2015) pour un usage de l'acétochlore en République Démocratique du Congo, cite un coût de 17$/litre.
Procédés de production
FTE 2015 Importer
La bibliographie indique deux procédés de production de l'acétochlore :
- par réaction de chlorure de chloroacétyle avec de l'azoméhine de 2-ethyl-6-méthylaniline et formaldéhyde, suivi par traitement avec de l'éthanol (Muller et Applebyki, 2010) ;
- par éthoxy méthylation d'une acétanilide (Ahrens, 1994).
Noms commerciaux
FTE 2015 Importer
Les noms commerciaux des produits phytosanitaires sont relativement différents d'un pays à l'autre, la PPDB cite ainsi les exemples de noms commerciaux suivants : Harness, Trophy, Trophee, Acenit, Guardian, Sacemid et Surpass.
En France, l'ACTA 2013 (2012) liste ainsi les noms commerciaux suivants : Trophée et Harness Microtech qui, avant leur interdiction, étaient respectivement distribué par Dow AgroSciences et Monsanto.
[12] Cf. le site internet de BASF (consulté en décembre 2016) http://www.agro.basf.fr/agroportal/fr/fr/cultures/inv_le_mais/herbicides_mais/dossier_desherbage_ du_mais_en_prelevee_apres_retrait_de_l_acetochlore/desherbage_du_mais_isard_dakota_p_solutions_ pour_remplacer_l_acetochlore.html
Utilisations
UTILISATIONS
DESCRIPTION QUALITATIVE
FTE 2015 Importer
L'ACTA 2013 (2012) et Béraud et Bernard (1999) indiquent une utilisation quasi exclusive comme herbicide pour la culture du maïs pour cette substance (application post-semi prélevée et post-levée précoce du maïs avant la levée des adventices).
Néanmoins, cette substance a, par le passé ou en dehors du territoire national, été utilisée sur une gamme plus large de cultures3 (chou, pois, oignons, pommes, poires, prunes, abricots, café, blé, betterave à sucre, canne à sucre, pommes de terre, …).
DONNEES QUANTITATIVES
FTE 2015 Importer
Ce paragraphe résume les informations disponibles dans la BNV-d13 quant aux ventes de l'acétochlore sur la période 2010-2015 sur le territoire métropolitain et les départements et régions d'outre-mer :
- Sur la période 2010-2012, les ventes sont stables à environ 1 000 tonnes par an. Cette quantité représente plusieurs pourcents des quantités totales d'herbicides vendues.
- Sur la période 2013-2015, suite au retrait de l'autorisation de mise sur le marché de cette substance, les ventes ont très fortement diminué mais sans néanmoins disparaitre (quelques centaines de kilos vendus en 2015). Cette quantité représente moins d'un centième de pourcent des quantités totales d'herbicides vendues.
De surcroit notons que ces chiffres de vente illustrent une situation géographiquement potentiellement contrastée. En effet, cette substance fait partie des 10 substances les plus vendues en 2008-2010 en Poitou-Charentes (FREDON Poitou-Charentes, 2011), territoire où la culture du maïs est bien implantée (cf. figure ci-après).
[13] Mise en place en 2009, la BNV-d (Banque nationale des ventes de produits phytosanitaires pour les distributeurs) est la base de données qui rassemble les informations déclarées par les distributeurs de produits phytosanitaires suite à la mise en place de la redevance pour pollutions diffuses. Cette redevance répond aux exigences de la loi sur l'eau de décembre 2006. Les données utilisées ici ont été extraites en décembre 2016.
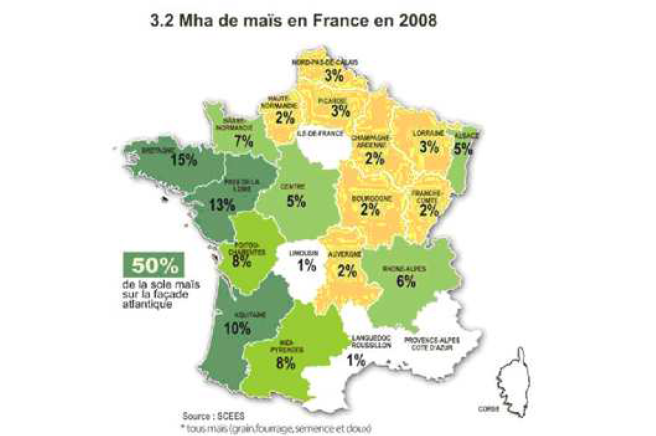
Figure 1 : Carte de la surface agricole utile dédiée à la culture de maïs en 2008 (source SCEES citée par BASF14).
14
http://www.agro.basf.fr/agroportal/fr/fr/cultures/inv_le_mais/basf_et_la_filiere_mais/chiffres_Filier e_mais.html (site consulté en décembre 2016).
Rejets dans l’environnement
Émissions anthropiques totales
FTE 2015 Importer
En première estimation, les émissions anthropiques totales peuvent être approchées par les utilisations phytosanitaires de ces substances (cf. §2). Néanmoins, mêmes si ces usages sont principalement dirigés vers les sols et les plantes, il est difficile d'identifier le ou les milieu(x) récepteur(s) de ces émissions (atmosphère, eaux ou sols).
Rejets dans l'environnement
FTE 2015 Importer
Pour l'acétochlore, aucune source naturelle n'a été identifiée lors de cette étude. Les rejets dans l'environnement sont donc localisés aux zones d'utilisation de cette substance et potentiellement, mais dans une bien moindre mesure, aux potentiels sites de formulation, d'empaquetage et/ou de stockage.
Les produits agricoles et agro-alimentaires (notamment importés depuis des zones hors UE) peuvent aussi être de faibles sources d'émission d'acétochlore dans l'environnement. Toutefois une limite de concentration (0,01 mg/kg ou 0,05 mg/kg selon les cas) s'applique à un grand nombre de produits dans l'UE15 .
Pollutions historiques et accidentelles
FTE 2015 Importer
Lors de cette étude, aucune information sur une éventuelle pollution historique et/ou accidentelle n'a été identifiée.
[15] Commission Regulation (EU) 2015/603
Présence environnementale
Atmosphère
FTE 2015 Importer
Selon l'INERIS (2014), avec une constante de Henry de 2,1.10-3 Pa.m3.mol-1 (donnée issue de EFSA, 2011), l'acétochlore est peu susceptible de se volatiliser suite à un traitement aux champs.
Avant son interdiction, l'acétochlore a été fréquemment observé dans le compartiment aérien, notamment en région Centre (Commissariat général au développement durable, 2010).
Toujours avant son interdiction, les concentrations atmosphériques observées pouvaient atteindre plusieurs nanogrammes par mètre cube d'air et étaient particulièrement observables au printemps (Hulin, 2008 ; Air Breizh, 2012 ; ASPA, 2015).
Aquatique
FTE 2015 Importer
Selon la base de données PPDB, l'acétochlore:
- est stable dans le milieu aquatique que ce soit vis-à-vis des phénomènes de photolyse aquatique ou d'hydrolyse ;
- est modérément soluble ;
- possède un temps de demi-vie dans le compartiment aquatique de 40,5 jours.
Selon ces données physico-chimiques, il est donc attendu que le compartiment eau soit le principal réservoir environnemental d'acétochlore.
Sur la période 2006-2010, en Poitou-Charentes17 , l'acétochlore est quantifiée essentiellement dans les eaux superficielles, à la suite des désherbages du maïs, au printemps et en été. Les teneurs observées dans les eaux de surface atteignent 0,19 µg.L-1 et 0,10 µg.L-1 pour les eaux souterraines.
L'ordre de grandeur de ces valeurs est confirmé par Botta et Dulio (2014) qui affichent une concentration maximale observée dans les eaux de surface à l'échelle nationale de 0,91 µg.L-1 et un percentile 90 à 0,16 µg.L-1.
Un bilan de la qualité des eaux souterraines établi en 2011 par l'Agence de l'Eau Adour-Garonne (AEAG, 2011) faisait apparaître une présence significative des deux métabolites acétochlore OXA et acétochlore ESA (taux de quantifications respectifs de 5 et 25%, taux de dépassement compris entre 5 et 10%). Cette situation est confirmée par les projets successifs TRANSPOLAR et ELISE du BRGM (BRGM, 2014) sur le bassin de l'Ariège, qui montraient que les métabolites étaient sensiblement plus présents que la molécule-mère dans les eaux souterraines du bassin. Cette situation a conduit l'ARS Aquitaine Limousin Poitou-Charentes à mettre en place un contrôle renforcé des ressources souterraines pour l'eau potable18 .
Par contraste, l'acétochlore est très peu fréquemment identifié dans les eaux souterraines du bassin Rhône-Méditerranée-Corse, ce qui est cohérent avec une plus faible présence du maïs dans cette région (AERMC, 2008).
Terrestre
FTE 2015 Importer
Selon l'INERIS (2014), avec un Koc16 compris entre 28 et 377 (données issues de EFSA, 2011), l'acétochlore n'est pas susceptible de s'adsorber de façon significative sur les particules solides et les sédiments.
[16] Le Koc est le coefficient de partage carbone organique/eau : cette valeur peut être considérée comme une indication sur l'aptitude d'une substance à être adsorbée ou désorbée sur ou depuis de la matière organique.
Lors de la rédaction de cette fiche, il n'a pas été possible d'identifier des mesures de concentration d'acétochlore dans le milieu terrestre. Rappelons que, par ses propriétés physico-chimiques, il n'est pas attendu que cette substance soit retrouvée en forte concentration dans les sols.
[17] http://www.reduction-pesticides-poitou-charentes.fr/IMG/pdf/Fiches_substances13-9VAH.pdf (site consulté en décembre 2016).
[18] http://www.port-de-lanne.fr/ARS%20point%20pesticides.pdf
Perspectives de réduction
Réduction des rejets
REDUCTION DES EMISSIONS D'ACETOCHLORE
FTE 2015 Importer
L'interdiction des usages agricoles de l'acétochlore limite les possibilités de réduction des rejets à un meilleur encadrement des utilisations dérogatoires. En effet, en plein champ, les eaux de ruissellement ne sont généralement pas récupérées (aucun traitement n'est donc envisageable).
A ce jour, nous ne disposons pas d'information permettant d'estimer l'évolution de l'imprégnation du milieu suite à la réduction des émissions.
Alternatives aux usages
ALTERNATIVES AUX USAGES DE L'ACETOCHLORE
FTE 2015 Importer
En France, la forte chute des ventes (présentée au §2) démontre que les solutions de remplacement de l'acétochlore ont déjà été mises en place par les agriculteurs.
Pour ce faire, BASF, fabriquant de cette substance, a par exemple communiqué pour préconiser des solutions de remplacement19 Arvalis, autre distributeur de la substance, a également publié des informations et conseils agricoles20 .
De même, de façon plus large, des traitements équivalents ayant recours à d'autres produits phytosanitaires peuvent être proposés : les correspondances sont listées, par exemple, dans l'index phytosanitaire (publication ACTA remise à jour annuellement).
D'autre part, d'autres stratégies de désherbage des cultures peuvent également être mises en avant en remplacement ou bien en complément des traitements phytosanitaires : l'ITAB (2012) préconise ainsi l'utilisation de la bineuse sur les cultures de maïs.
[19] Voir http://www.agro.basf.fr/agroportal/fr/fr/cultures/inv_le_mais/herbicides_mais/dossier_desherbage_ du_mais_en_prelevee_apres_retrait_de_l_acetochlore/desherbage_du_mais_temoignages_ingenieurs_t echniques_filieres.html
20Voir https://www.arvalis-infos.fr/des-solutions-pour-remplacer-l-acetochlore-@/view-15233-arvarticle.html
Ainsi, la substitution de l'acétochlore par d'autres molécules ne semble pas poser de problème technique. En revanche, il convient de veiller à ce que les substitutions n'impliquent pas un recours accru à une autre substance présentant des risques équivalents (voire plus élevés) pour la santé et/ou pour l'environnement.
Conclusion
FTE 2015 Importer
Suite à son interdiction en France en 2013, les quantités d'acétochlore vendues en France ont très fortement reculé. L'usage agricole de cette substance en tant que produit phytosanitaire étant le seul usage identifié, une diminution de l'imprégnation des milieux est donc attendue. Néanmoins, à ce jour, nous ne disposons pas de de données in -situ traduisant cet état de fait.
Malgré l'interdiction et la décroissance de la présence de l'acétachlore dans les eaux souterraines, les métabolites de ce produit phytosanitaire restent encore significativement présents dans les eaux souterraines de certaines régions de l'Ouest de la France.
Quoiqu'il en soit, l'exemple de la substitution de l'acétochlore par d'autres substances phytosanitaires illustre la possibilité d'effectuer ce type de substitution, y compris dans le domaine agricole.
Archives
Dernière vérification le 29/03/2024
Documents
Exporter la substance
Choisissez le format de l'export :










