Configuration de votre affichage
Vous avez activé le mode de configuration de l'affichage qui permet de sélectionner les informations que vous souhaitez afficher sur la fiche substance. Une fois que vous aurez sélectionné les rubriques à afficher, vous pouvez revenir au mode de consultation de la fiche substance en cliquant à nouveau sur le bouton de filtrage.
Diclofenac (15307-86-5)
Informations générales
Dernière vérification le 29/03/2024
Identification
Numero CAS
15307-86-5
Nom scientifique (FR)
Acide diclofénaque
Nom scientifique (EN)
Autres dénominations scientifiques (Autre langues)
Code EC
239-348-5
Code SANDRE
5349
Numéro CIPAC
-
Formule chimique brute
\(\ce{ C14H11Cl2NO2 }\)
Code InChlKey
Code SMILES
<p>OC(=O)Cc1ccccc1Nc2c(Cl)cccc2Cl</p>
Physico-Chimie
Dernière vérification le 29/03/2024
Généralités
Poids moléculaire
296.16 g/mol
Tableau des paramètres
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Bibliographie
Comportement et devenir dans les milieux
Dernière vérification le 29/03/2024
Matrices
Milieu eau douce
VGE/NQE Importer
Volatilisation :
D'après sa faible valeur de constante de Henry
-73 (4,8 * 10Pa.m/mol), le diclofenac est peu susceptible de se volatiliser.
Milieu sédiment eau douce
VGE/NQE Importer
Adsorption :
Dans la mesure où le diclofénac est un acide faible (pKa compris entre 3,97 et 4,7), celui-ci est sous forme d'anion dans les milieux de pH neutre, ce qui lui confère une faible capacité – confirmée par un faible Koc – à s'adsorber sur les matières solides. Cette capacité est corrélée négativement au pH. A pH neutre, l'anion diclofénac est donc principalement retrouvé sous forme dissoute dans la phase aqueuse. (Fent et al., 2006)
Persistance
Biodégradabilité
VGE/NQE Importer
Biodégradabilité :
La biodégradation est, avec la photodégradation, l'un des processus principaux de dégradation du diclofénac. (Jiskra etHollender, 2008)
Dégradabilité abiotique
VGE/NQE Importer
Hydrolyse :
Les substances pharmaceutiques prévues pour être administrées par voie orale, dont le diclofénac fait partie, sont souvent résistantes à l'hydrolyse. (Andreozzi et al., 2003)
Photolyse :
L'efficacité de la photodégradation du diclofénac est dépendante de la radiation lumineuse qui dépend elle-même de la profondeur, de la saison, de la latitude et des phénomènes météorologiques. (Jiskra etHollender, 2008)
Bioaccumulation
Organismes aquatiques
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Conclusion sur la bioaccumulation
VGE/NQE Importer
Bioaccumulation :
BCF = 3,16 (calculé, méthode de régression)
BAF = 1490 (calculé, modèle Arnot et Gobas, 2003)
(US-EPA, 2012)
Bibliographie
Toxicologie
Dernière vérification le 29/03/2024
Valeurs de référence
Introduction
VGE/NQE Importer
SANTE HUMAINE
Ce chapitre traite de la toxicité chronique induite par la substance sur l'homme soit via la consommation d'organismes aquatiques contaminés, soit via l'eau de boisson.
Pour l'évaluation des effets sur la santé humaine, seuls les résultats sur mammifères sont considérés comme pertinents. Contrairement à l'évaluation des effets pour les prédateurs, les effets de type cancérigène ou mutagène sont également pris en compte.

Le diclofénac n'a pas fait l'objet d'une évaluation par les organismes ECHA, IARC, US EPA mais a été largement étudié par les autorités sanitaires des médicaments qui n'ont pas alerté sur ces effets. Deux études de cancérogenèse ont été réalisées l'une chez le rat et l'autre chez la souris pour des expositions par voie orale (Novartis, 2012). Chez le rat, il n'a pas été induit d'augmentation statistiquement significative de l'incidence des tumeurs à 2 mg/kg pc/j. Chez la souris, aucun effet n'a été observé jusqu'à 2 mg/kg pc/j. Aucun effet mutagénique n'a été identifié par le test d'Ames.
Dans les tableaux ci-dessous, ne sont reportés pour chaque type de test que les résultats permettant d'obtenir les NOEC ou la valeur toxicologique de référence (VTR) les plus protectrices. Compte tenu du
mode d'exposition envisagée, seuls les tests sur mammifères exposés par voie orale (dans l'alimentation ou par gavage) ont été recherchés.
Les résultats de toxicité sont principalement donnés sous forme de doses journalières : NOAEL (No Observed Adverse Effect Level), ou LOAEL (Lowest Observed Adverse Effect Level). NOAEL et LOAEL sont exprimées en termes de quantité de substance administrée par unité de masse corporelle de l'animal testé, et par jour.
TOXICITE
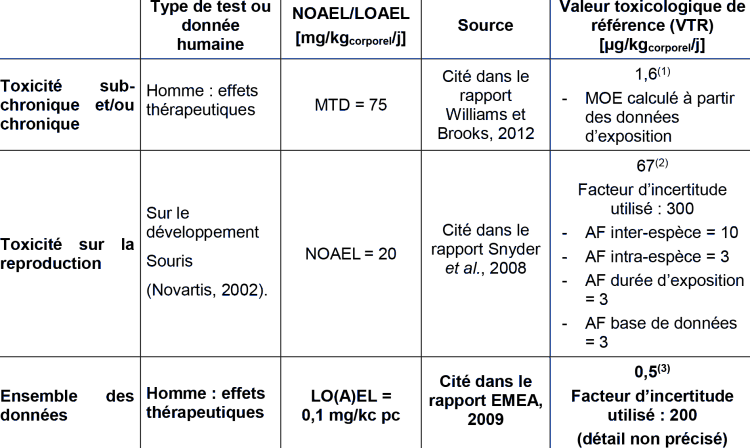
(1) Cette VTR a été déterminée par le Drinking Water Inspectorate (DWI, Watts et al., 2007).
(2) Cette VTR a été déterminée par l'American Water Works Association (AWWA, 2008) et reprise dans Bruce et al., 2010.
(3) Cette VTR a été déterminée par l'Agence européenne pour l'évaluation des produits de médecine (EMEA, 2003). Elle est reprise dans un document de la même agence en 2009
Choix de la VTR
Trois valeurs sont disponibles, qui utilisent des modes de construction différents mais présentent toutes des limites majeures relatives à la transparence de leur construction.
La valeur du Drinking Water Inspectorate (DWI) est basée sur une approche par MOE, elle retient un MTD de 75 mg/kg qui est cohérent avec les données fournies par les différents organismes. Cette valeur est divisée par le niveau d'exposition. Si cette démarche générale est largement expliquée, le détail du calcul n'est pas explicitement précisé.
La valeur de l'American Water Works Association (AWWA) est établie à partir d'une étude sur le développement chez la souris réalisée par le laboratoire pharmaceutique Novartis. Cette étude n'est pas rapportée dans les différents documents consultés. Le niveau de NOAEL de 20 mg/kg pc/j est supérieur à celui des autres études chez le rat pour lesquels les NOAEL sont de 0,3 à 0,5 mg/kg pc/j. Le facteur d'incertitude de 300 apparait raisonnable même si le détail facteur est discutable. En effet, si le facteur 10 est justifié pour tenir compte des différences entre l'animal et l'homme, l'utilisation d'un
facteur 3 pour tenir compte de la variabilité au sein de l'espèce humaine ne parait pas suffisant à l'inverse l'utilisation d'un facteur 3 pour l'extrapolation d'une exposition sub-chronique à chronique n'est généralement pas justifié pour une exposition sur deux générations.
La valeur de l'EMEA ne repose pas sur une étude spécifique mais sur l'ensemble des données pharmacologiques et toxicologiques. Cette démarche prend en compte à la fois les études chez l'animal mais aussi les données humaines même si ces dernières ne sont pas décrites. Au regard des données toxicologiques disponibles rapportées par cette agence, le LOAEL retenu est plus bas que les NOAEL rapportés dans les différentes études. Le choix de cette valeur semble raisonnable même s'il n'est pas clairement expliqué. Le facteur d'incertitude n'est pas détaillé mais sa valeur semble protectrice au regard des études prises en compte.
L'ensemble du profil toxicologique du diclofénac n'est pas disponible alors que de nombreuses études cliniques ont très probablement été réalisées. Pour chacune des valeurs développées, un ou plusieurs éléments clés sont manquants et ne permettent pas de juger de la qualité scientifique de ces valeurs. Ces résultats sont cependant en cohérence avec les doses thérapeutiques chez l'homme.
Par prudence et en l'absence d'éléments supplémentaires, il est proposé de retenir la valeur la plus robuste et la plus protectrice pour les populations, c'est-à-dire celle élaborée par l'EMEA : 0,5 µg/kgcorporel/j.
Valeurs de l'ANSES et/ou de l'INERIS
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Autres valeurs des organismes reconnus
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Bibliographie
Ecotoxicologie
Dernière vérification le 29/03/2024
Introduction
VGE/NQE Importer
Evaluations existantes :
Diclofenac EQS Dossier prepared by the Sub-Group on Review of the Priority Substances List under Working Group E on Chemical Aspects in the context of the Common Implementation Strategy for the Water Framework Directive (E.C., 2011a).
Effets endocriniens :
Le diclofénac n'est pas cité dans les documents stratégiques communautaires concernant les perturbateurs endocriniens (E.C., 2004 ; E.C., 2007 ; E.C., 2011b) ni dans le rapport d'étude de la DG ENV sur la mise à jour de la liste prioritaire des perturbateurs endocriniens à faible tonnage (Petersen et al., 2007).
Critères PBT / POP :
La substance n'est pas citée dans les listes PBT/vPvB1 (C.E., 2006) ou
POP2 (PNUE, 2001).
Normes de qualité existantes :
-Norme de qualité environnementale pour les eaux douces de surface couvrant la protection des organismes aquatiques et des prédateurs supérieurs de ces organismes – Suisse (Oekotoxzentrum, 20143) : 0,05 µg.l-1 en moyenne annuelle (AA-EQS). Cette valeur est inférieure à la proposition faite par l'INERIS, car elle est déterminée directement sur la base des données d'histopathologie auxquelles sont appliquées un facteur d'extrapolation. La proposition de VGE de l'INERIS faite dans cette fiche, elle, couvre les effets histologiques observés (jusqu'à 0,5 µg.L-1), mais ceux-ci ne sont pas directement intégrés dans le jeu de données sur la base duquel est déterminé la PNEC (cf. discussion de ce point en page 14).
Substance(s) associée(s) :
Produits de dégradation :
4'-OH-DCF
5-OH-DCF
Acyl glucuronide of DCF
Sulfate conjugate of 4'-OH-DCF
Sulfate conjugate of 5-OH-DCF
Acyl glucuronide of 4'-OH-DCF
Acyl glucuronide of 5-OH-DCF
Acyl glucuronide of 3'-OH-DCF
Ether glucuronide of 4'-OH-DCF
Diclofenac methyl ester
Hydroxydiclofenac glucuronide (potentiellement actif)
(8-Chloro-9H-carbazol-1-yl)acetic acid
5-OH-DCF quinine imine
(Lahti et al., 2011 ; Mehinto et al., 2010 ; Gröning et al., 2007 ; Agüera et al., 2005)
[1] Les PBT sont des substances persistantes, bioaccumulables et toxiques et les vPvB sont des substances très persistantes et très bioaccumulables. Les critères utilisés pour la classification des PBT sont ceux fixés par l'Annexe XIII du règlement n° 1907/2006 (REACH).
[2] Les Polluants Organiques Persistants (POP) sont des substances persistantes (aux dégradations biotiques et abiotiques), fortement liposolubles (et donc fortement bioaccumulables), et volatiles (et peuvent donc être transportées sur de longues distances et être retrouvée de façon ubiquitaire dans l'environnement). Les critères utilisés pour la classification POP sont ceux fixés par l'Annexe 5 de la Convention de Stockholm placée sous l'égide du PNUE (Programme des Nations Unies pour l'Environnement).
[3] http://www.oekotoxzentrum.ch/expertenservice/qualitaetskriterien/vorschlaege/index_EN
Dangers
Description
VGE/NQE Importer
ORGANISMES AQUATIQUES
Dans les tableaux ci-dessous, sont reportés pour chaque taxon, uniquement les résultats des tests d'écotoxicité montrant la plus forte sensibilité à la substance. Toutes les données présentées ont fait l'objet d'un examen par l'INERIS.
Ces résultats d'écotoxicité sont principalement exprimés sous forme de NOEC (No Observed Effect Concentration), concentration sans effet observé, d'EC10 concentration produisant 10% d'effets et équivalente à la NOEC, ou de EC50, concentration produisant 50% d'effets. Les NOEC sont principalement rattachées à des tests chroniques, qui mesurent l'apparition d'effets sub-létaux à long terme, alors que les EC50 sont plutôt utilisées pour caractériser les effets à court terme.
ECOTOXICITE
Sauf mention contraire, l'ensemble des espèces ont été exposées à la forme commercialement disponible du diclofénac : le diclofénac sodium.
Suite à l'examen des études par l'INERIS, ont été invalidées pour tout ou partie4 ou non évaluées en raison d'un manque d'informations des données des études suivantes (et donc non répertoriées dans les tableaux ci-dessous) : Boström and Berglund, 2015, Cleuvers and heinrich, 2008 in Lee et al, 2011, Cleuvers et al, 2003, Cleuvers et al, 2003/2004, Cleuvers et al, 2004, Damanesco de Oliveira et al, 2015, DeLorenzo, 2008, Dietrich et al, 1999, Ericson et al, 2010, Ferrari et al, 2003/2004, Ferrari et al, 2004, Garric et al. 2006, Haap, 2008, Han et al., 2006, Islas-Flores et al, 2013, Lee et al, 2011, Lfw, 2003, Maletzki, 2010, Oskarsson et al., 2012, Oviedo-gomez et al., 2010, Quinn et al, 2011, Schmidt et al, 2011, Stepanova et al, 2013.
Compte tenu des capacités de dégradation rapide de la substance (photodégradation et biodégradation), ont été invalidées toutes les données issues d'essais réalisés en conditions statiques ou avec simple renouvellement (inférieur ou égal à 24h) du milieu et basées sur des concentrations nominales d'exposition uniquement. Cela concerne notamment de nombreuses études réalisées sur l'inhibition de la croissance des algues en aigu comme en chronique, ainsi que sur la mortalité et la reproduction des crustacés.
[4] « tout ou partie », dans le sens où il se peut que, par exemple, des données issues d'une même référence bibliographique soient invalidées pour une espèce, et non pour une autre, ou invalidées en aigu et non en chronique, ou encore que certaines EC50 soient invalidées mais que des NOEC soient retenues, etc.
ECOTOXICITE AQUATIQUE AIGUË
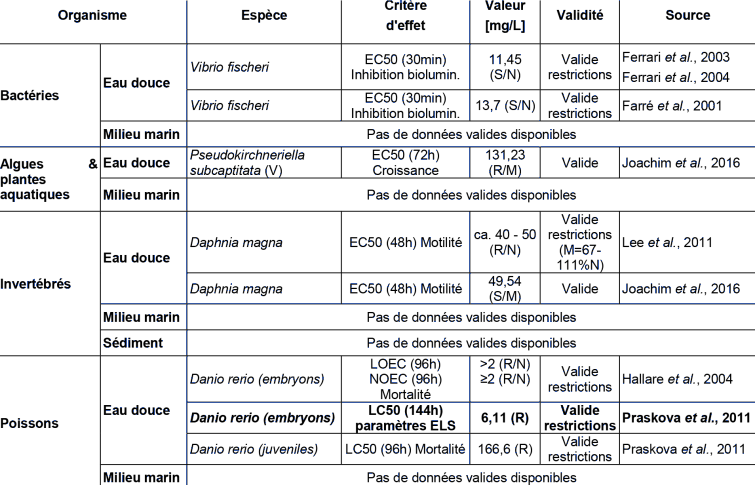
Signification des initiales suivant le nom d'espèce des algues et plantes aquatiques : VB pour algues vertes et bleues, V pour algues vertes, D pour diatomées et M pour macrophytes.
Régime des expérimentations réalisées : S = statique ; R = avec renouvellement du milieu toutes les 24h ou 48h ; FC = flux continu
Analyse des concentrations d'exposition dans le milieu : N = concentrations d'effets exprimées en concentrations nominales ; N* = concentrations d'effets exprimées en concentrations nominales, avec mesures des concentrations d'exposition réelles démontrant une perte de moins de 20% ; M = concentrations d'effets exprimées en concentrations effectivement mesurées.
ECOTOXICITE AQUATIQUE CHRONIQUE
Parmi les données reportées ci-dessous, une étude menée par l'INERIS (Joachim et al., 2016) a été réalisée dans un mésocosme pour étudier les effets du diclofénac sur un écosystème lotique incluant diverses espèces (macrophytes, macro-invertébrés et Epinoche à trois épines). Cette exposition a eu lieu en flux continu durant une période de 172 jours.
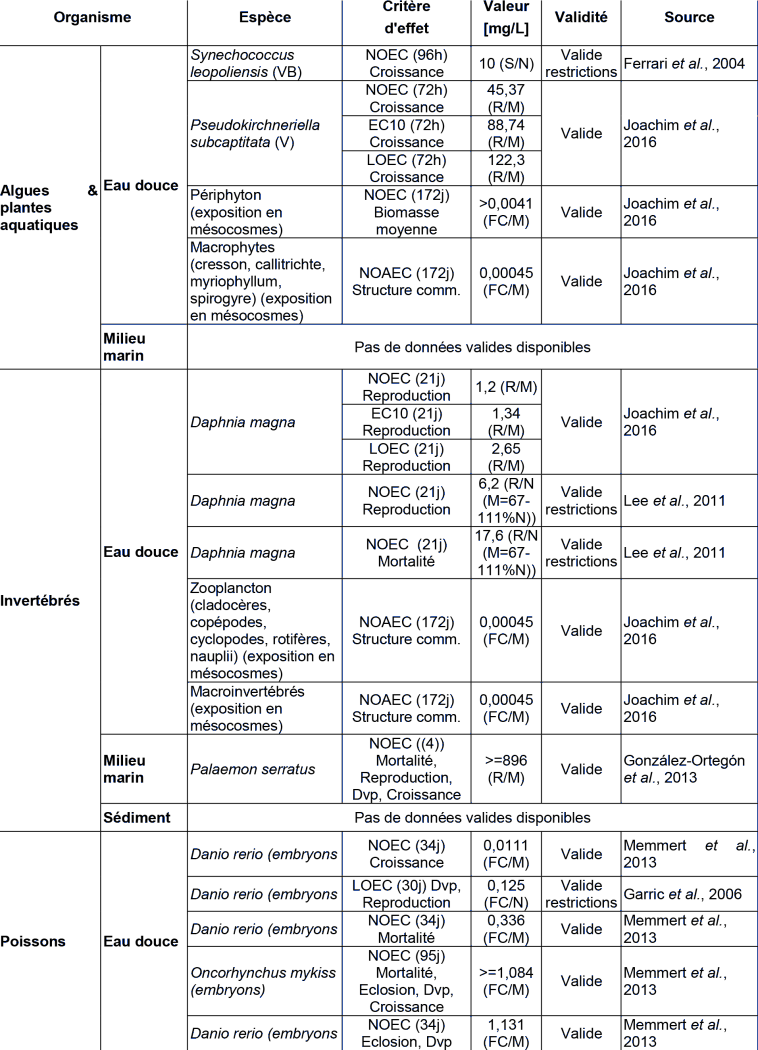
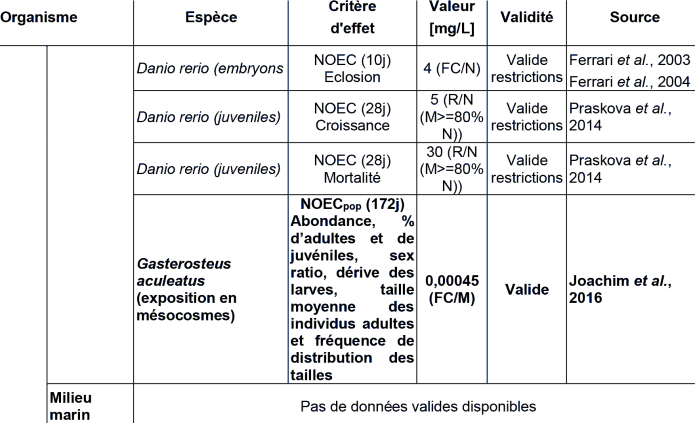
Signification des initiales suivant le nom d'espèce des algues et plantes aquatiques : VB pour algues vertes et bleues, V pour algues vertes, D pour diatomées et M pour macrophytes.
Régime des expérimentations réalisées : S = statique ; R = avec renouvellement du milieu toutes les 12h, 24h ou 48h ; FC = flux continu
Analyse des concentrations d'exposition dans le milieu : N = concentrations d'effets exprimées en concentrations nominales ; N* = concentrations d'effets exprimées en concentrations nominales, avec mesures des concentrations d'exposition réelles démontrant une perte de moins de 20% ; M = concentrations d'effets exprimées en concentrations effectivement mesurées.
Les études validées et ci-dessus reportées démontrent que lors d'expositions chroniques, le poisson est le taxon le plus sévèrement affecté par l'exposition au diclofénac sodium, y compris pour l'observation d'effets tels que la croissance. Il est à noter que la NOEC de 0,011 mg.L-1 reportée dans le tableau ci-dessus sur la base des travaux de Memmert et ses collaborateurs (2013) n'est pas celle retenue par les auteurs de cette publication mais celle retenue par l'INERIS sur la base de l'expertise des données brutes de celle-ci.
De nombreuses études, dont le détail n'est pas mentionné dans ce document, ont porté sur l'observation d'effets hépatiques et rénaux chez les poissons et plus spécifiquement sur la manifestation d'effets histologiques sur les tissus des organes internes (parmi lesquels Schwaiger et al., 2004 ; Triebskorn et al., 2007; Triebskorn et al., 2004 ; Hoeger et al., 2005 ; Mehinto et al., 2010). Ces publications rapportent des effets à des NOEC aussi basses que 1, voir 0,5 µg.L-1. La prise en compte de ces résultats a été très débattue (cf. Wolf et al., 2014) au motif de la pertinence écologique des effets histologiques.
Enfin, de très nombreuses autres données d'effets écotoxicologiques réalisées avec observations de critères dits « non conventionnels » sont également disponibles pour le diclofénac sodium (biomarqueurs d'effets, notamment cytochromes, espèces réactives à l'oxygènes et critères d'immunotoxicité).
Dans le cadre de la détermination de la présente Valeur Guide Environnementale, les effets non conventionnels n'ont pas été pris en compte afin de suivre les recommandations du guide technique européen pour la détermination des normes de qualité environnementale (E.C., 2011c). Pour ce qui est des effets histologiques, ils n'entrent pas directement en compte dans la détermination de la VGE pour les raisons suscitée, mais ils seront couverts par la VGE.
Valeurs de danger
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Synthèse
Biote
VGE/NQE Importer
EMPOISONNEMENT SECONDAIRE
Ce chapitre traite de la toxicité chronique induite par la substance sur les prédateurs via la consommation d'organismes aquatiques contaminés (appelés biote, i.e. poissons ou invertébrés vivant dans la colonne d'eau ou dans les sédiments). Il s'agit donc d'évaluer la toxicité chronique de la substance par la voie d'exposition orale uniquement.
Dans les tableaux ci-dessous, ne sont reportés pour chaque type de test que les résultats permettant d'obtenir les NOEC ou la valeur toxicologique de référence (VTR) les plus protectrices. N'ont été recherchés que des tests sur mammifères ou oiseaux exposés par voie orale (exposition par l'alimentation ou par gavage). Toutes les données présentées ont été validées par l'Agence Européenne des Médicaments (EMA5).
Les résultats de toxicité sont principalement donnés sous forme de doses journalières : NOAEL (No Observed Adverse Effect Level), ou LOAEL (Lowest Observed Adverse Effect Level). NOAEL et LOAEL sont exprimées en termes de quantité de substance administrée par unité de masse corporelle de l'animal testé, et par jour.
Pour calculer la norme de qualité liée à l'empoisonnement secondaire des prédateurs, il est nécessaire de connaître la concentration de substance dans le biote n'induisant pas d'effets observés pour les prédateurs (exprimée sous forme de NOEC). Il est possible de déduire une NOEC à partir d'une NOAEL grâce à des facteurs de conversion empiriques variables selon les espèces testées. Les facteurs utilisés ici sont ceux recommandés par le guide technique européen pour la détermination de normes de qualité (E.C., 2011c). Les valeurs de ces facteurs de conversion dépendent de la masse corporelle des animaux et de leur consommation journalière de nourriture. Celles-ci peuvent donc varier d'une façon importante selon le niveau d'activité et le métabolisme de l'animal, la valeur nutritive de sa nourriture, etc. En particulier elles peuvent être très différentes entre un animal élevé en laboratoire et un animal sauvage.
Afin de couvrir ces sources de variabilité, mais aussi pour tenir compte des autres sources de variabilité ou d'incertitude (variabilité inter et intra-espèces, extrapolation du court terme au long terme, etc.) des facteurs d'extrapolation sont nécessaires pour le calcul de la QSbiota sec pois. Les valeurs recommandées pour ces facteurs d'extrapolation sont données dans le guide technique européen pour la détermination des normes de qualité environnementale (E.C., 2011c). Un facteur d'extrapolation supplémentaire (AFdose-réponse) est utilisé dans le cas où la toxicité a été établie à partir d'une LOAEL plutôt que d'une NOAEL.
[5] L'Agence Européenne des Médicaments (EMA) a porté jusqu'en 2004 le nom d'Agence Européenne pour l'Evaluation des Médicaments (European Agency for the Evaluation of Medicinal Products : EMEA).
Les données obtenues sur les mammifères terrestres et les oiseaux, utilisées pour la détermination des valeurs guides pour la protection des prédateurs vis-à-vis de l’empoisonnement secondaire, sont répertoriées dans les tableaux ci-dessous.
ECOTOXICITE POUR LES VERTEBRES TERRESTRES
TOXICITE ORALE POUR LES MAMMIFERES


Parmi les études de toxicité chronique présentées dans le tableau ci-dessus, celle rapportant l'effet le plus sensible est l'étude de 90 jours chez le chien (Cité dans le rapport EMEA, 2003). Dans cette étude, un NOAEL de 0,3 mg/kg pc/j..
Concernant les études sur la reproduction, les niveaux à retenir sont similaires avec une valeur minimale de 0,25 mg/kg pc/j pour l'étude deux générations chez le rat, soit une NOEC de 2,5 mg/kgbiot, (EMEA, 2003).
TOXICITE ORALE POUR LES OISEAUX

Valeurs écotoxicologiques
Introduction
Dans cette rubrique, sont reportées des valeurs de référence pour la protection des écosystèmes aquatiques et de la santé humaine via l’environnement.
Dans cette rubrique, sont reportées des valeurs de référence pour la protection des écosystèmes aquatiques et de la santé humaine via l’environnement.
Elles peuvent avoir un statut de « Valeur réglementaire » si elles sont issues
- de réglementations européennes et issues par exemple de dossiers d’évaluation des risques dans le cadre de processus d’autorisation de mise sur le marché des substances chimiques (c’est le cas des Concentrations Prédites Sans Effet pour l’environnement (PNEC) issues des dossiers réglementaires sous REACh ou dans le cas de la réglementation des produits biocides) ou issues de « Normes de Qualité Environnementale » (NQE) de la Directive Cadre européenne sur l’Eau (DCE) ;
- de réglementations françaises telles que les arrêtés de mise en application de la DCE à l’échelle nationale.
Elles peuvent être des « Valeurs guides » lorsque ce sont des propositions scientifiques de l’INERIS qui ne sont pas reportées dans des textes réglementaires. C’est le cas de toutes les valeurs établies par l’INERIS pour guider l’évaluation de la qualité des milieux aquatiques pour les substances qui n’ont pas, ou pas encore, un statut réglementaire dans le contexte de la DCE.
Les « Valeurs Guides Environnementales » (VGE) et les « Normes de Qualité Environnementale » (NQE) sont les outils consacrés pour l’évaluation de la qualité des eaux de surface, dont l’établissement est basé sur une même méthodologie européenne dédiée (E.C., 2018).
Leur construction, d’un point de vue méthodologique, est donc similaire.
Valeurs guides
Description
VGE/NQE Importer
NORMES DE QUALITE POUR LA COLONNE D'EAU
Les normes de qualité pour les organismes de la colonne d'eau sont calculées conformément aux recommandations du guide technique européen pour la détermination des normes de qualité environnementale (E.C., 2011c). Elles sont obtenues en divisant la plus faible valeur de NOEC ou d'EC50 valide par un facteur d'extrapolation (AF, Assessment Factor).
La valeur de ce facteur d'extrapolation dépend du nombre et du type de tests pour lesquels des résultats valides sont disponibles. Les règles détaillées pour le choix des facteurs sont données dans le guide technique européen pour la détermination des normes de qualité environnementale (E.C., 2011c).
En ce qui concerne les organismes marins, selon le guide technique pour la détermination de normes de qualité environnementales (E.C., 2011c), la sensibilité des espèces marines à la toxicité des substances organiques peut être considérée comme équivalente à celle des espèces dulçaquicoles, à moins qu'une différence ne soit montrée.
![]()
Une concentration annuelle moyenne est déterminée pour protéger les organismes de la colonne d'eau d'une possible exposition prolongée.
Pour le diclofénac, on dispose de données pour les algues et plantes aquatiques, les crustacés et les poissons lors d'essais en expositions aiguës et chroniques. De plus, en exposition chronique, des données sont disponibles pour les rotifères et les échinodermes. Les données sans effet les plus faibles sont obtenues pour l'étude réalisée en mésocosmes sur 172 jours, avec des NOEC population et communauté de 0,45 10-3 mg.L-1. Compte tenu de la complétude de cette étude (milieu mésocosme, effets communauté et populationnel observés, durée d'exposition), un facteur d'extrapolation de 3 s'applique à cette NOEC, conformément au guide technique européen pour la détermination des normes de qualité environnementale (E.C., 2011c). L'INERIS propose donc la valeur suivante :
![]()
Cette proposition d'AA-QSwater_eco de 0,15 µg.L-1 couvre les potentielles altérations histologiques observées par certains auteurs à 1, voir 0,5 µg.L-1.
En ce qui concerne les organismes marins, le jeu de données disponibles pour le diclofénac ne permet pas de mettre en évidence une différence de sensibilité entre les espèces marines et dulçaquicoles. Pour le milieu marin, le facteur d'extrapolation appliqué doit prendre en compte les incertitudes additionnelles telles que la sous-représentation des taxons clés et une diversité d'espèces plus importante. Des données valides sont disponibles pour un seul taxon additionnel marin (échinodermes), les crustacés étant déjà représentés dans le jeu de données d'eau douce. Ainsi, conformément au guide technique européen pour la détermination des normes de qualité environnementale (E.C., 2011c) un facteur d'extrapolation additionnel de 5 s'applique pour déterminer la AA-QSmarine_eco, par rapport à l'eau douce. L'INERIS propose donc la valeur suivante :
![]()
Cette proposition d'AA-QSmarine_eco de 0,05 µg.L-1 couvre les potentielles altérations histologiques observées par certains auteurs à 1, voir 0,5 µg.L-1.
- •Concentration Maximum Acceptable (MAC et MACmarine)
La concentration maximale acceptable est calculée afin de protéger les organismes de la colonne d'eau de possibles effets de pics de concentrations de courtes durées (E.C., 2011c).
Pour le diclofénac, on dispose de données pour plus de 3 niveaux trophiques (algues, plantes aquatiques, rotifères, crustacés, poissons). Un facteur d'extrapolation de 10 s'applique donc, conformément au guide technique européen pour la détermination des normes de qualité environnementale (E.C., 2011c), sur la plus faible EC50 disponible dans le jeu de données. L'INERIS propose donc la valeur suivante :
![]()
Cette proposition de MAC couvre les effets intervenant potentiellement sur les stades précoces de la vie chez les poissons entre 2 et 6 mg.L-1 (NOECmortalité embryons ≥ 2 mg.L-1 selon Hallare et al., 2004).
En ce qui concerne les organismes marins, le jeu de données disponible pour le diclofénac ne permet pas de mettre en évidence une différence de sensibilité entre les espèces marines et dulçaquicoles. Pour le milieu marin, le facteur d'extrapolation appliqué doit prendre en compte les incertitudes additionnelles telles que la sous-représentation des taxons clés et une diversité d'espèces plus importante. Aucune donnée pour un taxon additionnel marin n'étant disponible par rapport au jeu de données d'eau douce, conformément au guide technique européen pour la détermination des normes de qualité environnementale (E.C., 2011c), un facteur d'extrapolation de 1000 s'applique pour déterminer la MACmarine. L'INERIS propose donc la valeur suivante :
![]()
Cette proposition de MACmarine couvre les effets intervenant potentiellement sur les stades précoces de la vie chez les poissons entre 2 et 6 mg.L-1 (NOECmortalité embryons≥ 2 mg.L-1, selon Hallare et al., 2004).
![]()
NORME DE QUALITE EMPOISONNEMENT SECONDAIRE (QSBIOTA_SEC POIS)
La norme de qualité pour l'empoisonnement secondaire (QSbiota sec pois) est calculée conformément aux recommandations du guide technique européen pour la détermination des normes de qualité environnementale (E.C., 2011c). Elle est obtenue en divisant la plus faible valeur de NOEC valide par les facteurs d'extrapolation recommandés (E.C., 2011c).
Pour le diclofénac, un facteur de 30 est appliqué car la NOEC retenue (2,5 mg.kg-1biota) correspond à un test sur la reproduction des rats, sur 2 générations. On obtient donc :
![]()
Cette valeur de norme de qualité pour l'empoisonnement secondaire peut être ramenée :
- •à une concentration dans l'eau douce selon la formule suivante :
- •à une concentration dans l'eau marine selon la formule suivante :
![]()
Avec :
BCF : facteur de bioconcentration,
BMF1 : facteur de bioamplification,
BMF2 : facteur de bioamplification additionnel pour les organismes marins.
Ce calcul tient compte du fait que la substance présente dans l'eau du milieu peut se bioaccumuler dans le biote. Il donne la concentration à ne pas dépasser dans l'eau afin de respecter la valeur de la norme de qualité pour l'empoisonnement secondaire déterminée dans le biote.
La bioaccumulation tient compte à la fois du facteur de bioconcentration (BCF, ratio entre la concentration dans le biote et la concentration dans l'eau) et du facteur de bioamplification (BMF, ratio entre la concentration dans l'organisme du prédateur en bout de chaîne alimentaire, et la concentration dans l'organisme de la proie au début de la chaîne alimentaire). En l'absence de valeurs mesurées pour le BMF, celles-ci peuvent être estimées à partir du BCF selon le tableau 4-6, page 123, du guide technique européen pour la détermination des normes de qualité environnementale (E.C., 2011c).
Ce calcul n'est donné qu'à titre indicatif. Il fait en effet l'hypothèse qu'un équilibre a été atteint entre l'eau et le biote, ce qui n'est pas véritablement réaliste dans les conditions du milieu naturel. Par ailleurs il repose sur un facteur de bioaccumulation qui peut varier de façon importante entre les espèces considérées.
Pour le diclofénac, un BCF de 10 et un BMF1 = BMF2 de 1 (cf.E.C., 2011c) ont été retenus. On a donc :
![]()
![]()
NORME DE QUALITE POUR LA SANTE HUMAINE VIA LA CONSOMMATION DES PRODUITS DE LA PECHE (QSBIOTA_HH)
La norme de qualité pour la santé humaine est calculée de la façon suivante (E.C., 2011c):
![]()
Cons. Journ. Moy. [kgbiota/j]
Ce calcul tient compte de :
- un facteur correctif de 10% (soit 0,1) : la VTR donnée ne tient compte en effet que d'une exposition par voie orale, et pour la consommation de produits de la pêche uniquement. Mais la contamination peut aussi se faire par la consommation d'autres sources de nourriture, par la consommation d'eau, et d'autres voies d'exposition sont possibles (inhalation ou contact cutané). Le facteur correctif de 10% (soit 0,1) permet de rendre l'objectif de qualité plus sévère d'un facteur 10 afin de tenir compte de ces autres sources de contamination possibles.
- la valeur toxicologique de référence (VTR), correspondant à une dose totale admissible par jour ; pour cette substance elle sera considérée égale à 0,5 µg/kgcorporel/j (cf. tableau ci-dessus),
- un poids corporel moyen de 70 kg,
- Cons. Journ. Moy : une consommation journalière moyenne de produits de la pêche (poissons, mollusques, crustacés) égale à 115 g par jour.
Ce calcul n'est donné qu'à titre indicatif. Il peut être inadapté pour couvrir les risques pour les individus plus sensibles ou plus vulnérables (masse corporelle plus faible, forte consommation de produits de la pêche, voies d'exposition individuelles particulières). Le facteur correctif de 10% n'est donné que par défaut, car la contribution des différentes voies d'exposition varie selon les propriétés de la substance (et en particulier sa distribution entre les différents compartiments de l'environnement), ainsi que selon les populations considérées (travailleurs exposés, exposition pour les consommateurs/utilisateurs, exposition via l'environnement uniquement). L'hypothèse cependant que la consommation des produits de la pêche ne représente pas plus de 10% des apports journaliers contribuant à la dose journalière tolérable apporte une certaine marge de sécurité (E.C., 2011c).
Pour le diclofénac, le calcul aboutit à :
![]()
Comme pour l'empoisonnement secondaire, la concentration correspondante dans l'eau du milieu peut être estimée en tenant compte de la bioaccumulation de la substance:
- •à une concentration dans l'eau douce selon la formule suivante :
- •à une concentration dans l'eau marine selon la formule suivante :
![]()
Pour le diclofénac, on obtient donc:
![]()
![]()
NORME DE QUALITE POUR LA SANTE HUMAINE VIA L'EAU DE BOISSON (QSdw_hh)
En principe, lorsque des normes de qualité dans l'eau de boisson existent, soit dans la Directive 98/83/CE (C.E., 1998), soit déterminées par l'OMS, elles peuvent être adoptées. Les valeurs réglementaires de la Directive 98/83/CE doivent être privilégiées par rapport aux valeurs de l'OMS qui ne sont que de simples recommandations.
Il faut signaler que ces normes réglementaires ne sont pas nécessairement établies sur la base de critères (éco)toxicologiques (par exemple les normes pour les pesticides avaient été établies par rapport à la limite de quantification analytique de l'époque pour ce type de substance, soit 0,1 µg.L-1). Pour les substances pharmaceutiques, la Directive 98/83/CE ne fixe pas de valeur limite.
La valeur seuil provisoire pour l'eau de boisson est calculée de la façon suivante (E.C., 2011c):
![]()
Ce calcul tient compte de:
- la valeur toxicologique de référence (VTR), correspondant à une dose totale admissible par jour ; pour cette substance elle sera considérée égale à 0,5 µg/kgcorporel/j (cf. tableau ci-dessus),
- Cons.moy.eau [L.j-1] : une consommation d'eau moyenne de 2 L par jour,
- un poids corporel moyen de 70 kg,
- un facteur correctif de 10% (soit 0,1) afin de tenir compte de ces autres sources de contamination possibles.
L'eau de boisson est obtenue à partir de l'eau brute du milieu après traitement pour la rendre potable. La fraction éliminée lors du traitement dépend de la technologie utilisée ainsi que des propriétés de la substance.
Ainsi, la norme de qualité correspondante dans l'eau brute se calcule de la manière suivante :
![]()
En l'absence d'information, on considèrera que la fraction éliminée est nulle et le critère pour l'eau de boisson s'appliquera alors à l'eau brute du milieu. Par ailleurs, on rappellera que ce calcul n'est donné qu'à titre indicatif et peut s'avérer inadéquat pour certaines substances et certaines populations.
Pour le diclofénac, on obtient :
![]()
![]()
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Synthèse
VGE/NQE Importer
VALEUR GUIDE POUR LES ORGANISMES BENTHIQUES (QSSED ET QSSED-MARIN)
Un seuil de qualité dans le sédiment est nécessaire (i) pour protéger les espèces benthiques et (ii) protéger les autres organismes d'un risque d'empoisonnement secondaire résultant de la consommation de proies provenant du benthos. Les principaux rôles des normes de qualité pour les sédiments sont de :
- Identifier les sites soumis à un risque de détérioration chimique (la norme sédiment est dépassée)
- Déclencher des études pour l'évaluation qui peuvent conduire à des études plus poussées et potentiellement à des programmes de mesures
- Identifier des tendances à long terme de la qualité environnementale (Art. 4 Directive 2000/60/CE).
Aucune information d'écotoxicité pour les organismes benthiques n'a été trouvée dans la littérature pour les organismes aquatiques.
A défaut, une valeur guide pour le sédiment peut être calculée à partir du modèle de l'équilibre de partage.
Ce modèle suppose que:
- il existe un équilibre entre la fraction de substances adsorbées sur les particules sédimentaires et la fraction de substances dissoutes dans l'eau interstitielle du sédiment,
- la fraction de substances adsorbées sur les particules sédimentaires n'est pas biodisponible pour les organismes et que seule la fraction de substances dissoutes dans l'eau interstitielle est susceptible d'impacter les organismes,
- la sensibilité intrinsèque des organismes benthiques aux toxiques est équivalente à celle des organismes vivant dans la colonne d'eau. Ainsi, la norme de qualité pour la colonne d'eau peut être utilisée pour définir la concentration à ne pas dépasser dans l'eau interstitielle.
Une valeur guide de qualité pour le sédiment peut être alors calculée selon l'équation suivante (E.C., 2011c) :
![]()
Avec
RHOsed : masse volumique du sédiment en [Kgsed.m-3sed]. En l'absence d'une valeur exacte, la valeur générique proposée par le document guide technique européen pour la détermination des normes de qualité environnementale (E.C., 2011c) est utilisée : 1300 kg.m-3 .
Ksed-eau : coefficient de partage sédiment/eau en m3/m3 . En l'absence d'une valeur exacte, les valeurs génériques proposées par le guide technique européen pour la détermination des normes de qualité environnementale (E.C., 2011c) sont utilisées. Le coefficient est alors calculé selon la formule suivante : 0,8 + 0,025 * Koc soit Ksed-eau = 2,8 – 138 m3/m3
Pour le diclofénac, on obtient :
![]()
QSsed wet weight = 0,321 µg.kg-1poids humide
La concentration correspondante en poids sec peut être estimée en tenant compte du facteur de conversion suivant :
![]()
![]()
Avec Fsolidesed : fraction volumique en solide dans les sédiments en [m3solide/m3susp]. En l'absence d'une valeur exacte, la valeur générique proposée par le document guide technique européen pour la détermination des normes de qualité environnementale (E.C., 2011c) est utilisée : 0,2 m3/m3 .
RHOsolide : masse volumique de la partie sèche en [kgsolide/m3solide]. En l'absence d'une valeur exacte, la valeur générique proposée par le document guide technique européen pour la détermination des normes de qualité environnementale (E.C., 2011c) est utilisée : 2500 kg.m-3 .
Pour le diclofénac, la concentration correspondante en poids sec est :
QSsed dry weight = QSsed wet weight * 2,6 = 0,321 * 2,6 = 0,836 µg.kg-1sed poids sec
Selon la même approche que pour le sédiment d'eau douce, une valeur guide de qualité pour le sédiment marin peut être calculée selon la formule suivante :
![]()
Pour le diclofénac, on obtient :
![]()
QSsed-marin wet weight = 0,064 µg.kg-1poids humide
La concentration correspondante en poids sec est alors la suivante:
QSsed-marin dry weight = 0,167 µg.kg-1sed poids sec
Le log Kow de la substance étant inférieur à 5, un facteur additionnel de 10 n'est pas jugé nécessaire.
Il faut rappeler que les incertitudes liées à l'application du modèle de l'équilibre de partage sont importantes. Les sédiments naturels peuvent avoir des propriétés très variables en termes de composition (nature et quantité de matières organiques, composition minéralogique), de granulométrie, de conditions physico-chimiques, de conditions dynamiques (taux de déposition/taux de resuspension). Par ailleurs ces propriétés peuvent évoluer dans le temps en fonction notamment des conditions météorologiques et de la morphologie de la masse d'eau. Si bien que le partage entre la fraction de substance adsorbée et la fraction de substance dissoute peut être extrêmement variable d'un sédiment à un autre et l'hypothèse d'un équilibre entre ces deux fractions ne semble pas très réaliste pour des conditions naturelles.
Par ailleurs, certains organismes benthiques peuvent ingérer les particules sédimentaires, et donc être contaminés par la fraction de substance adsorbée sur ces particules, ce qui n'est pas pris en compte par la méthode.
![]()
PROPOSITION DE VALEUR GUIDE ENVIRONNEMENTALE (VGE)
Elle est définie à partir de la valeur la plus protectrice parmi tous les compartiments étudiés.
![]()
La norme de qualité pour la protection des organismes aquatiques est la valeur la plus faible retenue pour la détermination de la norme de qualité environnementale pour le diclofénac, soit une valeur de 0,15 µg.L-1 pour les eaux douces et 0,05 µg.L-1 pour les eaux estuariennes et marines.
![]()
Valeurs réglementaires
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Bibliographie
Données technico-économiques
Dernière vérification le 29/03/2024
Tableaux de synthèse
Généralités
| CAS | 15307-86-5 |
|---|---|
| SANDRE | 5349 |
| Substance prioritaire dans le domaine de l’eau (DCE) | non |
| Substance soumise à autorisation dans Reach | non |
| Substance soumise à restriction dans Reach | non |
| Substance extrêmement préoccupante (SVHC) | non |
| Réglementations |
FTE 2015 Importer Les principaux textes réglementaires sont concernant le diclofenac présentés ci-après.
Les principaux textes réglementaires concernant les conditions d'autorisation de mise sur le marché des produits pharmaceutiques à usage humain et à usage vétérinaire sont :
Selon les deux directives 2001/83/CE et 2001/82/CE, une évaluation du risque environnemental est nécessaire pour toutes les demandes d'autorisation de mise sur le marché pour les médicaments à usage humain et vétérinaire. Une procédure d'évaluation du risque environnemental a été développée par l'Agence Européenne des Médicaments pour les nouveaux médicaments mis sur le marché communautaire. Il existe deux guides d'application pour les pharmaceutiques : un à usage humain3 (prenant effet au 1er décembre 2006) et un usage vétérinaire4 (prenant effet au 1er décembre 2007 et révisé au 1er mars 2009). Ces textes considèrent les risques pour l'environnement associés à l'utilisation, le stockage et le rejet des médicaments. Soulignons que les risques associés à leur production ne sont pas mentionnés. De plus, le champ de cette directive ne concerne que les nouveaux médicaments ainsi que ceux concernés par une modification d'importance majeure (Bouvier et al., 2010). Selon la directive 2003/4 du 28 janvier 2003 concernant l'accès du public à l'information en matière d'environnement, il est donc possible d'accéder à une partie de cette évaluation (dans la limite du secret industriel et commercial). Bouvier et al. (2010) répertorient, dans l'annexe 11 de leur rapport, les médicaments présentant un chapitre Ecotoxicité/évaluation du risque environnemental sur le site de l'EMA : Le diclofenac ne fait pas partie de ces derniers. Ces directives spécifient également que, au cas par cas, des mesures appropriées seront prises pour limiter l'impact environnemental de ces substances. Il est également précisé que, par contre, cet impact ne devrait en aucun cas être un critère d'interdiction à la mise sur le marché de ces substances. Produits pharmaceutiques et REACHConcernant les activités de production, les dispositions du Règlement CE n°1907/2006 REACH ne sont pas applicables aux substances utilisées dans les médicaments à usage humain et vétérinaire excepté pour les titres suivants :
[3] http://www.ema.europa.eu/docs/en_GB/document_library/Scientific_guideline/2009/10/WC500003978.pdf [4] http://www.ema.europa.eu/docs/en_GB/document_library/Scientific_guideline/2009/10/WC500004386.pdf Produits pharmaceutiques et Directive Cadre sur l'EauLe diclofenac n'est pas mentionné dans la liste des substances prioritaires de la Directive Cadre sur l'Eau (Directive 2000/60 du 23 octobre 2000) et il n'a pas été retenu en 2008 parmi les substances soumises à révision pour leur possible identification comme substance prioritaire ou comme substance dangereuse prioritaire (Annexe III – Directive 2008/105/EC du Parlement européen et du Conseil établissant des normes de qualité environnementale dans le domaine de l'eau). De la même façon, le diclofenac n'est pas mentionné dans l'arrêté du 08/07/10 établissant la liste des substances prioritaires et fixant les modalités et délais de réduction progressive et d'élimination des déversements, écoulements, rejets directs ou indirects respectivement des substances prioritaires et des substances dangereuses visées à l'article R. 212-9 du code de l'environnement. La Commission Européenne, en janvier 2012, a proposé d'ajouter quinze substances chimiques à la liste des trente-trois polluants qui sont surveillés et contrôlés dans les eaux de surface de l'Union Européenne. Il s'agit d'une nouvelle mesure visant à améliorer la qualité des eaux des rivières, lacs et eaux côtières. Parmi ces quinze substances figurent des substances pharmaceutiques dont le diclofenac (Commission Européenne, 2012). Produits pharmaceutiques et Installations ClasséesConcernant la réglementation des installations classées, l'industrie pharmaceutique est classée dans l'industrie des biens de consommation et regroupe 3 secteurs d'activité :
Les 2 derniers secteurs sont à l'usage de la médecine humaine et de la médecine vétérinaire. Produits pharmaceutiques et Eau potableLes eaux potables doivent répondre aux normes européennes transcrites en droit français dans le Code de la Santé Publique. Si les textes spécifient que l'eau de consommation humaine ne doit contenir aucun élément chimique ou microbiologique nuisible à la santé, aucun médicament ne figure dans la liste des paramètres à analyser (Académie de Pharmacie, 2008). Enfin, le diclofenac n'appartient pas à la liste de micropolluants concernés par la circulaire du 29 septembre 2010 relative à la surveillance de la présence de micropolluants dans les eaux rejetées au milieu naturel par les stations de traitement des eaux usées. AUTRESL'Anses a établi une hiérarchisation, vis-à-vis des risques de présence dans l'eau potable, des résidus de médicaments d'intérêt pour l'analyse des ressources et des eaux traitées (AFSSA, 2008). Trois critères de hiérarchisation ont été sélectionnés : le tonnage, l'activité et l'affinité pour l'eau. Sur les 210 molécules listées initialement pour les médicaments humains, 41 molécules, 11 métabolites et la caféine ont été classées prioritaires. Le diclofenac n'appartient pas à la liste des médicaments humains et de leurs métabolites actifs prioritaires à rechercher dans les eaux. On notera que cette hiérarchisation a servi de base à une campagne nationale de mesures de 45 substances pharmaceutiques (voir paragraphe 4.2.1). Besse et Garric (2008) ont également publié une méthodologie de priorisation, vis-à-vis des risques pour l'environnement, des produits pharmaceutiques basée sur trois étapes :
Ils ont ainsi retenu 40 molécules-mères et 11 métabolites dont le diclofenac. |
Production et utilisation
Production et ventes
Données économiques
FTE 2015 Importer
En 2009, la France était parmi les principaux producteurs européens de médicaments, après l'Allemagne et la Suisse comme le montre la Figure 1 ci-après.
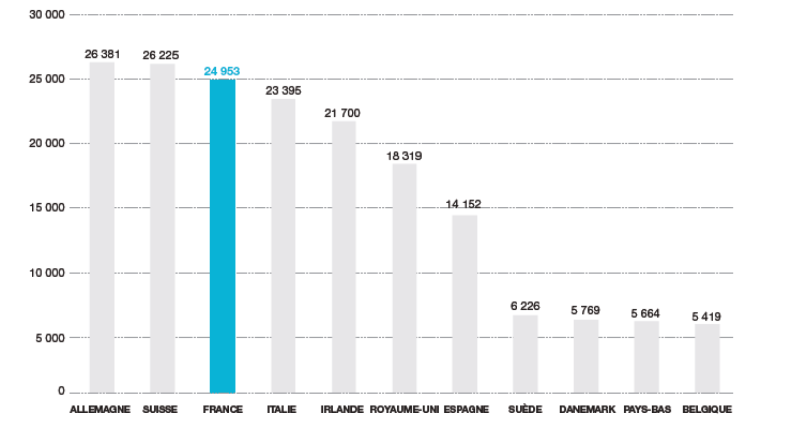
Figure 1. Production pharmaceutique en Europe : principaux pays producteurs européens en 2009 (en millions d'euros) (LEEM, 2011b).
Toutefois, nous n'avons pas identifié d'informations concernant une potentielle production française de diclofenac.
L'évolution des exportations et des importations françaises de médicaments est présentée sur la Figure 2 ci-après.
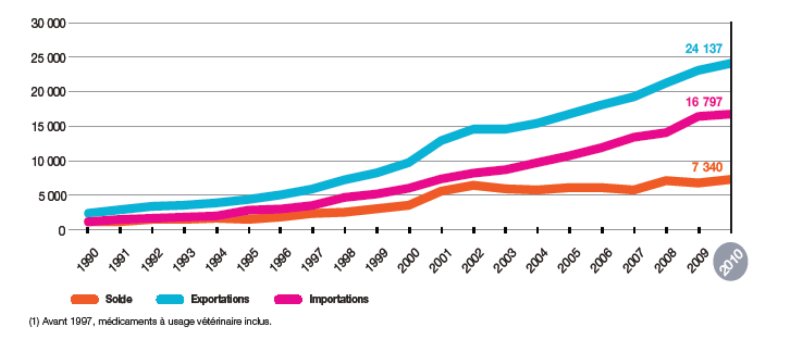
Figure 2. Evolution des exportations et des importations françaises de médicaments en millions d'euros (LEEM, 2011b).
Nous n'avons néanmoins pas d'information sur l'évolution des exportations/importations pour le diclofenac.
PROCEDES DE PRODUCTION DU DICLOFENAC
Deux mécanismes réactionnels permettent de synthétiser le diclofenac selon Buschmann, 2002.
Le premier à partir du N-Phényl-2,6 -dichloroaniline, développé par Moser et al. (1990), est présenté sur la Figure 3 ci-après :
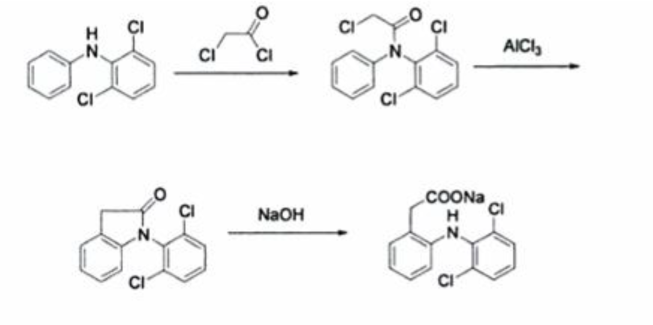
Figure 3. Synthèse du diclofenac par Moser et al. (1990).
Une autre synthèse à partir de l'acide chloro-2-benzoïque est également utilisée (citée par Buschmann, 2002) et est présentée sur la Figure 4 ci-après :
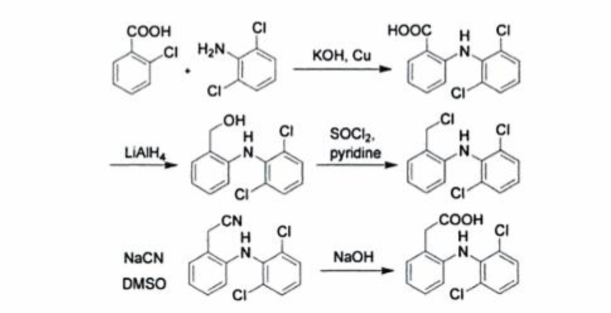
Figure 4. Synthèse du diclofenac (issu de Buschmann, 2002).
Lors de ce travail, nous n'avons pas identifié d'informations concernant la voie de synthèse utilisée en pratique.
Utilisations
SECTEURS D'UTILISATION
FTE 2015 Importer
DONNEES ECONOMIQUES
La France était le quatrième consommateur mondial de médicaments après les Etats-Unis (197 802 millions de dollars), le Japon (56 675 millions de dollars) et l'Allemagne (27 668 millions de dollars) avec 25 630 millions de dollars en 2006 (Académie de Pharmacie, 2008). En 2009, la France avec l'Allemagne est devenue le premier consommateur de médicaments au sein de l'Union Européenne aussi bien de médicaments à usage humain que de médicaments à usage vétérinaire (Bouvier et al., 2010). Concernant le marché des médicaments vétérinaires en Union Européenne, cela peut s'expliquer par l'importance de l'élevage français, tous cheptels confondus.
A défaut d'informations concernant les tonnages de médicament consommés en France, l'évolution du chiffre d'affaires en médicaments est présentée sur la Figure 5 ci-dessous.
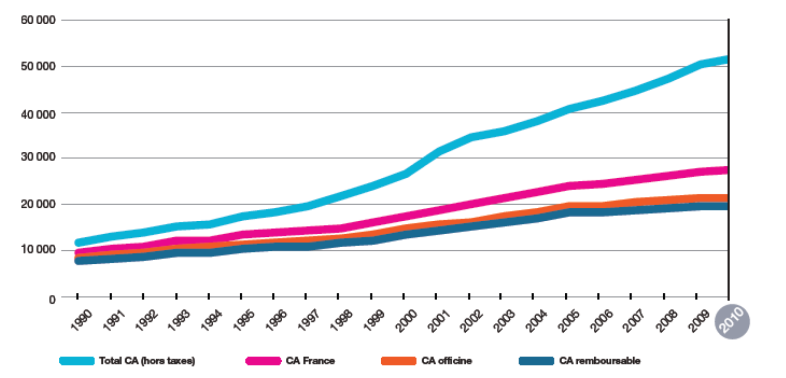
Figure 5. Evolution du chiffre d'affaires 5 (CA) concernant les médicaments (prix fabricant HT, millions d'euros) d'après LEEM, 2011b.
On constate ainsi une augmentation constante du chiffre d'affaires depuis 1990 pour atteindre 51 471 millions d'euros en 2010.
L'évolution de la consommation de médicaments en France depuis 1990 par les ménages est présentée sur le Tableau 3 ci-après. Cette consommation est rapportée en nombre d'unité. Le nombre d'unités (une unité équivaut à une boîte ou un flacon ou un tube…) est un indicateur de l'évolution de la consommation dans la mesure où il y a peu de changements de conditionnement ou de dosage. Cependant, une forte pathologie hivernale augmente le nombre de petits conditionnements consommés par rapport à une année moyenne (c'est le contraire pour une faible pathologie saisonnière). Par ailleurs, le développement récent des conditionnements trimestriels diminue artificiellement la consommation en volume (LEEM, 2011b).
Tableau 3. Evolution de la consommation de médicaments en France par les ménages en nombre d'unité (LEEM, 2011b).
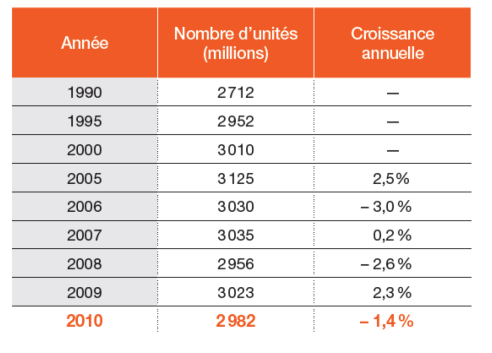
L'évolution du nombre d'unités de médicaments consommés en France ne suit pas de tendance nette depuis 2005. Celle-ci fluctue autour de + ou – 3 % environ.
L'évolution de la consommation des médicaments des ménages (en millions d'euros) est présentée dans le Tableau 4 ci-après.
Tableau 4. Evolution de la consommation des médicaments des ménages (y compris autres produits pharmaceutiques, produits sanguins, préparations magistrales, honoraires spéciaux du pharmacien d'officine mais hors médicaments hospitaliers) d'après LEEM (2010).
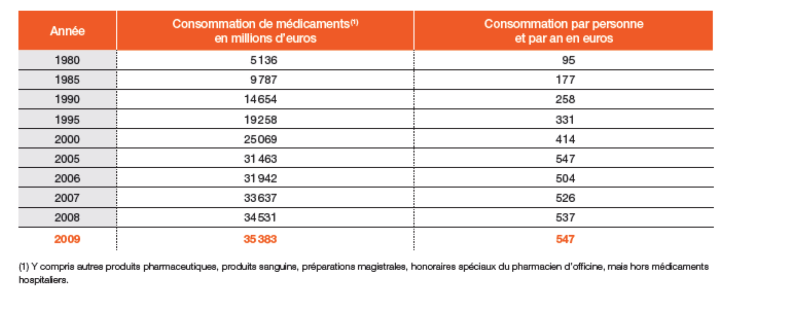
Rapportée à la population française, la consommation de médicaments et autres produits pharmaceutiques a été en moyenne de 547 euros par habitant en 2009. Il s'agit d'une moyenne qui recouvre une très grande diversité puisque ce sont surtout les personnes âgées et celles atteintes de maladies graves qui consomment le plus.
Les médicaments à usage humain les plus prescrits en France sont des antalgiques à base de paracétamol et des anti-inflammatoires (Dulio et Morin, 2009).
En 2004, la consommation française de diclofenac était de 9 896 kg (Besse et al., 2008). Celle-ci aurait augmenté de plus de 20 % en 2007 (rapport 2007/2004 environ égal à 1,27) d'après Besse (2010).
Selon une autre source (Sadezky et al., 2008) cohérente avec la précédente, la consommation moyenne annuelle française de diclofenac est de 10 tonnes/an (consommation calculée, dans le cadre du programme KNAPPE, à partir des données de 1999 à 2006).
Cela correspond à une consommation moyenne de 0,167 g en diclofenac par habitant et par an.
SECTEURS D'UTILISATION
Le diclofenac est principalement utilisé dans les médicaments à usage humain.
Concernant les médicaments à usage vétérinaire, cette substance n'est plus utilisée en France. Aucune spécialité à destination des animaux n'est recensée dans le dictionnaire des Médicaments Vétérinaires5 . D'une façon plus générale, les animaux sont extrêmement sensibles aux principes actifs des anti-inflammatoires non stéroïdiens humains6 . Selon le Professeur Enriquez, 2011, une gamme spécifique d'anti-inflammatoire pour les animaux a été ainsi développée. Néanmoins, l'usage du diclofenac à destination vétérinaire est encore recensé dans différents pays 7 .
A notre connaissance, il n'existe aucun usage non médical du diclofenac.
[5] http://www.wk-vet.fr/mybdd/index.php
[6] A titre d'exemple, la population de trois espèces de vautours a diminué jusqu'à 99 % en Inde en raison d'une large utilisation de diclofenac chez le bétail. En se nourrissant de carcasses d'animaux ainsi traités, les vautours développeraient une insuffisance rénale mortelle en absorbant de très fortes doses d'anti-inflammatoires non-stéroïdiens (The Economist. (2007). "Vultures." from http://www.economist.com/node/8521912?story_id=E1_RVNTJTN).
[7] http://www.oie.int/fileadmin/Home/fr/Publications_%20%26_Documentation/docs/pdf/Bull_2008-2-FRA.pdf
Rejets dans l’environnement
Émissions atmosphériques
FTE 2015 Importer
LES EMISSIONS INDUSTRIELLES DANS LE MILIEU ATMOSPHERIQUE
- Industrie du médicament
Il n'existe que très peu de données concernant les émissions vers le milieu naturel de composés pharmaceutiques par les usines de fabrication de ces produits. Il est généralement admis que les émissions de composés thérapeutiques sont proches de zéro dans le mode de fonctionnement normal des sites de fabrication, comme en témoignent les bonnes pratiques de fabrication et la régulation des émissions suivies par les industries pharmaceutiques, aussi bien au niveau des solvants que des résidus de composés (Velagaleti et al., 2002).
Lors de ce travail, nous n'avons pas identifié d'informations spécifiques concernant les rejets atmosphériques des usines de production de diclofenac. Néanmoins, celles-ci peuvent être considérées comme faibles voire négligeables.
Incinération des médicaments
Parmi les circuits de fin de vie du diclofenac, seule l'incinération est susceptible d'émettre cette substance vers l'atmosphère. Compte tenu du fait que les médicaments non utilisés (MNU) et les déchets médicamenteux hospitaliers sont incinérés dans des installations répondant aux normes environnementales les plus strictes, avec notamment des traitements de fumées, les rejets afférents devraient être a priori insignifiants (Académie de Pharmacie, 2008) et en particulier pour le diclofenac.
A noter que depuis le 1er janvier 2009, tous les médicaments collectés en pharmacie par l'association Cyclamed ne sont plus recyclés et redistribués mais incinérés.
LES EMISSIONS NON INDUSTRIELLES DANS LE MILIEU ATMOSPHERIQUE
Les rejets atmosphériques de médicaments concernent un nombre limité de molécules, mais essentiellement des anesthésiques volatils de type fluothane qui sont consommés en milieu hospitalier mais aussi des médicaments comme l'eucalyptol qui sont éliminés par voie pulmonaire (Académie de Pharmacie, 2008).
Concernant le diclofenac, les émissions dans l'air semblent très faibles (voir paragraphe 4.1.3).
Émissions vers les eaux
FTE 2015 Importer
LES EMISSIONS INDUSTRIELLES DANS LE MILIEU AQUATIQUE
Il n'existe que très peu de données concernant les émissions vers le milieu naturel de composés pharmaceutiques par les usines de fabrication de ces produits. Il est généralement admis que les émissions de composés thérapeutiques sont proches de zéro dans le mode de fonctionnement normal des sites de fabrication, comme en témoignent les bonnes pratiques de fabrication et la régulation des émissions suivies par les industries pharmaceutiques, aussi bien au niveau des solvants que des résidus de composés (Velagaleti et al., 2002).
Néanmoins, il n'est pas impossible que des rejets de substances pharmaceutiques puissent se produire. Une étude allemande rapporte une évaluation de rejets de 45 kg.j-1our de diclofenac dans le Rhin, à Mayence, à proximité de plusieurs sites de production (Ternes, 2001 cité par Académie de Pharmacie, 2008).
LES EMISSIONS NON INDUSTRIELLES DANS LE MILIEU AQUATIQUE
Dans la majorité des cas, les stations d'épuration constituent le premier réceptacle des rejets humains de substances pharmaceutiques. On y retrouve les rejets issus des agglomérations et les rejets plus spécifiques des structures hospitalières (Togola, 2006).
Les apports urbains sont très variables, selon les modes de consommation, voire par région (Bussi, 2000). D'autre part, selon les saisons, la consommation en substances, et donc les apports à la station varient (Castiglioni et al., 2005).
Les flux émis par les hôpitaux peuvent être conséquents. Si on considère en moyenne que la consommation domestique d'eau est d'environ 100 litres/personne/jour (Halling-Sørensen et al., 1998), la consommation en milieu hospitalier est estimée à 750 litres/lit/jour en France (Emmanuel et al., 2005). Généralement, ces effluents hospitaliers subissent un premier traitement dans une station d'épuration interne au complexe, avant de rejoindre les réseaux urbains et les stations d'épuration classiques (Togola, 2006).
A ce jour, nous n'avons pas identifié d'informations spécifiques à ce sujet concernant le diclofenac.
Rejets dans l'environnement
FTE 2015 Importer
Il existe différentes voies de rejet des médicaments dans l'environnement (Dulio et Morin, 2009 ; Académie de Pharmacie, 2008) :
- les rejets lors des procédés industriels de fabrication des substances (source mineure) ;
- les rejets directs des médicaments non utilisés via les déchets ménagers ou via les réseaux d'assainissement (source non négligeable) ;
- les rejets par excrétion suite à l'utilisation par le patient (source principale de contamination) ;
- les rejets d'élevages animaux (ne concerne pas le diclofénac).
Ayscough et al. (2002) résument les différentes voies possibles d'émissions de substances pharmaceutiques dans l'environnement (voir Figure 6 ci-après).
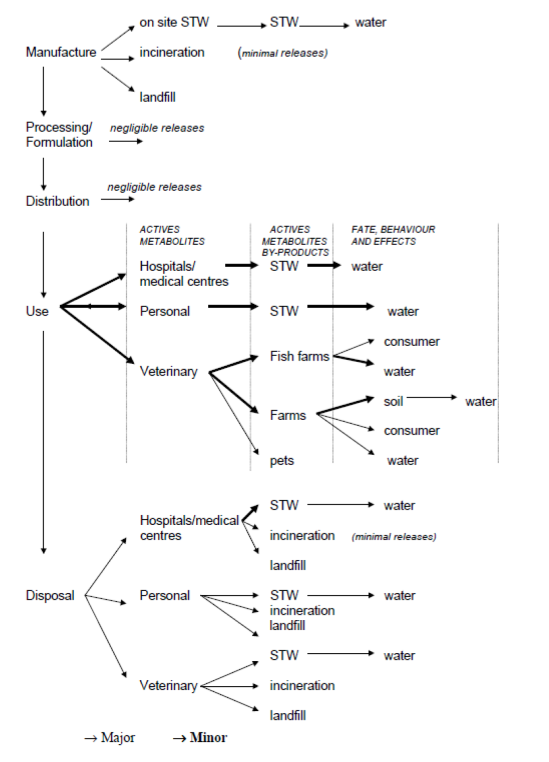
STW : Sewage treatment works – Stations de traitement des eaux usées
Figure 6. Voies de contamination de l'environnement par les médicaments (Ayscough et al., 2002).
A partir de ces sources, les principales voies d'apport aux eaux de surface sont les effluents d'eaux usées municipales, le lessivage et le ruissellement des terres agricoles ainsi que les activités aquacoles (Pépin, 2006).
Le diclofenac n'est pas présent naturellement dans l'environnement. Aucune émission non anthropique n'est donc observée.
Selon l'Académie de Pharmacie (2008), l'une des principales voies d'introduction des médicaments dans l'environnement est la dispersion des médicaments au travers des déchets ménagers. En effet, les médicaments jetés avec les déchets ménagers peuvent polluer les sols et les eaux en cas d'enfouissement en décharge (Togola et al., 2008).
En France, depuis 1995, une étude barométrique auprès du grand public est réalisée chaque année sur les comportements en matière de tri sélectif des MNU. L'étude est effectuée sur un panel de 1 000 personnes représentatif de la population française âgée de 18 ans et plus. En 2010, l'enquête confirme un niveau de tri élevé, puisque les ¾ des Français (74 %) déclarent déposer leurs Médicaments Non Utilisés chez le pharmacien. Ce chiffre est quasiment stable depuis dix ans (Cyclamed, 2010). En 2011, Cyclamed a fait réaliser une autre étude pour évaluer le « gisement » des médicaments non utilisés des médicaments français (Cyclamed, 2011). Cette enquête a permis d'évaluer un « gisement » en masse annuel de MNU des ménages français se situant entre 24 000 et 29 000 tonnes. Il en a été déduit que Cyclamed récupérait environ 50 % des MNU. On notera un certain écart entre les deux études. Néanmoins, comparativement au Royaume-Uni, une importante quantité des médicaments est envoyé en incinération et donc ne se retrouve pas dans les eaux de surface. Concernant le diclofenac, par un calcul « grossier » et en se basant sur une consommation de 10 tonnes/an, on peut estimer qu'entre 2,6 et 5 tonnes par an sont jetées dans les ordures ménagères ou dans les eaux usées.
Les pertes/fuites dans les réseaux d'assainissement, variant entre 5 et 25 %, peuvent également être à l'origine d'émissions de substances pharmaceutiques dans l'environnement. De plus, pendant des périodes de fortes pluies, si la capacité de traitement de la station d'épuration est dépassée, cela donne lieu à une émission incontrôlée de substances pharmaceutiques dans le milieu aquatique (Dulio et Morin, 2009 ; Académie de Pharmacie, 2008).
Les animaux d'élevage sont également une source d'émissions de substances pharmaceutiques dans l'environnement par les produits vétérinaires (notamment les antiparasitaires et les antibiotiques) (Togola et al., 2008). Néanmoins, comme nous l'avons vu précédemment, le diclofenac n'a plus d'usage vétérinaire en France.
Les sols peuvent être également contaminés par l'épandage sur les champs des boues des stations d'épuration (Académie de Pharmacie, 2008). L'Académie nationale de Pharmacie a fait un calcul concernant ces rejets avec pour hypothèses que :
- le rendement moyen d'élimination des médicaments est d'environ 60 % (via leur « capture » par les boues) ;
- un quart de ces produits « capturés » est stocké (soit 15 % du total des médicaments introduits dans les stations d'épuration) ;
- 50 % des boues de stations d'épuration font l'objet d'un épandage agricole.
La conclusion de ce calcul approximatif est qu'environ 7,5 % de tous les médicaments rejetés dans les eaux se retrouvent dans le milieu terrestre.
Sur cette base, on peut ainsi, toujours de manière grossière, évaluer la quantité de diclofenac émis dans le milieu terrestre via les boues d'épandage. Cette quantité serait de l'ordre de 195 à 375 kg par an pour une consommation de 10 tonnes/an.
FACTEURS D'EMISSIONS DES PARTICULIERS AVANT TRAITEMENT EN STATION D'EPURATION
Différents sources de la littérature ont estimé les facteurs d'émissions pour le diclofenac et cela, avant traitement en station d'épuration. Ces études sont présentées ci-après.
Radke et al. (2009) ont déterminé les bilans en masse de plusieurs produits pharmaceutiques acides sur une distance de 15 km le long d'une rivière située dans le nord de la Bavière, en Allemagne. Dans ce cadre, ils ont calculé un rejet horaire moyen en amont de la station d'épuration de 63 ± 38 g.j-1our en diclofenac, correspondant à un rejet par habitant de 870 ± 520 µg/hab/jour.
Kasprzyk-Hordern et al. (2009) ont estimé la consommation en différentes substances pharmaceutiques de communes du sud du Pays de Galles à partir des mesures réalisées à l'entrée de stations d'épuration et les données du National Health Service du Pays de Galles. Concernant le diclofenac, les valeurs varient entre 0,2 et 2,3 g.j-1our/1 000 habitants soit entre 200 à 2 300 µg.j-1our/hab.
Sadezky et al. (2008) reportent une consommation moyenne en diclofenac de 0,167 g par an et par habitant pour la France (valeurs estimées à partir des données recueillies entre 1999 et 2006) soit 457 µg.j-1our/hab.
Heberer et Feldmann, 2005 ont étudié la contribution d'un hôpital militaire et des ménages sur la charge totale en diclofenac et carbamazepine dans les effluents en entrée d'une station d'épuration municipale à Berlin. Au total, 4,4 kg de diclofenac par semaine (226 kg.an-1) sont déversés dans les eaux de surface par la station d'épuration, qui traite les eaux usées domestiques à la fois d'environ un million d'habitants et de grandes quantités d'effluents hospitaliers (environ 12 060 lits d'hôpital).
En résumé, les différents facteurs d'émission de diclofenac vers les stations d'épuration sont regroupés dans le Tableau 5 ci-après.
Tableau 5. Facteurs d'émission de diclofenac avant traitement.

FACTEURS D'EMISSIONS DES PARTICULIERS APRES TRAITEMENT EN STATION D'EPURATION
Des modélisations de concentrations dans les eaux de rivière ont été établies par Johnson et al. (2007) pour le diclofenac à partir des quantités consommées, de leur élimination chez l'homme et leur devenir potentiel dans les stations d'épuration d'un même bassin versant. Le facteur d'émissions utilisé, dans le cadre de la modélisation, pour les stations d'épuration (après traitement) est de 105 µg/hab/jour.
Miege et al. (2009) ont conçu une base de données afin d'évaluer l'occurrence et l'efficacité d'élimination des composés pharmaceutiques et cosmétiques dans les stations d'épuration. Ils ont répertorié 6 641 données concernant 184 composés, issues de 117 publications scientifiques (cf. paragraphe 4.2.1). De cette base de données, des concentrations moyennes en diclofenac en entrée et sortie dans les stations d'épuration (procédé à boues activées) ont été déterminées de 1,34 et 0,680 µg.L-1 respectivement soit un rendement moyen d'environ 50 %. En confrontant ce rendement d'élimination avec les facteurs d'émissions avant traitement présentés ci-dessus, on peut calculer, de façon grossière, des facteurs d'émissions après traitement (par boues activées) en station d'épuration. Ces chiffres sont présentés dans le Tableau 6 ci-après.
Tableau 6. Facteurs d'émissions de diclofenac après traitement par boues activées.

Le comportement du diclofenac a été décrit dans les différents compartiments de l'environnement. La photodégradation et la biodégradation ont été identifiées comme les principaux processus de dégradation de la substance (Jiskra et Hollender, 2008 ; Buser et al., 1998).
On notera que dans le rapport de l'Anses daté de juin 2010, l'annexe II présente, de façon générale, les différents processus influençant le comportement des résidus de médicaments dans l'environnement (AFSSA, 2010) sans précision spécifique par rapport au diclofenac.
Présence environnementale
Atmosphère
FTE 2015 Importer
Comme nous l'avons vu précédemment, les rejets médicamenteux vers l'atmosphère sont faibles (Académie de Pharmacie, 2008). La tension de vapeur et la constante d'Henry du diclofenac, respectivement de 8,17.10-6 Pa et constante de Henry de 1.10-10 , indiquent qu'il est très peu volatil et peu enclin à se diffuser vers l'air à partir des milieux terrestres et aquatiques (Jiskra et Hollender, 2008).
Dans l'atmosphère, le comportement des médicaments va être, comme pour la plupart des composés organiques, principalement contrôlé par les réactions avec les radicaux hydroxyles (OH) en influençant leur temps de résidence dans la troposphère (US EPA, 2000 cité par Pépin, 2006). De plus, d'après cette même source, la photolyse directe et les réactions avec les radicaux nitrates et avec l'ozone contribuent à leur élimination de l'atmosphère.
Le temps de demi-vie dans l'atmosphère du diclofenac a été calculé à 2 heures (HSDB, 2011).
Lors de ce travail, nous n'avons pas identifié d'informations spécifiques sur les concentrations en diclofenac dans l'atmosphère.
Aquatique
FTE 2015 Importer
Dans le milieu aquatique, le devenir des médicaments est fonction de leurs propriétés physico-chimiques et des conditions du milieu. Les facteurs physiques et chimiques locaux tels que le pH, la température, la dureté, la concentration en matières en suspension et le potentiel d'oxydoréduction expliquent en grande partie le comportement environnemental des médicaments dans l'eau (Pépin, 2006). Le diclofenac présente une solubilité de 2,37 mg.L-1 et est très peu volatil (pression de vapeur de 8,17.10-6 Pa et constante de Henry de 1.10-10) (Jiskra et Hollender, 2008).
Le diclofenac fait partie de la famille des acides carboxyliques et possède une constante pKa de 4,16, expliquant sa présence sous forme d'ions négativement chargés dans les eaux de pH supérieur à 5.
Bioaccumulation
Selon Stamm et al.(2008) cités par Jiskra et Hollender (2008), pour les produits pharmaceutiques polaires dont le coefficient de partage octanol-eau (log Kow) est inférieur à 4,5, la bioaccumulation n'est généralement pas significative. Concernant le diclofenac, ce coefficient est de 4,51 donc il est possible qu'il possède une tendance à la bioaccumulation.
Hydrolyse
Comme les produits pharmaceutiques sont principalement fabriqués pour être absorbés par voie orale, ils sont conçus de façon à être insensibles aux réactions chimiques comme l'hydrolyse (Andreozzi et al., 2003).
Photodégradation
Le processus de photodégradation se différencie entre deux mécanismes : photolyse directe et indirecte. En ce qui concerne la photolyse directe, la molécule pharmaceutique absorbe le rayonnement solaire, ce qui conduit à une rupture de la molécule. La photolyse indirecte implique des molécules naturelles (photo-sensibilisantes) tels que les nitrates générant des espèces réactives sous l'effet des radiations solaires.
La photodégradation dépendant de l'intensité lumineuse : Andreozzi et al. (2003) ont exposé des échantillons de diclofenac dilués dans l'eau à différentes intensités lumineuses, simulant différentes latitudes et les saisons. Ils ont montré que la situation géographique n'est pas vraiment importante pour l'efficacité de la photodégradation en été, mais que des différences importantes entre les différentes latitudes, en particulier en hiver, peuvent se produire. Un temps de demi-vie aquatique de 5 jours a été estimé pour le diclofenac à une latitude de 50°N et en hiver. De faibles intensités lumineuses au nord en hiver peuvent réduire l'efficacité de la photodégradation de façon drastique. Le spectre d'adsorption du diclofenac et du rayonnement UV se chevauche entre 300 à 330 nm. Bartels et von Tümpling (2007) ont constaté une diminution beaucoup plus lente du diclofenac par temps de pluie et nuageux par rapport aux jours ensoleillés. La photodégradation est également fonction de la profondeur de la colonne d'eau.
Buser et al. (1998) ont déterminé expérimentalement un temps de demi-vie par photodégradation inférieur à 1 heure pour le diclofenac dans les lacs (en octobre et à une latitude 47° N) montrant ainsi que le processus de photodégradation pouvait contribuer à l'élimination rapide du diclofenac dans les milieux.
Andreozzi et al. (2003) ont également étudié le rôle des molécules naturelles photosensibilisantes. Les résultats pour le diclofenac ont montré un temps de demi-vie jusqu'à 1,6 fois plus rapide pour des concentrations en nitrate de 10 mg.L-1. D'autre part, une concentration en acide humique de 5 mg.L-1 réduit le taux de photodégradation du diclofenac en absorbant la lumière (temps de demi-vie 2,2 fois plus important).
A noter qu'Aguera et al. (2005) ont identifié plusieurs produits de photodégradation.
Biodégradation
Selon Stamm et al. (2008), la biodégradation joue un rôle majeur en tant que « puits » pour de nombreux produits pharmaceutiques et a lieu principalement dans les stations d'épuration. La biodégradation se produit également dans le milieu aquatique. Par exemple, Gröning et al. (2007) ont détecté trois métabolites issus de la biodégradation du diclofenac (le 4'hydroxydiclofenac, 5-hydroxy-diclofenac et le 5-hydroxydiclofenac quinone imine).
Un recensement non exhaustif de différentes études de la littérature est présenté ci-après. Celui-ci est organisé suivant le type de milieu aquatique (eau de surface, souterraine, boissons…). Un tableau de synthèse est présenté à la fin de ce paragraphe.
Dans les eaux de surface
Les résultats de l'étude de Budzinski et Togola (2006) réalisée entre mars 2002 et juin 2005 dans différents estuaires français et concernant le diclofenac sont présentés dans le Tableau 7 ci-après :
Tableau 7. Concentrations extrêmes (ng.L-1) mesurées dans les différents estuaires en France (Budzinski et Togola, 2006).

LD : Limite de Détection
Togola et Budzinski (2008) ont également mis en évidence une contamination des eaux de surface de l'Hérault par, entre autre, le diclofenac avec des concentrations minimales et maximales, respectivement de 1,36 et 33,2 ng.L-1.
Des modélisations de concentrations dans les eaux de rivière ont été établies par Johnson et al. (2007) pour le diclofenac à partir des quantités consommées, de leur élimination chez l'homme et leur devenir potentiel dans les stations d'épuration d'un même bassin versant. Les résultats de cette étude ont mis en évidence des teneurs en diclofenac de l'ordre de 1 ng.L-1. Néanmoins, à quelques endroits, notamment en aval de petites stations d'épuration, des concentrations supérieures à 25 ng.L-1 ont été calculées.
Une campagne de mesure exploratoire a été menée par l'Agence de l'Eau Artois-Picardie (2010) dans le but de dresser une image ponctuelle de la présence des substances médicamenteuses dans les eaux de surface du bassin Artois-Picardie (Agence de l'eau Artois-Picardie, 2010). Les prélèvements ont été effectués en juin 2010 sur des milieux soumis à de faibles pressions anthropiques ainsi que sur des milieux où les pressions sont identifiées. Au total, 38 sites ont été sélectionnés et 54 substances médicamenteuses analysées (dont le diclofenac), à usage humain et/ou vétérinaire, représentant différentes classes thérapeutiques. Les résultats ont mis en évidence la présence de 8 substances médicamenteuses appartenant à 6 classes thérapeutiques différentes, sur un total de 20 stations. La carbamazepine (anti-épileptique) et le diclofenac sont les substances les plus présentes dans le bassin. La gamme de concentration en Artois-Picardie pour le diclofenac est de 0,02 à 0,2 µg.L-1. Cette gamme de concentrations est cohérente avec celle rapportée d'après la littérature par Garric et Ferrari (2005) et Johnson et al. (2007) (cf. ci-dessus) dans les eaux de surface, à savoir entre 0,001 et 0,2 µg.L-1. A noter que dans le rapport de l'Agence de l'Eau Artois-Picardie, il est bien spécifié que les résultats sont à nuancer : les limites de quantification des laboratoires sont trop élevées par rapport aux niveaux de concentrations des substances médicamenteuses habituellement retrouvées dans les eaux de surface. La limite de quantification du diclofenac était de 0,02 µg.L-1.
Une campagne de mesure lancée en 2006 par l'Agence de l'Eau Adour-Garonne a mis en évidence des concentrations en diclofenac inférieures à 62 ng.L-1 dans 10 % des échantillons d'eaux brutes analysés (Dulio et Morin, 2009).
Dans le cadre d'une campagne de surveillance organisée par le Joint Research Centre, plus de 100 rivières des 27 pays européens ont été échantillonnés afin d'évaluer l'occurrence des polluants organiques polaires persistants en Europe. 35 composés ont été sélectionnés et analysés dont des substances pharmaceutiques (Loos et al., 2009). Pour l'ensemble de ces pays, la fréquence de détection du diclofenac était de 83 %, la concentration moyenne de 17 ng.L-1, la médiane de 5 ng.L-1 et une concentration maximale de 247 ng.L-1 (maximum mesuré en Hongrie) et une limite de détection de 1 ng.L-1.
Dans le cadre du programme européen KNAPPE (Knowledge and Need Assessment on Pharmaceutical Products in Environmental waters) dont l'objectif est de définir l'état de l'art sur les produits pharmaceutiques à usage humain dans les milieux aquatiques, des mesures de substances pharmaceutiques ont été réalisées en Europe. Les principaux résultats pour les concentrations mesurées dans les eaux de surface en diclofenac sont présentés dans le Tableau 8 ci-dessous (Sadezky et al., 2008) :
Tableau 8. Concentrations en diclofenac mesurées dans le cadre du programme KNAPPE – eaux de surface (Sadezky et al., 2008).

L'Agence de l'eau Seine Normandie a ciblé des sites destinés à la production d'eau pour consommation humaine -nappes souterraines peu profondes non captives, sources et forages (certains karstiques) -caractérisés par un environnement de surface représentatif d'une pression homogène (ex. élevage, industrie, domestique, etc.). Quatre campagnes de mesure ont été réalisées entre 2006 et 2008. Sur chacun des 151 échantillons prélevés, 30 molécules médicamenteuses ou dérivés, appartenant à 8 classes thérapeutiques particulièrement utilisées et dotées d'une certaine persistance dans l'environnement ont été recherchées, y compris des métabolites (Tracol et Duchemin, 2009). Le diclofenac faisait partie des molécules médicamenteuses recherchées lors de ces campagnes de mesure. Dans les eaux souterraines, le diclofenac appartient au groupe de molécules les plus souvent détectées avec des concentrations comprises entre 5 et 30 ng.L-1. Dans les eaux superficielles, les concentrations en diclofenac se sont révélées inférieures à 10 ng.L-1 (limite de quantification de l'ordre du ng.L-1).
Dans les eaux souterraines
Les eaux souterraines n'englobent pas que les nappes phréatiques. Elles représentent un ensemble assez hétérogène dont la vulnérabilité est très variable selon la profondeur, la nature des terrains et la protection géologique (Académie de Pharmacie, 2008). Les écarts de concentration suivants ont été observés pour de nombreux médicaments à Berlin (mesures réalisées entre le mois de mai et celui de décembre 1999) par Heberer (2002). Concernant le diclofenac, la gamme de concentrations est de « non détecté » à 380 ng.L-19 .
[9] Cette source ne précise la limite de détection associée à ces mesures.
Dans les eaux de boisson
Une étude sur les résidus médicamenteux dans les eaux de consommation a été confiée à l'Anses par la Direction générale de la santé afin d'estimer l'occurrence de ces résidus (Anses, 2011). Ainsi, une campagne nationale de mesures de 45 substances pharmaceutiques d'origine humaine, vétérinaire ou de leurs métabolites a été lancée sur la base d'une liste établie par l'Anses et l'Afssaps10 . Bien que le diclofenac n'appartienne pas à la liste des molécules prioritaires établie par l'Anses et l'Afssaps, il a été ajouté à la liste des molécules recherchées en raison de sa présence dans l'essai inter‐laboratoire et du fait qu'il est fréquemment cité dans la littérature. La stratégie de sélection des sites de prélèvements a permis de couvrir près d'un quart de la population en France métropolitaine et dans les DOM. Tous les départements ont pu être investigués. Les prélèvements ont été effectués sur des ressources utilisées pour la production d'eau destinée à la consommation humaine (eau de surface et eau souterraine) et sur des eaux traitées, en sortie de station de potabilisation.
Concernant le diclofenac, une concentration maximale de 16 ng.L-1 a été mesurée dans les eaux brutes avec une fréquence de détection de 2,6 % et une fréquence de résultats quantifiables de 1,1 %. Dans les eaux traitées, ce composé n'a pas été détecté, ni quantifié.
Les principaux résultats de cette étude sont les suivants :
- pour environ 75 % des échantillons d'eau traitée qu'elles soient d'origine souterraine ou superficielle, aucune des 45 molécules n'a été quantifiée (hors caféine qui est, par ailleurs, un marqueur de l'activité humaine) ;
- pour les 25 % d'échantillons positifs, les analyses révèlent généralement la présence simultanée d'une à quatre molécules ;
- parmi les 45 molécules recherchées, 26 n'ont jamais été retrouvées, dix-neuf ont été détectées au moins 1 fois, parmi lesquelles 5 étaient présentes à des concentrations trop faibles pour pouvoir être quantifiées ;
- hormis la caféine, les molécules les plus fréquemment retrouvées sont, selon un ordre décroissant, la carbamazépine (anti-épileptique) et son principal métabolite (10-11 époxycarbamazépine) ainsi que l'oxazépam (anxiolytique) qui est à la fois une molécule mère et un métabolite de benzodiazépines et l'hydroxyibuprofène, métabolite de l'ibuprofène (la fréquence de détection de du diclofenac dans les eaux traitées est de l'ordre de 1,4 %) ;
- plus de 90 % des échantillons présentent une concentration maximale cumulée inférieure à 25 ng.L-1 et moins de 5 % des échantillons présentent une concentration maximale cumulée supérieure à 100 ng.L-1 ;
- la comparaison entre les eaux traitées et les eaux brutes montre un bon abattement (60 %) obtenu par désinfection (chlore) et une efficacité de l'ordre de 75 à 80 % pour les filières de filtration et les traitements poussés.
[10] AFSSA (2008). Hiérarchisation des résidus de médicaments d'intérêt pour l'analyse des ressources et des eaux traitées.
Jones et al.(2005) ont fait une revue des contaminations des eaux de boisson à travers le monde. Le diclofenac est parmi les composés présents avec une concentration maximale de 6 ng.L-1 mesurée en Allemagne.
Dans les stations d'épuration
Ca paragraphe traite des différents niveaux de concentrations en diclofenac mesurées dans les eaux brutes et les effluents de stations d'épuration afin d'évaluer la présence de cette substance dans le milieu aquatique. L'efficacité des différents types de traitement en station d'épuration est explicitée dans la dernière partie de cette fiche technico-économique, partie relative aux traitements des rejets de dicflofenac (voir paragraphe 5.1).
Les concentrations mesurées en station d'épuration pour le diclofenac dans le cadre du programme KNAPPE, sont présentées dans le Tableau 9 ci-après (Sadezky et al., 2008).
Tableau 9. Concentrations en diclofenac mesurées dans le cadre du programme KNAPPE – stations d'épuration (Sadezky et al., 2008).

Le projet AMPERES a pour objectifs de mesurer la composition en micropolluants des eaux usées et traitées et de quantifier l'efficacité d'élimination de différentes filières d'épuration vis-à-vis de ces contaminants (boues activées, biofiltration, filtres plantés de roseaux, bioréacteurs à membranes immergées, traitement tertiaire oxydant ou filtrant).
Dans le cadre de ce projet, 33 substances pharmaceutiques (dont le diclofenac) et 5 hormones ont été choisies en tant que substances cibles à retenir dans le projet. Soulier et al. (2011) ont montré que les anti-inflammatoires sont quantifiés dans 80 à 97 % des échantillons dans les eaux brutes, entre 80 et 100 % dans les eaux traitées secondaires et sont légèrement moins souvent quantifiées dans les eaux traitées tertiaires (de 50 à 81 %). Concernant le diclofenac, il est quantifié dans plus de 90 % des échantillons d'eaux brutes, 100 % des échantillons dans les eaux traitées secondaires et plus de 80 % dans les échantillons d'eaux traitées tertiaires. On notera que, dans le cas du traitement secondaire, le diclofenac appartient au groupe de substances pour lequel il existe une grande variabilité sur les rendements d'élimination avec des écarts supérieurs à 20 %.
En entrée de station d'épuration, le diclofenac appartient au groupe de substances, quantifié dans des gammes de concentrations allant du centième de µg.L-1 à la dizaine de µg.L-1. En aval de traitement secondaire, le diclofenac appartient au groupe de substances quantifié dans des gammes de concentrations allant de quelques dixièmes de µg.L-1 à quelques µg.L-1.
Miege et al. (2009) ont conçu une base de données afin d'évaluer l'occurrence et l'efficacité d'élimination des composés pharmaceutiques et cosmétiques dans les stations d'épuration. Ils ont répertorié 6 641 données concernant 184 composés, issues de 117 publications scientifiques. L'exploitation de ces données a permis, d'une part, d'identifier les composés les plus étudiés et, d'autre part, de déterminer des valeurs étayées :
- de fréquences de quantification ;
- de concentrations dans la phase dissoute des eaux résiduaires urbaines [influents] et des eaux épurées [effluents] ;
- de rendements d'élimination de ces composés dans les stations d'épuration.
Le diclofenac fait partie des produits pharmaceutiques et cosmétiques les plus recherchés dans les eaux résiduaires brutes et traitées. Le diclofenac est donc parmi les substances les plus documentées car souvent prescrites par les médecins et donc rejetées régulièrement dans l'environnement via les stations d'épuration. L'étude de Miege et al. (2009) a mis en évidence les valeurs suivantes pour le diclofenac dans les stations d'épurations avec un procédé à boues activées (Tableau 10) :
Tableau 10. Concentrations en diclofenac dans les stations d'épuration avec un procédé à boues activées (Miege et al., 2009).
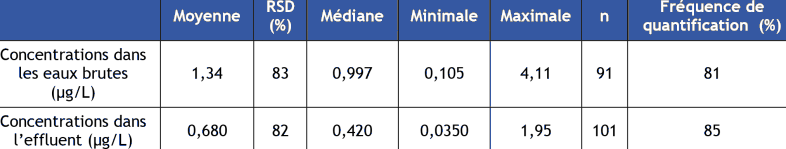
RSD : écart type relatif
Les concentrations en produits pharmaceutiques dans les eaux brutes dépendent essentiellement du degré de prescription et de la métabolisation par l'organisme humain. Elles peuvent également varier en fonction de la transformation des composés dans les réseaux de collecte (en amont de la station d'épuration) et de la dilution par les eaux claires parasites (pouvant atteindre 50 % dans les réseaux) selon les auteurs.
Les concentrations dans les effluents vont, quant-à-elles, dépendre principalement des concentrations dans les eaux brutes et du rendement d'élimination dans la station d'épuration (Miege et al., 2009).
Dans les eaux marines
En France, des prélèvements ont été réalisés dans la Calanque de Cortiuou à environ 300 m du rejet de la station d'épuration de Marseille qui ne réalise pas de traitement biologique. Les anti-inflammatoires non stéroïdiens (dont le diclofenac) présentent de très forts niveaux de concentrations, compris entre 200 et 8 000 ng.L-1 selon les composés (Budzinski et Togola, 2006).
Les données sur la contamination de ce milieu par les substances pharmaceutiques sont relativement peu nombreuses. Un rapport du projet KNAPPE réunit des données de mesures de contamination des eaux marines côtières dans le monde (Sadezky et al., 2008). Concernant le diclofenac, les concentrations marines côtières rapportées en France sont de 0,032 µg.L-1 pour la moyenne des concentrations et de 0,101 µg.L-1 pour la concentration maximale (ces valeurs sont calculées à partir de 8 données).
Thomas et al. (2007) ont noté des concentrations en diclofenac dans les eaux marines côtières comprises entre < 0,008 et 0,195 µg.L-1 pour une concentration médiane de 0,008 µg.L-1 (concentrations mesurées dans des estuaires au Royaume-Uni). Ces valeurs sont comparables à celles mesurées dans le cadre du projet KNAPPE.
Le Tableau 11 ci-après reprend de façon synthétique les différentes concentrations mesurées en diclofenac dans les différents compartiments du milieu aquatique.
Tableau 11. Concentrations en diclofenac mesurées dans le milieu aquatique.
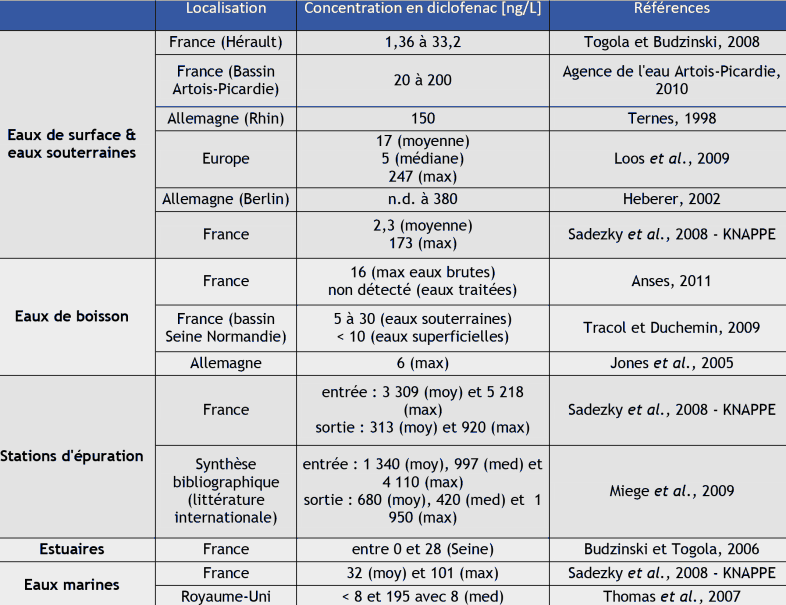
n.d. : non détecté
Dans les sédiments
Lors de ce travail, nous n'avons identifié que peu de données sur les concentrations en produits pharmaceutiques dans les sédiments. Les principales sources de médicaments dans le sol et les sédiments sont considérés être les antibiotiques et les hormones de croissance qui sont utilisés dans l'agriculture plutôt qu'en médecine humaine (Stockholm County Council, 2005 ; Thiele-Bruhn, 2003).
Le BRGM a réalisé des campagnes de mesure dans le bassin Loire-Bretagne en 2006 (Togola et al., 2008). Une douzaine de points de prélèvements répartis sur le bassin ont été suivis. Ces points comprenaient des eaux de surface, des eaux côtières/estuariennes, des eaux souterraines et des sédiments. Le diclofenac fait parti des substances pharmaceutiques étudiées lors de ces campagnes de mesure. Néanmoins, le diclofenac n'appartient pas au groupe de substances les plus fréquemment détectées dans cette matrice (au contraire du propanolol, un bétabloquant ou l'acide salicylique).
Terrestre
FTE 2015 Importer
Le comportement des médicaments dans les sols et les sédiments est fonction des conditions du milieu et des propriétés physico-chimiques spécifiques à chaque médicament. Les facteurs influençant le devenir des médicaments dans ces milieux sont le pH, la température, la capacité d'échange cationique (CEC), l'humidité ainsi que les concentrations de nutriments, d'argiles, de matières organiques et de matières humiques (Boxall, 2008).
Les mécanismes généraux de migration des substances dans les sols sont la percolation, le ruissellement et le lessivage.
Scheytt et al. (2005) ont déterminé des coefficients de sorption du diclofenac dans des sédiments sableux. Cette étude a montré une sorption très dépendante du type de sédiment. Même des sédiments possédant un contenu en carbone organique comparable montrent des valeurs de sorption différentes. Ainsi, ces travaux ont montré que la sorption du diclofenac, même dans les sols sableux, est confirmée.
De plus, si le produit pharmaceutique est apporté en surface du sol, avant de parvenir à la nappe, celui-ci doit s'infiltrer au travers de la zone non saturée de l'aquifère et en premier lieu au travers des horizons pédologiques. Un retard à l'infiltration et/ou une rétention des produits peuvent être alors observés. Chefetz et al. (2008) signalent ainsi la rétention de la carbamazépine et du diclofenac dans les 5 à 15 premiers centimètres du sol. A titre d'exemple, des essais sur colonnes (Scheytt et al., 2006) montrent aussi un facteur de retard8 au transfert qui est de 4,8 pour le diclofenac.
[8] Exprime le retard d'un contaminant pendant son transport dans l'eau dû à son adsorption sur la matière organique du sol.
Les principales sources de médicaments dans le sol et les sédiments sont considérés être les antibiotiques et les hormones de croissance qui sont utilisés dans l'agriculture et plutôt qu'en médecine humaine (Stockholm County Council, 2005 ; Thiele-Bruhn, 2003).
Toutefois, lors de ce travail, nous n'avons pas identifié d'informations spécifiques sur les concentrations en diclofenac dans les sols.
Perspectives de réduction
Réduction des rejets
LES STATIONS D'EPURATION
FTE 2015 Importer
L'élimination des résidus pharmaceutiques dans les stations d'épuration et dans les usines de production d'eau potable a été étudiée dans le cadre du projet KNAPPE (cf. paragraphe 4.2.1 ; Buntner, 2008). L'influence de la configuration du réacteur, le temps de séjour des boues (SRT), le temps de séjour hydraulique (HRT), la température (saison), les conditions redox et la concentration des substances pharmaceutiques spécifiques dans les eaux usées en entrée et sortie de stations d'épuration sont les paramètres recensés pour la comparaison des différentes technologies.
Concernant le diclofenac, les conclusions sont les suivantes :
Cette substance est faiblement éliminée pour un temps de séjour dans les boues inférieur à boues inférieur à 20 jours. L'augmentation du SRT (pour des périodes supérieures à 20 jours) supérieures à 20 jours) semble améliorer l'élimination de cette substance (cf. CASP : Conventional Activated Sludge Processes (boues actives) ; CASP-TF – Conventional Activated Sludge Processes combined with Trickling Filter (boues actives couplé à un lit bactérien), SBR – Sequencing Batch Reactor (boues actives par traitement séquentiel); MBR – Membrane Biological Reactor (bioréacteur à membrane); FBR – Fixed Bed Reactor ; Lagoon (lagunes).
-Figure 7 a) ;
Le diclofenac se révèle être plus sensible aux temps de rétention hydraulique supérieurs à 25 heures (cf. CASP : Conventional Activated Sludge Processes (boues actives) ; CASP-TF – Conventional Activated Sludge Processes combined with Trickling Filter (boues actives couplé à un lit bactérien), SBR – Sequencing Batch Reactor (boues actives par traitement séquentiel); MBR – Membrane Biological Reactor (bioréacteur à membrane); FBR – Fixed Bed Reactor ; Lagoon (lagunes).
- Figure 7 b) ;
Concernant l'influence de la configuration du réacteur, les réacteurs de boues activées activées couplés avec un filtre biologique ou les lagunes montrent un bon abattement du abattement du diclofenac (cf. CASP : Conventional Activated Sludge Processes (boues actives) ; CASP-TF – Conventional Activated Sludge Processes combined with Trickling Filter (boues actives couplé à un lit bactérien), SBR – Sequencing Batch Reactor (boues actives par traitement séquentiel); MBR – Membrane Biological Reactor (bioréacteur à membrane); FBR – Fixed Bed Reactor ; Lagoon (lagunes).
- Figure 7 c) ;
- Il y a très peu d'informations disponibles sur l'influence des conditions redox sur l'élimination des substances médicamenteuses ;
- Il n'y a pas d'influence des conditions climatiques sur l'élimination des substances médicamenteuses ;
- Les solutions de pré ou post-traitement telle que l'ozonation peuvent se révéler efficace (A noter que les données sont essentiellement disponibles concernant les process d'ozonation).
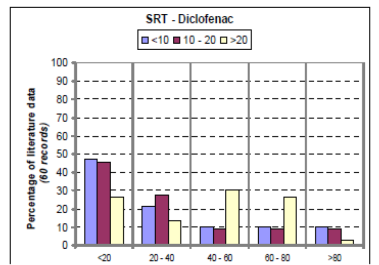
a
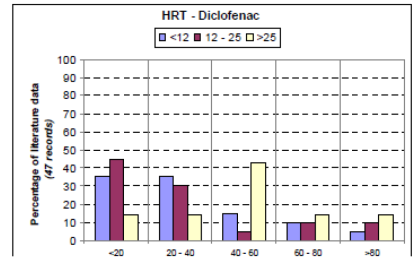
b
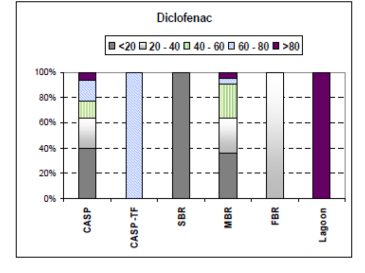
c
CASP : Conventional Activated Sludge Processes (boues actives) ; CASP-TF – Conventional Activated Sludge Processes combined with Trickling Filter (boues actives couplé à un lit bactérien), SBR – Sequencing Batch Reactor (boues actives par traitement séquentiel); MBR – Membrane Biological Reactor (bioréacteur à membrane); FBR – Fixed Bed Reactor ; Lagoon (lagunes).
Figure 7. Elimination du diclofenac dans les stations d'épuration en fonction du temps de séjour des boues en jour (a), du temps de séjour hydraulique en heure (b) et du type de réacteur (c) (Buntner, 2008).
Dans le cadre du projet AMPERES, des études ont été conduites sur 21 stations d'épuration afin d'estimer la composition en substances pharmaceutiques des eaux usées et traitées. Au cours du projet, 21 stations d'épuration ont été étudiées dont 12 filières différentes. Les analyses ont porté sur 81 échantillons d'eaux dont 32 eaux usées brutes, 33 eaux traitées secondaires et 16 eaux traitées tertiaires. Cette étude a permis de comparer l'efficacité de différents procédés d'épuration sur la base des rendements d'épuration. En comparant les concentrations en entrée et en sortie de traitements secondaires (boues activées, biofiltration, bioréacteur à membrane immergées, filtres plantés de roseaux, lit bactérien), il a été mis en évidence que les procédés d'épuration secondaires permettent une « bonne » élimination des substances pharmaceutiques, sans les éliminer totalement (les traitements biologiques secondaires de type boues activées en aération prolongée imposent des rendements supérieurs à 70 % pour 50 % des substances pharmaceutiques étudiées). Néanmoins, on notera que le diclofenac appartient au groupe de substances pour lequel il existe une grande variabilité sur les rendements d'élimination avec des écarts supérieurs à 20 %. (Soulier et al., 2011).
Concernant les traitements tertiaires, deux types ont été étudiés lors des campagnes de mesure : les traitements d'affinage (décantation rapide, filtration sur sable et lagunage tertiaire) et les traitements avancés (ozonation, filtration sur charbon actif et osmose inverse). Il a été montré que les traitements tertiaires appliquent une élimination plus poussée des substances pharmaceutiques des eaux. Cette diminution est plus importante dans le cas de traitement tertiaires avancés. Le Tableau 12 ci-dessous indiquent les rendements d'élimination complémentaires (%) de la filière eau par traitement tertiaire (Soulier et al., 2011).
Tableau 12. Rendements d'élimination complémentaire (%) de la filière eau par traitement tertiaire (Soulier et al., 2011).

Les valeurs de concentration des substances pharmaceutiques dans les boues sont faibles, elles sont de l'ordre de la centaine de ng/g de masse sèche. Les bilans de matières montrent que le phénomène prépondérant pour les substances pharmaceutiques n'est pas l'accumulation dans les boues, mais la dégradation.
D'autre part, Miege et al. (2009) ont montré que les rendements d'élimination des produits pharmaceutiques obtenus par décantation primaire sans addition de réactifs physico-chimiques sont faibles (inférieurs à 40 %) au regard de ceux obtenus avec des procédés biologiques pouvant dépasser 90 %. Les rendements des bioréacteurs à membranes immergées sont équivalents à ceux d'un procédé à boues activées faible charge pour plusieurs composés comme le diclofenac. Les rendements des lagunes naturelles semblent également comparables à ceux des procédés à boues activées faible charge. Cela peut s'expliquer par les forts temps de séjour hydraulique, un temps de séjour des boues élevé (plusieurs années) et par le phénomène de photodégradation.
Pour chaque type de procédé, Miege et al. (2009) se sont également intéressés à l'effet de concentration dans les eaux brutes sur le rendement vis-à-vis des produits pharmaceutiques et cosmétiques. Ils ont observé un rendement d'élimination plus élevé pour le diclofenac lorsque la concentration dans les eaux brutes est plus forte avec le procédé à boues activées faible charge. Les données collectées dans la base de données ne permettent cependant pas de conclure quand à l'influence des paramètres opératoires (temps de rétention hydraulique, temps de séjour des boues ou température au sein des réacteurs biologiques).
Un autre axe de réduction des émissions au niveau des stations d'épuration est la réduction des pertes/fuites dans les réseaux d'assainissement qui peuvent varier entre 5 et 25 % (Dulio et Morin, 2009 ; Académie de Pharmacie, 2008).
Selon le rapport de l'Académie de Pharmacie (2008), le coût engendré par une optimisation des STEP pour l'élimination de traces de molécules indésirables est considérable et pourrait conduire à réaliser des filières technologiques proches de celles utilisées en production d'eau potable ce qui serait économiquement très important. Un rapport de l'Agence de la Protection Environnementale (EPA) de Suède montre que des traitements supplémentaires dans les STEP doubleraient leur consommation d'énergie et augmenteraient la facture d'eau des particuliers de 10 à 100 % (Bocaly, 2010).
Dans un premier temps, les préconisations du rapport de l'Académie de Pharmacie, 2008 sont les suivantes :
- réaliser une collecte la plus large possible des rejets et réduire les fuites des réseaux ;
- limiter les rejets liés aux déversoirs d'orage qui rejettent directement dans le milieu les eaux usées non traitées dans les cas d'orage afin de protéger la STEP ;
- fiabiliser et mettre aux normes européennes la totalité les unités existantes avec un système d'assurance de la qualité.
Afin de réduire les volumes d'eau à traiter et de pouvoir ainsi utiliser des traitements très efficaces qui peuvent être très onéreux, une technologie (appelée NoMix) permettant la collecte séparée des urines est actuellement en cours (Programme Novaquatis11). La majorité des produits pharmaceutiques (67 % à 27 % selon Rossi, 2008, 80 à 90 % selon Montiel, 2006) est excrétée via les urines. Ainsi, cette technique permettrait de récupérer une proportion significative des médicaments consommés par la population à une concentration 100 fois plus élevée que dans les effluents d'eaux usées municipaux (Zabczynsky, 2008) et 150 à 500 fois plus élevée dans les effluents d'hôpitaux (Montiel, 2006). L'investissement dans la technologie NoMix : 900 à 1 300 euros par toilette (Rossi, 2008).
Des expériences ont été menées dans des établissements de soin pour équiper des toilettes de ce type de technologie permettant de séparer les solides des liquides afin de traiter spécifiquement et localement les urines pour ne pas rejeter les résidus dans les égouts. Mais, l'étude coût/bénéfice reste à faire (Académie de Pharmacie, 2008).
[11] http://www.novaquatis.eawag.ch/index_EN
Remarquons que concernant les installations d'eau potable, le diclofenac est efficacement éliminé par ozonation avec des concentrations supérieures 0,5 mg O3 .L-1 (Huber et al., 2003). Le couplage ozone-peroxyde d'hydrogène permet une dégradation complète du diclofenac (Zwiener et Frimmel, 2000).
Vogna et al. (2004) ont étudié l'efficacité de dégradation du diclofenac par l'ozonation et le couplage UV-H2O2. Ce composé peut être dégradé soit par déchloration ou soit par minéralisation.
Toutefois, il est nécessaire :
- de considérer que le contact avec l'ozone ou le chlore peut induire la production de sous-produits ou de métabolites de dégradation auxquels il convient de prêter attention pour en évaluer les effets biologiques potentiels (Académie de Pharmacie, 2008) ;
- de garder en mémoire que ces techniques à coût abordable pour la potabilisation de l'eau n'ont pas été étudiées du point de vue de leur faisabilité en tant que procédés de réduction des émissions.
RECOMMANDATIONS & MESURES DE PREVENTION
FTE 2015 Importer
- Académie nationale de Pharmacie (Académie de Pharmacie, 2008)
Les recommandations de l'Académie nationale de Pharmacie se regroupent en trois axes :
- Limiter et contrôler les rejets (optimisation de la fabrication, amélioration des traitements de rejets ponctuels, optimisation de l'efficacité des stations d'épuration) ;
- Evaluer les risques liés aux rejets ;
- Développer des actions de formation et d'éducation (sensibilisation des étudiants qui se destinent à la chimie pharmaceutique et aux professions de la santé, éviter par principe toute surconsommation de substances médicamenteuse et développer le rôle des pharmaciens dans la sensibilisation et l'éduction thérapeutique et environnementale du public).
Afin de limiter les rejets, en particulier pour les industries chimiques et pharmaceutiques, l'Académie Nationale de Pharmacie propose les mesures de prévention suivantes :
- Utilisation sur les eaux usées de techniques physiques telles que l'osmose inverse, la nano-filtration ou l'adsorption sur charbon actif, méthodes efficaces mais très couteuses ;
- Traitement des concentras obtenus, limitant ainsi les transferts vers l'environnement ;
- Mise en place de traitements complémentaires tels que l'ozonation si nécessaires (comme nous l'avons vu précédemment pour le diclofenac). On notera, néanmoins, que ce traitement d'ozonation/peroxyde d'oxygène est susceptible de former des sous-produits nocifs pour l'homme.
AQUAREF (Dulio et Morin, 2009)
En ce qui concerne les mesures de prévention, les consommateurs devraient être sensibilisés sur le fait qu'ils peuvent contribuer directement à la protection de l'environnement en évitant de rejeter dans le réseau d'assainissement ou les déchets municipaux, les produits pharmaceutiques expirés ou non utilisés.
Des réseaux de récupération sont actuellement en place dans environ 20 pays européens pour permettre la récolte des produits expirés ou non utilisés et ainsi éviter qu'ils soient rejetés, mélangés aux autres déchets urbains.
OIEau (Bocaly, 2010)
Dans son rapport, Bocaly, 2010 propose également que les rejets hospitaliers soient traités sur place pour limiter les rejets dans les eaux usées municipales, et par la suite dans l'environnement, des grandes quantités de substances qu'ils contiennent.
- Modèle suédois (Janusinfo, 2011)
Un classement des substances pharmaceutiques en fonction du risque environnemental qu'elles présentent et un système d'information sur ce classement ont été réalisés en Suède. Ce système, qualifié en Europe de « modèle suédois », permet de choisir le composé le plus « vert » c'est à dire présentant le plus faible risque pour l'environnement lorsque plusieurs composés de même efficacité peuvent être utilisés. Les informations résultant de ce schéma sont fournies aux médecins et aux patients et sont disponibles sur le site http://www.janusinfo.se/. Les critères de classification sont basés sur le risque environnemental (rapport PEC12/PNEC13) ainsi que le danger pour l'environnement : PBT index (persistance, bioaccumulation et toxicité).
En France, le C2DS (Comité Développement Durable Santé) a pris exemple sur l'initiative suédoise et devrait pouvoir tester ce système préventif dans une dizaine d'établissements français (Actu-Environnement, 2011).
Programme KNAPPE (Zabczynsky, 2008)
Différentes stratégies de réduction des produits pharmaceutiques dans l'environnement ont été proposées dans le cadre du programme KNAPPE. Celles-ci sont présentées sur la Figure 8 ci-après.
[12] PEC : Concentration Environnementale prévisible
[13] PNEC : Concentration Prédite Sans Effet -concentration d'une substance chimique au-dessous de laquelle il ne devrait pas y avoir d'effets nocifs sur les organismes des écosystèmes considérés (Annexe I du règlement REACH)
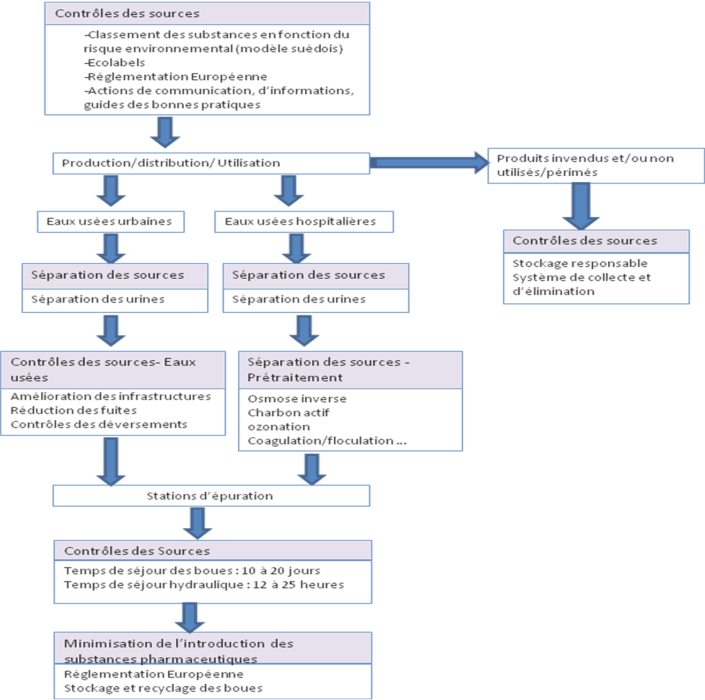
Figure 8. Stratégies de réduction des substances pharmaceutiques dans l'environnement (programme KNAPPE, Zabczynsky, 2008).
Kampa et Vidaurre (2008) ont identifié les outils possibles pour réduire les substances pharmaceutiques dans l'environnement (outils techniques, économiques…). Une des propositions serait de soutenir l'achat de substances « vertes » par les consommateurs et par le biais par exemple d'une subvention couvrant les différences de prix entre les médicaments « verts » et leurs homologues plus « dangereux » pour l'environnement (mise en place d'un ecolabel visant entre autre les processus de production).
Ils proposent également de convaincre les hôpitaux d'ajouter le profil environnemental parmi leurs critères de choix des médicaments lors des achats.
- Plan national pour limiter les résidus médicamenteux dans l'eau (Ministères de l'Ecologie et de la Santé, 2011)
Le 30 mai 2011, un Plan national sur les résidus de médicaments dans l'eau a été lancé en France. Ce plan est structuré en une action transversale (prioriser les différentes molécules et métabolites pour lesquels les travaux doivent être engagés) ainsi qu'en 3 grands axes :
- Axe A : évaluation des risques environnementaux et sanitaires (renforcement de la connaissance de l'état des milieux, amélioration des connaissances sur l'exposition aux résidus de médicaments et ses effets sur l'environnement et la santé) ;
- Axe B : gestion des risques environnementaux et sanitaires (mise en place d'un dispositif de surveillance, réduction des émissions dans l'environnement, former les professionnels et informer le grand public et les professionnels, plan de communication sur les résidus de médicaments dans les eaux) ;
- Axe C : renforcer et structurer les actions de recherche (lancement d'études économiques et sociales pour mesurer l'acceptabilité du risque et renforcement et structuration des actions de recherche).
Concernant la réduction des émissions, les ateliers de travail sont les suivants :
- Amélioration de l'évaluation réglementaire de l'impact environnemental des médicaments ;
- Développement de la surveillance ciblée des différents rejets potentiels de substances médicamenteuses (définition de valeurs limites d'émission) ;
- Analyse de la faisabilité de mesures de réduction à la source des rejets médicamenteux (limitation de leur dispersion) ;
- Analyse de la pertinence d'améliorer les traitements des eaux usées et potables (appréciation du coût-efficacité et évaluation des sous-produits générés).
On notera que dans ce cadre, une méthode d'évaluation des risques sanitaires est attendue pour fin 201114 . Cette méthode sera proposée par l'AFSSAPS et l'ANSES et sera appliquée notamment à la carbamazépine puis aux autres molécules identifiées lors de la campagne nationale (Anses, 2011).
Divers
Kümmerer (2009) présente dans une partie de son article, l'état de l'art en matière de gestion du risque concernant les substances pharmaceutiques. Actuellement, il existe trois axes stratégiques pour réduire la présence de ces substances dans l'environnement :
- une approche technique (traitements avancés) pour une gestion du risque à court et moyen terme ;
- l'éducation, la formation et l'information (médecins, infirmières, patients…) pour une gestion à moyen terme ;
- le développement de la chimie « verte » (pour la substitution des composés « dangereux ») pour une gestion à long terme.
Concernant l'approche technique, une des propositions actuelles est de séparer les effluents des hôpitaux des eaux usées urbaines. Néanmoins, Kümmerer (2009) se demande si cette solution est pertinente du point de vue économique et environnemental étant donné que la contribution totale des hôpitaux à la charge totale des effluents d'une station d'épuration urbaine est de moins de 10 % pour la majorité des substances et même très fréquemment inférieure à 3 %. L'auteur dresse également un bilan des carences des technologies avancées actuellement proposées pour le traitement des substances pharmaceutiques (telles que les process d'oxydation, la filtration, le charbon actif …) dont les suivantes :
- l'efficacité dépend du type de substance ;
- aucune des technologies ne peut éliminer tous les composés pharmaceutiques ;
- certains produits de la réaction des processus d'(photo)oxydation présentent des propriétés mutagènes et toxiques….
[14] http://www.actu-environnement.com/ae/news/pollution-eaux-rivieres-medicaments-pnrm-13189.php4
A Bellecombe, en Haute-Savoie, un nouveau centre hospitalier ouvrira ses portes au public en 2012. Localisé à proximité de la station d'épuration de la ville, le site pilote de Bellecombe (Sipibel) constitue un lieu d'expérimentation unique pour mesurer, en les comparant avec les rejets urbains, si les rejets hospitaliers présentent un risque en termes de résidus. Une première campagne de mesure a eu lieu en février 2011 et une seconde se déroulera en décembre 2011. Les résultats de ces mesures permettront d'établir un état des lieux précis de la qualité de l'eau avant la mise en service de l'hôpital. Une période de trois ans permettra ensuite de conduire des analyses et essais de traitement, la finalité du projet étant d'apporter un éclairage sur l'impact des rejets hospitaliers et sur l'intérêt d'un traitement spécifique avant la station d'épuration, afin de minimiser les rejets dans le milieu naturel (Agence de l'eau Rhône Méditerranée Corse, 2011 et Actu-Environnement, 2011).
http://www.start-project.de/index.htm L'Allemagne a également mis à disposition un guide pratique : Les moyens d'intervention pour réduire la pollution de l'eau : principes actifs de médicaments pour l'homme. Ce guide est disponible sur internet : (Start Project, 2009).
Conclusion
FTE 2015 Importer
Le diclofenac est un médicament appartenant à la classe des anti-inflammatoires non-stéroïdien. En France, son usage est limité à l'homme (pas d'usage vétérinaire).
Depuis une quinzaine d'années, les techniques analytiques se sont suffisamment améliorées pour permettre de quantifier la présence des médicaments dans l'environnement. Le diclofenac fait partie des substances pharmaceutiques les plus étudiées et rencontrées dans l'environnement. Les émissions de diclofenac se font principalement vers le milieu aquatique via les rejets en stations d'épuration urbaines et sont le résultat de l'utilisation par le patient. Son abattement en station d'épuration peut varier selon le mode de traitement entre 40 et 90 %.
Afin de réduire les émissions de diclofenac dans l'environnement et de manière plus générale les substances médicamenteuses, dont les risques pour l'homme et l'environnement sont encore incertains, des préconisations ont été proposées ou mises en place. Celles-ci se déclinent sur 3 grands axes :
- Un axe technique avec l'utilisation des traitements des eaux avancés et une réduction des pertes par les réseaux d'assainissement ;
- Un axe éducatif et informatif auprès des professionnels de la santé et des patients ;
- Un axe de développement de la pharmacie « écologique » ou chimie verte.
Bibliographie
Archives
Dernière vérification le 29/03/2024
Documents
Exporter la substance
Choisissez le format de l'export :

