Configuration de votre affichage
Vous avez activé le mode de configuration de l'affichage qui permet de sélectionner les informations que vous souhaitez afficher sur la fiche substance. Une fois que vous aurez sélectionné les rubriques à afficher, vous pouvez revenir au mode de consultation de la fiche substance en cliquant à nouveau sur le bouton de filtrage.
Toluène (108-88-3)
Informations générales
Dernière vérification le 18/12/2025
Identification
Numero CAS
108-88-3
Nom scientifique (FR)
Toluène
Nom scientifique (EN)
Autres dénominations scientifiques (FR)
Autres dénominations scientifiques (Autre langues)
Code EC
203-625-9
Code SANDRE
1278
Numéro CIPAC
-
Formule chimique brute
\(\ce{ C7H8 }\)
Code InChlKey
Code SMILES
c(cccc1)(c1)C
Classification CLP
Type de classification
Harmonisée
ATP insertion
CLP00
Description de la classification
Classification harmonisée selon réglement 1272/2008 ou CLP
| Mention du danger - Code | H225 |
|---|---|
| Mention du danger - Texte | Liquide et vapeurs très inflammables |
| Classe(s) de dangers | Liquides inflammables |
| Libellé UE du danger | - |
| Limites de concentration spécifique | - |
| Facteur M | - |
| Estimation de toxicité aigüe | - |
| Mention du danger - Code | H315 |
|---|---|
| Mention du danger - Texte | Provoque une irritation cutanée |
| Classe(s) de dangers | Corrosion / Irritation cutanée |
| Libellé UE du danger | - |
| Mention du danger - Code | H336 |
|---|---|
| Mention du danger - Texte | Peut provoquer somnolence ou vertiges |
| Classe(s) de dangers | Toxicité spécifique pour certains organes cibles (exposition unique) |
| Libellé UE du danger | - |
| Limites de concentration spécifique | - |
| Facteur M | - |
| Estimation de toxicité aigüe | - |
| Mention du danger - Code | H304 |
|---|---|
| Mention du danger - Texte | Peut être mortel en cas d'ingestion et de pénétration dans les voies respiratoires |
| Classe(s) de dangers | Danger par aspiration |
| Libellé UE du danger | - |
| Mention du danger - Code | H361d |
|---|---|
| Mention du danger - Texte | Susceptible de nuire au fœtus. |
| Classe(s) de dangers | Toxicité pour la reproduction |
| Libellé UE du danger | - |
| Mention du danger - Code | H373 |
|---|---|
| Mention du danger - Texte | Risque présumé d'effets graves pour les organes (indiquer tous les organes affectés, s'ils sont connus) à la suite d'expositions répétées ou d'une exposition prolongée (indiquer la voie d'exposition s'il est formellement prouvé qu'aucune autre voie d'exposition ne conduit au même danger) |
| Classe(s) de dangers | Toxicité spécifique pour certains organes cibles (exposition répétée) |
| Libellé UE du danger | - |
| Limites de concentration spécifique | - |
| Facteur M | - |
| Estimation de toxicité aigüe | - |
Méthodes analytiques
Air
Prélèvement
Analyse
Eau
Analyse
Sol
Analyse
Règlementations
Physico-Chimie
Dernière vérification le 29/03/2024
Généralités
Poids moléculaire
92.15 g/mol
Tableau des paramètres
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Bibliographie
Comportement et devenir dans les milieux
Dernière vérification le 09/09/2025
Matrices
Milieu eau douce
Volatilisation :
D'après la constante de Henry (537 Pa.m3.mol-1), calculée à partir de la pression de vapeur (3000 Pa) et de la solubilité (515 mg.L-1), le toluène en solution aqueuse a une forte tendance à se volatiliser. (E.C., 2003a)
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Milieu sédiment eau douce
Adsorption :
D'après le Koc (177 L.kg-1), la substance semble être modérément adsorbable. (E.C., 2003a)
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Milieu terrestre
Bien que moyennement mobile dans les sols, il peut atteindre les eaux souterraines.
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Persistance
Biodégradabilité
Biodégradabilité :
Le toluène est facilement biodégradable. Cependant, il pourrait persister dans les eaux naturelles à de faibles concentrations (< 100 µg.L-1).
La présence d'autres produits chimiques organiques (thiophene, pyrrole, méthylpyrrole et benzofurane) diminue la dégradation du toluène de 100% à 10% après 4 jours. (E.C., 2003a)
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Dégradabilité abiotique
Hydrolyse :
Aucune réaction d'hydrolyse n'est attendue en conditions environnementales. (E.C., 2003a)
Photolyse :
La substance n'absorbe pas les rayons lumineux de longueurs d'ondes supérieures à 290 nm. Elle n'est donc pas susceptible de subir une photolyse directe en conditions environnementales. (E.C., 2003a)
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Milieu eau douce
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Milieu terrestre
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Bioaccumulation
Organismes aquatiques
Plusieurs résultats d'essais sont disponibles :
- Poissons : Leuciscus idus (3 jours) BCF : 90,
- Mollusques : Tapes semidecussata (2 - 8 jours) BCF : 1,7.
Un BCF de 90 peut être retenu mais de façon générale, la substance présente un faible potentiel de bioaccumulation (ce qui est confirmé par le faible coefficient de partage octanol-eau).
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Organismes terrestres
Aucun résultat d’essai valide n’a pu être trouvé dans la littérature.
Conclusion sur la bioaccumulation
Bioaccumulation :
La valeur maximale de 90 observée chez Leuciscus idus melanotus est utilisée dans l'évaluation de risque du toluène. Ce résultat suggère que la bioconcentration du toluène chez les organismes aquatiques est faible. (E.C., 2003a)
Bibliographie
Toxicologie
Dernière vérification le 05/10/2025
Introduction
L'ensemble des informations et des données toxicologiques provient de diverses monographies publiées par des organismes reconnus pour la qualité scientifique de leurs documents (ATSDR, 1994, 2000 ; EU, 2003 ; IARC, 1999 ; INRS, 2021 ; US EPA, 2005). Les références bibliographiques aux auteurs sont citées pour permettre un accès direct à l’information scientifique mais n’ont pas fait l’objet d’un nouvel examen critique par les rédacteurs de la fiche. Ces données ont été complétées par une recherche bibliographique sur les dernières années.
Toxicocinétique
Chez l'homme
Absorption
La principale voie de pénétration du toluène est la voie respiratoire, l’ingestion restant un phénomène accidentel ou volontaire.
Par inhalation, l’absorption est rapide : 10 à 15 minutes après le début de l’exposition (Carlsson, 1982). Le taux d’absorption (environ 50 %) est proportionnel au niveau de ventilation pulmonaire (Löf et al., 1993).
Par voie orale, le toluène est entièrement absorbé (100 %) (Baelum et al., 1985).
L’absorption cutanée est lente (14 à 23 mg.cm-2.h-1) et faible, environ 1% (Dutkiewicz et Tyras, 1968 ; Riihimäki et Pfäffli, 1978).
Distribution
Le toluène se distribue et s’accumule dans les tissus adipeux et richement vascularisés, notamment le cerveau, mais aussi de nombreux autres compartiments (foie, rein, moelle osseuse).
Métabolisme
Quatre-vingt-dix-neuf pour cent du toluène sont métabolisés sous forme d’acide benzoïque après oxydation par les cytochromes P450 hépatiques principalement les isoformes 2E1 (Nakajima, 1997) (figure X). Puis, toujours au niveau hépatique, l’acide benzoïque réagit principalement avec la glycine pour former l’acide hippurique. Parmi les autres métabolites formés, les crésols présentent une action toxique : ils pourraient former de la méthylhydroquinone et de la méthylbenzoquinone, qui pourraient être à l’origine d’effets cancérigènes ou d’effets sur la reproduction (Murata et al., 1999 ; Woiwode et al., 1979 ; Woiwode et Drysch, 1981).
Schéma métabolique (INRS, 2021) :
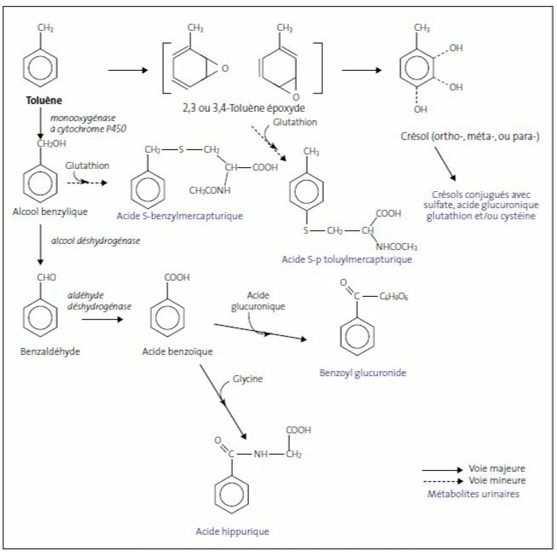
Élimination
Le toluène est éliminé principalement par voie pulmonaire sous forme inchangée (15 %), ou par voie urinaire, sous forme de métabolites (80 à 90%) présents majoritairement sous forme d’acide hippurique ou d’acides mercapturiques comme métabolites mineurs. Enfin, l’excrétion rénale de l’acide S-p-toluylmercapturique est bien corrélée l’exposition au toluène (Angerer et al., 1998).
Chez l'animal
Absorption
Inhalation : Le taux d’absorption par inhalation varie en fonction du niveau de ventilation, il est d’environ 90% (Bergman, 1979 ; Egle et Gochberg, 1976 ; Hobara et al., 1984).
Voie orale : L’absorption orale du toluène est presque complète (>99%) chez le rat, après un gavage (El Masry et al., 1956 ; Smith et al., 1954 ; Turkall et al., 1991).
Voie cutanée : L’absorption cutanée varie avec la concentration et la durée de l’exposition, mais reste faible (Morgan et al., 1991).
Distribution
Pour des expositions aussi bien par inhalation que par voie orale, il a été montré que le toluène était retrouvé dans le foie et dans une moindre mesure dans le cerveau chez le rat ou le chien (Benignus et al., 1984 ; Harabuchi et al., 1993 ; Ikeda et al., 1990 ; Pyykko et al., 1977)
Un passage placentaire est observé : environ 74% de la concentration mesurée chez la mère est retrouvée chez le fœtus 2 h suivant une exposition par inhalation à 1 375 ou 2 700 mg.m-3 pendant 24 h chez le rat (Ungvary, 1984). Les concentrations de toluène dans le lait maternel sont environ 5 fois plus élevées (Da-Silva et al., 1991).
Métabolisme
Comme chez l’homme, la majorité du toluène est métabolisée par des oxydations au niveau hépatique par les cytochromes P450, principalement les isoformes 2E1. Il est oxydé successivement en alcool benzylique, en benzaldéhyde puis en acide benzoïque qui est conjugué avec la glycine pour former l’acide hippurique (métabolite majoritaire) ou avec l’acide glucuronique pour former le benzylglucuronide (métabolite secondaire). Une voie de métabolisation mineure (environ 1 % du toluène) consiste en une oxydation du toluène en ortho-, méta- ou para-crésol qui sont ensuite conjugués avec des sulfates ou de l’acide glucuronique (EU, 2003 ; INRS, 2021).
Élimination
La majorité du toluène est éliminé par voie urinaire sous forme de métabolites principalement l’acide hippurique. Le toluène non métabolisé est exhalé ou éliminé par voie urinaire.
Autre
Mécanisme d'action :
Plusieurs hypothèses pourraient expliquer le mécanisme d’action du toluène.
Certains métabolites tels que les o-crésols pourraient agir directement du fait de propriétés neuroactives (EU, 2003)
Au niveau moléculaire, le toluène pourrait se substituer au cholestérol membranaire ce qui modifierait la fluidité membranaire et altérerait les communications entre les cellules et les mouvements ioniques normaux (Engelke et al., 1996). La présence de toluène dans les régions hydrophobes des protéines et les interactions liées altèrerait l’activité des enzymes membranaires et/ou des récepteurs spécifiques (Balster, 1998). Le toluène augmenterait la fonction de l’acide gamma-aminobutyrique de type A (GABAA) (Mihic et al., 1994), atténuant le récepteur N-méthyl-D aspartate stimulé par le flux calcique (Cruz et al., 1998) et activant les systèmes dopaminergiques (Von Euler, 1994a) et inhibant les canaux calciques sensibles au voltage (Tillar et al., 2002). Le toluène inhiberait le signal de transduction par stimulation des récepteurs humains de l’acide muscarinique dans les cellules ovariennes du hamster chinois (Tsuga et al., 2002)
Des altérations moléculaires pourraient également être liées à l’oxydation par les radicaux libres (Burmistrov et al., 2001) et la présence de marqueurs du stress oxydatif a été récemment rapportée dans le foie et le rein de rats traités par le toluène et dans le sang de travailleurs exposés (Salihu, 2022 ; Dehghan Haghighi, 2022).
Synthèse
Chez l’homme, après inhalation, l’absorption est d’environ 50 %, l’absorption par voie orale est de 100%. Le toluène s’accumule dans les tissus adipeux mais il est également retrouvé dans de nombreux organes (cerveau, foie...). Il est métabolisé en acide benzoïque au niveau hépatique puis en acide hippurique. Le toluène est éliminé au niveau pulmonaire sous forme inchangé ou dans les urines sous forme de métabolites.
Chez l’animal, l’absorption du toluène est complète pour des expositions par voie orale et peut être de 90 % par inhalation. La voie cutanée est secondaire. Le toluène passe la barrière placentaire et est retrouvé dans le lait maternel. Le métabolisme du toluène chez l’animal est proche de celui observé chez l’homme et son élimination se fait aussi principalement dans l’urine sous forme de métabolites conjugués. Le mécanisme d’action du toluène pourrait passer par des altérations membranaires ou une action via les radicaux libres.
Equivalents biosurveillance
Description
VBI issues de la population générale adulte (Biotox, 2022)

Toxicité aiguë
Généralités
Chez l’homme, la toxicité aiguë du toluène est relativement faible quelle que soit la voie d’exposition.
Chez l'homme
Toutes voies
Chez l'homme, la toxicité aiguë du toluène est relativement faible quelle que soit la voie d'exposition.
Inhalation
Par inhalation, des expositions comprises entre 281 et 562 mg.m-3 (73 et 147 ppm) induisent des maux de tête, des vertiges, une irritation des muqueuses et une somnolence (Echeverria et al., 1989). Aux concentrations inférieures ou égales à 150 mg.m-3 (40 ppm), la survenue de ces symptômes est moins fréquente (Andersen et al., 1983). Dans cette étude menée chez 16 volontaires, exposés 6 heures par jour, pendant 4 jours consécutifs, aux concentrations de 0 – 10 – 40 – 100 ppm (0 – 40 – 150 – 380 mg.m-3), aucun effet n’est observé à 10 et 40 ppm. A 100 ppm, des effets neurologiques (sensation d’ivresse, mal de tête, étourdissement) ont été observés.
L’étude de Kobald et al. (2015) a été réalisée sur 33 volontaires sains répartis aléatoirement en 2 groupes (l’historique des sujets est non renseignée, l’âge moyen est de 25 ans) : un groupe témoin de 16 individus dont 9 femmes et un groupe exposé de 17 individus dont 10 femmes. L’exposition au toluène est réalisée dans une chambre d’exposition à une concentration analytique unique de 200 ppm (760 mg.m-3) pendant 40 minutes. Des tests comportementaux ont été réalisés hors de la chambre d’exposition, en se basant sur des tâches d’attention et de discrimination visuelle. Les résultats montrent un effet du toluène sur la discrimination visuelle, plus particulièrement dans la condition LOB (discrimination visuelle en présence d’un distracteur lié à l’orientation de l’objet).
Une autre étude a exposé des sujets cliniquement sensibles au toluène (9 hommes et 11 femmes d’âge moyen 39,5 ans) de manière contrôlée à 15 ppm de toluène pendant 20 minutes (Little et al., 1999). Ces sujets ont ensuite été soumis à une batterie de tests neuropsychologiques. Le mode de recrutement de ces sujets n’est pas précisé et il n’y a pas de groupe témoin dans cette étude mais les tests ont été réalisés chez les sujets avant et après l’exposition. Les tests comportent notamment des tests de mémoire immédiate ou retardée, des temps de réaction, des modifications de lettres, « digit symbol » et des tests relatifs à la vision des couleurs. Une altération des performances est observée au cours de ces tests.
Voie orale
L’ingestion de 60 mL de toluène (625 mg.kg-1) a entrainé la mort d’un homme de 51 ans dans les 30 minutes après l’ingestion (Ameno et al., 1989). La cause probable de la mort est attribuée à une dépression sévère du système nerveux central. Les troubles observés sont généralement réversibles dans les quelques heures suivant l’arrêt de l’exposition.
voie oculaire
Des effets irritants oculaires sont observés pour des expositions de 7 h dès 281 mg.m-3 (75 ppm) chez le volontaire sain (Echeverria et al., 1989).
Synthèse
Chez l'homme, la toxicité aiguë du toluène est modérée avec des effets neurologiques quelle que soit la voie d’exposition. Des effets irritants ont également été observés.
Chez l'animal
Inhalation
Les effets observés par inhalation sont un larmoiement, une rhinorrhée, une polypnée, une ataxie, une agitation, des perturbations de l’équilibre, une incoordination motrice, une narcose, une salivation (pour les concentrations les plus élevées) et aussi des modifications neurochimiques. Ces effets sont réversibles.
Les effets hépatiques liés à l’exposition au toluène ont été investigués. L’exposition subaiguë par inhalation à des vapeurs de toluène, 4 heures par jour, pendant 7 jours, à des concentrations comprises entre 1 400 et 1 500 ppm (5 360 et 5 745 mg.m-3), induit chez le rat Wistar des altérations hépatiques visualisées par une expression histologique de marqueurs de dommage tels que les protéines du choc thermique et le cytochrome P450 2E1 (Gotohda et al., 2009).
Voie orale
Une exposition unique par voie orale, administrée par gavage, aux doses de 250 à 1 000 mg.kg-1, induit des altérations de l’intégrité du système visuel mesurées par le test flash des potentiels évoqués (Dyer et al., 1988). Une dépression statistiquement significative de l’amplitude est identifiée dès la dose de 250 mg.kg-1.j-1. De cette étude, un LOAEL de 250 mg.kg-1.j-1 a été établi. Des expositions à 375 mg.m-3 (100 ppm), 3 heures par jour pendant 5 jours ou 4 heures chez le rat DA/HAN, induisent un nystagmus optocinétique* pouvant être à l’origine de vertiges (Hogie et al., 2008).
*Certains types de mouvements des yeux lorsque ces derniers sont soumis à des déplacements d'objets qui défilent dans un champ visuel.
Voie cutanée
Le toluène est un irritant cutané (Exxon, 1988), oculaire (Exxon, 1995 ; Guillot et al., 1982b ; Sugai et al., 1990) chez le lapin et respiratoire chez la souris (De Ceaurriz et al., 1981 ; Muller et Greff, 1984 ; Nielsen et Alarie, 1982), pour des expositions à des concentrations élevées. Il n’est pas classé corrosif ou sensibilisant par l’Union Européenne.
Synthèse
Chez l’animal, le toluène est faiblement toxique suite à des expositions aiguës : DL50 comprises entre 5 500 à 7 500 mg.kg-1 et CL50 comprises entre 12,5 à 45,8 mg.L-1 (3 262,5 à 11 954 ppm). Les principaux effets rapportés correspondent à des effets irritants locaux ou des effets neurologiques.
L’ensemble des doses et concentrations létales pour les différentes voies d’exposition sont regroupées dans le tableau ci-dessous :

Toxicité à doses répétées
Effets généraux
Chez l'homme
Inhalation
Effets neurologiques:
A concentrations élevées, des effets neurologiques sévères comportant des dysfonctionnements cérébraux tels que des tremblements, une ataxie, une ototoxicité, des troubles de la mémoire ainsi qu’une atrophie du cervelet sont décrits.
L’exposition professionnelle de type chronique aux solvants induit un syndrome psycho-organique (Arlien -Soborg, 1992). Deux études ont permis d’identifier la survenue de ce syndrome suite à des expositions au toluène, d’une part pour des expositions de 12 ans à des concentrations de 190 à 304 mg.m-3 (50 à 79 ppm) associées à des expositions antérieures pouvant atteindre 3 800 mg.m-3 (992 ppm) (Larsen et Leira, 1988), d’autre part pour des expositions moyennes de 43 et 157 mg.m-3 (11 et 41 ppm) pendant environ 29 ans (Orbaek et Nise, 1989). Les principaux symptômes associés sont une neurasthénie et une diminution des performances lors de tests psychomoteurs. Les études récentes confirment ces effets et soulignent l’importance de la durée de l’exposition comme facteur principal de survenue des effets rapportés (Herpin et al., 2009).
Les études visant à identifier des diminutions des performances par des tests neuropsychologiques confirment les résultats obtenus dans les cas d’études de toxicité aiguë.
Les études réalisées en milieu professionnel montrent qu’une exposition chronique à des concentrations comprises entre 30 et 130 ppm (115 et 500 mg.m-3) induit notamment des atteintes neurologiques (Abbate et al., 1993 ; Boey et al., 1997 ; Cavalleri et al., 2000 ; Chouanière et al., 2002 ; Eller et al., 1999 ; Foo et al., 1990 ; Gericke et al., 2001 ; Murata et al., 1993 ; Nakatsuka et al., 1992 ; Neubert et al., 2001 ; Shaper et al., 2003 ; Vrca et al., 1995 ; Zavalic et al., 1998a ; Zavalic et al., 1998b ; Zupanic et al., 2002). Pour ces études, différents tests ont été utilisés : des tests neurocomportementaux, auditifs, visuels, … Les principales altérations rapportées sont une altération du comportement, des potentiels évoqués auditifs et visuels, des paramètres électro-physiologiques, de la vision des couleurs ou de la vitesse critique de fusion. Ainsi, dans l’étude de Zavalic et al. (1998a), une augmentation, non statistiquement significative, de l’indice de confusion des couleurs est rapportée chez les salariés de la chaussure pour des expositions chroniques au toluène de 35 ppm (134 mg.m-3), les effets étant corrélés chez le groupe exposé à 132 ppm (498 mg.m-3). Une perte d’audition dans les hautes fréquences est notée après des expositions au toluène. Une LOAEC de 563 mg.m-3 (147 ppm) a été définie (Morata et al., 1993). Les résultats des principales études sont rapportés dans le tableau ci-après. La méta-analyse de (Meyer-Baron, 2005) a porté sur 22 études (Antti-Poika et al., 1985 ; Boey et al., 1997 ; Cherry et al., 1984 ; Cherry et al., 1985 ; Chia et al., 1987 ; Chouanière et al., 2002 ; Deschamps et al., 2001 ; Eller et al., 1999 ; Foo et al., 1993 ; Gericke et al., 2001 ; Haenninen et al., 1987 ; Iregren, 1982 ; Kang et al., 2005 ; Kempe et al., 1980 ; Larsen et Leira, 1988 ; Lee et al., 1988 ; Morck et al., 1988 ; Neubert et al., 2001 ; Orbaek et Nise, 1989 ; Seeber et al., 2004 ; Ukai et al., 1993) mais seules 10 d’entre elles ont été retenues. Cette méta-analyse a montré que le toluène induisait une baisse des performances dans 5 des 6 tests neuropsychologiques explorant les domaines de l’attention et de la visualisation spatiale et de la compétence motrice pour des niveaux d’exposition compris entre 33 et 89 ppm (126 et 340 mg.m-3).
Principales études épidémiologiques rapportant des effets neurologiques (d’après US EPA, 2005a)



Certains auteurs identifient des effets pour des expositions à des concentrations légèrement inférieures (Tanaka et al., 2003). Dans cette étude, menée sur 20 travailleurs exposés à de faibles concentrations de toluène comprises entre 15,3 et 31,4 ppm (59 et 120 mg.m-3), les concentrations urinaires en acide hippurique ont été comparées aux concentrations atmosphériques en toluène et se sont révélées bien corrélées. Les atteintes du système nerveux central sont apparues associées aux expositions au toluène.
En revanche, les résultats de certaines études sont moins concluants du fait des tests utilisés et des faibles niveaux d’exposition rapportés (Seeber et al., 2004).
Enfin, il a été mis en évidence que l’exposition combinée au toluène et au bruit, liée aux activités professionnelles, pouvait agir en synergie dans la perte d’audition des hautes fréquences (Schäper et al., 2008).
Des études menées chez des individus exposés au toluène de manière chronique dans le cadre d’une consommation abusive ont permis d’identifier que le toluène altérait de manière préférentielle la substance blanche et les régions périventriculaire ou subcorticale. Toutefois, dans ce type de contexte, il s’agit très souvent de co-expositions par addictions multiples (Yücel et al., 2008).
Effets hépatiques :
L’atteinte hépatique n’est pas clairement établie : deux études réalisées chez des salariés donnent des résultats contradictoires. La première, réalisée par (Waldron et al., 1982), ne retrouve pas de modification des niveaux d’aspartate aminotransférase et d’alanine aminotransférase chez des hommes exposés professionnellement à 375 mg.m-3 (98 ppm).
Effets rénaux :
Aucune altération rénale n’est détectée pour une exposition professionnelle à 382 mg.m-3 (100 ppm) pendant 6,5 heures (Nielsen et al., 1985), alors que dans certains cas d’expositions accidentelles ou chez les toxicomanes inhalant du toluène, à des concentrations plus élevées, surviennent des atteintes rénales (oligurie, myoglobinurie) qui seraient secondaire à une rhabdomyolyse (Reisin et al., 1975) et des acidoses (Gerkin et Lo Vecchio, 1998 ; Goodwin, 1988 ; Jone et Wu, 1988 ; Meulenbelt et al., 1990 ; Patel et Benjamin, 1986). Pour des expositions comprises entre 97 et 232 mg.m-3 (26-62 ppm), il n’y a pas d’élévation des marqueurs urinaires précoces des atteintes rénales glomérulaires (micro-albumine, N-acétyl D-glucosaminidase et alanine-aminopeptidase), mais une altération de la fonction identifiée par l’élévation de la clairance de la créatinine (Stengel et al., 1998).
Effets cardiovasculaires :
Il n’existe pas de données mentionnant des altérations des paramètres sanguins chez l’homme. Une légère augmentation de la pression systolique est observée pour des expositions professionnelles de 375 mg.m-3 (98 ppm) pendant 20 ans, alors que la pression diastolique demeure inchangée (Morck et al., 1985).
Synthèse
Chez l’homme, des expositions chroniques au toluène induisent des effets neurotoxiques sévères pour des expositions à des concentrations élevées. Aux concentrations rencontrées lors d’expositions professionnelles, des effets neurotoxiques surviennent pour des expositions comprises entre 30 et 130 ppm (115 et 500 mg.m-3) ; il s’agit de troubles du comportement, d’altérations de la réponse au test des potentiels évoqués visuels ou de la vision des couleurs. Des effets hépatiques et rénaux sont parfois décrits.
Chez l'animal
Inhalation
Effets neurologiques
Les nombreuses études réalisées chez l’animal permettent de confirmer les effets observés chez l’homme. Ces effets correspondent à des effets neurotoxiques : une atteinte de l’hippocampe, une modification des neurotransmetteurs et une ototoxicité. Cette dernière est rapportée pour des expositions aux concentrations comprises entre 700 et 1 500 ppm (2 681 et 5 745 mg.m-3) (Campo et al., 1997 ; Johnson et Canlon, 1994 ; Lataye et Campo, 1997 ; Lataye et al., 1999 ; Loquet et al., 1999 ; McWilliams et al., 2000 ; Pryor et al., 1984).
Des rats mâles exposés au toluène aux concentrations de 0 – 40 – 80 - 160 - 320 ppm (0 – 153 – 306 – 612 – 1 225 mg.m-3), 6 heures par jour, 5 jours par semaine pendant 4 semaines, suivi par une période de post-exposition de 29 à 40 jours, présentent une diminution du poids du cerveau au niveau du putamen et des zones sous-corticales limbiques aux concentrations de 80 ppm (306 mg.m-3) et au-delà (Hillefors-Berglund et al., 1995).
Chez la souris, des expositions sub-chroniques à des concentrations élevées de toluène de 0 - 1 000 – 3 600 – 6 000 ppm (0 – 3 830 – 13 800 – 22 980 mg.m-3) 30 minutes par jour pendant 40 jours, induisent une altération des performances, suggérant un impact sur les fonctions cognitives et psychomotrices (Bowen et McDonald, 2008). Pour des expositions au toluène à des niveaux plus faibles de l’ordre de 40 ppm (153 mg.m-3), 104 heures par semaine, pendant 16 semaines chez des rats Sprague-Dawley, il a été montré des altérations neurocomportementales et neurochimiques induisant une narcose, une diminution de l’activité d’apprentissage et des altérations des transmissions de dopamine et de sérotonine (Berenguer et al., 2003 ; Berenguer et al., 2004).
L’inhalation chronique de toluène à une concentration de 500 mg.m-3 chez le rat, 4 heures par jour, 5 jours par semaine pendant un mois, augmente l’activité de l’enzyme glutathion peroxydase dans les tissus cérébraux, ce qui témoigne de la libération accrue de radicaux libres et de l’augmentation du phénomène de peroxydation lipidique (Burmistrov et al., 2001).
Effets immunologiques
Une étude de toxicité sub-chronique par inhalation a été menée chez des souris C3H, exposés à 0 ou 50 ppm (0 ou 190 mg.m-3), 6 heures par jour et 5 jours par semaine pendant 6 ou 12 semaines (Fujimaki et al., 2007). A la dose de 50 ppm, il est observé une augmentation significative du nombre total de lymphocytes et de macrophages dans le liquide de lavage broncho-alvéolaire. Une diminution significative de la production d’interféron-gamma et de substance P est constatée. L’augmentation de la production de neurotrophine-3 dans le fluide broncho-alvéolaire n’a été constatée que lors de l’exposition pendant 12 semaines. Cette étude suggère qu’une exposition à long terme au toluène module la réponse inflammatoire des voies aériennes via une signalisation neurologique.
Une interaction entre les systèmes immunitaire et neurologique est probable au niveau de l’hippocampe l les neurotrophines et leurs récepteurs (Win-Shwe et Fujimaki, 2010). Des expositions à de relativement faibles niveaux de toluène pourraient altérer les fonctions de l’hippocampe en modulant les gènes dépendant des neurotrophines et leurs signaux. Il a été montré que cette stimulation allergique diminue le seuil de sensibilité au toluène chez une espèce de souris particulièrement sensible, la souris C3H/HeN (Win-Shwe et Fujimaki, 2010). Une autre étude menée chez la même espèce de souris a montré que la modification des biomarqueurs de l’immunité non-spécifique était dépendante du stade de développement lors de la période d’exposition : au cours de la gestation, chez le jeune (2 ou 8 jours après la gestation) (Win-Shwe et al., 2012).
Autres effets
Des rats F344/N et des souris B6C3F1 ont été exposés à des concentrations de 0 - 100- 625 – 1 250 – 2 500 – 3 000 ppm de toluène, 6,5 heures par jour, 5 jours par semaine, pendant 14 semaines et à des concentrations de 0 – 600 – 1 200 ppm de toluène, 6,5 heures par jour, 5 jours par semaine, pendant 2 ans (Huff, 1990). Chez le rat, aux concentrations élevées supérieures à 1 250 ppm (4 688 mg.m-3), une diminution du nombre des leucocytes de 12 à 18% est observée ainsi que des augmentations relatives des poids de certains organes (reins, foie, cerveau, cœur, poumons et testicules). Les études de 15 semaines et 2 ans du NTP (Huff, 1990) rapportent des érosions de l’épithélium olfactif et une dégénérescence de l’épithélium nasal pour les expositions à des concentrations de 600 et 1 200 ppm (2 250 et 4 500 mg.m-3) et une augmentation non statistiquement significative des ulcères du pré-estomac (portion aglandulaire de l’estomac des rongeurs) chez les mâles aux deux concentrations. Une augmentation des néphropathies est également rapportée pour la concentration la plus élevée (1 200 ppm ou 4 500 mg.m-3). Chez la souris, des altérations relatives du poids des poumons sont observées dès 100 ppm (375 mg.m-3) et à des concentrations supérieures pour les autres organes (reins, foie).
Voie orale
Une série d’étude a été menée chez la souris exposée pendant 28 jours au toluène via l’eau de boisson à des doses de 0 – 5- 22 -105 mg.kg-1.j-1 (Hsieh et al., 1989, 1991) ou de 0 – 22 84 mg.kg-1.j-1 (Hsieh et al., 1990). Ces études ont évalué différents paramètres du système immunitaire dont le poids de la rate et du thymus et leur histologie et des tests in vitro ((prolifération lymphocytaire stimulée par les mitogènes, réaction lymphocytaire mixte, test de production d'IL-2 et réponse des anticorps PFC)ont été réalisés. Ces tests ont mis en évidence une altération du système immunitaire (diminution statistiquement significative du poids du thymus et de la réponse à l’ensemble des tests in vitro) pour des expositions à 84 ou 105 mg.kg-1.j-1 mais ne sont pas retrouvés à 22 mg.kg-1.j-1. Une autre étude menée chez des souris, exposées par voie orale au toluène à des doses de 5 à 105 mg.kg-1.j-1 dans l’eau de boisson pendant 28 jours, a mis en évidence une augmentation significative des neurotransmetteurs monoamines (noradrénaline, dopamine et sérotonine) mesurée pour toutes les doses. De cette étude, un LOAEL de 5 mg.kg-1.j-1 est défini (Hsieh et al., 1990).
Une étude de toxicité sub-chronique a été menée par gavage chez le rat F-344 (NTP, 1990). Des groupes de 10 rats (par sexe et par groupe) ont reçu du toluène dans de l’huile de maïs aux doses de 0 - 312 - 625 - 1 250 - 2 500 - 5 000 mg.kg-1, 5 jours par semaine pendant 13 semaines. Les doses de toluène ajustées à 7 j/7 sont de 0 - 223 - 446 - 893 - 1 786 - 3 571 mg.kg-1.j-1. Tous les animaux exposés à la dose de 3 571 mg.kg-1.j-1 sont morts au cours de la première semaine et ont été éliminés de la suite de l’étude. Une mortalité importante est également observée chez les animaux exposés à la dose de 1 786 mg.kg-1.j-1. De nombreux effets toxiques sont rapportés à la dose de 1 786 mg.kg-1.j-1 correspondant à des états de prostration, d’hypoactivité, d’ataxie, de piloérection, de larmoiement, d’hypersalivation et de tremblements corporels. Une diminution du poids corporel des mâles est la seule altération significative (p<0,05) rapportée à cette dose. Il n’y a pas d’altérations des paramètres hématologiques ou urinaires. Certaines modifications des paramètres biochimiques sont cependant rapportées : augmentation significative (p<0,05) de la glutamo- oxaloacétique transaminase sérique (SGOT) chez les mâles exposés à la dose de 1 786 mg.kg-1.j-1 et une augmentation de l’activité cholinestérase chez les femelles exposées à la même dose. Différentes altérations pathologiques et des modifications du poids du foie, des reins, du cerveau et de la vessie sont observées. Chez les mâles, les poids relatifs et absolus du foie et des reins sont significativement (p<0,05) augmentés dès la dose de 446 mg.kg-1.j-1. Des anomalies histopathologiques hépatiques (hypertrophie hépatocellulaire) à la dose de 1 786 mg.kg-1.j-1, rénales (néphrose et altérations de l’épithélium tubulaire), cérébrale (minéralisation focalisées et nécroses neuronales) et de la vessie (hémorragies musculaires) sont rapportées. Aucune inclusion hyaline n’est observée au niveau tubulaire proximal. De cette étude, un NOAEL de 223 mg.kg-1.j-1 est déterminé ainsi qu’un LOAEL de 446 mg.kg-1.j-1 basé sur les modifications pondérales hépatiques et rénales chez le rat mâle.
L’exposition de rats âgés de 1, 4, 12 et 24 mois à des doses de toluène de l’ordre de 1 000 mg.kg-1.sem-1, a montré une influence de l’âge sur l’augmentation de la susceptibilité et de la variabilité de l’activité motrice pour des expositions par voie orale (MacPhail et al., 2012).
Chez la souris B6C3F1, des doses de 0 – 312 – 625 – 1 250 – 2 500 – 5 000 mg.kg-1 de toluène dans l’huile de maïs ont été administrées par gavage pendant 13 semaines (Huff, 1990). Toutes les souris meurent à la dose la plus élevée et une forte mortalité survient également à la dose de 1 250 mg.kg-1. Une augmentation statistiquement significative du poids relatif du foie des mâles est décrite aux doses de 1 250 et 2 500 mg.kg-1 ainsi qu’une augmentation statistiquement significative du poids relatif et absolu du foie des femelles aux doses de 312 mg.kg-1. Une augmentation des poids relatifs du cerveau et des testicules et du poids absolu des reins est observée chez les mâles à 5 000 mg.kg-1.
Synthèse
Chez l’animal, les effets rapportés confirment ceux décrits chez l’homme pour des expositions par inhalation. Pour les expositions par voie orale, le toluène induit des effets neurologiques, des altérations du poids du foie, des reins, du cerveau, associées à des modifications histopathologiques hépatiques et rénales.
Effets cancérigènes
Généralités
Peu d’études ont évalué la cancérogénicité du toluène tant chez l’homme que chez l’animal.
Classifications
| Organisme | Classification | Année |
|---|---|---|
| UE | Non classé | 2008 |
| IARC | Groupe 3 : l’agent (ou le mélange) ne peut être classé pour sa cancérogénicité pour l’homme | 1999 |
| US EPA | Non classé | 2005 |
Chez l'homme
Inhalation
L’IARC (1999) rapporte 8 études notant la présence de toluène au niveau des expositions dont une seule correspond à une exposition majoritaire au toluène. Cette étude épidémiologique a porté sur une cohorte suédoise de 1 020 salariés de la rotogravure exposés principalement au toluène, pendant un minimum de 3 mois, au cours de la période 1925 à 1985 (Svensson et al., 1990). Elle a été réalisée dans 8 usines, les niveaux d’exposition sont documentés depuis 1943 pour l’une d’entre elles et depuis 1969 pour les autres. D’après ces données d’exposition et les concentrations, mesurées de toluène dans le sang et dans les graisses sous cutanées, les niveaux moyens d’exposition ont été estimés à environ 450 ppm (1 700 mg.m-3) dans les années 40 et 50 et de l’ordre de 30 ppm (113 mg.m-3) depuis le milieu des années 80. De plus, l’exposition concomitante au benzène est considérée comme ayant cessé au début des années 60. Cette étude montre un excès de mortalité pour l’ensemble des cancers SMR de 1,4 (95 %, IC : 1,0-1,9). Un excès de risque est observé pour les cancers du tractus respiratoire SMR de 1,4 (95 %, IC : 0,7-2,5), de l’estomac SMR : 2,7 (95 %, IC :1,1-5,6) ou colorectaux SMR de 2,2 (95 %, IC :0,9-4,5). Il n’existe pas d’excès de risque pour les cancers du système urinaire, les leucémies, les lymphomes ou les myélomes.
En 2005, l’US EPA considère que les études chez l’homme ne permettent pas de conclure.
Chez l'animal
Inhalation
Une étude a été menée chez les rats Fischer F344 (120 mâles et 120 femelles) exposés par inhalation à des concentrations de 0 – 112 – 375 – 1 125 mg.m-3 (0 – 30 – 100 – 300 ppm) de toluène, 6,5 heures par jour, 5 jours par semaine pendant 24 mois (Gibson et Hardisty, 1983). Aucun signe clinique n’a été observé lors de l’exposition et aucune altération pathologique ou histopathologique n’a été relevée. Dans cette étude, il semblerait que les niveaux d’exposition retenus soient trop faibles pour mener à bien une étude de cancérogenèse.
Deux études de cancérogenèse de 2 ans (rat et souris) pour des expositions par inhalation au toluène jusqu’à des concentrations de 1 200 ppm (4 600 mg.m-3), 6,5 heures par jour 5 jours par semaine (Huff, 2003 ; NTP, 1990) montrent qu’il n’y a pas d’effet observé chez le rat. En revanche, chez la souris, des adénomes non malins de la pars intermedia de l’hypophyse (type de tumeur très rare) sont retrouvés chez les femelles quelle que soit la concentration (460, 2 298, 4 598 mg.m-3) (120, 600, 1 200 ppm) et chez les mâles pour la plus forte concentration (4 598 mg.m-3 soit 1 200 ppm). Un seul adénome a été observé dans chacun des lots.
Voie orale
Une augmentation significative de l’incidence des tumeurs mammaires et des tumeurs malignes lymphoïdes a été observée chez un lot de 80 rats Sprague-Dawley mâles exposés à500 mg.kg-1 de toluène par gavage en une fois 4 à 5 jours par semaine pendant 104 semaines (Maltoni et al., 1983 ; Maltoni et al., 1985).
Voie cutanée
Chez la souris, une exposition a été pratiquée par voie cutanée au toluène, 2 fois par semaine, à un volume de 50 µL sur une surface de 1 cm2 au niveau de la région interscapulaire rasée du dos de 50 mâles pendant toute leur vie (Broddle et al., 1996). Cette exposition montre la survenue d’irritations cutanées et le développement de tumeurs. La différence statistique de l’incidence des tumeurs est juste en dessous du seuil de significativité (p = 0,055).
Synthèse
Il existe peu de données relatives aux effets cancérigènes du toluène aussi bien chez l’homme que chez l’animal et les rares données disponibles ne révèlent aucun développement de tumeurs néoplasiques ou de survenue de tumeurs. L’IARC classe le toluène en groupe 3, il n’est pas classé par l’US EPA et l’UE.
Effets génotoxiques
Généralités
Les nombreux essais réalisés sur Salmonella typhimurium se sont révélés négatifs même ceux utilisant les techniques de pré-incubation (EU, 2003). Les études de mutation génique, d’échanges de chromatides sœurs, de micronoyaux et de réparation d’ADN se sont toutes révélées négatives in vitro et in vivo pour des concentrations non cytotoxiques. Le toluène n’est donc ni mutagène ni génotoxique pour les modèles animaux testés aussi bien in vitro que in vivo. Certaines études sur les lymphocytes sanguins périphériques se sont révélées équivoques chez l’homme mais il est difficile, dans ses études, de différencier la part imputable au toluène de celle des autres solvants présents (EU, 2003). Une étude menée in vitro sur une lignée de cellules de l’épithélium pulmonaire humain (A549) exposées pendant une heure à 0,25 ppm montre la survenue de dommages à l’ADN mesurés par le test des comètes (Pariselli et al., 2009). Ces dommages sont réparés dans les 24 heures suivant l’exposition.
En l’absence d’effets cancérogènes et mutagènes, le toluène est considéré comme une substance à effet à seuil.
Classifications
| Organisme | Classification | Année |
|---|---|---|
| UE | Non classé | 2008 |
In vitro
Synthèse
Le toluène n’est ni mutagène ni génotoxique chez l’animal, les résultats sur cellules humaines sont équivoques, l’UE ne l’a pas classé.
Effets sur la reproduction
Chez l'homme
Toutes voies
L’impact du toluène sur les concentrations plasmatiques de FSH (hormone folliculo-stimulante), de LH (hormone lutéotrope) et de testostérone a été évaluée chez 262 hommes employés dans deux usines de l’industrie de la photographie au Danemark (Morck et al., 1988). Les résultats de cette étude sont difficilement exploitables en raison de l’absence de groupe témoin.
Deux études cas-témoin menées dans 2 industries suédoises (impression en héliogravure) montrent l’influence du toluène sur les niveaux des hormones LH, FSH et testostérone lors d’expositions professionnelles à des concentrations de 36 ppm (138 mg.m-3) (valeur moyenne) ou comprises entre 5 et 45 ppm (19 et 172 mg.m-3) (Svensson et al., 1992a ; Svensson et al., 1992b). Ces résultats montrent que le toluène à faible dose induit un effet sur l’axe hypothalamo-hypophysaire avec une diminution secondaire de la sécrétion de testostérone. Une action du toluène sur les mécanismes de la régulation endocrine est donc possible mais ne permet pas l’établissement d’une relation dose-effet.
Aucune étude relative à la qualité du sperme n’est disponible. Toutefois, les études de fertilité ne rapportent aucun effet pour des expositions comprises entre 10 et 200 ppm (38,3 et 766 mg.m-3) (Plenge-Bonig et Karmaus, 1999).
Chez la femme, le toluène n’induit pas de troubles menstruels (Ng et al., 1992a) pour des expositions moyennes de 88 ppm (337 mg.m-3), comprises entre 50 et 150 ppm soit 191,5 et 574,5 mg.m-3. Il semblerait, cependant, que des expositions quotidiennes à de faibles niveaux (< 10 mg.m-3) de toluène puissent induire une diminution de la fertilité chez la femme (Plenge-Bonig et Karmaus, 1999). Toutefois, il n’est pas exclu que d’autres facteurs d’exposition tels que le bruit ou le stress puissent également être impliqués dans les phénomènes observés.
Chez les salariées exposées au toluène, il a été montré une augmentation du risque de fausses couches et d’avortements spontanés pour des niveaux d’exposition de l’ordre de 50 à 150 ppm (191,5 à 574,5 mg.m-3) (Ng et al., 1992b ; Taskinen et al., 1994).
Synthèse
Si des effets sur la fertilité sont rapportés chez l’homme lors de l’exposition au toluène, ils ne permettent pas d’établir un lien causal fort. Chez les femmes, une augmentation du risque d’avortements spontanés a été décrite.
Chez l'animal
Inhalation
Chez la souris, le toluène passe la barrière placentaire : les concentrations chez les fœtus peuvent atteindre 75 % de celles mesurées dans le sang maternel (Ungvary et al., 1982). Le toluène se retrouve aussi dans le lait maternel à des concentrations 5 fois supérieures à celles mesurées dans le sang maternel (Da-Silva et al., 1991).
Il existe peu d’études sur la fertilité disponibles chez l’animal. Les études de fertilité chez le rat montrent l’absence d’effet pour des expositions à des concentrations de 2 000 ppm (7 500 mg.m-3) (API, 1985 ; Thiel et Chahoud, 1997).
De même, une exposition de 15 semaines, par inhalation, chez le rat ne montre pas de modifications de la morphologie des spermatozoïdes chez le mâle, ni de la cytologie vaginale, chez la femelle, pour des expositions de 383, 2 394 et 4 787 mg.m-3 (100, 625 et 1 250 ppm), 6,5 heures par jour, 5 jours par semaine (Huff, 1990).
Cependant, une autre étude plus complète est disponible chez le rat Sprague Dawley (Ono et al., 1996). Les mâles sont exposés pendant 90 jours dont 60 jours avant l’accouplement. Les femelles sont exposées pendant 14 jours avant l’accouplement puis jusqu’au 7ème jour de la gestation. Les animaux ont été exposés 6 heures par jour à des concentrations de 600 et 2 000 ppm (2 300 et 7 500 mg.m-3) de toluène, à 98 % de pureté. Il n’y a pas d’altérations des poids des femelles témoins ou exposées. Les femelles sont chacune accouplées avec un mâle exposé à la même dose. A 2 000 ppm (7 500 mg.m-3), la mortalité fœtale est plus élevée que chez les témoins ainsi que le nombre de mères porteuses de fœtus mort. Chez les mâles, exposés à 2 000 ppm (7 500 mg.m-3), l’augmentation du poids des reins est accompagnée d’une altération basophilique, d’une nécrose tubulaire et d’une diminution du poids du thymus. Les poids relatifs et absolus de l’épididyme sont diminués à 2 000 ppm (7 500 mg.m-3). Il n’y a pas d’altérations histopathologiques des testicules et de l’épididyme. Le nombre de cellules spermatogéniques aux 3 stades (spermatogonie, spermatocyte I, spermatides) n’est pas altéré. Le nombre de spermatozoïdes est significativement diminué (20 à 25 %) à 2 000 ppm (7 500 mg.m-3).
L’étude de Thiel et Chambon (1997) montre qu’il n’y a pas de différence significative entre les lots témoins et traités à l’exception de l’indice de fertilité qui est statistiquement augmenté pour le lot exposé à 600 ppm (2 300 mg.m-3). Il n’y a pas de relation dose-effet rapportée.
Une étude récente, menée chez le rat Long-Evans, montre une probable diminution de la synthèse et de la sécrétion de testostérone, par une diminution statistiquement significative de l’ARN messager de bêta 3-hydroxystéroïde désydrogénase (Tsukahara et al., 2009).
Synthèse
Chez le rat, les principaux effets correspondent à une altération des cellules de la reproduction survient pour des expositions à 2 000 ppm (7 500 mg.m-3).
Effets sur le développement
Classifications
| Organisme | Classification | Année |
|---|---|---|
| UE | Catégorie 2 : substance préoccupante pour la fertilité dans l’espèce humaine ou pour l’homme en raison d’effets toxiques possible sur le développement | 2008 |
Chez l'homme
Inhalation
Une revue de la littérature (Bukowski, 2001) montre qu’il existe très peu d’études relatives aux effets du toluène sur le développement suite à des expositions en milieu professionnel. Les principaux effets rapportés sont une augmentation des avortements spontanés pour des niveaux d’exposition de l’ordre de 50 à 150 ppm (191,5 à 574,5 mg.m-3) (Axelsson et Rylander, 1982 ; Ng et al., 1992b ; Taskinen et al., 1994) et des malformations congénitales (McDonald et Lavoie, 1987 ; Taskinen et Anttila, 1989). Ces études sont difficilement exploitables compte tenu de l’exposition à d’autres polluants, du nombre restreint d’individus impliqués dans l’étude et des faibles niveaux d’exposition. L’étude de Ng et al. (1992b), bien que plus complète reste de qualité scientifique discutable. Il s’agit d’une étude transversale réalisée dans une manufacture de matériel radiophonique de Singapour, portant sur 86 employées, dont 55 femmes fortement exposées et 31 faiblement exposées. Une augmentation significative des taux d’avortements spontanés entre les semaines 12 et 28 de la gestation est rapportée chez les femmes fortement exposées au toluène (88 ppm soit 337 mg.m-3).
Même si les résultats de ces études sont difficiles à interpréter, une exposition professionnelle au toluène chez les mères pourrait induire des déficits cognitifs chez les enfants (Grandjean et Landrigan, 2006).
Par ailleurs, les principaux effets rapportés sont des effets tératogènes essentiellement au niveau du système nerveux central (Arnold et al., 1994 ; Pearson et al., 1994).
Chez l'animal
Toutes voies
La majorité de ces études correspond à des expositions pratiquées par inhalation chez le rat.
Inhalation
Chez le rat, l’exposition au toluène ne semble pas induire de malformations chez les fœtus sauf à des concentrations élevées compatibles avec celles retrouvées dans les utilisations abusives chez la femme enceinte soit 8 000 – 12 000 – 16 000 ppm (30 640 – 45 960 – 61 280 mg.m-3), 30 minutes 2 fois par jour, du 8ème au 20ème jour de gestation (Bowen et al., 2009). A des niveaux d’exposition communément rencontrés, le toluène serait à l’origine d’une diminution du poids à la naissance, d’un retard de développement post-natal et d’une altération du comportement (EU, 2003).
Une étude combinée de fertilité et de tératogénicité sur deux générations de rats exposés aux concentrations de 375, 1 875 ou 7 500 mg.m-3 (98, 490 ou 1 957 ppm), 6 h/j, 7 j/7 montre une diminution du poids corporel des fœtus et des nouveau-nés et un retard d’ossification à la concentration la plus élevée (API, 1985). La toxicité maternelle est faible à ce niveau d’exposition, il est donc possible de définir une NOAEC de 1 875 mg.m-3 (490 ppm) pour la toxicité du développement.
Des expositions à 375 ou 1 500 mg.m-3 (98 ou 391,5 ppm), par inhalation, chez la rate pendant la période de gestation, montrent l’absence de toxicité maternelle, de modification du sex-ratio chez les fœtus, d’embryo-toxicité, de retard pondéral fœtal ou d’effet sur le développement (API, 1978). A partir de cette étude, il est possible de définir une NOAEC de 1 500 mg.m-3 (391,5 ppm).
Diminution du poids de naissance et retard du développement
Une diminution du poids des fœtus, du poids à la naissance et un retard du développement post-natal est rapporté par plusieurs études (Hass et al., 1999 ; Hougaard et al., 1999 ; Huntingdon Research Centre, 1992a, 1992b ; Ono et al., 1995 ; Thiel et Chahoud, 1997). Les LOAEC proposées sont de l’ordre de 1 000 à 2 000 ppm (3 750 à 7 500 mg.m-3) et les NOAEC sont comprises entre 400 et 750 ppm (1 500 et 2 872 mg.m-3).
Une étude a été pratiquée chez la rate pendant la période de gestation pour des expositions à 937, 2 815, 5 625 ou 11 250 mg.m-3 (245, 735, 1 468 ou 2 936 ppm) (Huntingdon Research Centre, 1992a). A 11 250 mg.m-3, de nombreux effets toxiques sont observés chez les mères exposées (tremblements des membres, mouvements incontrôlés, larmoiements, polypnée, hypersalivation, nystagmus (Succession de mouvements rythmiques des globes oculaires, linéaires ou rotatoires)). Une diminution du poids corporel des fœtus et une augmentation du nombre total de malformations sont observées à partir de 5 625 mg.m-3 (1 468 ppm).
Une étude sur deux générations a été menée chez le rat Sprague Dawley (mâles et femelles), exposé à des concentrations de toluène (à 99,9 % de pureté) de 0 – 100 – 500 – 2 000 ppm (soit 0 – 375 – 1 875 – 7 500 mg.m-3), 6 heures par jour, 7 jours par semaine (Roberts et al., 2003). Aucun effet sur la fertilité, la fonction de reproduction, le comportement des mères et des jeunes au cours de la période de lactation chez les femelles et les mâles de la première génération n’est observé mais une inhibition de la croissance des jeunes des générations F1 et F2, exposés à 2 000 ppm (7 500 mg.m-3) est mise en évidence. Le poids des jeunes des générations F1 et F2 est diminué de manière statistiquement significative lors de l’exposition via le lait maternel.
Une deuxième étude a été réalisée chez le rat Sprague Dawley, par exposition corps entier au toluène (pureté 99,9 %) du 6ème au 15ème jour de la gestation, à des concentrations de 0 – 250 – 750 – 1 500 – 3 000 ppm (0 – 938 – 2 812 – 5 625 – 11 250 mg.m-3), 6 h/j (Roberts et al., 2007). Des signes de toxicité sont rapportés chez les mères (ataxie, hypersensibilité, augmentation de la consommation d’eau, diminution de la consommation de nourriture) à 3 000 ppm et dans une moindre mesure à 1 500 ppm. Les effets sur les fœtus correspondent à une réduction de la taille de la portée pour une exposition à 3 000 ppm et une diminution du poids moyen des fœtus à 1 500 et 3 000 ppm. Des réductions et des absences d’ossification sont également rapportées à ces deux concentrations. Une diminution des poids moyens des fœtus est également observée à 250 ppm mais pas à 750 ppm. Aucune relation dose-effet n’a pu être établie et les effets relatifs aux deux concentrations sur l’ossification ne sont pas statistiquement significatifs.
Une autre étude a été menée chez des rates Wistar gestantes exposées à 0 – 300 – 600 – 1 000 – 1 200 ppm (1 131, 2 262, 3 830 et 4 524 mg.m-3) de toluène à 99 % de pureté, 6 h//j, 7 j/7, du 9ème jour au 21ème jour de la gestation (Thiel et Chahoud, 1997). Une diminution non statistiquement significative de la croissance pondérale maternelle est rapportée pour les expositions à 1 000 et 1 200 ppm (3 830 et 4 600 mg.m-3), pour les animaux de la génération parents P. Une diminution non statistiquement significative de la taille des portées est mentionnée chez les rates exposées à 1 200 ppm (4 600 mg.m-3), ainsi qu’une augmentation de la mortalité chez les jeunes non sevrés. Les poids des jeunes de la génération F1 sont plus faibles chez les rates exposées à 1 000 et 1 200 ppm (3 830 et 4 600 mg.m-3) que chez ceux des lots témoins. Le développement au cours de la période de lactation (déploiement du pavillon auriculaire, poussée dentaire et ouverture des yeux) et le réflexe d’ontogenèse sont similaires dans les différents groupes, excepté pour le groupe exposé à 1 200 ppm (4 600 mg.m-3) où la poussée dentaire est légèrement retardée. Un retard de l’ouverture vaginale d’au moins 5 jours est rapporté chez les deux groupes exposés à 1 000 et 1 200 ppm (3 830 et 4 600 mg.m-3). Il n’y pas d’altération significative de l’activité spontanée à 24 heures ni de retard d’apprentissage. A partir de cette étude, une NOAEC de 2 262 mg.m-3 (600 ppm) et une LOAEC de 3 830 mg.m-3 (1000 ppm) ont été définies.
Troubles du comportement
Des altérations du comportement ont été rapportées chez des rats exposés au toluène pendant la période de développement du cerveau (Hass et al., 1999 ; Hougaard et al., 1999). Chez le rat Wistar exposé, 6 heures par jour, du 7ème au 20ème jour de la gestation à la concentration de 0 ou 1 800 ppm (4 600 mg.m-3), les mesures de la fonction auditive montrent une diminution statistiquement significative chez le jeune mâle (Hougaard et al., 1999). Une diminution statistiquement significative de la fonction cognitive a été mesurée au moyen du test « Morris water maze » chez les rats des deux sexes avec des effets mesurés plus marqués chez les femelles. Dans une autre étude, des rats femelles Wistar ont été exposés au toluène aux concentrations de 0 - 1 200 ppm (0 - 4 600 mg.m-3), 6 heures par jour, du 7ème jour de la gestation au 18ème jour après la naissance : une altération de la fonction cognitive, évaluée au moyen du test « Morris water maze », est rapportée chez les jeunes femelles âgées de 3,5 mois (Hass et al., 1999).
Un phénomène d’apoptose neuro-dégénérative de la couche des grains du cervelet est observé chez les jeunes mâles, nés de femelles rats gestantes exposées, 6 h//j du 7ème jour de la gestation au 18ème jour après la naissance à 1 200 ppm (4 600 mg.m-3) et 1 800 ppm (6 900 mg.m-3) (Dalgaard et al., 2001). Chez ces jeunes, le toluène induit de manière statistiquement significative une apoptose du cervelet (partie du cortex cérébelleux) au 21ème jour après la naissance. Ce phénomène n’est pas retrouvé aux autres temps d’investigation (11 et 90ème jour après la naissance).
Il existe très peu d’études chez la souris. Des signes de fœtotoxicité (altération du nombre de côtes) sont rapportés chez la souris CD-1 exposée à 400 ppm (1 500 mg.m-3), 7 j/7, du 7ème au 16ème jour de la gestation (Courtney et al., 1986). Ces effets ne sont pas retrouvés à 200 ppm (750 mg.m-3). Une diminution du poids de naissance, une diminution de la croissance pondérale post-natale ainsi qu’un retard d’acquisition des réflexes en l’absence de toxicité maternelle ont été rapportés pour des expositions à 2 000 ppm (7 500 mg.m-3) de toluène, pendant 60 minutes, pratiquées 3 fois par jour du 12ème au 17ème jour de la gestation (Jones et Balster, 1997). Aucun effet n’est observé pour une exposition à 400 ppm (1 520 mg.m-3). De cette étude, une LOAEC de 2 000 ppm (7 660 mg.m-3) est définie pour la toxicité du développement.
Les seules études disponibles chez le lapin (Chbb HM) sont difficilement exploitables en l’absence de toxicité maternelle à la plus forte dose retenue (BASF, 1989 ; Klimisch et al., 1992). Klimisch et al. (1992) ont montré un retard de développement du squelette dès les doses de 100 ou 300 ppm (383 ou 1 150 mg.m-3) pour des expositions au toluène, 6 heures par jour, du 6ème au 18ème jour après l’insémination. L’étude réalisée par BASF (1989) montre une altération des carotides aux concentrations de 100 et 500 ppm (375 et 1 875 mg.m-3), 6 heures par jour, du 6ème au 18ème jour après l’insémination mais aucune anomalie du squelette n’a pu être décelée.
[1] Succession de mouvements rythmiques des globes oculaires, linéaires ou rotatoires.
Voie orale
Les rares études disponibles pour des expositions par voie orale, sont des études incomplètes car réalisées sur une seule dose, avec un nombre d’animaux insuffisant pour lesquelles les résultats sont difficilement exploitables (Gospe et al., 1994 ; Gospe et al., 1996 ; Gospe et Zhou, 1998 ; Gospe et Zhou, 2000 ; Kostas et Hotchin, 1981). Les fœtus présentent une diminution pondérale, des retards d’ossification, des cerveaux de petite taille et un défaut de myélinisation lors d’expositions au toluène par gavage à la dose de 520 ou 650 mg.kg-1.j-1, en solution dans l’huile de maïs, du 6ème au 19ème jour de la gestation.
Synthèse
Les données, chez l’homme ainsi que celles chez l’animal, semblent mettre en évidence un retard du développement qui se manifeste par une diminution du poids à la naissance, un retard du développement post-natal et une neurotoxicité avec des troubles du comportement plus marqués chez les femelles. Le toluène est classé en catégorie 2 par l’Union Européenne.
Valeurs accidentelles
Autres seuils accidentels
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Valeurs réglementaires
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Valeurs guides
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Valeurs de référence
Introduction
Une Valeur Toxicologique de Référence (VTR) est un indice qui est établi à partir de la relation entre une dose externe d'exposition à une substance et la survenue d'un effet néfaste. Les valeurs toxicologiques de référence proviennent de différents organismes. Pour accéder à une information actualisée, nous conseillons au lecteur de se reporter directement sur les sites internet des organismes qui les élaborent.
Valeurs de l'ANSES et/ou de l'INERIS
Description
Effets à seuil - Exposition aiguë par inhalation :
L’ATSDR a établi un MRL de 2 ppm (7,6 mg.m-3) pour une exposition aiguë par inhalation au toluène (ATSDR, 2017).
Cette valeur est établie à partir d’une étude menée chez des travailleurs identifiés comme étant cliniquement sensibles au toluène et exposés de manière expérimentale à 15 ppm pendant 20 minutes (Little et al., 1999). Une batterie de tests neuropsychologiques comportant notamment des tests de mémoire immédiate ou retardée, des temps de réaction, des modifications de lettres, « digit symbol » et des tests relatifs à la vision des couleurs ont été pratiqués avant et après exposition. Les effets sont observés lors de ces tests ce qui conduit à retenir la valeur de 15 ppm comme un LOAEC.
Facteurs d’incertitude : un facteur de 9 est appliqué correspondant à un facteur 3 pour tenir compte de la variabilité intra-espèce et un facteur 3 pour tenir compte de l’utilisation d’une LOAEC.
Calcul : 15 ppm x 1/9 = 1,66 ppm arrondi à 2 ppm (soit 7,6 mg.m-3)
Indice de confiance : Cet organisme n’attribue pas d’indice de confiance.
L'OEHHA propose un REL de 5000 µg.m-3 (5 mg.m-3) pour une exposition aiguë de 1 h par inhalation au toluène (OEHHA, 2020) .
Cette valeur est issue d'une étude expérimentale chez l’homme (Andersen et al., 1983). Les sujets ont été exposés à 0, 10, 40, 100 ppm (0, 38, 150, 380 mg.m-3) durant 6 heures. Des effets neurologiques (sensation d’ivresse, mal de tête, étourdissement) ont été observés à 100 ppm (380 mg.m-3). Ces effets ne sont pas retrouvés aux concentrations de 10 et 40 ppm. Une NOAEC de 40 ppm (150 mg.m-3) a été établi pour cette étude. Un ajustement pour une exposition d’une heure a été pratiqué.
Facteurs d’incertitude : un facteur 30 a été appliqué pour la variabilité au sein de la population (variabilité intra-spécifique) correspondant à un facteur 3 pour la composante toxicocinétique et 10 pour la composante toxicodynamique.
Calcul : 150 mg.m-3 x 1/30 = 5 mg.m-3 (1,3 ppm)
Indice de confiance : Cet organisme n’attribue pas d’indice de confiance.
L’ANSES propose une VTR de 21 mg.m-3 (6 ppm) pour une exposition aiguë par inhalation au toluène (ANSES, 2017).
Cette valeur est basée sur une étude chez le volontaire sain exposé pendant 40 minutes à la concentration de 200 ppm (752 mg.m-3) de toluène (Kobald et al., 2015). Les effets neurologiques correspondant à une altération de la discrimination visuelle et une mesure électroencéphalographique ont été retenus comme effet critique. Il s’agit d’effet critique bien objectivés. Une LOAEC de 752 mg.m-3 a été retenue. Un ajustement temporel pour une exposition continue pendant 24 h a été réalisé en utilisant une modélisation PBPK. LOAECADJ = 323 mg.m-3 (86 ppm).
Facteur d’incertitude : Un facteur d’incertitude de 15 a été appliqué correspondant à un facteur 5 pour prendre en compte les variations intra-espèces et un facteur 3 en raison de l’utilisation d’une LOAEC.
Calcul : LOAECADJ x 1/15 = 323 mg.m-3 mg.m-3 x 1/15 = 21,53 mg.m-3 (arrondi à 21 mg.m-3 soit 6 ppm)
Indice de confiance : l’ANSES accorde un indice de confiance fort dans sa valeur correspondant à un indice fort pour la nature et la qualité des données, pour le choix de l’effet critique et le mode d’action, pour le choix de l’étude clé et un indice moyen pour le choix de la dose critique.
Effets à seuil - Exposition chronique par inhalation :
L’US EPA (IRIS) propose une RfC de 5 mg.m-3 pour une exposition chronique par inhalation au toluène (US EPA (IRIS), 2005).
Cette valeur est établie à partir d’études épidémiologiques réalisées lors d’expositions professionnelles au toluène (Abbate et al., 1993 ; Boey et al., 1997 ; Cavalleri et al., 2000 ; Eller et al., 1999 ; Foo et al., 1990 ; Morata et al., 1993 ; Nakatsuka et al., 1992 ; Neubert et al., 2001 ; Vrca et al., 1995 ; Zavalic et al., 1998b). L’effet le plus sensible est une atteinte neurologique correspondant à des troubles de la vision en couleur, des altérations de l’audition, une diminution des performances lors d’analyses de comportement, des altérations de la vitesse de conduction nerveuse motrice et sensitive. La plupart des études ont identifié des NOAEC de l’ordre de 25 à 50 ppm (96 à 191 mg.m-3) ce qui permet de déterminer une NOAEC moyenne[1] de 34 ppm (128 mg.m-3) puis une NOAEC ajustée de 46 mg.m-3. Ce dernier prend en compte le volume d’air inhalé au cours de 8 heures de travail (10 m3), le volume d’air inhalé pendant 24 heures (20 m3) et rapporte l’exposition de la semaine de travail (5 j) à une semaine complète (7 j).
Facteurs d’incertitude : un facteur de 10 est appliqué pour tenir compte des différences intra-espèces.
Calcul : (128 mg.m-3 x 10 m3/ 20 m3 x 5 j/ 7 j) x 1/10 = 46 mg.m-3 x 1/10 = 4,6 mg.m-3 (5 mg.m-3)
Indice de confiance : La confiance de l’US EPA pour sa valeur est élevée.
L’ATSDR a établi un MRL de 1 ppm (3,8 mg.m-3) pour une exposition chronique par inhalation au toluène (ATSDR, 2017).
Cette valeur est établie à partir de plusieurs études menées chez le travailleur (Schäper et al., 2003 ; Schäper et al., 2004 ; Schäper et al., 2008 ; Seeber et al., 2004 ; Seeber et al., 2005 ; Zupanic et al., 2002). Dans ces différentes études, il a été montré l’absence d’effets neurologiques jusqu’à 45 ppm. Cette valeur a été retenue comme une NOAEC.
Un ajustement temporel a été réalisé pour passer d’une exposition discontinue à une exposition continue : NOAEC ADJ = 45 ppm x 5 j/7 j x 8 h/24 h = 10 ppm
Facteurs d’incertitude : un facteur de 10 est appliqué pour tenir comptede la variabilité intra-espèce (facteur de 10).
Calcul : 10 ppm x 1/10 = 1 ppm (3,8 mg.m-3)
Indice de confiance : Cet organisme n’attribue pas d’indice de confiance.
L’OMS a établi une valeur guide de 0,26 mg.m-3 pour une exposition hebdomadaire au toluène (OMS, 2000)
Les résultats de plusieurs études en milieu professionnel permettent de définir une LOAEC d’environ 332 mg.m-3 (88 ppm) pour les effets sur le système nerveux central (altération du neurocomportement) lors d’expositions chroniques au toluène (Foo et al., 1990 ; Foo et al., 1993). Cette valeur est ajustée pour une exposition continue.
Facteurs d’incertitude : un facteur de 100 est appliqué et correspond à un facteur de 10 pour les variations intra-espèces et d’un autre facteur de 10 du fait que la valeur utilisée pour la dérivation est une LOAEC. Un facteur supplémentaire de 3 est ajouté pour tenir compte des effets potentiels sur le système nerveux au cours du développement.
Calcul : 332 mg.kg-1.j-1 x 8 h/24 h x 5 j/7 j x 1/300 = 0,26 mg.m-3
Indice de confiance : Cet organisme n’attribue pas d’indice de confiance.
Santé Canada a établi une CT de 2,3 mg.m-3 pour une exposition chronique par inhalation au toluène (Sante Canada, 2021)
Cette valeur est établie à partir deux études menées chez le travailleur (Seeber et al., 2004 ; Seeber et al., 2005). Dans ces études, il a été montré l’absence d’effets neurologiques (fonction cognitive : attention, mémoire et fonction psychomotrice). La valeur de 26 ppm (98 mg.m-3) a été retenue comme une NOAEC.
Un ajustement temporel a été réalisé pour passer d’une exposition discontinue à une exposition continue : NOAEC ADJ = 45 ppm x 5 j/7 j x 8 h/24 h = 23 mg.m-3
Facteurs d’incertitude : un facteur de 10 est appliqué pour tenir compte la variabilité intra-espèce.
Calcul : 23 mg.m-3 x 1/10 = 2,3 mg.m-3
Indice de confiance : Cet organisme n’attribue pas d’indice de confiance.
Le RIVM propose une TCA de 0,4 mg.m-3 pour une exposition chronique par inhalation au toluène (Baars et al., 2001).
Cette valeur est basée sur celle proposée par l'US EPA en 1992 pour une exposition chronique par inhalation.
Le toluène est un irritant pulmonaire induisant des effets toxiques pour le système nerveux central, chez l’homme, pour des concentrations de l’ordre de 383 mg.m-3. A partir d’études d’exposition chronique, la LOAEC retenue chez l’homme est de 332 mg.m-3 (88 ppm) (Foo et al., 1990). Cette valeur est supportée par les résultats d’une étude expérimentale, chez le rat, qui permet de retenir une LOAEC de 2 261 mg.m-3 (600 ppm) pour les effets dégénératifs de l’épithélium nasal (NTP, 1990). Cette valeur extrapolée pour l’homme est une LOAECHEC de 79 mg.m-3. In fine, la valeur retenue est la LOAEC de 332 mg.m-3, qui est ajustée en prenant compte le volume d’air inhalé au cours de 8 heures de travail (10 m3), le volume d’air inhalé pendant 24 heures (20 m3), l’exposition pendant une semaine de travail (5 j) rapportée à une semaine complète (7 j).
Facteurs d’incertitude : un facteur de 10 est appliqué pour tenir compte des différences intra-espèces, un autre facteur de 10 tient compte de l’utilisation d’une LOAEC. Un facteur supplémentaire de 3 est appliqué en raison de l’absence de données liée au nombre restreint d’expérimentations et au manque de caractérisation des expositions pratiquées chez l’animal.
Calcul : 332 mg.m-3 x10 m3/20 m3 x5 j/7 j x 1/300 = 0,395 mg.m-3 arrondi à 0,4 mg.m-3
Indice de confiance : Le RIVM accorde une confiance élevée dans sa valeur.
L'OEHHA propose un REL de 0,42 mg.m-3 pour une exposition chronique par inhalation au toluène (OEHHA, 2003) .
Cette valeur est établie à partir de l’étude épidémiologique pour des expositions professionnelles au toluène (Zalavic et al., 1998a). L’effet le plus sensible est une atteinte neurologique correspondant à des troubles de la vision en couleur à 587 mg.m-3 (156 ppm). La NOAEC de 132 mg.m-3 (35 ppm) et la BMCL05 de 45,1 mg.m-3 a été calculée. Un ajustement à une durée d’exposition continue a été réalisé en retenant un volume inhalé de 10 m3/j pour les 8 h d’activité professionnelle et de 20 m3 pour 24 h : BMCL05 ADJ = 45,1 mg.m-3 x 10 m3/20 m3 x 5 j/7 j = 16,2 mg.m-3
Facteurs d’incertitude : un facteur 39 a été appliqué pour la variabilité au sein de la population (variabilité intra-espèce) correspondant à 3,9 pour la composante toxicocinétique et 10 pour la composante toxicodynamique.
Calcul : 16,2 mg.m-3 x 1/39 = 0,42 mg.m-3 (0,11 ppm)
Indice de confiance : Cet organisme n’attribue pas d’indice de confiance
L’Anses a établi un VTR de 19 mg.m-3 (5 ppm) pour une exposition chronique par inhalation au toluène (Anses, 2017).
Cette valeur est établie à partir d’une étude d’expositions chroniques chez les salariés de l’industrie de la chaussure (Zavalic et al., 1998a). Elle a également été retenue comme étude clé par l’US EPA et l’OEHHA. Contrairement aux autres organismes, l’Anses a considéré l’augmentation significative par rapport aux témoins de l’indice de confusion des couleurs (CCI) comme l’effet critique qui peut être associé à une LOAEC de 132 ppm. Ainsi, le niveau d’exposition du groupe composé essentiellement de femmes et noté E1 est considéré comme un NOAEC (32 ppm, 123 mg.m-3).
Le choix de cette concentration critique associée aux effets neurotoxiques observés chez l’homme est soutenu par les concentrations du même ordre de grandeur retrouvées dans les autres études épidémiologiques. La NOAEC de 32 ppm issue de l’étude de Zavalic et al. (1998) a été ajustée sur le temps par utilisation d’un modèle PBPK qui permet de déterminer une concentration ajustée de 96 mg.m-3 (25 ppm) pour extrapoler la durée de travail dans l’étude vers une exposition continue
Facteurs d’incertitude : un facteur de 5 est appliqué pour tenir compte de la variabilité intra-espèce (facteur de 5).
Calcul : 96 mg.m-3 x 1/5 = 19,2 mg.m-3 arrondie à 19 mg.m-3
Indice de confiance : L’ANSES attribue un indice confiance fort dans sa valeur correspondant à un indice de confiance fort pour la nature et la qualité des données, l’effet critique et le mode d’action, le choix de la dose critique et un indice moyen concernant la qualité de l’étude.
Effets à seuil - Exposition aiguë par voie orale :
L’ATSDR a établi un MRL de 0,8 mg.kg-1.j-1 pour une exposition orale aiguë au toluène (ATSDR, 2017).
Cette valeur est établie à partir d’une étude expérimentale, chez le rat, exposé par gavage à une dose unique de 0, 250, 500 ou 1 000 mg.kg-1 de toluène (Dyer et al., 1988). Le test utilisé est le test des potentiels évoqués. Les résultats ont permis de déterminer un LOAEL de 250 mg.kg-1.j-1 pour les effets neurologiques.
Facteurs d’incertitude : un facteur total de 300 est appliqué pour tenir compte du fait que le MRL est établi à partir d’un LOAEL (facteur de 3), de la variabilité intra-espèce (facteur de 10) et de la variabilité inter-espèce (facteur de 10).
Calcul : 250 mg.kg-1.j-1 x 1/300 = 0,8 mg.kg-1.j-1
Indice de confiance : Cet organisme n’attribue pas d’indice de confiance
Effets à seuil - Exposition sub-chronique par voie orale :
L’ATSDR a établi un MRL de 0,2 mg.kg-1.j-1 pour une exposition sub-chronique par voie orale au toluène (ATSDR, 2017).
Cette valeur est établie à partir de trois études menées chez des souris mâles exposées au toluène pendant 28 jours via l’eau de boisson aux doses de 0 – 5- 22 -105 mg.kg-1.j-1 (Hsieh et al., 1989, 1991) ou 0 – 22 84 mg.kg-1.j-1 (Hsieh et al., 1990). Collectivement, les résultats de ces études montrent une absence d’effet sur le système immunitaire à 22 mg.kg-1.j-1 qui est retenue comme un NOAEL.
Facteurs d’incertitude : un facteur de 100 est appliqué pour tenir compte de la variabilité intra-espèce (facteur 10) et de la variabilité inter-espèce (facteur 10).
Calcul : 20 mg.kg-1.j-1 x 1/100 = 0,2 mg.kg-1.j-1
Indice de confiance : Cet organisme n’attribue pas d’indice de confiance
Effets à seuil - Exposition chronique par voie orale :
L’US EPA (IRIS) propose une RfD de 0,08 mg.kg-1.j-1 pour une exposition chronique par voie orale au toluène (US EPA (IRIS), 2005).
Cette valeur a été établie à partir d’une étude de 13 semaines par gavage chez le rat. L’effet retenu est l’augmentation du poids du rein (NTP, 1990). Chez le rat, le NOAEL retenu est de 223 mg.kg-1.j-1 et le LOAEL retenu de 446 mg.kg-1.j-1. Après modélisation de l’augmentation du poids absolu des reins des rats mâles, une benchmark dose limite (BMDL) (limite inférieure de l’intervalle de confiance) de 238 mg.kg-1.j-1 est calculée pour une augmentation de 10 % de la réponse.
Facteurs d’incertitude : un facteur de 3 000 est appliqué pour tenir compte des différences inter- et intra-espèces (100), de l’extrapolation d’une étude sub-chronique à une étude chronique (10) et du nombre limité de données et des résultats d’immunotoxicité contradictoires (3).
Calcul : BMDL / 3 000 = 238 mg.kg-1.j-1/ 3 000 = 0,08 mg.kg-1.j-1
Indice de confiance : L’indice de confiance de l’US EPA dans sa valeur est modéré.
L’OMS a établi une TDI de 0,223 mg.kg-1.j-1 pour une exposition chronique par voie orale au toluène (OMS, 2011) .
Cette valeur a été établie à partir d’une étude expérimentale réalisée chez la souris par administration de toluène par gavage pendant 13 semaines (NTP, 1990). Un LOAEL de 312 mg.kg-1 a été établi pour les effets hépatotoxiques non statistiquement significatifs, un ajustement de la durée d’exposition a été réalisé.
Facteurs d’incertitude : un facteur de 1 000 est appliqué et correspond à un facteur de 100 pour les variations inter- et intra-espèces et d’un autre facteur de 10 pour tenir compte de la courte durée de l’étude et du fait que la valeur utilisée pour la dérivation est un LOAEL.
Calcul : 312 mg.kg-1.j-1 x 5 j/7 j x 1/1 000 = 223 μg.kg-1.j-1
Indice de confiance : Cet organisme n’attribue pas d’indice de confiance.
Santé Canada a établi une DJT de 0,0097 mg.kg-1.j-1 pour une exposition chronique par voie orale au toluène (Sante Canada, 2021)
Cette valeur a été établie à partir de deux études épidémiologiques en milieu professionnel (Seeber et al., 2004, 2005) utilisées pour la construction d’une valeur pour des expositions chroniques par inhalation et décrite plus haut. Sur la base de la NOAEC de 26 ppm (98 mg.m-3), une modélisation PBPK a permis de calculer une dose sanguine interne de 0,0075 mg.L-1. Cette dose interne a été convertie en dose externe en supposant une ingestion de 1,5 L/j soit une NOAECHEC de 0,097 mg.kg pc .j-1.
Facteurs d’incertitude : un facteur 10 a été appliqué pour la variabilité au sein de la population (variabilité intra-espèce).
Calcul : 0,097 mg.kg-1.j-1 1/10 = 9,7 μg.kg-1.j-1
Indice de confiance : Cet organisme n’attribue pas d’indice de confiance.
Le RIVM propose une TDI de 0,223 mg.kg-1.j-1 pour une exposition chronique par voie orale (Baars et al., 2001).
La valeur proposée est construite de la même manière que celle retenue par l'OMS pour une exposition chronique par voie orale.
Cette valeur a été établie à partir d’une étude expérimentale réalisée chez la souris par administration de toluène par gavage pendant 13 semaines (NTP, 1990). Un LOAEL de 312 mg.kg-1 a été établi pour les effets hépatotoxiques non statistiquement significatifs, un ajustement de la durée d’exposition a été réalisé.
Facteurs d’incertitude : un facteur de 1 000 est appliqué et correspond à un facteur de 100 pour les variations inter- et intra-espèces et d’un autre facteur de 10 pour tenir compte de la courte durée de l’étude et du fait que la valeur utilisée pour la dérivation est un LOAEL.
Calcul : 312 mg.kg-1.j-1 x 5 j/7 j x 1/1 000 = 223 μg.kg-1
Indice de confiance : Le RIVM accorde une confiance élevée dans sa valeur.
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Synthèse
Effets à seuil - Exposition aiguë par inhalation :
L'ANSES retient la valeur de 21 mg.m-3 pour une exposition aiguë par inhalation au toluène (ANSES, 2017)
Trois organismes proposent des VTR pour des expositions aiguës par inhalation l’ATSDR (2018), l’OEHHA (2020) et l’ANSES (2017).
La valeur de l’ANSES et celle de l’OEHHA sont établies à partir d’une étude chez le volontaire sain et celle de l’ATSDR à partir d’une étude chez le volontaire mais déjà sensible au toluène.
L’étude chez le volontaire (Andersen et al., 1983) est de qualité acceptable. L’effet critique neurologique est en lien avec le profil toxicologique mais est moins objectivé que celui évalué par Kobald et al., (2015). Enfin, les effets critiques observés dans l’étude de Little et al., (1999) sont moins objectivés et réalisés sur une durée d’exposition plus courte.
Dans ces conditions, l’étude retenue par l’ANSES apparait la mieux adaptée. C’est donc la valeur définie par l’ANSES qui est conseillée.
Indice de confiance : l’ANSES accorde un indice fort dans sa valeur.
Effets à seuil - Exposition chronique par inhalation :
L'Anses retient la valeur de 19 mg.m-3 pour une exposition chronique par inhalation au toluène (Anses, 2017)
Les 7 organismes proposent une valeur pour une exposition chronique par inhalation au toluène. Les effets retenus sont des effets neurologiques (US EPA, 2005, ATSDR, 2017, OMS, 2000, Santé Canada, 2021, RIVM, 2001, OEHHA, 2020, Anses, 2017). Tous les organismes retiennent des valeurs issues d’études chez l’homme. Le RIVM retient une ancienne valeur de l’US EPA, il n’y a donc plus lieu de la retenir. L’ATSDR, l’US EPA, Santé Canada et l’OMS retiennent plusieurs études chez l’homme. Le mode de calcul de la valeur est détaillé et une NOAEC ajustée a été calculée pour tenir compte de la durée de l’exposition dans le document de l’US EPA..
En 2017, l’Anses reprend le même panel d’études que les autres organismes et retient une seule étude, celle de Zavalic et al. (1998a) mais s’appuie sur le panel d’études pour le choix de l’effet particulièrement pertinent et de la concentration critique. L’OEHHA retient la même approche basée sur la même étude mais les calculs et le choix des facteurs d’incertitude sont discutables. L’Ineris retient la valeur de l’Anses.
Indice de confiance : L’Anses attribue un indice confiance fort dans sa valeur.
Effets à seuil - Exposition aiguë par voie orale :
L’Ineris propose de retenir pour une exposition aiguë au toluène par voie orale la VTR aiguë de 0,8 mg.kg-1.j-1.
La seule valeur disponible est proposée par l’ATSDR. L’étude est de bonne qualité, la valeur construite est cohérente. L’Ineris retient cette valeur.
Indice de confiance : moyen en raison de la limitation des données disponibles.
Effets à seuil - Exposition sub-chronique par voie orale :
L’Ineris propose de retenir pour une exposition sub-chronique au toluène par voie orale la VTR sub-chronique de 0,2 mg.kg-1.j-1.
La seule valeur disponible est proposée par l’ATSDR., elle est construite à partir de 2 études expérimentales chez la souris et une série d’études in vitro dont les résultats sont complémentaires et concordants. Ces études sont de qualité recevable. La construction de la valeur est cohérente avec le profil toxicologique. L’Ineris retient cette valeur.
Indice de confiance : l’indice de confiance est faible en raison de l’adéquation entre l’effet critique, la dose associée et le raisonnement à l’origine de la construction de la valeur.
Effets à seuil - Exposition chronique par voie orale :
L’Ineris propose de retenir pour une exposition chronique au toluène par voie orale la VTR chronique de 0,0097 mg.kg-1.j-1.
Quatre VTR sont proposées par l’US EPA (2005), l’OMS (2011), Santé Canada (2021) et le RIVM (2001).
Les valeurs de l’US EPA, de l’OMS et du RIVM sont toutes les trois basées sur la même étude expérimentale pour une exposition chronique par voie orale mais retiennent des effets critiques différents chez le rat ou chez la souris. Dans tous les cas, il s’agit d’effets mineurs survenant à des niveaux d’exposition inférieurs aux effets neurotoxiques observés dans l’étude. L’OMS se base sur des effets hépatiques non statistiquement significatifs chez la souris et le mode d’élaboration n’est pas clairement justifié. Le RIVM propose de retenir la même démarche que celle de l’OMS. L’US EPA retient les effets sur le rein. Le mode de calcul de la VTR de l’US EPA est le plus détaillé. L’US EPA choisit de retenir un facteur d’incertitude supplémentaire pour tenir compte du nombre limité de données et des résultats contradictoires relatifs à l’immunotoxicité ce qui conduit à un facteur d’incertitude global très élevé.
La valeur de Santé Canada est construite sur une extrapolation voie à voie à partir d’effets neurotoxiques, observés au cours d’expositions professionnelles, pertinents au regard des effets de la substance. L’extrapolation voie à voie n’est généralement pas recommandée pour la construction d’une VTR malgré tout dans le cas présent elle repose sur une modélisation PBPK qui parait adaptée. C’est la valeur de Santé Canada que l’Ineris retiendra.
Indice de confiance : L’indice de confiance est moyen en raison de la pertinence de l’effet critique retenu, du choix de l’étude et de la transposition de voie à voie.
Effets sans seuil :
Le toluène n’induit pas d’effet sans seuil.
Autres valeurs des organismes reconnus
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Bibliographie
Ecotoxicologie
Dernière vérification le 05/10/2025
Introduction
Le toluène a fait l'objet d'une évaluation de risque qui a été réalisée conformément au règlement 793/93 (E.C., 1993) et dont le rapport final est disponible sur le site de l'Ex-Bureau Européen des substances chimiques (E.C., 2003a). Les données issues de ce rapport n'ont pas fait l'objet d'une validation supplémentaire.
Evaluations existantes : E.C. (2003a). European Union Risk Assessment Report for Toluene (CAS n°108-88-3) (final report)*
Critères PBT / POP :
La substance ne remplit pas les critères PBT/vPvB1 (C.E., 2006) ou POP2 (PNUE, 2001).
[1] Les PBT sont des substances persistantes, bioaccumulables et toxiques et les vPvB sont des substances très persistantes et très bioaccumulables. Les critères utilisés pour la classification des PBT sont ceux fixés par l'Annexe XIII du règlement n° 1907/2006 (REACH).
[2] Les Polluants Organiques Persistants (POP) sont des substances persistantes (aux dégradations biotiques et abiotiques), fortement liposolubles (et donc fortement bioaccumulables), et volatiles (et peuvent donc être transportées sur de longues distances et être retrouvée de façon ubiquitaire dans l'environnement). Les critères utilisés pour la classification POP sont ceux fixés par l'Annexe 5 de la Convention de Stockholm placée sous l'égide du PNUE (Programme des Nations Unies pour l'Environnement).
Normes de qualité existantes :
Union Européenne : objectif de qualité pour la vie aquatique = 10 µg.L-1 (3)
AllemagnePays-Bas : norme de qualité pour les eaux prélevées destinées à la consommation = 10 µg.L-1 (ETOX, 2007), : objectif de qualité pour les eaux prélevées destinées à la consommation = 7 µg.L-1 (valeur cible), 730 µg.L-1 (valeur maximale admissible) (ETOX, 2007), 44
Canada : critère de qualité pour la vie aquatique, l'eau douce = 2 µg.L-1 (ETOX, 2007), 4
Canada : critère de qualité pour l'eau potable = 24 µg.L-1 (ETOX, 2007) 4
USA : critère de qualité pour l'eau de consommation et la consommation de poisson = 6800 µg.L-1 (ETOX, 20074).
[3] Comité Scientifique consultatif pour l'examen de la Toxicité et de l'Écotoxicité des substances chimiques de la Commission européenne.
[4] Les données issues de cette source () ne sont données qu'à titre indicatif ; elles n'ont donc pas fait l'objet d'une validation par l'INERIS. http://webetox.uba.de/webETOX/index.do
Substance(s) associée(s) :
-
Dangers
Description
ORGANISMES AQUATIQUES
Dans les tableaux ci-dessous, pour chaque taxon sont reportés uniquement les résultats des tests d'écotoxicité montrant la plus forte sensibilité à la substance. Toutes les données présentées sont issues du rapport d'évaluation des risques européenne, et n'ont donc pas fait l'objet d'une validation supplémentaire.
Ces résultats d'écotoxicité sont principalement exprimés sous forme de NOEC (No Observed Effect Concentration), concentration sans effet observé, d'EC10 concentration produisant 10% d'effets et équivalente à la NOEC, ou de EC50, concentration produisant 50% d'effets. Les NOEC sont principalement rattachées à des tests chroniques, qui mesurent l'apparition d'effets sub-létaux à long terme, alors que les EC50 sont plutôt utilisées pour caractériser les effets à court terme.
ECOTOXICITE AQUATIQUE AIGUË
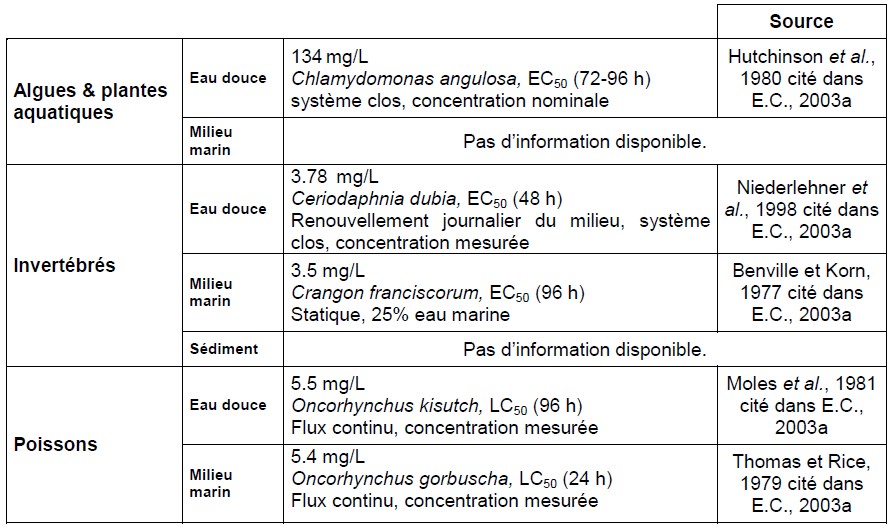

Algues:
La plupart des données présentées sont basées sur les concentrations nominales. Néanmoins, les précautions mises en œuvre au cours des tests pour limiter la volatilisation de la substance ont permis de conclure la validité de ces études (CE, 2003).
De plus, des estimations (Q)SAR conduisent à des CE50 (72 - 96 h) de 8,8 mg.L-1 et CE50 (72 h) de 11 mg.L-1 (CE, 2003).
Invertébrés:
Bien qu’il existe d’autres études sur invertébrés, seules les études reprises dans le tableau sont considérées comme valides. En effet, les conditions opératoires ont bien pris en compte le caractère volatil de la substance conduisant à des résultats de CL50 compris entre 3,5 et 30,6 mg.L-1. Ainsi, les études présentant les valeurs les plus faibles sont celles réalisées sur une espèce marine, Crangon franciscorum (CE50 = 3,5 mg.L-1) et une espèce d’eau douce, Ceriodaphnia dubia (CE50 = 3,8 mg.L-1).
Poissons:
Les essais poissons retenus sont des essais qui ont été validés pour le respect des critères de validité et pour la prise en compte de la volatilité de la substance soit par des dosages réguliers pour les expériences réalisées en condition statique (Benville et Korn, 1977 ; Buccafusco et al., 1981 ; Korn et al., 1979 ; Thomas et Rice, 1979) soit par la mise en œuvre d'un renouvellement continu du milieu (Brenniman et al., 1976 ; Devlin et al., 1982 ; Geiger et al., 1990 ; Moles et al., 1981). Aucune différence significative entre organismes d’eau douce et organismes marins n’a pu être observée. D’autres résultats d’études sont également disponibles dans le rapport européen (CE, 2003). De manière générale, les organismes aquatiques sont exposés au toluène via la respiration, ce qui induit un changement de perméabilité au niveau des branchies et un empoisonnement interne au dioxyde de carbone. Dès lors, le toluène cause des effets toxiques via le mécanisme de narcose.
ECOTOXICITE AQUATIQUE CHRONIQUE
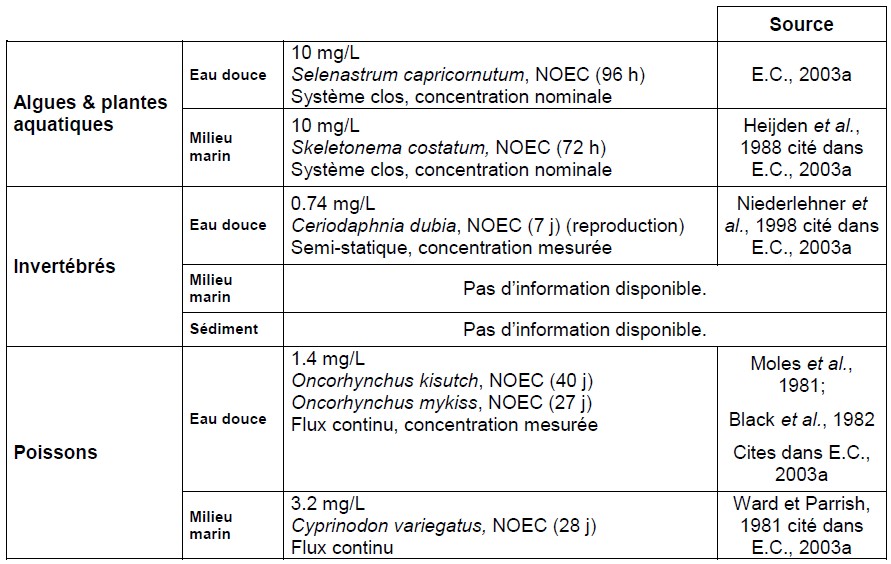

Algues :
Comme précisé plus haut, la plupart des données sont basées sur les concentrations nominales. Néanmoins, les précautions mises en œuvre au cours des tests pour limiter la volatilisation de la substance ont permis de conclure la validité de ces études (CE, 2003).
Une estimation (Q)SAR (US EPA, 1994) a permis de déterminer une NOEC (96 h) de 1,8 mg.L-1.
Invertébrés :
L’essai sur Daphnia magna réalisé par (Kühn et al., 1989) en semi-statique présente également un suivi de la concentration en toluène. Cet essai a donc, été considéré comme valide.
Par contre, la NOEC issue de l’essai sur Daphnia magna et réalisée en semi-statique a été calculée à l’aide du QSAR (Hermens et al., 1984), et les conditions de modélisation ne sont pas claires. Cet essai a donc été jugé comme non valide.
Enfin, l’essai sur Ceriodaphnia dubia réalisé par Niederlehner et al. (1998) en semi-statique, présente également un suivi de la concentration en toluène. La NOEC obtenue (0,74 mg.L-1) est la plus basse de l’ensemble des données long terme. Cette valeur sera utilisée pour le calcul de la PNECEAU.
Poissons :
Tous les essais rapportés ont été réalisés en système dynamique avec suivi analytique des concentrations et sont donc considérés comme valides. Aucune différence significative entre organismes d’eau douce et organismes marins n’a pu être observée.
Sédiments:
Aucun résultat d’essai sur organismes benthiques n’a été trouvé dans les sources bibliographiques consultées.
ECOTOXICITE POUR LES VERTEBRES TERRESTRES POUR L'EMPOISONNEMENT SECONDAIRE
Ce chapitre traite de la toxicité chronique induite par la substance sur les prédateurs via la consommation d'organismes aquatiques contaminés (appelés biota, i.e. poissons ou invertébrés vivant dans la colonne d'eau ou dans les sédiments). Il s'agit donc d'évaluer la toxicité chronique de la substance par la voie d'exposition orale uniquement.
Dans les tableaux ci-dessous, ne sont reportés pour chaque type de test que les résultats permettant d'obtenir les NOEC ou la valeur toxicologique de référence (VTR) les plus protectrices. N'ont été recherchés que des tests sur mammifères ou oiseaux exposés par voie orale (exposition par l'alimentation ou par gavage). Toutes les données présentées ont été jugées valides.
Les résultats de toxicité sont principalement donnés sous forme de doses journalières : NOAEL (No Observed Adverse Effect Level), ou LOAEL (Lowest Observed Adverse Effect Level). NOAEL et LOAEL sont exprimées en termes de quantité de substance administrée par unité de masse corporelle de l'animal testé, et par jour.
Pour calculer la norme de qualité liée à l'empoisonnement secondaire des prédateurs, il est nécessaire de connaître la concentration de substance dans le biota n'induisant pas d'effets observés pour les prédateurs (exprimée sous forme de NOEC). Il est possible de déduire une NOEC à partir d'une NOAEL grâce à des facteurs de conversion empiriques variables selon les espèces testées. Les facteurs utilisés ici sont ceux recommandés par le guide technique européen (Tableau 22, page 129, E.C., 2003b) et le projet de guide technique européen pour la détermination de normes de qualité (E.C., 2009). Les valeurs de ces facteurs de conversion dépendent de la masse corporelle des animaux et de leur consommation journalière de nourriture. Celles-ci peuvent donc varier d'une façon importante selon le niveau d'activité et le métabolisme de l'animal, la valeur nutritive de sa nourriture, etc. En particulier elles peuvent être très différentes entre un animal élevé en laboratoire et un animal sauvage.
Afin de couvrir ces sources de variabilité, mais aussi pour tenir compte des autres sources de variabilité ou d'incertitude (variabilité inter et intra-espèces, extrapolation du court terme au long terme, etc.) des facteurs d'extrapolation sont nécessaires pour le calcul de la QSbiota sec pois. Les valeurs recommandées pour ces facteurs d'extrapolation sont données dans le guide technique européen (tableau 23, page 130, E.C., 2003b). Un facteur d'extrapolation supplémentaire (AFdose-réponse) est utilisé dans le cas où la toxicité a été établie à partir d'une LOAEL plutôt que d'une NOAEL.
Les données obtenues sur les mammifères terrestres et les oiseaux, utilisées pour la détermination des valeurs guides pour la protection des prédateurs vis-à-vis de l’empoisonnement secondaire, sont répertoriées dans les tableaux ci-dessous.
TOXICITE ORALE POUR LES MAMMIFERES
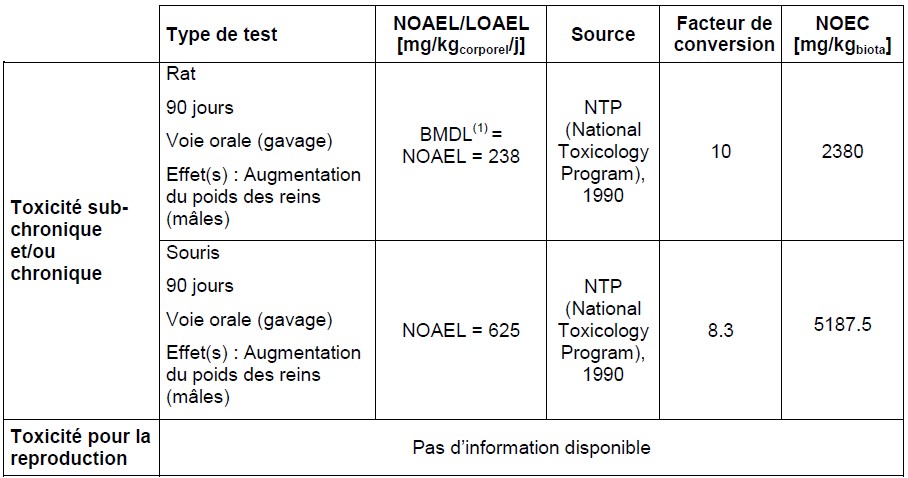
(1) BMDL : BenchMark Dose limit (95%). La « benchmark dose » (ou BMD) est une méthode alternative qui est de plus en plus préconisée car elle permet de s'affranchir de la variabilité inhérente aux expérimentations animales lors de l'utilisation d'un NOAEL comme dose critique. L'objectif est de déterminer la dose (ou la limite inférieure de l'intervalle de confiance correspondant) produisant un effet critique avec une augmentation de la fréquence ou de la sévérité particulière, conventionnellement fixée à 1, 5 ou 10 %.
TOXICITE ORALE POUR LES OISEAUX

L’ensemble des études de toxicité aiguë et chronique sur organismes terrestres proviennent du Rapport Européen d’évaluation des risques (CE, 2003). Ces études ont donc déjà fait l’objet d’une évaluation par les experts Européens et n’ont pas été réévaluées dans ce présent document.
Paramètres d’écotoxicité aiguë :
L’étude conduite sur Eisenia fetida permet uniquement d’encadrer la valeur de la CL50 entre 150 et 280 mg.kg-1 de sol (Heijden Van der et al., 1988).
Regno et al. (1998) ont conduit un test de type Polytox sur un mélange de 12 souches de cultures microbiennes aérobiques. Ils ont ainsi mesuré l’effet du toluène sur la respiration microbienne avec comme matrice un sol sablonneux dont le taux d’humidité variait. Des CI50 de 310, 370, 380 et 430 mg.kg-1 ont été déterminées pour des sols dont le taux d’humidité était respectivement de 33 %, 50 %, 80 % et 100 %.
Synthèse des principaux résultats pour des organismes terrestres lors d’expositions aiguës :

Paramètres d’écotoxicité chronique :
L’étude de Hulzebos et al. (1993) sur la laitue (Lactuca sativa) a été réalisée en suivant la ligne directrice OCDE 208 sur un sol agricole dont les caractéristiques étaient : pH 7,5, matières organiques 1,4%, argile 12%, humidité 80%). La concentration en toluène a été mesurée en début d’expérience mais pas à la fin. En début d’expérience, la concentration était < à 50% de la concentration nominale. Dès lors, cette étude a été invalidée sur la base du peu de fiabilité des concentrations réelles auxquelles les laitues ont été exposées.
L’essai long terme sur Eisenia fetida a été réalisé sur sol artificiel (Heijden Van der et al., 1988). Différentes NOEC 28 jours ont été évaluées sur des critères tels que : la mortalité, la production de cocons ainsi que la condition des vers basée sur une inspection visuelle. Les résultats ont donné les valeurs de NOEC suivantes : ≤ 150 mg.kg-1 pour la mortalité, < 250 mg.kg-1pour la production de cocons et comprise entre 15 et 50 mg.kg-1 sur la base de l’observation visuelle des vers.
Les processus microbiens de respiration et d’ammonification au niveau du sol ont été étudiés sur marne sableuse et humide. Pour ces 2 processus, les valeurs de NOEC se situent entre 360 et 1 300 mg.kg-1 pour le processus de respiration et entre 100 et 1 100 mg.kg-1 pour le processus d’ammonification. Par contre, il s’avère que la nitrification est le processus le plus touché avec une NOEC < 26 mg.kg-1, cette valeur a donc été retenue comme valeur clef.
Synthèse des principaux résultats pour des organismes terrestres lors d’expositions chroniques :

Valeurs de danger
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Synthèse
Sédiments d'eau douce
Aucun résultat d’essai sur organismes benthiques n’a été trouvé dans les sources bibliographiques consultées.
Sédiments marins
Aucun résultat d’essai sur organismes benthiques n’a été trouvé dans les sources bibliographiques consultées.
Valeurs écotoxicologiques
Introduction
Dans cette rubrique, sont reportées des valeurs de référence pour la protection des écosystèmes aquatiques et de la santé humaine via l’environnement.
Elles peuvent avoir un statut de « Valeur réglementaire » si elles sont issues
- de réglementations européennes et issues par exemple de dossiers d’évaluation des risques dans le cadre de processus d’autorisation de mise sur le marché des substances chimiques (c’est le cas des Concentrations Prédites Sans Effet pour l’environnement (PNEC) issues des dossiers réglementaires sous REACh ou dans le cas de la réglementation des produits biocides) ou issues de « Normes de Qualité Environnementale » (NQE) de la Directive Cadre européenne sur l’Eau (DCE) ;
- de réglementations françaises telles que les arrêtés de mise en application de la DCE à l’échelle nationale.
Elles peuvent être des « Valeurs guides » lorsque ce sont des propositions scientifiques de l’INERIS qui ne sont pas reportées dans des textes réglementaires. C’est le cas de toutes les valeurs établies par l’INERIS pour guider l’évaluation de la qualité des milieux aquatiques pour les substances qui n’ont pas, ou pas encore, un statut réglementaire dans le contexte de la DCE.
Les « Valeurs Guides Environnementales » (VGE) et les « Normes de Qualité Environnementale » (NQE) sont les outils consacrés pour l’évaluation de la qualité des eaux de surface, dont l’établissement est basé sur une même méthodologie européenne dédiée (E.C., 2018).
Leur construction, d’un point de vue méthodologique, est donc similaire.
Valeurs guides
Description
NORMES DE QUALITE POUR LA COLONNE D'EAU
Les normes de qualité pour les organismes de la colonne d'eau sont calculées conformément aux recommandations du guide technique européen pour l'évaluation des risques dus aux substances chimiques (E.C., 2003b) et au projet de guide technique européen pour la détermination des normes de qualité environnementale (E.C., 2009). Elles sont obtenues en divisant la plus faible valeur de NOEC ou d'EC50 valide par un facteur d'extrapolation (AF, Assessment Factor).
La valeur de ce facteur d'extrapolation dépend du nombre et du type de tests pour lesquels des résultats valides sont disponibles. Les règles détaillées pour le choix des facteurs sont données dans le tableau 16, page 101, du guide technique européen (E.C., 2003b).
Moyenne annuelle (AA-QSwater_eco) :
Une concentration annuelle moyenne est déterminée pour protéger les organismes de la colonne d'eau d'une possible exposition prolongée.
Pour le toluène, on dispose de données valides pour 3 niveaux trophiques à la fois en aigu et en chronique. Le résultat le plus faible a été obtenu sur Ceriodaphnia dubia, avec une valeur de NOEC sur 7 jours égale à 0.74 mg.L-1. Conformément à la note d du tableau 16 du TGD (E.C., 2003b), la norme de qualité est déterminée en appliquant à la plus faible NOEC un facteur d'extrapolation de 10.
AA-QSwater_eco = 0.74 mg/L /10 = 74 μg/L
Notons que cette valeur a été validée comme PNECaqua (concentration prédite sans effet) lors de l'évaluation européenne de la substance (E.C., 2003a).
- Concentration Maximum Acceptable (MAC):
La concentration maximale acceptable est calculée afin de protéger les organismes de la colonne d'eau de possibles effets de pics de concentrations de courtes durées. Pour la détermination de la MAC, le document guide pour l'évaluation des effets des substances avec des rejets intermittents est utilisée (ECHA, 2008, E.C., 2009)
On dispose de données aiguës sur les trois niveaux trophiques (algues, invertébrés, poissons), la plus faible étant celle sur Crangon franciscorum, EC50 (96 h) = 3.5 mg.L-1. Un facteur d'extrapolation de 100 s'applique pour calculer la MAC :
MAC = 3.5/100 = 0.035 mg/L, soit 35 μg/L
Selon le projet de document guide technique pour la détermination de normes de qualité environnementale (E.C., 2009), lorsque la détermination de la MAC conduit à une valeur plus faible que la AA-EQS, la MAC est fixée à une valeur égale à la AA-QSwater_eco (moyenne annuelle) :

VALEUR GUIDE DE QUALITE POUR LE SEDIMENT (QSSED)
Un seuil de qualité dans le sédiment est nécessaire (i) pour protéger les espèces benthiques et (ii) protéger les autres organismes d'un risque d'empoisonnement secondaire résultant de la consommation de proies provenant du benthos. Les principaux rôles des normes de qualité pour les sédiments sont de :
- Identifier les sites soumis à un risque de détérioration chimique (la norme sédiment est dépassée)
- Déclencher des études pour l'évaluation qui peuvent conduire à des études plus poussées et potentiellement à des programmes de mesures
- Identifier des tendances à long terme de la qualité environnementale (Art. 4 Directive 2000/60/CE).
Aucune information d'écotoxicité pour les organismes benthiques n'a été trouvée dans la littérature.
A défaut, une valeur guide pour le sédiment peut être calculée à partir du modèle de l'équilibre de partage. Ce modèle suppose que:
- il existe un équilibre entre la fraction de substances adsorbées sur les particules sédimentaires et la fraction de substances dissoutes dans l'eau interstitielle du sédiment,
- la fraction de substances adsorbées sur les particules sédimentaires n'est pas biodisponible pour les organismes et que seule la fraction de substances dissoutes dans l'eau interstitielle est susceptible d'impacter les organismes,
- la sensibilité intrinsèque des organismes benthiques aux toxiques est équivalente à celle des organismes vivant dans la colonne d'eau. Ainsi, la norme de qualité pour la colonne d'eau peut être utilisée pour définir la concentration à ne pas dépasser dans l'eau interstitielle.
NB : La pollution actuelle peut être suivie dans les matières en suspension et les couches superficielles du sédiment. Les couches profondes intègrent la contamination historique sur des dizaines voire des centaines d'années et ne sont pas jugées pertinentes pour caractériser la pollution actuelle. Les paramètres par défaut préconisés par Lepper (2002) et le guide technique européen (E.C., 2003b) ont été choisis empiriquement pour caractériser les matières en suspension et les couches superficielles. Matières en suspension et couches superficielles contiennent relativement plus d'eau et de matière organique que les couches profondes du sédiment.
Une valeur guide de qualité pour le sédiment peut être alors calculée selon l'équation suivante (adaptation de l'équation 70 page 113 du guide technique européen, E.C., 2003b) :

Avec
RHOsup : masse volumique de la matière en suspension en [Kgsed.m-3sed]. En l'absence d'une valeur exacte, la valeur générique proposée par Lepper, 2002) et le guide technique européen (équation 18 page 44, E.C., 2003b) est utilisée : 1150 kg.m-3 .
Kpsusp-eau : coefficient de partage matière en suspension/eau en m 3/m3 . En l'absence d'une valeur exacte, les valeurs génériques proposées par Lepper, 2002) et le guide technique européen (équation 24 page 47, E.C., 2003b) sont utilisées. Le coefficient est alors calculé selon la formule suivante : 0.9 + 0.025 * Koc soit Kpsusp-eau = 5.325 m 3/m3 .
Ainsi, on obtient :

QSsed wet weight = 342.65 µg/kg (poids humide)
La concentration correspondante en poids sec peut être estimée en tenant compte du facteur de conversion suivant :

Avec :
Fsolidesusp : fraction volumique en solide dans les matières en suspension en [m3solide/m3susp]. En l'absence d'une valeur exacte, la valeur générique proposée par Lepper (2002) et le guide technique européen (tableau 5 page 43, E.C., 2003b) est utilisée : 0.1 m3/m3 .
RHOsolide : masse volumique de la partie sèche en [kgsolide/m3solide]. En l'absence d'une valeur exacte, la valeur générique proposée par Lepper, 2002) et le guide technique européen (tableau 5 page 43, E.C., 2003b) est utilisée : 2500 kg.m-3 .
Pour le toluène, la concentration correspondante en poids sec est :
QSsed dry_weight = 342.65 * 4.6 = 1576.2 µg.kg-1sed poids sec
Le LogKow de la substance étant inférieur à 5, un facteur additionnel de 10 n'est pas jugé nécessaire.
Il faut rappeler que les incertitudes liées à l'application du modèle de l'équilibre de partage sont importantes. Les sédiments naturels peuvent avoir des propriétés très variables en termes de composition (nature et quantité de matières organiques, composition minéralogique), de granulométrie, de conditions physico-chimiques, de conditions dynamiques (taux de déposition/taux de resuspension). Par ailleurs ces propriétés peuvent évoluer dans le temps en fonction notamment des conditions météorologiques et de la morphologie de la masse d'eau. Si bien que le partage entre la fraction de substance adsorbée et la fraction de substance dissoute peut être extrêmement variable d'un sédiment à un autre et l'hypothèse d'un équilibre entre ces deux fractions ne semble pas très réaliste pour des conditions naturelles.
Par ailleurs, certains organismes benthiques peuvent ingérer les particules sédimentaires, et donc être contaminés par la fraction de substance adsorbée sur ces particules, ce qui n'est pas pris en compte par la méthode.
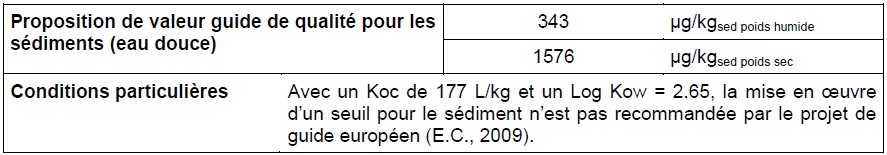
NORME DE QUALITE EMPOISONNEMENT SECONDAIRE (QSBIOTA_SEC POIS)
La norme de qualité pour l'empoisonnement secondaire (QSbiota sec pois) est calculée conformément aux recommandations du guide technique européen (E.C., 2003b). Elle est obtenue en divisant la plus faible valeur de NOEC valide par les facteurs d'extrapolation recommandés dans le tableau 23 page 130 du guide (E.C., 2003b).
Pour le toluène, un facteur de 90 est appliqué car la durée du test retenu (NOEC à 2380 mg.kg-1biota sur rat) est de 90 jours. On obtient donc :
QSbiota_sec pois = 2380 [mg/kgbiota] / 90 = 26444 μg/kgbiota
Cette valeur de norme de qualité pour l'empoisonnement secondaire peut être ramenée à une concentration dans l'eau selon la formule suivante :

Avec :
BCF : facteur de bioconcentration,
BMF : facteur de biomagnification.
Ce calcul tient compte du fait que la substance présente dans l'eau du milieu peut se bioaccumuler dans le biote. Il donne la concentration à ne pas dépasser dans l'eau afin de respecter la valeur de la PNEC pour l'empoisonnement secondaire déterminée dans le biote.
La bioaccumulation tient compte à la fois du facteur de bioconcentration (BCF, ratio entre la concentration dans le biote et la concentration dans l'eau) et du facteur de bioamplification (BMF, ratio entre la concentration dans l'organisme du prédateur en bout de chaîne alimentaire, et la concentration dans l'organisme de la proie au début de la chaîne alimentaire). En l'absence de valeurs mesurées pour le BMF, celles-ci peuvent être estimées à partir du BCF selon le tableau 29, page 160, du guide technique européen (E.C., 2003b).
Ce calcul n'est donné qu'à titre indicatif. Il fait en effet l'hypothèse qu'un équilibre a été atteint entre l'eau et le biote, ce qui n'est pas véritablement réaliste dans les conditions du milieu naturel. Par ailleurs il repose sur un facteur de bioaccumulation qui peut varier de façon importante entre les espèces considérées.
Pour le toluène, un BCF de 90 (valeur maximale) observé chez Leuciscus idus melanotus (E.C., 2003a) et un BMF de 1 (cf. E.C., 2003b) ont été retenus. On a donc :
QSwater sp = 26444 [μg/kgbiota] / (90 *1) = 293.82 μg/L
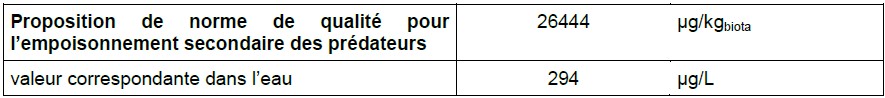
NORME DE QUALITE POUR LA SANTE HUMAINE VIA LA CONSOMMATION DES PRODUITS DE LA PECHE (QSBIOTA_HH)
La norme de qualité pour la santé humaine est calculée de la façon suivante (Lepper, 2005):

Ce calcul tient compte de :
- un facteur correctif de 10% (soit 0.1) : la VTR donnée ne tient compte en effet que d'une exposition par voie orale, et pour la consommation de produits de la pêche uniquement. Mais la contamination peut aussi se faire par la consommation d'autres sources de nourriture, par la consommation d'eau, et d'autres voies d'exposition sont possibles (inhalation ou contact cutané). Le facteur correctif de 10% (soit 0.1) permet de rendre l'objectif de qualité plus sévère d'un facteur 10 afin de tenir compte de ces autres sources de contamination possibles.
- la valeur toxicologique de référence (VTR), correspondant à une dose totale admissible par jour ; pour cette substance elle sera considérée égale à 80 µg/kgcorporel/j (cf. tableau ci-dessus),
- un poids corporel moyen de 70 kg,
- Cons. Journ. Moy : une consommation journalière moyenne de produits de la pêche (poissons, mollusques, crustacés) égale à 115 g par jour,
Ce calcul n'est donné qu'à titre indicatif. Il peut être inadapté pour couvrir les risques pour les individus plus sensibles ou plus vulnérables (masse corporelle plus faible, forte consommation de produits de la pêche, voies d'exposition individuelles particulières). Le facteur correctif de 10% n'est donné que par défaut, car la contribution des différentes voies d'exposition varie selon les propriétés de la substance (et en particulier sa distribution entre les différents compartiments de l'environnement), ainsi que selon les populations considérées (travailleurs exposés, exposition pour les consommateurs/utilisateurs, exposition via l'environnement uniquement). L'hypothèse cependant que la consommation des produits de la pêche ne représente pas plus de 10% des apports journalier contribuant à la dose journalière tolérable apporte une certaine marge de sécurité (E.C., 2009).
Pour le toluène, le calcul aboutit à:
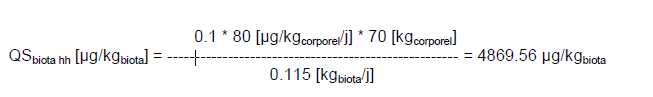
Comme pour l'empoisonnement secondaire, la concentration correspondante dans l'eau du milieu peut être estimée en tenant compte de la bioaccumulation de la substance :

Pour le toluène, on obtient donc:
QSwater_hh food = 4869.56 / (90*1) = 54.1 µg.L-1

NORME DE QUALITE POUR LA SANTE HUMAINE VIA L'EAU DE BOISSON (QSdw_hh)
La norme de qualité pour l'eau de boisson est calculée de la façon suivante (Lepper, 2005) :
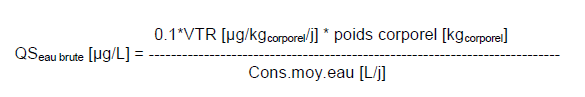
Ce calcul tient compte de:
- la valeur toxicologique de référence (VTR), correspondant à une dose totale admissible par jour ; pour cette substance elle sera considérée égale à 80 µg/kgcorporel/j (Cf. tableau ci-dessus),
- Cons.moy.eau [L.j-1] : une consommation d'eau moyenne de 2 L par jour,
- un poids corporel moyen de 70 kg,
- un facteur correctif de 10% (soit 0.1) afin de tenir compte de ces autres sources de contamination possibles.
L'eau de boisson est obtenue à partir de l'eau brute du milieu après traitement pour la rendre potable. La fraction éliminée lors du traitement dépend de la technologie utilisée ainsi que des propriétés de la substance.

En l'absence d'information, on considèrera que la fraction éliminée est nulle et le critère pour l'eau de boisson s'appliquera alors à l'eau brute du milieu. Par ailleurs, on rappellera que ce calcul n'est donné qu'à titre indicatif et peut s'avérer inadéquat pour certaines substances et certaines populations.
Pour le toluène, on obtient :


Les PNEC suivantes, élaborées par d’autres organismes internationaux, ont été identifiées :
PNEC disponibles pour des organismes pélagiques d’eau douce :

(7) Canadian environmental quality guidelines
(8) Norme de qualité environnementale (sol, eau, air)
(9) Wasserwirtschaft in Deutschland Teil II - Gewässergüte oberirdischer Binnengewässer
PNEC disponibles pour des organismes terrestres :

(11) Environmental quality standards in the Netherlands
(12) Recommandation pour la qualité des sols
Compte-tenu des informations disponibles, l’INERIS propose la valeur suivante :

Justification scientifique :
1) Méthode du facteur d’extrapolation
Les études validées pouvant être utilisées pour dériver la PNECsol sont celles dont les valeurs de NOEC ont été déterminées à partir des bactéries nitrifiantes (< 26 mg.kg-1) et sur vers de terre (15 mg.L-1) (Heijden Van der et al., 1988). Comme deux études sont disponibles sur 2 niveaux trophiques différents, un facteur d’extrapolation de 50 (guide ECHA R.10, 2008) peut être utilisé sur la plus faible des données (CE, 2003).
D’où :
PNECSOL = 0,3 mg.kg-1 poids humide
2) Méthode du coefficient de partage
Par ailleurs, à titre comparatif, la PNECsol peut être déterminée en utilisant la méthode du coefficient de partage (guide ECHA R.10, 2008). La valeur obtenue à l’aide des calculs ci-dessous est identique à celle déterminée dans le rapport européen (CE, 2003) :
Calcul :
PNECsol = Ksol-eau/RHOsol ´ PNECeau ´ 1 000
RHOsol = Densité du sol (humide) (valeur par défaut : 1 700 kg/m3)
Ksol‑eau = Coefficient de partage sol eau (5,55 m3/m3)
= Fairsol ´ Kair-eau + FeauSol + FsolidSol ´ KpSol /1 000) ´ RHOsolid
Kair-eau : Coefficient de partage entre l’air et l’eau (0,23)
Fairsol : Fraction d’air dans le sol (défaut : 0,2 m3.m-3)
Feausol : Fraction d’eau dans le sol (défaut : 0,2 m3.m-3)
Fsolidsol : Fraction solide dans le sol (défaut : 0,6 m3.m-3)
Kpsol : Coefficient de partage eau-sol (3,54 L.kg-1)
RHOsolid : Densité de la phase solide (défaut 2500 kg.L-1)
D’où :
PNECsol de 0,26 mg.kg-1 poids humide = 0,29 mg.kg-1 poids sec.
En conclusion, les valeurs de PNECsol déterminées avec les deux méthodes (facteur d’évaluation et équilibre de partage) sont concordantes. Une valeur arrondie de PNECsol de 0.3 mg.kg-1 sol humide sera donc retenue, conformément au rapport d’évaluation européen (CE, 2003).
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Synthèse
PROPOSITION DE NORME DE QUALITE ENVIRONNEMENTALE (NQE)
La NQE est définie à partir de la valeur de la norme de qualité la plus protectrice parmi tous les compartiments étudiés.
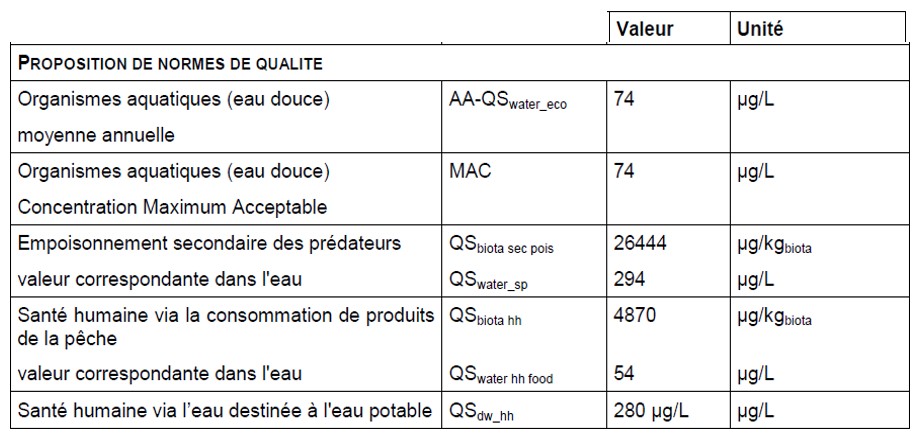
Pour le toluène, la norme de qualité pour la santé humaine via la consommation des produits de la pêche est la valeur la plus faible pour l'ensemble des approches considérées. La proposition de NQE pour le toluène est donc la suivante :
PROPOSITION DE NORME DE QUALITE ENVIRONNEMENTALE

PROPOSITION DE NORMES DE QUALITE POUR LE SEDIMENT
Avec un Koc de 177 L.kg-1 et un Log Kow = 2.65, la mise en œuvre d'un seuil pour le sédiment n'est pas recommandée par le projet de guide européen (E.C., 2009).
Sol

Valeurs réglementaires
Description
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Bibliographie
Données technico-économiques
Dernière vérification le 29/03/2024
Tableaux de synthèse
Généralités
| CAS | 108-88-3 |
|---|---|
| SANDRE | 1278 |
| Substance prioritaire dans le domaine de l’eau (DCE) | non |
| Substance soumise à autorisation dans Reach | non |
| Substance soumise à restriction dans Reach | oui |
| Substance extrêmement préoccupante (SVHC) | non |
| Réglementations |
FTE 2015 Importer Les paragraphes ci-après présentent les principaux textes en vigueur à la date de la rédaction de cette rubrique. Cet inventaire n’est pas exhaustif. TEXTES GENERAUXLes rejets de toluène sont réglementés par l'arrêté du 2 février 1998. Le toluène est considéré par ce texte comme une substance nocive pour l'environnement. La valeur limite mensuelle de concentration de ses rejets ne doit pas dépasser 4 mg.L-1 si le flux du rejet dépasse 10 g.j-1 . Le toluène étant un COV, son utilisation est soumise à la directive 1999/13/CE qui vise à réduire les émissions de COV en Europe (objectif de réduction globale de 40 % en 2010 pour la France (IFEN, 2008). Cette directive est complétée par la directive 94/63/CEE du 20 décembre 1994 relative à la lutte contre les émissions de composés organiques volatils (COV) résultant du stockage de l'essence et de sa distribution des terminaux aux stations-service. De plus, le décret n°2007-1115 du 19/07/07, portant publication du Protocole à la Convention de 1979 sur la pollution atmosphérique transfrontière à longue distance relatif à la réduction de l'acidification, de l'eutrophisation et de l'ozone troposphérique (ensemble neuf annexes), fait à Göteborg le 30 novembre 1999, précise les valeurs limites pour les émissions de composés organiques volatils, dont le toluène, provenant des sources fixes. Ainsi, d'une part, le plafond d'émission pour les composés organiques volatils défini pour la France et pour l'année 2010 a été fixé à 1 100 milliers de tonnes de COV soit un pourcentage de réduction des émissions de 63 % par rapport à 1990, prise comme année de base. D'autre part et à titre d'exemple, la valeur limite pour les émissions de COV provenant des opérations de stockage et de distribution d'essence, à l'exception des opérations de soutage des navires de mer, a été fixée à 10 g COV/Nm3 , méthane compris. Le décret n° 2007-1467 du 12/10/07 relatif au livre V de la partie réglementaire du code de l'environnement et abrogeant le décret n° 2007-33 du 08/01/07 excepté l'article 4 relatif aux conditions de mise sur le marché et d'emploi du toluène, du trichlorobenzène et des huiles de dilution et des pneumatiques contenant des hydrocarbures aromatiques polycycliques précise que « un programme national d'action destiné à prévenir, réduire ou éliminer la pollution des eaux de surface, des eaux de transition et des eaux marines intérieures et territoriales par les substances (dont le toluène) est approuvé par le ministre chargé de l'environnement ». Le toluène fait partie de la liste des substances concernées par l'arrêté du 31/01/08 relatif au registre et à la déclaration annuelle des émissions polluantes et des déchets. Ainsi, les industriels doivent déclarer leurs rejets en toluène à partir des valeurs seuils suivantes : 200 kg.an-1 dans le sol et 0 kg.an-1 dans l'eau. Le toluène fait également partie des substances concernées par le règlement n°166/2006 du 18/01/06 concernant la création d'un registre européen des rejets et des transferts de polluants, et modifiant les directives 91/689/CEE et 96/61/CE du Conseil. Le toluène est défini comme liquide inflammable selon la rubrique 1430 cat. B de la nomenclature des ICPE1 et il est assujetti aux rubriques :
La présence de toluène en tant que substance ou dans un mélange, est limitée à une concentration de 0,1 % en poids dans les adhésifs ou dans les peintures en spray destinés au marché grand public. (Annexe XVII du Règlement REACh, telle que mise à jour par le Règlement No 552/2009 du 22 Juin 2009). [1] Décret 53-578 du 20 mai 1953 modifié, relatif à la nomenclature des installations classée pour la protection de l’environnement mise à jour par le ministère de l’environnement et du développement durable. REGLEMENTATION AYANT ATTRAIT AUX DECHETSL'arrêté du 28/10/10 relatif aux installations de stockage de déchets inertes et abrogeant l'arrêté du 15/03/06 fixant la liste des types de déchets inertes admissibles dans des installations de stockage de déchets inertes et les conditions d'exploitation de ces installations indique les valeurs limites à respecter dans ce cadre soit pour le toluène, une valeur limite de 6 mg/kg de déchet sec. LABEL ECOLOGIQUECréé en 1992, l'Eco-label européen est le seul label écologique officiel européen utilisable dans tous les pays membres de l'Union Européenne. Le label écologique communautaire repose sur le principe d'une "approche globale" qui "prend en considération le cycle de vie du produit à partir de l'extraction des matières premières, la fabrication, la distribution, et l'utilisation jusqu'à son recyclage ou son l'élimination après usage. La qualité et l'usage sont également pris en compte. Il a été institué par le règlement (CEE) n°880/92 du Conseil du 23 mars 1992, publié dans le JOCE du 11 avril 1992. Il distingue des produits ou services plus respectueux de l'environnement. Ses critères garantissent l'aptitude à l'usage des produits et une réduction de leurs impacts environnementaux tout au long de leur cycle de vie. Dans ce cadre, la décision 2009/544/CE de la Commission du 13 août 2008 établissant des critères écologiques pour l'attribution du label écologique communautaire aux peintures et vernis d'intérieur fixe une teneur en COV à ne pas dépasser suivant le type de peinture (à titre d'exemple, une valeur limite en COV de 15 g.L-1 avec eau est donnée pour les peintures d'intérieur mates (murs/plafonds). Il en va de même pour la décision 2009/543/CE qui concernent les peintures et vernis d'extérieur (à titre d'exemple, une valeur limite en COV de 90 g.L-1 avec eau est donnée pour les vernis et lasures extérieure pour finitions, y compris lasures opaques). La circulaire du 5 janvier 2009 encadre l'Action nationale de recherche et de réduction des rejets de substances dangereuses dans l'eau par les installations classées (RSDE). Le toluène fait ainsi partie des substances étudiées par l'action RSDE. La directive CE/76/464 du 4 mai 1976 concerne la pollution causée par certaines substances dangereuses déversées dans le milieu aquatique de la communauté. Le toluène fait partie de la liste II de familles et groupes de substances, réglementées par la directive du Parlement et du Conseil n°2000/60/CE du 23 octobre 2000, établissant un cadre pour une politique communautaire dans le domaine de l'eau (Directive Cadre sur l'Eau ou DCE ; CE/2000/60). A noter que le toluène ne fait pas parti des 33 substances prioritaires de la DCE. Le toluène est également concerné par la Directive n° 98/70/CE du 13/10/98 concernant la qualité de l'essence et des carburants diesel et modifiant la directive 93/12/CEE du Conseil, directive limitant la composition des carburant en hydrocarbures aromatiques. Ainsi, parmi les spécificités environnementales applicables aux carburants sur le marché destinés aux véhicules équipés de moteur à allumage commandé, la valeur limite maximale pour les hydrocarbures aromatiques est de 35 % v/v. |
| Classification CLP | Voir la classification CLP |
| Valeurs et normes appliquées en France |
FTE 2015 Importer Les paragraphes ci-après présentent les principales valeurs et normes en vigueur à la date de la rédaction de cette rubrique. Cet inventaire n’est pas exhaustif. VALEURS UTILISÉES EN MILIEU DE TRAVAIL EN FRANCEDes valeurs limites d'exposition professionnelle dans l'air des locaux de travail ont été établies en France pour le toluène (article R 231-58 du Code du travail ; INRS, 2008) :
[2] VME : valeurs limites de moyenne d'exposition (mesurées ou estimées sur la durée d'un poste de travail de 8 heures, elles sont destinées à protéger les travailleurs des effets à moyen ou long terme). [3] VLCT : valeurs limites d'exposition à court terme (mesurées sur une durée maximale de 15 minutes. Leur respect prévient les risques d'effets toxiques immédiats ou à court terme). VALEURS UTILISÉES POUR LA POPULATION GÉNÉRALELa directive n°2008/50/CE du 21/05/08 concernant « la qualité de l'air ambiant et un air pur pour l'Europe » précise la liste des composés organiques volatils (dont le toluène fait partie) pour lesquels des mesures sont conseillées, en tant que précurseurs de l'ozone. Pour la qualité de l'air, la concentration en toluène recommandée vis-à-vis de la santé humaine par l'OMS est de 0,26 mg.m -3 en moyenne hebdomadaire (en ambiance de travail) et 1 mg.m-3 en moyenne sur une demi-heure (seuil olfactif) (WHO, 2000). En ce qui concerne les réglementations relatives à la qualité des eaux de consommation, le toluène n'est ni concerné par le décret n°2001-12204 , ni par la directive 98/83/CE5 . Néanmoins, l'OMS définit une valeur guide pour l'eau potable de 0,7 mg.L-1 (WHO, 2008). [4] Décret du 20 décembre 2001 relatif aux eaux destinées à la consommation humaine à l'exclusion des eaux minérales naturelles. [5] Directive du conseil du 3 novembre 1998 relative à la qualité des eaux destinées à la consommation humaine. |
| Informations complémentaires |
Le toluène est un composé de la famille des hydrocarbures aromatiques issus des matières fossiles. Sa forme simple en fait une des molécules de base de la chimie et de la pétrochimie. Il se présente sous la forme d’un liquide volatil et fait donc partie de la famille des composés organiques volatils (COV). |
Production et utilisation
Production et ventes
Données économiques
FTE 2015 Importer
PRODUCTION
En 2003, il existait trois sites de production en France, situés à Berre, Feyzin et Gonfreville l'Orcher (Commission Européenne, 2003a). Parmi ces trois sites, deux (Feyzin et Gonfreville l'Orcher) appartenaient au groupe Total, principal producteur de toluène en France. Le groupe Shell produisait le toluène dans sa raffinerie de l'étang de Berre. Actuellement, le groupe Shell ne produit plus de toluène en France8 . En 2007, le site de Gonfreville (Total Petrochemicals) a produit 27 800 tonnes de toluène9 . Lors de notre étude, nous n'avons pas obtenu le tonnage de toluène éventuellement produit par les autres sites.
Selon (SESSI, 2008), la production française de toluène commercial est restée relativement stable voir en légère hausse ces dernières années. Ainsi, en 2006, cette production s'établissait à 164 000 tonnes, alors qu'elle était en 2001 de 134 000 tonnes.
De plus, selon la Commission Européenne (2003c), l'Union Européenne produisait dans les années 1995-1997 chaque année près de 16,75 millions de tonnes de toluène dont 14 millions de tonnes sous forme de mélanges incorporés à l'essence et 2,75 millions sous forme de toluène commercial.
[9] http://www.societechimiquedefrance.fr/extras/Donnees/orga/benzene/texbenz.htm
PRIX DU TOLUENE
Le prix moyen du toluène en France était en 2004 de 380 €.t-1 , représentant une vente de 51 millions d'Euros10 . Le toluène étant un produit dérivé du pétrole, son prix dépend entre autres facteurs, du prix de cette matière première, ainsi que de l'accroissement de la demande et des capacités de raffinage. Ainsi, selon les chiffres du commerce extérieur, le prix du toluène a augmenté de 30 % entre 2003 et 2005 (Direction générale des douanes, 2005).
De plus, en considérant qu'en moyenne les essences contiennent 8,6 % de toluène11 (Commission Européenne, 2003c), et que la consommation française d'essence était en 2004 de 11 675 t (CPDP, 2005), près de 1 000 t de toluène ont été consommées via les essences cette année-là, ce qui représente un chiffre de 380 000 euros.
[10] http://www.insee.fr/sessi/panorama/pano05/so_pano05.htm
Procédés de production
FTE 2015 Importer
Le toluène est issu de la transformation de matières premières fossiles (pétrole, gaz et charbon). Il est produit en mélange avec d'autres substances (benzène, xylènes…) à la suite de différents procédés pétrochimiques tels que le reformage catalytique, le vapocraquage et la désalkylation (Commission Européenne, 2003c).
A la suite des opérations pétrochimiques, les fractions de mélange les plus riches en toluène vont être distillées et purifiées pour obtenir du toluène commercial pur à 99 %.
Utilisations
SECTEURS D'UTILISATION
FTE 2015 Importer
DONNEES ECONOMIQUES
Du fait de ses multiples utilisations, le toluène est présent sur de nombreux sites industriels français. Une liste exhaustive serait impossible à établir dans le cadre de ces fiches, néanmoins, les plus gros consommateurs semblent être les entreprises de pétrochimie comme Arkema ou Rhodia mais nos travaux n'ont pas permis de confirmer ou d'infirmer l'usage actuel de toluène par ces sociétés.
SECTEURS D'UTILISATION
Le toluène11 commercial a une multitude d'applications. Celles-ci sont détaillées dans le Tableau 8 (Commission Européenne, 2003c) :.
Tableau 8. Répartition des principales applications du toluène commercial.
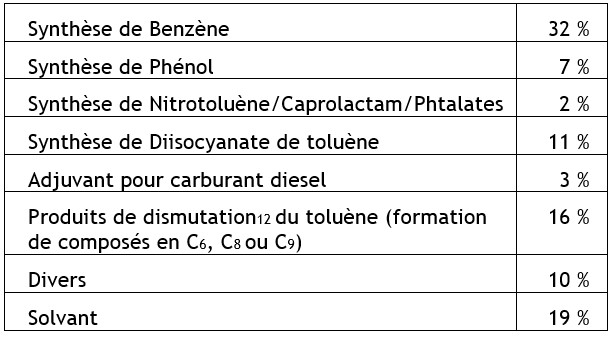
A l'échelle de l'Union Européenne, on va donc retrouver le toluène commercial dans un grand nombre d'industries (cf. Tableau 9 ci-après, Commission Européenne, 2003c) :
Tableau 9. Utilisations industrielles du toluène commercial en Europe.
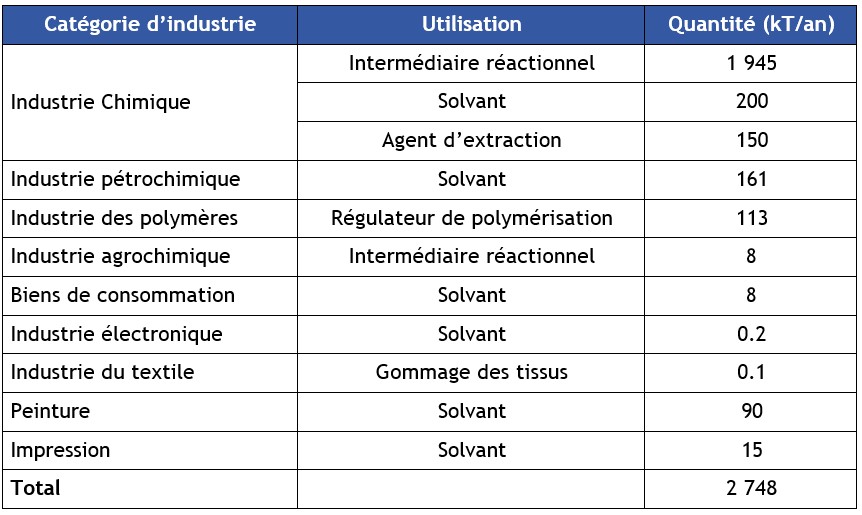
Les utilisations du toluène en tant que solvant, à l'échelle française, sont présentées dans le Tableau 10 ci-après (INRS, 2005).
Tableau 10. Répartition des utilisations de toluène en tant que solvant.

A noter que ces pourcentages sont calculés sur la base de la quantité de toluène totale utilisée dans les domaines des solvants, c'est-à-dire pour l'année 2004, environ 18 000 tonnes.
De plus, le toluène est un des principaux constituants des essences sans plomb. Il a été massivement incorporé à l'essence au milieu des années 80 pour remplacer le tétraméthyle de plomb : il sert à améliorer l'indice d'octane. Ainsi, selon différentes sources citées par la Commission Européenne, 2003c, on considère qu'en moyenne, les essences contiennent 8,6 % de toluène. Toutefois ces dernières années, de nouvelles réglementations14 ont pu faire évoluer ce pourcentage. Avec une consommation d'essence de 11 675 kt par an (CPDP, 2005), en 2004, en France, la consommation de toluène dans les essences s'élevait environ à 1 million de tonnes. Cette consommation d'essence est en diminution depuis 2004 pour atteindre 8 800 kt en 200915 .
[11] Le toluène est ajouté, de façon volontaire, dans les essences afin d'en élever leur indice d'octane
[12] La dismutation est une réaction d'oxydo-réduction dans laquelle une espèce chimique joue à la fois le rôle d'oxydant et de réducteur.
[13] Les meubles meublants sont les meubles destinés à l'usage et à l'ornement des appartements.
[14] Directive 98/70/CE sur la composition des carburants en Europe.
[15] http://www.insee.fr/fr/themes/tableau.asp?ref_id=NATnon11329®_id=0
Rejets dans l’environnement
Sources naturelles
FTE 2015 Importer
Les sources naturelles de toluène sont les incendies de forêts (combustion incomplète des matières végétales), les éruptions volcaniques et les émissions de composés organiques volatils de la végétation (Environnement Canada, 2004). Ces sources sont de moindre importance en comparaison avec les émissions anthropiques produites par les différents processus de conversion du pétrole (Commission Européenne, 2003c).
Émissions atmosphériques
FTE 2015 Importer
Comme nous l'avons vu précédemment les émissions atmosphériques vont être majoritairement liées aux usages du toluène dans les solvants ou l'essence. Ainsi, ces rejets sont présentés dans le paragraphe 3.6 consacré aux émissions dus aux usages.
Émissions vers les eaux
FTE 2015 Importer
De 2003 à 2007 s'est déroulée en France une action de recherche et de réduction des rejets de substances dangereuses dans l'eau (action « 3RSDE »). Deux campagnes de mesure ont permis de réaliser l'inventaire de 106 substances chimiques dans 21 régions françaises dans les rejets aqueux de 2 876 sites volontaires (majoritairement des installations classées), 167 stations d'épuration urbaines et 22 centres de production d'électricité (INERIS, 2008). Concernant le toluène, il a été quantifié dans 23,2 % des sites. Les principaux flux de toluène identifiés sont émis pour 26 % par les stations d'épuration mixtes ou industrielles et pour 73 % par les industriels. Les principaux secteurs industriels concernés sont la chimie et l'industrie pétrolière (selon l'INERIS (2008) 96 % de l'ensemble des sites industriels concernés par les rejets de toluène sont raccordés à une station d'épuration).
A noter que les sites concernés par cette étude étaient les suivants :
- 2648 sites industriels ;
- 39stations d'épuration relevant de la nomenclature des Installations classées (IC) : collectives industrielles16 ou mixtes17 ;
- 167 stations d'épuration urbaines relevant de la loi sur l'eau (mixte et non mixte18 , non IC) ;
- 22 centres de production d'électricité nucléaire ou thermique.
Les données statistiques correspondant aux flux en toluène rejetés lors des campagnes de mesures sont présentées dans le Tableau 11 ci-après.
Tableau 11. Flux de toluène identifiés dans le cadre de l'action 3RSDE (INERIS, 2008).
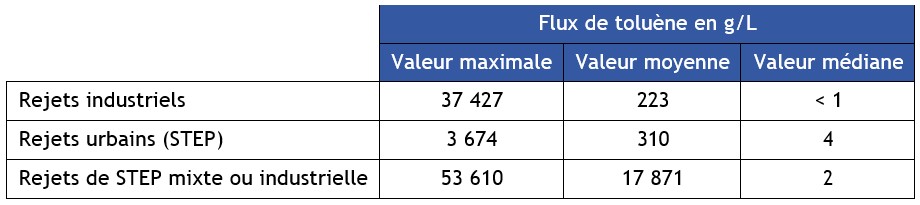
Selon les données du Registre Français des émissions polluantes (IREP19), les émissions industrielles en toluène vers le milieu aquatique pour 2009 ont été de 17 083 kg.an-1 soit un flux d'environ 47 kg.j-1our dont :
- 7 768 kg.an-1 rejetés dans le milieu naturel (sans présager d'un éventuel traitement en amont du rejet) ;
- 9 314 kg.an-1 émis vers la station d'épuration à laquelle l'industriel est raccordé.
Les industriels qui émettent le plus de toluène vers le milieu aquatique appartiennent au secteur de la chimie et parachimie. Parmi les 6 plus gros émetteurs de toluène (rejet supérieur à 1 000 kg.an-1), entre 2007 et 2009, 3 sites ont vu leurs émissions diminuer et deux augmenter. Concernant le dernier site, seules les valeurs pour l'année 2009 sont disponibles.
[16] Station d'épuration collective d'eaux résiduaires industrielles en provenance d'au moins une installation classée soumise à autorisation
[17] Station d'épuration mixte (recevant des eaux résiduaires domestiques et des eaux résiduaires industrielles) ayant une capacité nominale de traitement d'au moins 10 000 équivalents-habitants lorsque la charge des eaux résiduaires industrielles en provenance d'installations classées autorisées est supérieure à 70 % de la capacité de la station en demande chimique en oxygène.
[18] Station d'épuration non mixte : ouvrage ne recevant que des eaux résiduaires domestiques
Rejets dans l'environnement
FTE 2015 Importer
Le toluène peut être émis dans l'environnement lors de sa production, de sa transformation (à savoir la fabrication d'autres substances chimiques), la formulation (mélange à d'autres substances) et de son utilisation. Le milieu atmosphérique est considéré comme le milieu récepteur privilégié vis-à-vis des rejets de toluène, principalement en raison de sa pression de vapeur élevée. Toutefois, des rejets vers les milieux aquatique et terrestre se produisent également (Commission Européenne, 2003c).
La principale source de rejet dans l'environnement est liée à la forte présence de toluène dans les essences. Dans ce cas, le toluène est émis soit directement lors de la vaporisation des essences (station essence, transport et stockage des carburants…), soit dans les gaz d'échappements des véhicules à essences (imbrûlés, volatilisation…). Les autres émissions proviennent des vapeurs de toluène utilisé comme solvant, des rejets de production et des rejets d'incinération (Commission Européenne, 2003c).
Selon la Commission Européenne (2003c) et diverses entreprises pétrolières (Commission Européenne, 2000), au début des années 2000, les émissions dans l'environnement se répartissaient selon les pourcentages suivant :
- trafic routier : 65 % ;
- solvant : 34 %;
- rejets de production et de transformation : 2 %.
Lors de nos travaux, nous n'avons pas trouvé de chiffres plus récents.
Bien que le toluène puisse être présent de façon naturelle dans l'environnement (feu de forêt, pétrole brut…), les rejets sont essentiellement d'origine humaine (Commission Européenne, 2003c).
Par rapport à l'ensemble des rejets de toluène, ceux liés à sa production et son utilisation comme intermédiaire réactionnel dans l'industrie n'apparaissent pas comme très importants. Néanmoins, ces rejets industriels, même s'ils sont peu importants au regard de l'ensemble
des rejets de toluène, constituent la principale source de rejets directs dans les milieux aquatiques (Commission Européenne, 2003c).
Les émissions industrielles proviennent essentiellement des industries chimiques et pétrochimiques. Une étude réalisée par la Commission Européenne (2003c) sur les principaux producteurs et utilisateurs industriels de toluène, estime que sur les 2 600 kt de toluène commercial produit par an en Europe, 14,6 kt sont émises dans l'environnement en moyenne par an. Ces rejets se font à hauteur de 35 % dans l'eau (soit 5,1 kt) et, pour le reste (soit 9,5 kt), vers l'atmosphère.
Outre les émissions dues aux usages non-industriels (ci-après traitées), des émissions diffuses en toluène peuvent se produire lors de déversements de produits chimiques et pétroliers ou à partir de réservoirs ou de réseaux souterrains présentant des fuites. Néanmoins, l'importance de ces émissions n'est pas connue. Le toluène peut également être rejeté dans les sols des sites d'élimination des déchets (Environnement Canada et Santé Canada, 1992).
Les émissions de toluène proviennent pour l'essentiel de son utilisation, soit dans les essences, soit en tant que solvant (peinture, encre…).
On considère (Commission Européenne, 2003c) qu'en moyenne les véhicules à essence rejettent 370 mg.km-1 de toluène soit, pour l'ensemble des véhicules à essences circulant en Europe, 400 à 500 kT par an. D'après le Tableau 12 (Guibet, 2005) on constate que le toluène représente 20 % des émissions d'hydrocarbures imbrûlés dans les gaz d'échappement d'un moteur à essence.
Tableau 12. Exemple de composition des «hydrocarbures imbrûlés » dans les gaz d'échappement d'un moteur à essence.

Les carburants diesel contiennent également du toluène, mais dans des concentrations moyennes inférieures à 0,2 % en masse. Les rejets de toluène issus des véhicules diesel sont donc négligeables par rapport aux rejets des véhicules à essence. Toutefois, au vu du parc des véhicules diesel circulant en Europe, ces quantités ne sont sans doute plus négligeables vis à vis d'autres sources de toluène émises dans l'environnement.
Les chiffres d'émissions du toluène par les gaz d'échappement ont pu énormément fluctuer durant ces vingt dernières années. En effet, le toluène a tout d'abord remplacé le tétraméthyle de plomb dans l'essence durant les années 80. Ses émissions ont alors fortement augmenté. Ensuite, depuis le milieu des années 90 et les normes européenne du programme Auto Oil, les constructeurs automobiles ont généralisé les pots catalytiques sur les véhicules. Or ceux-ci diminuent les rejets de COV et le nombre de véhicules diesel, moins émetteurs de COV non méthaniques, a augmenté (CITEPA, 2010). Ainsi, les émissions de COVNM (composés organiques volatils non méthanique) ont diminué, en France, d'un facteur de 5,9 entre 1995 et 2009, passant de 805 t à 136 t (CITEPA, 2010).
Concernant l'usage du toluène en tant que solvant dans des produits, lors de ce travail, nous n'avons pas identifié d'informations pertinentes.
Enfin le toluène est également émis lors de la combustion de biomasse pour le chauffage. Cette dernière source d'émission pourrait représenter une source importante de rejet de COV dans l'air, mais à ce jour nous n'avons trouvé aucune étude quantifiant les retombées indirectes de ces substances dans les milieux aqueux.
[20] La teneur totale en HC, dans les gaz d'échappement secs, est de l'ordre de 500 ppm.
Pollutions historiques et accidentelles
FTE 2015 Importer
Le toluène étant un produit facilement biodégradable, il n'existe pas véritablement de pollution historique. Toutefois, on peut trouver des traces de toluène autour de lieux ayant subi des fuites d'hydrocarbures (stockage d'essence…) ou au niveau d'anciens sites ayant eu des activités impliquant l'utilisation de toluène.
A noter à titre d'exemple que fin 2004, un contrôle inopiné de la DRIRE21 d'une société d'imprimerie située en Essonne utilisant comme solvant du toluène a révélé un dépassement de la norme relative aux émissions de toluène. Ces émissions provenaient d'un dysfonctionnement des récupérateurs de solvants (perte d'étanchéité des vannes)22 .
[21] La DRIRE Ile de France correspond à l'actuelle direction régionale et interdépartementale de l'environnement et de l'énergie (DRIEE).
Présence environnementale
Atmosphère
FTE 2015 Importer
Comme le toluène présente une pression de vapeur relativement élevée et une solubilité modérée dans l'eau, le milieu atmosphérique va constituer une part importante de sa répartition et de son devenir (Environnement Canada et Santé Canada, 1992).
Air extérieur
Les concentrations moyennes atmosphériques en toluène dans les zones urbaines à l'échelle mondiale varient entre 2 et 200 µg.m -3 . Les concentrations les plus fortes sont enregistrées dans les zones urbaines avec un fort trafic routier. Les niveaux en toluène les plus faibles (entre 0,2 et 4 µg.m-3) sont, quand à eux, relevés dans les zones rurales (WHO, 2004).
Selon l'ATSDR (cité par INERIS, 2005), les concentrations ubiquitaires que l'on peut trouver sont de 0,2 µg.m -3 dans l'air.
En 2009, le réseau de mesures d'AIRPARIF a enregistré une concentration moyenne annuelle représentant un niveau de fond pour l'agglomération parisienne en toluène de 4,2 µg.m -3 . Des concentrations supérieures, de l'ordre de 9,2 à 19,6 µg.m -3 , ont été relevées au niveau du boulevard périphérique (Auteuil) et de la Place Victor Basch, deux stations de mesure représentatives du trafic routier (AIRPARIF, 2010). Ces niveaux sont en diminution par rapport à ceux de l'année 2005 avec des valeurs, cette année là, de 5,5, de 15,2 et de 30,0 µg.m -3 respectivement pour les niveaux de fond, au niveau du périphérique (Auteuil) et Place Victor Basch.
En Alsace, le réseau de surveillance régional a noté une diminution significative de la concentration moyenne annuelle en toluène entre 2003 et 2009 passant de 4,5 µg.m -3 à 1,4 µg.m -3 avec un minimum de 1,1 µg.m-3 en 2008 (ASPA, 2010).
Deux campagnes de mesures ont été réalisées en juin 2007 et mars 2008 par l'INERIS et AIRPARIF sur le thème de l'exposition au benzène (et au toluène) des personnes vivant au voisinage des stations-service. Les observations ont montré un impact des stations-service sur les concentrations en toluène dans l'air extérieur quelle que soit la configuration du site, avec des concentrations comprises entre 36,2 et 76,8 µg.m-3 mesurées dans la rue pour le cas le plus défavorable (fort trafic et conditions de dispersion défavorables).
Air intérieur
Dans le cadre de la campagne nationale réalisée entre 2003-2005 par l'Observatoire de la qualité de l'air intérieur (OQAI), les concentrations dans l'air intérieur de 20 composés cibles23 ont été mesurées dans 567 résidences réparties sur l'ensemble du territoire français métropolitain, représentatif du parc de résidences principales françaises. Cette campagne a permis de dresser un état des lieux de la qualité de l'air intérieur et de souligner la spécificité de la pollution à l'intérieur des logements par rapport à l'extérieur. Le toluène fait partie des principaux composés identifiés dans les logements français (OQAI, 2006). Les résultats sont présentés dans le Tableau 14 ci-après.
Tableau 14. Concentrations en toluène mesurées en air intérieur (OQAI, 2006).
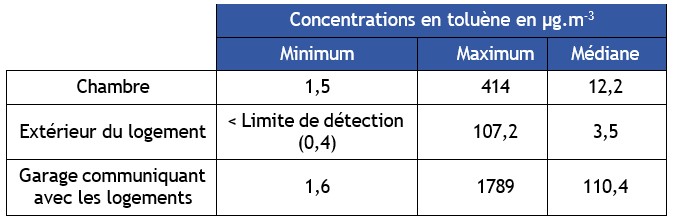
[23] acétaldéhyde ; acroléine ; benzène ; 2-butoxyéthanol ; acétate de 2-butoxyéthyle ; 1,4-dichlorobenzène ; ethylbenzène ; formaldéhyde ; hexaldéhyde ; 1-méthoxy-2-propanol ; acétate de 1-méthoxy-2-propyle ; ndécane; n-undécane ; styrène ; tétrachloroéthylène; toluène; trichloroéthylène; 1,2,4-triméthylbenzène ; m+p-xylène; o-xylène
Aquatique
FTE 2015 Importer
Eaux de pluie
Des concentrations en toluène dans les eaux de pluie ont été mesurées en Allemagne, montrant des valeurs comprises entre 0,13 et 0,70 µg.L-1 (IPCS, 1985).
Entre 1999-2000, des mesures en toluène dans les eaux de pluie sur le campus d'une université ont montré des valeurs de l'ordre de 0,35 µg.L-1 (Okochi et al., 2004).
Eaux de surface
Des analyses réalisées dans les fleuves allemands (le Rhin et l'Elbe) entre 1985 et 1996 donnent des concentrations médianes de 0,5 g.L-1 pour des concentrations moyennes de 0,975 µg.L-1 (Herrchen et Müller, 1997).
Entre 1993 et 1996, les concentrations en toluène ont été mesurées sur 22 sites dans la région du Northumbria au Royaume-Uni (UK Environment Agency, 1997 cité par Commission Européenne, 2003c). Ces mesures ont été effectuées à proximité de sites choisis comme pouvant rejeter du toluène. Les mesures de concentrations en toluène ont révélé des niveaux moyens compris entre :
- < 0,1 et 1,26 µg.L-1 en amont des sites émetteurs de toluène (1 à 3 kilomètres) ;
- 4,5 et 9,3 µg.L-1 au niveau des sites ;
- 1,11 et 5,7 µg.L-1 en aval des sites (200 mètres à 3 kilomètres).
De même, en 1993, en Slovaquie, des mesures ont été réalisées au niveau d'une rivière (Morava) recevant des rejets industriels (pétrole, sucre) et domestiques (sans traitement) (Al-
Rekabi et al., 1996 cités par Commission Européenne, 2003c). Les concentrations en toluène étaient comprises entre 0,03 et 0,58 µg.L-1 en hiver ; 1,05 et 3,49 µg.L-1 au printemps et 0,64 et 2,24 µg.L-1 dans l'année.
Sédiments
Des concentrations en toluène ont également été mesurées dans les sédiments lors de l'étude réalisée au niveau de la rivière Morava, en Slovaquie. Celles-ci se sont révélées plus importantes que celles mesurées dans les eaux de surface et de l'ordre de :
- 10,1 à 69,5 µg.kg-1 en hiver ;
- 7,4 à 290 µg.kg-1 au printemps ;
- 6,2 à 166 µg.kg-1 en été ;
- 4,3 à 192,2 µg.kg-1 sur l'année.
Rejets industriels et stations d'épuration
Dans le cadre de l'action 3RSDE, des concentrations en toluène ont été mesurées dans les rejets aqueux de sites industriels et stations d'épuration (INERIS, 2008). Les campagnes de mesure ont permis de mettre en évidence les résultats présentés dans le Tableau 13 ci-après.
Tableau 13. Concentrations en toluène mesurées dans le cadre de l'action 3RSDE (INERIS, 2008).
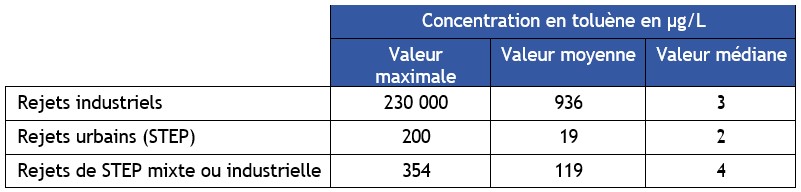
A noter que des données plus récentes de concentrations en toluène dans les eaux de surface et dans les sédiments n'ont pas été identifiées lors de ce travail.
Terrestre
FTE 2015 Importer
Dans les sols
Il existe actuellement assez peu de mesures disponibles de toluène dans les sols.
Sans préciser l'origine des prélèvements, la Commission européenne, dans son rapport datant de 2003, rapporte les concentrations suivantes :
- aux Pays-Bas, de 10 µg.kg-1 (concentration moyenne) ;
- en Floride (USA), < 0,04 µg.kg-1 de sol (pour 7 échantillons prélevés sur des sites non contaminés) ;
- au Canada, dans les sols de raffineries, < 0,1 à 10 µg.kg-1 (pour 5 des 10 échantillons prélevés).
Le ministère de l'Environnement et de l'Énergie de l'Ontario rapporte des valeurs de 1,3 et 0,92 μg·kg -1 comme centile 98 des concentrations de toluène dans les sols de parcs ruraux et de vieux parcs urbains, n'ayant pas été affectés par des sources locales ponctuelles de pollution (Environnement Canada, 2004).
Dans les boues de station d'épuration
D'après les mesures réalisées dans les années 1990, les concentrations en toluène mesurées dans les boues de stations d'épuration sont comprises en moyenne entre 0,1 et 100 mg.kg-1 avec des valeurs maximales pouvant atteindre 700 mg.kg-1 (Commission Européenne, 2003c).
Perspectives de réduction
Réduction des rejets
REDUCTION DES EMISSIONS PAR SUBSTITUTION OU PROCEDES DE SUBSTITUTION
FTE 2015 Importer
LE TOLUENE COMMERCIAL
LES SOLVANTS
De façon générale, le meilleur moyen pour réduire les rejets de COV et donc de toluène est de limiter avant tout son utilisation et donc d'agir à la source de la pollution. Pour cela plusieurs solutions sont envisageables, lorsque le toluène est, en particulier, employé comme solvant (ADEME, 2004).
Il est tout d'abord important de développer des bonnes pratiques au sein des unités utilisant des solvants (ADEME, 2004) :
- Sensibilisation et formation du personnel vis à vis de la pollution des COV ;
- Bon entretien des équipements ;
- Confinement des machines pour organiser des circuits fermés ;
- Optimisation des rendements des procédés de nettoyage (rinçage à contre courant) utilisant les solvants ;
- Récupération et recyclage des solvants dans les procédés chimiques.
Le Tableau 15 suivant fournit des exemples de produits de substitution pour certaines activités qui pourraient limiter l'usage du toluène :
Tableau 15. substitution des solvants organiques en peinture (xylène, toluène, éthylbenzène…) selon ADEME, 2004).
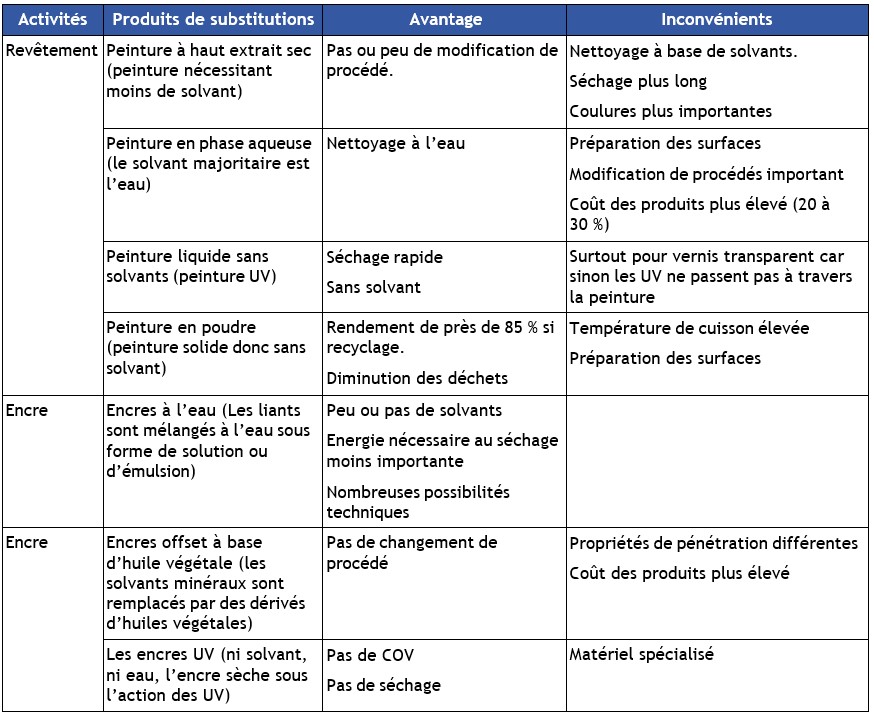
En 2003, en France, sur les 840 000 t de peintures et vernis produits, 375 000 t étaient à base de solvant aqueux, 36 000 t à base de poudre thermodurcissable et 5 000 t à séchage UV. Ainsi, près de la moitié des peintures et vernis produits en France ne contiennent plus de solvant d'origine minérale (FIPEC, 2004). A noter que selon cette même source, pour l'année 2007, 937 500 t de peintures et vernis ont été produits dont 439 000 t à base de solvant aqueux et 46 000 t à base de poudre thermodurcissable.
Selon la FIPEC24 , les COV sont amenés à disparaître progressivement du secteur des peintures et encres sauf pour de rares applications pour lesquelles il n'existe pas encore de solutions de remplacement (marine, aérospatiale). Néanmoins, certaines nouvelles solutions comme les peintures à l'eau posent encore quelques problèmes de pollution. Souvent les utilisateurs nettoient leurs matériels directement à l'eau alors qu'il est préférable de récupérer les eaux de nettoyage ainsi que les restes de produits pour les faire ensuite traiter. Une solution pourra être des peintures aqueuses composées de plastifiants d'origine végétale.
De nombreuses entreprises proposent aujourd'hui des produits sans solvants dangereux servant à divers usages (décapages, peintures, nettoyage des surfaces, dégraissage). On peut citer, l'exemple de la société SID25 qui propose des produits à base de solvants oxygénés ou à base végétale, en substitution de diluants comme le xylène ou le toluène. Des entreprises telles Novance et Oléon ont développé des agro-solvants26 . De même, le groupe Total remplace le toluène par une gamme naphténique à haut pouvoir solvant27 .
Deux autres exemples de substitution ayant été mis en place dans le secteur de l'imprimerie où des diluants contenant du toluène étaient utilisés :
- dans une usine de sérigraphie où était utilisé un diluant contenant environ 50 % en masse de toluène. Ce diluant a été remplacé par deux produits de substitution (diluants organiques sans toluène28). Il n'y a pas d'information sur le coût de cette alternative. Néanmoins, les employés ont approuvé ce changement, essentiellement du fait que l'odeur des nouveaux diluants est moins forte et plus agréable ;
- dans une imprimerie d'étiquettes, le toluène était également présent dans un diluant cellulosique. Deux solutions alternatives ont été mise en place à base de diluants organiques sans toluène pour deux processus de nettoyage différents29 .
On peut également utiliser des procédés moins coûteux en matières premières (cf. Tableau 16 ci-après).
Tableau 16. Procédés permettant de réduire les émissions de COV (ADEME, 2004).
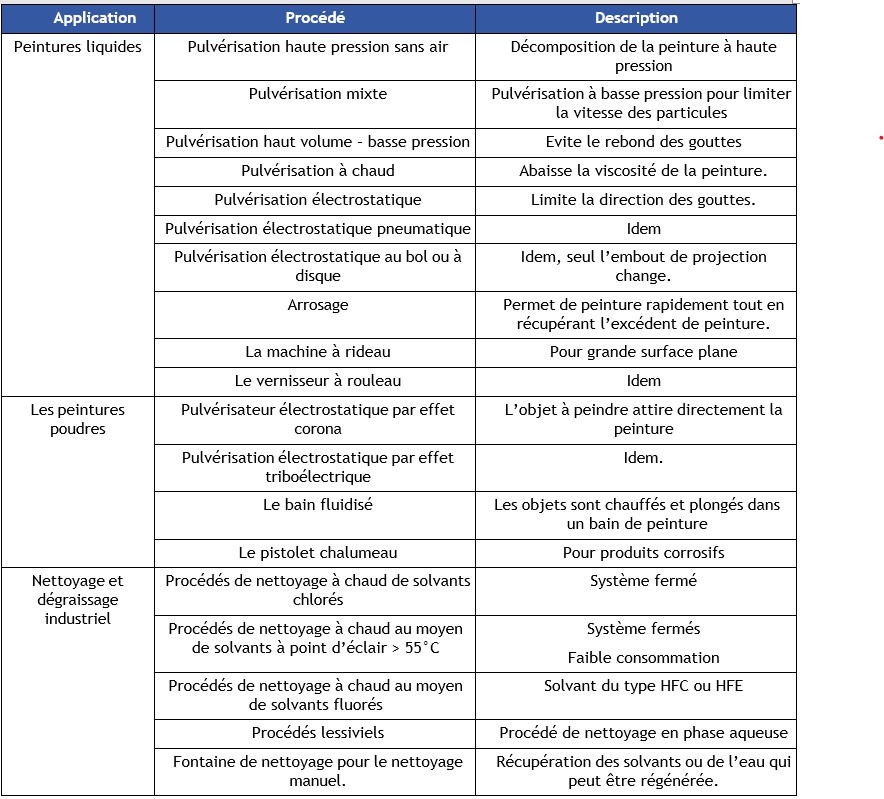
Il existe donc de nombreuses autres solutions de substitution du toluène lorsqu'il est employé comme solvant. Toutefois, avant de faire de telles substitutions, il est important de savoir si le nouveau procédé ou le nouveau produit utilisé aura moins d'impacts sur l'environnement que le toluène. On peut faire appel, pour cela, à des études d'éco-conception ou d'analyse du cycle de vie. Il existe pour cela certains guides ou bases de données qui s'appuient sur des solvants de substitution30 .
Selon des informations recueillies en 2006, en ce qui concerne les prix des produits de substitution, ils sont en général plus chers que le toluène, mais ont une plus faible fluctuation car ils dépendent moins du pétrole.
- le produit proposé par une entreprise de nettoyage des encres et des peintures et pour le dégraissage des surfaces est vendu en moyenne deux fois plus cher que le produit équivalent à base d'hydrocarbures uniquement.
- Une entreprise propose une gamme de produits dérivés d'ester de colza pour le nettoyage et le dégraissage ou pouvant servir d'additif dans les peintures. Ces produits vendus à partir de 1€.kg-1 sont en moyenne deux fois plus chers que les équivalents pétroliers (white spirit), mais une augmentation de la demande et surtout une augmentation des capacités de production pourrait avoir un effet bénéfique sur le coût de ces produits.
- De plus, le marché des peintures sans solvants est beaucoup plus ancien (début des années 50) et beaucoup plus développé. Le prix de ces peintures est donc le même que le prix des peintures contenant des COV.
[24] FIPEC : Fédération des industries des peintures, encres, couleurs, colles et adhésifs.
[25] SID : société industrielle de diffusion : www.sid.tm.fr
[26] http://www.novance.com/ et http://www.oleon.com/solvents.html
[27] http://www.total.be/be/becorporate.nsf/VS_OPM/1318808E6A557118C1256F0B00457314?OpenDocument
[28] http://www.catsub.eu/singeloplysning.aspx?ID=519&sprog=fr
[29] http://www.catsub.eu/singeloplysning.aspx?ID=523&sprog=fr
[30] Citons : Commission européenne () ; l'US EPA () ; solvent alternative guide () ; groupe européen de l'industrie des solvants http://ec.europa.eu/environment/air/pollutants/stationary/solvents/links_en.htm http://epa.gov/http://www.p2pays.org/ref/19/18161/altern.cfm.htmhttp://esig.org
LE TOLUENE, INTERMEDIAIRE REACTIONNEL
Le toluène commercial sert en particulier à la synthèse du benzène dont les quantités extraites du pétrole ne suffisent pas à répondre à une demande en augmentation de 3 % par an entre 1998 et 2003 (INERIS, 2005b).
Le toluène sert également à la synthèse du phénol, intermédiaire fortement utilisé en synthèse chimique. Pour cette synthèse, le toluène peut être substitué par d'autres produits comme le benzène et le chlorobenzène. Toutefois ces deux composés sont également considérés comme des substances dangereuses selon la directive 76/464.
Le toluène est également fortement utilisé dans la synthèse du diisocyanate de toluène qui rentre dans la fabrication de produits polyuréthanes (mousses, matières plastiques). Mais il ne semble exister aucun produit de substitution au toluène pour effectuer cette synthèse.
En tant qu'intermédiaire réactionnel, il apparaît donc très difficile de substituer le toluène par d'autres composés. En effet, les composés aromatiques sont à la base d'une très grande quantité de produits chimiques, et la substitution du toluène ne peut se faire que par d'autres composés aromatiques (benzène, chlorobenzène, …) également jugés préoccupants pour les milieux aquatiques.
LE TOLUENE EN MELANGE DANS LES ESSENCES
Les émissions de toluène sont liées d'une part aux pertes par évaporation de carburant, d'autre part aux émissions à l'échappement :
- En Europe, les émissions par évaporation tendent à se réduire, en raison de la généralisation de systèmes de récupération des vapeurs d'essences sur les modèles récents de véhicules. Les constructeurs automobiles installent aujourd'hui des procédés (canister) qui stockent les vapeurs d'essences provenant du réservoir, et permettent au moteur de les recycler évitant ainsi une partie des rejets de COV (Peugeot, 2006).
- De même, depuis 2001, les postes de chargement des dépôts et raffineries, les cuves de stations services et les camions de ravitaillement sont équipés d'unités de récupération des COV. A noter que la directive 94/63/CE relative à la récupération des vapeurs d'essence lors du stockage a été complétée par la directive 2009/126/CE concernant la récupération des vapeurs d'essence, lors du ravitaillement en carburant des véhicules à moteur dans les stations-service.
- Depuis 1993, les constructeurs ont équipé les voitures nouvellement fabriquées, de filtres et de pots catalytiques. Actuellement, la meilleure technique disponible pour les véhicules essence est le pot catalytique à trois voies et en boucle fermée (UNECE, 2005). Ces pots ont une efficacité supérieure à 90 % concernant l'élimination des hydrocarbures (Douaud, 2010). Toutefois, les réactions catalytiques se font entre 300°C et 1000°C, elles n'ont donc pas lieu tant que le pot catalytique n'a pas atteint sa température de fonctionnement, ce qui prend en général 3 minutes (correspondance IFP, 2005). La catalyse des hydrocarbures imbrûlés en sortie de pots d'échappements des moteurs à essences n'a donc pas lieu sur des petits parcours. De plus, les pots perdent de leur efficacité avec le temps et l'usure du moteur. Ils doivent donc être changer régulièrement (2 ans en moyenne). Même si elle ne les supprime pas, l'utilisation des pots catalytiques permet de diminuer sensiblement les rejets de COV.
Grâce à ces procédés, les émissions de COVNM, ont diminué, en France, de 984 tonnes entre 1988 et 2004, passant de 1 176 t à 291 t (Commission Européenne, 2003c). Entre 1990 et 2006, une nette diminution des émissions du transport routier (-79 % sur la période) a été enregistrée. Cette baisse est consécutive à l'équipement des véhicules à essence en pots
catalytiques, par la diésélisation du parc automobile (peu émetteur de COV non méthanique) (IFEN, 2008).
En outre, pour réduire les émissions de toluène à l'échappement, on peut modifier la composition des essences, et en particulier réduire les teneurs en composés aromatiques. La teneur maximale des essences en composés aromatiques était jusqu'en 2005 de 42 %, mais cette valeur limite est passée à 35 % en Janvier 2005 (IFP, 2005).
Pour modifier la composition des carburants, on peut également avoir recours aux biocarburants. En effet, l'éthanol, l'ETBE et les huiles végétales pures (EMHV) améliorent la combustion des moteurs à essence, ce qui a pour conséquence de diminuer les émissions d'hydrocarbures imbrûlés. Une introduction de ces biocarburants dans des proportions admissibles par les moteurs actuels (20 % au maximum) pourrait donc entraîner une diminution des rejets de toluène. Toutefois, cette introduction doit tenir compte des normes de qualités des essences. Il ne faut pas en particulier que l'introduction d'éthanol entraîne une augmentation de la pression de vapeur saturante, ce qui aurait pour conséquence d'augmenter les émissions de COV31 . Pour cela, les producteurs d'essences doivent proposer de nouvelles compositions de leurs produits, ce qui pourrait entraîner des modifications importantes de leurs installations de productions. Dans un contexte français de surproduction d'essences, ces modifications ne représentent pas d'intérêt économique pour les producteurs.
Suite à l'adoption en 2003 d'une directive européenne « biocarburants » (Directive 2003/17/CE), le plan biocarburant français adopté en 2005 a fixé comme objectif 5,75 % d'incorporation de biocarburants en 2007 et 7 % en 2010. Depuis, la directive européenne 2009/28/CE du 23 avril 2009 fixe à chaque Etat Membre l'objectif d'atteindre 10 % d'énergies renouvelables dans la consommation d'énergie du secteur des transports en 2020, objectif atteignable en particulier grâce aux biocarburants (ADEME32).
L'amélioration du rendement des moteurs à essence, le recours à des voitures hybrides moins consommatrices, l'augmentation du parc de véhicules diesel (lequel ne contient pas de toluène) et l'arrivée sur le marché de véhicules électriques pourraient également entraîner une diminution des rejets. Toutefois, les réductions d'émission de toluène amenées par ces évolutions technologiques risquent d'être partiellement voire totalement compensées par l'augmentation des volumes de trafic prévue d'ici 2015. En fait, pour diminuer durablement les émissions de toluène dues au trafic routier, il faudrait développer de nouvelles sources d'énergie pour les transports (électricité et piles à combustible…). Toutefois, le déploiement à grande échelle de tels développements technologiques semble peu probable d'ici à 2015.
De même, une diminution du trafic routier entraînerait automatiquement une diminution des rejets de toluène, mais là encore les perspectives ne sont pas favorables.
[31] Les émissions de COV dépendent de la tension de vapeur saturante des essences. Plus cette tension est faible, plus les émissions diminuent.
[32] http://www2.ademe.fr/servlet/KBaseShow?sort=-1&cid=96&m=3&catid=23699
REDUCTION DES EMISSIONS PAR TRAITEMENT DES REJETS
FTE 2015 Importer
Les émissions industrielles représentent proportionnellement une source de rejet minoritaire de toluène dans les milieux aquatiques et plus généralement dans l'environnement. Mais ces rejets constituent les principales émissions directes de toluène dans l'eau, pouvant entraîner des pollutions ponctuelles importantes. Sous l'influence des services déconcentrés de l'Etat et des différentes législations, des actions de réduction des émissions de COV ont été menées par les industriels depuis plusieurs années. Elles auraient notamment permis de réduire de 30 % les émissions industrielles de COV entre 2000 et 2007 (IFEN33).
LE TRAITEMENT DES COV
Le toluène étant un composé organique volatil, ses émissions concernent essentiellement le milieu atmosphérique. Elles représentent même les ¾ des émissions industrielles et peuvent intervenir aux différents stades de production et d'utilisation du produit. Comme pour tous les autres COV, les rejets gazeux représentent la très grande majorité des rejets de toluène. Il existe pour traiter ces rejets différents procédés, le plus souvent généralisables à l'ensemble des COV (Techniques de l'ingénieur, 1998 ;Commission Européenne, 2003b). On distingue les procédés de récupération et les procédés de destruction.
Le Tableau 17 ci-après présente les différents procédés applicables aux traitements des COV (Commission Européenne, 2003b).
Tableau 17. Différents procédés applicables aux traitements des COV (Commission Européenne, 2003b)34 .
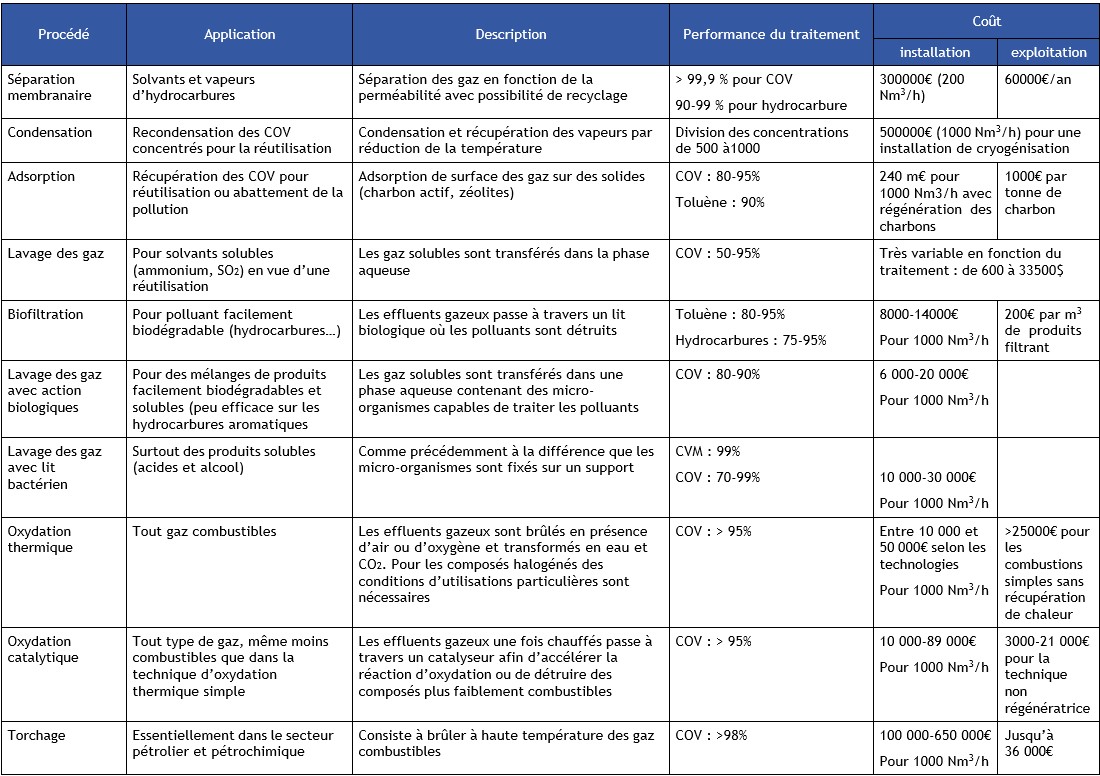

En outre, on peut également estimer le coût de la réduction des émissions de COV par les industriels en étudiant le marché de la lutte contre les Composés Organiques Volatils. Celui-ci a été estimé à 32,4 Million € en 2004, en augmentation de +20% par rapport à 2003. Il devrait encore continuer à augmenter de 20 % en 2005, pour atteindre 38,8 Million € (Actu® environnement35). Selon l'UFIP (Union Française des Industries Pétrolières) interrogée en 2006, la réduction des émissions de COV, de 91 000 t, tout au long de la chaîne pétrolière, a coûté, au total, aux industriels du secteur, 630 M€.
[34] Au moment de la rédaction de cette fiche, ce document est en cours de révision. Une version provisoire est disponible . ftp://ftp.jrc.es/pub/eippcb/doc/cww_d1_10-2009.pdf
[35] http://www.actu-environnement.com/ae/news/1358.php4
LE TRAITEMENT DES EFFLUENTS AQUEUX
Les procédés de traitement des effluents aqueux contenant du toluène peuvent être très variables. Toutefois citons quelques exemples (Commission Européenne, 2003b):
- Dans les raffineries de pétrole, on fait appel à des procédés de déshuilage et dégraissage associés généralement à des procédés de flottation et de coagulation. Ils permettent d'extraire des matières flottantes d'une densité inférieure à celle de l'eau comme c'est le cas pour les hydrocarbures (Techniques de l'ingénieur, 1999). Dans le cas d'un système API (American Petroleum Institute separator), on peut atteindre des performances se situant entre 90 et 95 %. Le coût d'un tel procédé est de 2 millions d'€ pour une capacité de traitement de 1200 m 3/h.
- On peut également citer le procédé de stripping adapté aux polluants volatils (Techniques de l'ingénieur, 1999). Ce procédé correspond à l'entraînement de produits volatils dissous dans l'eau par l'action d'un autre gaz. Les produits ainsi récupérés peuvent être soit réutilisés dans les processus de fabrication, soit détruits par combustion dans un four ou récupérés dans des solutions où ils sont fixés et/ou oxydés. Ce procédé est particulièrement efficace pour les hydrocarbures aromatiques (BTX) pour lesquels on peut atteindre 99 % de performances. Le coût d'une telle installation est de 4 à 5 millions d'€ (exemple d'une raffinerie avec un traitement par stripping d'eau de 30 m 3/h).
- Il est également possible d'utiliser des procédés par adsorption sur charbon actif dans le cas où les polluants sont peu concentrés. Un tel procédé permet par exemple de traiter jusqu'à 95 % d'un effluent contenant jusqu'à 80 mg/g de benzène. Un tel procédé capable de traiter jusqu'à 60 m 3/h d'effluents coût 75 000 £, auquel il faut ajouter 1000 à 2000 £ pour le retraitement d'une tonne de charbon actif.
AUTRES SOLUTIONS
Quelque soit le solvant, un bon moyen de réduire les émissions consiste en la réduction de leur production. On peut, pour cela, les recycler, soit directement sur les sites d'utilisation comme vu précédemment (en récupérant par exemple les vapeurs), soit en les faisant retraiter par des usines spécialisées. Plusieurs usines sont spécialisées dans le retraitement des solvants et du toluène en particulier (comme par exemple : C.M.S. High-Tech36 , DISLAUB37 , SPEICHIM38).
[36] http://www.cms-high-tech.fr/recyclage_solvant/cms_recyclage_solvants.html
[37] http://www.dislaub.fr/dislaub/activites-regeneration-solvants.html
[38] http://www.groupe-seche.com/majic/pageServer/0501000021/fr/SPEICHIM-Mourenx.html
Conclusion
FTE 2015 Importer
Le toluène est un hydrocarbure aromatique fortement présent dans les industries pétrochimiques et chimiques. Il est utilisé dans une multitude d'applications et sa demande est en augmentation.
La présence de toluène dans les milieux aquatiques est due, tout d'abord, aux rejets indirects engendrés par le trafic routier. Ces rejets proviennent soit de la vaporisation des essences (station d'essence, transport et stockage des carburants…), soit des gaz d'échappements des véhicules à essences (imbrûlés, volatilisation…). En se basant sur les chiffres du CITEPA (2010), on peut constater que les rejets dans l'air de COVNM provoqués par le transport, ont été divisés par 5,9 entre 1995 et 2009. Ils ont aussi été divisés par 2,1 dans le secteur de la transformation d'énergie. Ces évolutions ont plusieurs origines :
- Equipement des véhicules routiers en pots catalytiques ;
- Améliorations apportées dans le stockage et la distribution d'hydrocarbures ;
- Augmentation du parc de véhicules diesel ;
- Diminution de la consommation des véhicules à essences (véhicules hybrides, amélioration du couple carburant/moteur…).
Notons que ces réductions ont été constatées dans un contexte d'augmentation du trafic routier de 1,6 % par an entre 1990 et 2004.
La seconde source de rejet importante du toluène est l'évaporation des solvants aromatiques. Depuis 1999, de nouvelles réglementations imposant la limitation des rejets de COV, ont obligé les industriels à réduire leurs émissions. Pour cela différentes solutions ont été développées.
- Développement de produits contenant peu ou pas de solvants aromatiques (peinture à l'eau, désaromatisation du white spirit…) ;
- Utilisation de techniques sans solvants (peinture poudre, encre UV…) ;
- Utilisation de techniques moins consommatrices de solvant (rinçage à contre courant, pulvérisation plus précise…) ;
- Recyclage des solvants par des techniques récupératrices.
Face à ces évolutions, le marché total des solvants en Europe a été en diminution régulière, passant de 5 260 000 t en 1990, 4 100 000 t en 2000 et 3 800 000 t prévues en 2007, soit une baisse de 28 % (BEWA, 2005).
Parallèlement à cette diminution de la consommation de solvants, on observe également une diminution des rejets industriels de COV vers l'atmosphère. Les émissions de COVNM des industries manufacturières ont ainsi diminué de 50 % entre 1990 et 2009, passant de 605 kt à 305 kt (CITEPA, 2010). Aujourd'hui, les techniques de traitement des COV ont des rendements épuratoires supérieurs à 90 % (Douaud, 2010) et elles ne cessent de se développer.
On peut donc espérer la poursuite de ces diminutions, entraînant par là même une réduction des rejets indirects de toluène dans les milieux aquatiques.
Pour les rejets directs, les différents procédés de traitement des hydrocarbures aromatiques dissous dans l'eau permettent d'atteindre des rendements épuratoires de l'ordre de 90 à 95 %. Toutefois, nous ne disposons pas de suffisamment d'information pour dresser un bilan du déploiement de ces solutions de traitement en France.
Les émissions de vapeurs de solvant pourront être diminuées en ayant recours à des solvants de substitution (solvants aqueux et agro-solvants) ou à des produits sans solvant (encres UV, peintures à hauts extrait sec).
Bibliographie
Archives
Dernière vérification le 29/03/2024
Documents
Exporter la substance
Choisissez le format de l'export :










