Configuration de votre affichage
Vous avez activé le mode de configuration de l'affichage qui permet de sélectionner les informations que vous souhaitez afficher sur la fiche substance. Une fois que vous aurez sélectionné les rubriques à afficher, vous pouvez revenir au mode de consultation de la fiche substance en cliquant à nouveau sur le bouton de filtrage.
Chlorobenzène (108-90-7)
Informations générales
Dernière vérification le 29/03/2024
Identification
Numero CAS
108-90-7
Nom scientifique (FR)
Chlorobenzène
Nom scientifique (EN)
Autres dénominations scientifiques (Autre langues)
Code EC
203-628-5
Code SANDRE
1467
Numéro CIPAC
-
Formule chimique brute
\(\ce{ C6H5Cl }\)
Code InChlKey
Code SMILES
c(cccc1)(c1)Cl
Classification CLP
Type de classification
Harmonisée
ATP insertion
CLP00/ATP09
Description de la classification
Classification harmonisée selon réglement 1272/2008 ou CLP
| Mention du danger - Code | H226 |
|---|---|
| Mention du danger - Texte | Liquide et vapeurs inflammables |
| Classe(s) de dangers | Liquides inflammables |
| Libellé UE du danger | - |
| Limites de concentration spécifique | - |
| Facteur M | - |
| Estimation de toxicité aigüe | - |
| Mention du danger - Code | H315 |
|---|---|
| Mention du danger - Texte | Provoque une irritation cutanée |
| Classe(s) de dangers | Corrosion / Irritation cutanée |
| Libellé UE du danger | - |
| Mention du danger - Code | H332 |
|---|---|
| Mention du danger - Texte | Nocif par inhalation |
| Classe(s) de dangers | Toxicité aiguë |
| Libellé UE du danger | - |
| Limites de concentration spécifique | - |
| Facteur M | - |
| Estimation de toxicité aigüe | - |
| Mention du danger - Code | H411 |
|---|---|
| Mention du danger - Texte | Toxique pour les organismes aquatiques, entraîne des effets à long terme |
| Classe(s) de dangers | Danger pour le milieu aquatique |
| Libellé UE du danger | - |
| Limites de concentration spécifique | - |
| Facteur M | - |
| Estimation de toxicité aigüe | - |
Physico-Chimie
Dernière vérification le 29/03/2024
Généralités
Poids moléculaire
112.56 g/mol
Tableau des paramètres
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Bibliographie
Comportement et devenir dans les milieux
Dernière vérification le 29/03/2024
Matrices
Atmosphère
FDTE/VTR Importer Dans l'atmosphère, le chlorobenzène est présent sous forme de vapeur.
Milieu eau douce
Volatilisation :
D'après la valeur de la constante de Henry, le chlorobenzène peut être considéré comme volatile.
FDTE/VTR Importer Dans l'eau, la demi-vie mesurée a été établie à 17,5 heures dans l'eau distillée, et à 3,80 heures dans une eau de rivière (Mansour 1996). Lorsqu'il est relargué dans l'eau, le chlorobenzène est adsorbé sur les matières en suspension et les sédiments. Les demi-vies du chlorobenzène dans l'eau de surface (150 jours) et dans les sédiments de rivière (75 jours) ont été rapportées par Lee et Ryan (1979). Une demi-vie de 46,2 jours a été mesurée dans des sédiments estuariens. Après autoclavage des sédiments, la demi-vie s'établissait à 490 jours, ce qui suggère une influence déterminante des processus biologiques dans la dégradation du chlorobenzène. La volatilisation du chlorobenzène à partir des eaux de surface est considérée comme un processus important de transfert intercompartiments. Des calculs de modélisation sur eau de rivière ont permis de calculer des temps de demi-vie de l'ordre de 3 heures, alors que des calculs similaires effectués sur des eaux de lac fixent les temps de demi-vie aux alentours de 4 jours.
Milieu sédiment eau douce
Milieu terrestre
FDTE/VTR Importer Dans le sol, la mobilité du chlorobenzène est modérée à élevée, les Koc ayant été établis entre 4,8 à 313,1 (HSDB, 2003; Walton et al., 1992).
Compte tenu de sa constante de Henry, sa volatilisation à partir de sols humides est probablement une voie de transfert privilégiée vers d'autres compartiments environnementaux.
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Persistance
Biodégradabilité
Biodégradabilité :
Certains essais standards ont montré que la substance n'était pas facilement biodégradable, notamment :
- 15 % après 28 jours (méthode OCDE 301C)
- 27 % après 63 jours (méthode OCDE 301B)
- 0 % après 28 jours (méthode OCDE 301C)
D'autres essais ont démontré que le chlorobenzène est probablement dégradable de façon inhérente. (IUCLID, 1996 MITI, 1992 Rittman et al., 1980 ; Freitag et al., 1984)
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Dégradabilité abiotique
Hydrolyse :
Le chlorobenzène ne subit probablement aucune hydrolyse en raison de l'absence de groupes fonctionnels hydrolysables. (Lyman et al., 1990)
Photolyse :
Pas d'information disponible.
FDTE/VTR Importer Dans l’atmosphère, le chlorobenzène est dégradé par réaction photochimique sous forme de radicaux hydroxylés. La demi-vie est de 21 jours (Atkinson, 1989). Parmi les radicaux formés, se trouve le monochlorobiphényle. Mansour (1996) a mis en évidence la formation de chlorophénols et de phénols comme sous-produit de la photolyse. Le chlorobenzène ne subit probablement aucune hydrolyse en raison de l'absence de groupes fonctionnels hydrolysables (Lyman et al., 1990).
Milieu eau douce
FDTE/VTR Importer La présence de matière organique dissoute dans l'eau interstitielle réduit de manière significative la quantité de chlorobenzène disponible pour la bioaccumulation (Knezovich et Harrison, 1988).
Milieu sédiment eau douce
FDTE/VTR Importer La biodégradation en milieu anaérobie a été mise en évidence dans des sédiments marins contaminés au chlorobenzène. La demi-vie correspondant a été établie à 46,2 jours (Masunaga et al., 1996). Certains essais standards ont montré que la substance n’était pas facilement biodégradable, notamment : - 15 % après 28 jours (méthode OCDE 301C) (IUCLID, 1996), - 27 % après 63 jours (méthode OCDE 301B) (IUCLID, 1996), - 0 % après 28 jours (méthode OCDE 301C) (CITI, 1992). D’autres essais ont démontré que le chlorobenzène est probablement dégradable de façon inhérente, notamment Rittmann et co-auteurs (1980) et Freitag et co-auteurs (1984).
Milieu terrestre
FDTE/VTR Importer La biodégradation du chlorobenzène dans les compartiments terrestres est variable. Certaines expériences ont montré une absence de minéralisation dans le sol après 8 mois. D'autres expériences menées à partir de consortium bactérien provenant de sols et d'eaux souterraines contaminés par des chlorobenzènes ont mis en évidence des demi-vies de biodégradation de 540 jours, 240 à 281 jours, et > 490 jours respectivement dans des sols sablo-argileux, graveleux, sableux. Le temps de minéralisation est considérablement réduit lors d'ajout de phosphate et d'ammonium dans les sols. De nombreux microorganismes, y compris les champignons, sont capables de dégrader, voire de minéraliser, les chlorobenzènes. Généralement, les produits directs de biodégradation sont le 2- et le 4-monochlorophénol (Haider et al., 1974 ; Ballschmitter et Scholz, 1980). La biodégradation microbienne est d'autant plus efficace que les consortiums sont acclimatés au chlorobenzène. Callahan et co-auteurs (1979) indiquent que la biodégradation du chlorobenzène est relativement lente, à moins qu'elle n'ait lieu en présence de microorganismes bénéficiant d'une source connexe de carbone.
Conclusion sur la persistance
FDTE/VTR Importer Compte tenu du potentiel de dégradation par photolyse et biodégradation, le chlorobenzène est relativement peu persistant dans l'environnement.
Bioaccumulation
Organismes aquatiques
FDTE/VTR Importer Les facteurs de bioconcentration dans les organismes aquatiques ont été calculés, et varient de 0,25 à 450 selon les espèces concernées. Chez la carpe, des BCF de 4,3 à 40, et de 3,9 à 23 ont été déterminés pour des concentrations aquatiques de 0,15 et 0,015 mg/L respectivement (CITI 1992).
Chez les larves d'insectes, Knezovich et Harrison (1988) ont calculé des BCF de 0,25 dans les sédiments, 11 dans les eaux interstitielles et 10 dans la colonne d'eau pour le chlorobenzène présent à l’équilibre. Lorsque les conditions d'équilibre n'étaient pas respectées, les BCF s'établissaient alors à 0,15, 310 et 5 respectivement.
Un BCF du chlorobenzène pour le vairon tête-de-boule a été établi à 450 par Veith et Kosian (1983).
Plusieurs résultats d'essais de bioaccumulation sont disponibles :
- Lepomis macrochirus : (14 jours) BCF = 41 (IUCLID, 1996),
- Pimephales promelas (28 jours) BCF = 447 (Veith et al., 1979),
- Cyprinus carpio (8 semaines) BCF = 3,9 - 40 (CITI, 1992).
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Organismes terrestres
FDTE/VTR Importer Aucune donnée fiable sur la présence de chlorobenzène dans les organismes terrestres animaux n'est disponible.
Pour les végétaux, le chlorobenzène a été détecté, mais non quantifié, dans les tissus de saxifrage (Saxifraga oppositofolia) le long de la côte de l'île Ellesmere dans l'arctique (France, 1997). Des échantillons de lichens prélevés à travers la province de l'Ontario (Canada) entre 1985 et 1987 contenaient du chlorobenzène (Muir et al., 1993). Aucune valeur fiable n'a cependant été rapportée.
Conclusion sur la bioaccumulation
Bioaccumulation/ Biomagnification :
Les facteurs de bioconcentration dans les organismes aquatiques ont été calculés, et varient de 0.25 à 450 selon les espèces concernées.
Chez la carpe (Cyprinus carpio), des BCF de 4.3 à 40, et de
- 3.9à 23 ont été déterminés après 8 semaines pour des concentrations aquatiques de 0.15 et 0.015 mg.L-1 respectivement.
Plusieurs résultats d'essais de bioaccumulation chez le poisson sont disponibles :
- Lepomis macrochirus (14 jours) BCF = 41,
- Pimephales promelas (28 jours) BCF = 447,
Un BCF de 447 est utilisé dans la détermination des normes de qualité ce qui correspond à un BMF1 de 1 auquel s'ajoute pour les organismes marins un BMF2 de (MITI, 1992 IUCLID, 1996 Veith et al., 1979)
Bibliographie
Toxicologie
Dernière vérification le 29/03/2024
Introduction
FDTE/VTR Importer L'ensemble des informations et des données toxicologiques provient de diverses monographies publiées par des organismes reconnus pour la qualité scientifique de leurs documents (OMS IPCS, 1991 ; ATSDR, 1990). Les références bibliographiques aux auteurs sont citées pour permettre un accès direct à l’information scientifique mais n’ont généralement pas fait l’objet d’un nouvel examen critique par les rédacteurs de la fiche.
Toxicocinétique
Chez l'homme
Absorption
FDTE/VTR Importer La principale voie d’absorption est l’inhalation. Une étude réalisée chez deux salariés montre que 38 % et 45 % de la dose administrée par inhalation sont absorbés lors d’une exposition au chlorobenzène à 0,84 et 0,5 ppm respectivement (Ogata et Shimada, 1983). Lors de l’exposition par la voie orale, au moins 31 % de la dose administrée sont absorbés chez l’homme (Ogata et Shimada, 1983).
Métabolisme
FDTE/VTR Importer Les deux principaux métabolites du chlorobenzène sont l’acide p-chlorophénylmercapturique et le 4-chlorocatéchol. Ceux-ci sont éliminés dans les urines lors d’une exposition par inhalation ou par voie orale chez l’homme. Les 2-, 3- ou 4-chlorophénol et le 3-chloro-catéchol sont des métabolites mineurs (ATSDR, 1990 ; OMS IPCS, 1991).
Élimination
FDTE/VTR Importer L’élimination lors de l’exposition par inhalation se fait aussi par voie respiratoire sous forme de chlorobenzène inchangé.
Chez l'animal
Absorption
FDTE/VTR Importer Lors de l’exposition par la voie orale au moins 18 % de la dose administrée (0,3 mmol/kg de chlorobenzène dans du polyéthylène glycol) sont absorbés chez le rat (Ogata et Shimada, 1983) et 22 % (0,5 g de chlorobenzène dans du chremophor EL administré 2 fois par jour pendant 4 jours) chez le lapin (Lindsay-Smith et al., 1972).
Distribution
FDTE/VTR Importer Il a été montré, que chez le rat, le chlorobenzène possède une distribution préférentielle vers les tissus adipeux notamment les graisses péri-rénales du fait de sa nature lipophile (Sullivan et al., 1983), mais il est également présent dans l’épididyme (Verschueren, 1983).
Métabolisme
FDTE/VTR Importer L’acide p-chlorophénylmercapturique et le 4-chlorocatéchol sont également retrouvés dans les urines chez le rat, la souris ou le lapin lors d’expositions par voie orale ou intra-péritonéale (Ogata et Shimada, 1983).
Equivalents biosurveillance
Description
FDTE/VTR Importer Indices biologiques d’exposition pour la population professionnelle : Urines (4-chlorocatéchol total) : 150 mg/g de créatinine Urines (p-chlorophénol total) : 25 mg/g de créatinine
Toxicité aiguë
Chez l'homme
Voie orale
FDTE/VTR Importer Des effets aigus réversibles sur le système nerveux central ont été décrits chez un enfant de 2 ans ayant ingéré 5 à 10 ml de chlorobenzène (Reich, 1934). Ils se manifestent par une perte des réflexes, une perte de connaissance, des spasmes et une cyanose.
Chez l'animal
Inhalation
FDTE/VTR Importer Une exposition de 2 heures à 4 300 ppm (20 124 mg/m3) de chlorobenzène entraîne la mort de 100 % des souris. Chez le lapin, une exposition par inhalation à des concentrations supérieures ou égales à 1 090 ppm pendant 2 heures induit des spasmes musculaires suivis d’une narcose (Rozenbaum et al., 1947). Chez le rat mâle et chez la souris femelle, la CL50 est respectivement de 13 490 mg/m3 (2 965 ppm) et de 8 581 mg/m3 (1 886 ppm) pour une exposition de 6 heures par inhalation (Bonnet et al., 1979, 1982).
Chez la souris, une exposition au chlorobenzène à une concentration de 4 796 mg/m3 induit une diminution de 50 % des capacités respiratoires ce qui témoigne d’une irritation respiratoire (De Ceaurriz et al., 1981).
Voie orale
FDTE/VTR Importer Lors de l'exposition par la voie orale, la mort survient 2 à 3 jours après une administration par gavage de 4 000 mg/kg de chlorobenzène dans de l'huile de maïs chez le rat mâle et femelle ou de 1 000 mg/kg chez la souris (NTP, 1985 ; Kluwe et Shimada, 1985).
Une exposition de 5 jours à 1 140 mg/kg/j de chlorobenzène administré par gavage induit des modifications du métabolisme des porphyrines (Rimington et Ziegler, 1963).
Synthèse
FDTE/VTR Importer Au-delà de quelques heures l'exposition au chlorobenzène, les effets observés sont une dépression du système nerveux central pouvant entraîner la mort.
Toxicité à dose répétées
Effets généraux
Chez l'homme
Inhalation
FDTE/VTR Importer Le chlorobenzène induit des troubles du système nerveux central. Ces effets sont observés lors d'expositions intermittentes par inhalation pour des niveaux supérieurs à ceux des STEL et pour des durées d’exposition pouvant aller jusqu’à 2 ans. Il s'agit de maux de tête, de vertiges, d'une somnolence, d'une torpeur, d'une dépression du système respiratoire central, d’hyperesthésie et de spasmes musculaires (Rozenbaum et al., 1947). Dans ce travail, il n'y a pas de données histologiques.
Voie cutanée
FDTE/VTR Importer Selon les travaux réalisés par le Shangaï Institute For Occupational Disease Prevention in the Chemical Industry entre 1970 et 1982, le chlorobenzène serait à l’origine de 26 des 1 951 cas de dermatoses survenues lors d’expositions professionnelles. Les effets observés sont essentiellement des dermatites eczématiformes, une pigmentation et des neuro-dermatites (Zong et Ma, 1985).
Chez l'animal
Inhalation
FDTE/VTR Importer Effets hématologiques:
Le chlorobenzène induit des effets hématologiques. Ces effets correspondent à une augmentation du nombre de réticulocytes chez le rat lors d'une exposition par inhalation à des concentrations supérieures ou égales à 75 ppm pendant 24 semaines. Cependant les troubles ne sont pas retrouvés chez le lapin (Dilley, 1977). Une leucopénie discrète et une lymphocytose ont été observées chez la souris lors de l'exposition par inhalation à 100 mg/m3 (soit 21,4 ppm) de chlorobenzène pendant 3 mois (Zub, 1978).
Effets hépatiques:
Différentes études, réalisées aussi bien par inhalation que par ingestion chez le rat, la souris, le lapin ou le chien ont montré une diminution de l’accroissement du poids corporel et de la survie pour les doses les plus élevées, une toxicité hépatique et rénale se manifestant par une augmentation des enzymes hépatiques sériques, du poids du foie et des reins, des modifications histo-pathologiques et une nécrose (Irish, 1963 ; Knapp et al., 1971 ; Dilley, 1977 NTP, 1983).
Les lésions hépatiques identifiées correspondent à une congestion hépatique, observée chez les rats mâles et à un moindre degré chez les lapins mâles, pour des expositions par inhalation à des concentrations supérieures ou égales à 75 ppm pendant 24 semaines (Dilley, 1977). Des hémorragies localisées et des foyers de lymphocytes péri-vasculaires sont observés. Une diminution des niveaux sériques de la lactate déshydrogénase et de la transaminase glutamique-oxaloacétique a été constatée en fin de période de traitement.
Une hypertrophie hépatique associée à une augmentation du poids du foie chez le rat mâle a été rapportée lors d’expositions quotidiennes à des vapeurs de chlorobenzène comprises entre 150 et 450 ppm sur deux générations (Nair et al., 1987).
Une congestion rénale liée à l'exposition a été décrite chez le lapin par Dilley (1977). Dans cette étude, les animaux sont exposés par inhalation à des concentrations de chlorobenzène supérieures ou égales à 75 ppm pendant 24 semaines. Un groupe de lapins a présenté une congestion rénale au bout de 5 semaines d’exposition. Celle-ci est associée à des foyers de lymphocytes interstitiels.
Effets immunologiques:
L’exposition à 910 mg/m3 de chlorobenzène réalisées lors de 32 administrations de 7 h/j sur une période de 44 jours n’induit pas d’effet chez le rat (Irish, 1963).
Voie orale
FDTE/VTR Importer Effets hépatiques:
Des effets hépatiques ont également été décrits lors de l'exposition par la voie orale. Il s'agit d'une augmentation des enzymes hépatiques sériques, d’une modification du poids du foie, des dégénérescences, des nécroses et des troubles du métabolisme des porphyrines. Des expositions chez des rats et des souris à des doses de 100 mg/kg/j (ATSDR, 1990) et de 125 mg/kg/j (NTP, 1985) de chlorobenzène induisent une augmentation du poids des organes. Des lésions microscopiques sont induites pour des doses supérieures ou égales à 250 mg/kg/j (NTP, 1985). Des nécroses hépatiques focalisées et des dégénérescences des hépatocytes centrilobulaires sont observées chez la souris. Ces effets sont présents de manière plus nette pour le groupe de rats exposé à des doses supérieures ou égales à 500 mg/kg/j. Il n'y a pas d'effet observé pour des expositions de 60 mg/kg/j.
Le chlorobenzène agirait comme un inducteur hépatique (Sullivan et al., 1983), mais de manière limitée. Lors d’une exposition à de très fortes doses (1 000 mg/kg de poids corporel), une induction de l’aniline hydroxylase est rapportée (Ariyoshi et al., 1975). Une induction de l’époxyde hydrolase hépatique est également observée chez le rat, mais les niveaux d’exposition ne sont pas précisés (Oesch et al., 1973). Par contre, contrairement aux autres dérivés chlorés du benzène, le chlorobenzène n’induit pas les cytochromes P450 ni les enzymes aminopyrine déméthylase ou aniline hydroxylase hépatique chez le rat. Quelle que soit la voie d’exposition, la proportion de chacun des métabolites formés est équivalente (Ogata et Shimada, 1983) et le métabolisme est directement lié à l’induction hépatique.
Chez le chien, une administration de capsules aux doses de 27,25, 54,5 ou 272,5 mg/kg/j, 5 jours par semaine pendant 13 semaines induit des altérations hépatiques à la dose la plus élevée (prolifération du canal biliaire, altérations cytologiques et infiltration leucocytaire du stroma) (Monsanto, 1967).
Lors de l'exposition par la voie orale, les effets rénaux sont également observés pour des niveaux d’exposition identiques à ceux induisant des effets sur le foie.
Dans le cadre d’une étude de 90 jours (NTP, 1985), des dégénérescences ou des nécroses focalisées du tube proximal sont observées pour des expositions par ingestion de chlorobenzène à des doses supérieures ou égales à 250 mg/kg chez la souris et supérieures ou égales à 500 mg/kg chez le rat. Des expositions répétées à des doses supérieures ou égales à 100 mg/kg/j pendant une période 90 à 99 jours (ATSDR, 1990) induisent une augmentation du poids des reins.
Effets immunologiques:
Des effets immunologiques ont été décrits chez le rat et la souris lors d’une exposition par la voie orale. En effet, des souris exposées au chlorobenzène à des doses supérieures ou égales à 250 mg/kg/j par gavage pendant 13 semaines présentent des nécroses thymiques et des déplétions lymphoïdes et myéloïdes de la moelle osseuse, de la rate ou du thymus (NTP, 1985). De cette étude, un LOAEL de 250 mg/kg/j est déterminé.
Cependant, l'ingestion de chlorobenzène pendant 60 à 90 jours à raison de 50 et 125 mg/kg de poids corporel chez le rat et de 125 mg/kg de poids corporel chez la souris, n’entraîne pas l’apparition d’effet (Knapp et al., 1971 ; NTP, 1983).
Effets cancérigènes
Classifications
| Organisme | Classification | Année |
|---|---|---|
| UE | FDTE/VTR Importer Non classé | 2004 |
| US EPA | FDTE/VTR Importer Groupe D : substance non classifiable quant à sa cancérogénicité pour l'homme | 1986 |
Chez l'homme
Synthèse
FDTE/VTR Importer Nous ne disposons pas de données chez l’homme.
Chez l'animal
Voie orale
FDTE/VTR Importer Les données chez l’animal sont jugées inadéquates par l’US EPA.
Une seule étude est retenue au cours de laquelle des rats et des souris ont été exposés au chlorobenzène par gavage. Le chlorobenzène est administré en solution dans de l’huile de maïs à la dose de 60 ou 120 mg/kg/j pour les rats et les souris femelles et de 30 et 60 mg /kg/j pour les souris mâles pendant 5 jours par semaine pendant 103 semaines. Dans ces conditions expérimentales, il n’y a pas d’effet cancérogène pour les deux sexes chez la souris et chez le rat femelle. Par contre chez le rat mâle, une augmentation significative de l’incidence des nodules néoplastiques hépatiques est rapportée uniquement lors de l’exposition à la dose de 120 mg/kg/j (NTP, 1985 ; Kluwe et Shimada, 1985). Ce résultat est jugé insuffisant pour classer le chlorobenzène comme cancérogène.
Effets génotoxiques
Classifications
| Organisme | Classification | Année |
|---|---|---|
| UE | FDTE/VTR Importer non classé | 2004 |
Effets sur la reproduction
Classifications
| Organisme | Classification | Année |
|---|---|---|
| UE | FDTE/VTR Importer non classé | 2004 |
Chez l'homme
Synthèse
FDTE/VTR Importer Il n'existe pas d'étude disponible chez l'homme par inhalation ou par voie orale.
Chez l'animal
Inhalation
FDTE/VTR Importer Chez le rat et le lapin, une exposition par inhalation à des concentrations pouvant atteindre 590 ppm pendant les périodes de l'organogenèse n'induit pas de malformations (John et al., 1984). La dose de 590 ppm induit une toxicité maternelle, traduite par une augmentation du poids du foie et une diminution de la consommation de nourriture. Une augmentation du poids corporel n’est rapportée que chez le rat.
Lors de l'étude sur deux générations de rats pour des expositions par inhalation à des concentrations de chlorobenzène allant jusqu'à 450 ppm, il n'y a pas d'effet sur la reproduction ou la fertilité (Nair et al., 1987). Malgré tout, une légère augmentation de l'incidence des altérations testiculaires de type dégénératif (uni- ou bilatérales) est retrouvée pour la concentration la plus élevée (450 ppm) chez les générations F1 et F0, et pour la dose intermédiaire de 150 ppm, uniquement pour la génération F1. Ceci ne semble cependant pas modifier l’accouplement, le nombre de gestations et les indices de fertilité masculine pour les deux générations concernées. Cependant des altérations rénales sont observées. Il s’agit d’une dilatation tubulaire associée à la présence d'éosinophiles, d'une néphrite interstitielle et d’une régénération focalisée de l’épithélium chez le rat mâle.
Voie orale
FDTE/VTR Importer Les rares études disponibles chez l’animal lors d’une exposition au chlorobenzène par voie orale ne suggèrent pas d'effet tératogène. Chez le rat, lors de l’administration par gavage de 100 ou 300 mg/kg de chlorobenzène dans de l’huile de maïs du 6ème au 15ème jour de la gestation, les différents paramètres étudiés (poids du fœtus, anomalies externes, anomalies du squelette et des tissus mous) ne montrent pas de différences par rapport au lot témoin. De plus, il n’y a pas d’altération du poids des mères (IBL, 1977).
Valeurs accidentelles
Autres seuils accidentels
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Valeurs réglementaires
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Valeurs de référence
Introduction
SANTE HUMAINE
Ce chapitre traite de la toxicité chronique induite par la substance sur l'homme soit via la consommation d'organismes aquatiques contaminés, soit via l'eau de boisson.
Dans les tableaux ci-dessous, ne sont reportés pour chaque type de test que les résultats permettant d'obtenir les NOEC ou la valeur toxicologique de référence (VTR) les plus protectrices. Compte tenu du mode d'exposition envisagée, seuls les tests sur mammifères exposés par voie orale (dans l'alimentation ou par gavage) ont été recherchés.
Toutes les données présentées ont été validées.
Les résultats de toxicité sont principalement donnés sous forme de doses journalières : NOAEL (No Observed Adverse Effect Level), ou LOAEL (Lowest Observed Adverse Effect Level). NOAEL et LOAEL sont exprimées en termes de quantité de substance administrée par unité de masse corporelle de l'animal testé, et par jour.
TOXICITE
Pour l'évaluation des effets sur la santé humaine, seuls les résultats sur mammifères sont considérés comme pertinents. Contrairement à l'évaluation des effets pour les prédateurs, les effets de type cancérigène ou mutagène sont également pris en compte.

(1) Cette VTR a été déterminée par l'US-EPA.

FDTE/VTR Importer Une Valeur Toxicologique de Référence (VTR) est un indice qui est établi à partir de la relation entre une dose externe d'exposition à une substance et la survenue d'un effet néfaste. Les valeurs toxicologiques de référence proviennent de différents organismes. Pour accéder à une information actualisée, nous conseillons au lecteur de se reporter directement sur les sites internet des organismes qui les élaborent.
Autres valeurs des organismes reconnus
Description
FDTE/VTR Importer Effets à seuil - Exposition chronique par inhalation :
Santé Canada propose une CA provisoire (pCA) de 10-2 mg/m3 pour une exposition chronique par inhalation (1991). Mise à jour en 2021
Cette valeur est issue d'une étude de toxicité chez le rat, exposé durant 24 semaines (7 h/j, 5 j/7) au chlorobenzène par inhalation (Dilley, 1977). Pour cette étude, un LOAEL de 341 mg/m3 a été établi pour les effets sur le foie (congestion). Cette valeur a été ajustée pour une exposition continue et pour une exposition chez l'enfant âgé de 5-11 ans.
Calcul : 341 mg/m3 x 7/24 h x 5/7 j x (0,11 m3/j/0,35 kg) / (12 m3/j/27 kg)* = 50,2 mg/m3
valeurs correspondant à une population d'enfants de 5 à 11 ans.
Facteurs d'incertitude : un facteur 10 a été appliqué pour l'extrapolation de l'animal à l'homme, un facteur 10 pour la variabilité au sein de la population humaine, un facteur 5 pour l'utilisation d'un LOAEL (les effets étant cependant faibles) et un facteur 10 pour la faible durée et les limitations de l'étude (un seul sexe et seulement deux doses testées).
Le RIVM propose une TCA provisoire (pTCA) de 0,5 mg/m3 pour une exposition chronique par inhalation (Baars et al., 2001).
Cette valeur est celle recommandée par l'OMS IPCS (1991). Elle est basée sur une étude de toxicité subchronique chez le rat et le lapin pour laquelle un LOAEL de 341 mg/m3 a été identifié pour des effets rénaux et hépatiques (congestions) (Dilley, 1977).
Selon le RIVM, la fiabilité de cette valeur est moyenne.
Facteur d'incertitude : un facteur 1 000 est appliqué.
L'OEHHA propose un REL de 1 mg/m3 pour une exposition chronique par inhalation (2003).
Cette valeur a été calculée à partir d'une étude expérimentale du développement sur deux générations chez le rat, exposé durant 11 semaines (6 h/j, 7 j/sem) à des concentrations en chlorobenzène de 0, 50, 150 et 450 ppm (Nair et al., 1987). Les effets critiques observés ont été une augmentation du poids du foie, une hypertrophie hépatocellulaire, une inflammation et une dégénérescence rénale, et une dégénérescence testiculaire. Le LOAEL a été établi à 150 ppm et le NOAEL à 50 ppm. Ajusté à une exposition continue (6 h/24), le NOAEL est de 13 ppm. La concentration équivalente chez l'homme est de 26 ppm (méthodologie non détaillée).
Facteurs d'incertitude : un facteur 3 est appliqué pour l'extrapolation des données animales à l'homme, un facteur 10 pour la variabilité au sein de la population humaine et un facteur 3 pour la durée subchronique de l'étude.
Calcul : 26 ppm x 1/100 = 0,3 ppm = 1 mg/m3
Effets à seuil - Exposition chronique par voie orale :
L’US EPA (IRIS) propose une RfD par voie orale de 0,02 mg/kg/j (1990).
Cette valeur a été calculée à partir de deux études expérimentales pratiquées chez le rat et le chien. Ces études ont été menées par Monsanto (1967) et Knapp et co-auteurs (1971) ; elles utilisent l’exposition de chiens beagle mâles et femelles à des doses pouvant atteindre 272,5 mg/kg/j, 5 jours par semaine, pendant 13 semaines. L’analyse histo-pathologique sur le foie a permis d’établir un NOAEL de 27,25 mg/kg/j ce qui correspond à la dose ajustée de 19 mg/kg/j et un LOAEL de 54,5 mg/kg /j.
Facteurs d’incertitude : Le facteur d’incertitude de 1 000 correspond à un facteur de 10 pour l’extrapolation de l’animal à l’homme, à un facteur de 10 pour l’incertitude de la limite de détection chez l’homme et à un autre facteur de 10 pour l’extrapolation d’une exposition sub-chronique à une exposition chronique.
Santé Canada propose une DJA de 0,43 mg/kg/j pour une exposition chronique par voie orale (1991). Mise à jour en 2021
Cette valeur est issue de deux études expérimentales chez le rat et la souris, exposés au chlorobenzène par gavage durant 2 ans (5 jours/semaine) (NTP, 1983 ; Kluwe et al., 1985). Un NOAEL de 60 mg/kg/j a été établi pour les effets hépatiques, soit une dose de 43 mg/kg/j pour une exposition continue.
Facteurs d'incertitude : un facteur 10 a été appliqué pour l'extrapolation de l'animal à l'homme et un facteur 10 pour la variabilité au sein de la population humaine.
Calcul : 60 mg/kg/j x 5 j/7 j x 1/100 = 0,43 mg/kg/j.
Le RIVM propose une TDI de 0,2 mg/kg/j pour une exposition chronique par voie orale (Baars et al., 2001).
Cette valeur a été calculée à partir d'une étude expérimentale chez le chien, exposé à des doses pouvant atteindre 272,5 mg/kg/j, 5 jours par semaine, pendant 13 semaines. (Knapp et al., 1971). Un NOAEL de 27,3 mg/kg/j a été établi pour les effets sur le foie, ce qui correspond à une dose ajustée de 19 mg/kg/j pour une exposition continue.
Selon le RIVM, la fiabilité de cette valeur est moyenne.
Facteur d'incertitude : un facteur 100 est appliqué pour la variabilité inter- et intraspécifique. Un facteur supplémentaire pour tenir compte de la durée subchronique de l'étude n'a pas été jugé nécessaire en raison de l'existence d'un NOAEL chronique (sur 2 ans) plus élevé (60 mg/kg/j) obtenu lors de l'étude du NTP (1985).
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Bibliographie
Ecotoxicologie
Dernière vérification le 29/03/2024
Introduction
Evaluations existantes :
-
Effets endocriniens :
Le chlorobenzène n'est pas cité dans la stratégie communautaire concernant les perturbateurs endocriniens (E.C., 2004a) et dans le rapport d'étude de la DG ENV sur la mise à jour de la liste prioritaire des perturbateurs endocriniens à faible tonnage (Petersen et al., 2007).
Critères PBT /POP :
La substance ne remplit pas les critères PBT/vPvB1 (C.E., 2006) ou POP2 (PNUE, 2001).
Normes de qualité existantes :
Canada : Critère de qualité pour les organismes aquatiques, eau douce = 1.3 µg.L-1 (ETOX, 20073)
Allemagne : Norme de qualité pour les eaux prélevées destinées à la consommation = 1 µg.L-1 (ETOX, 20073)
Etats-Unis : Critère de qualité pour la consommation d'eau et de poisson = 680 µg.L-1 (ETOX, 20073)
Etats-Unis : Critère de qualité pour la consommation de poisson et la protection de la santé = 21 000 µg.L-1 (ETOX, 20073)
Substance(s) associée(s) :
-
[1] Les PBT sont des substances persistantes, bioaccumulables et toxiques et les vPvB sont des substances très persistantes et très bioaccumulables. Les critères utilisés pour la classification des PBT sont ceux fixés par l'Annexe XIII du règlement n°1907/2006 (REACH).
[2] Les Polluants Organiques Persistants (POP) sont des substances persistantes (aux dégradations biotiques et abiotiques), fortement liposolubles (et donc fortement bioaccumulables), et volatiles (et peuvent donc être transportées sur de longues distances et être retrouvée de façon ubiquitaire dans l'environnement). Les critères utilisés pour la classification POP sont ceux fixés par l'Annexe 5 de la Convention de Stockholm placée sous l'égide du PNUE (Programme des Nations Unies pour l'Environnement).
[3] Les données issues de cette source (http://webetox.uba.de/webETOX/index.do) ne sont données qu'à titre indicatif ; elles n'ont donc pas fait l'objet d'une validation par l'INERIS.
FDTE/VTR Importer L'objectif de cette rubriqueest d'estimer les effets à long terme sur la faune et la flore, les résultats nécessaires à cette évaluation sont présentés. Lorsqu'un nombre suffisant de résultats d'écotoxicité chronique est disponible, les résultats d'écotoxicité aigus ne sont pas fournis. Lorsque l'écotoxicité chronique n’est pas suffisamment connue, les résultats d'écotoxicité aigus sont présentés et peuvent servir de base pour l'extrapolation des effets à long terme.
Dangers
Description
ORGANISMES AQUATIQUES
Dans les tableaux ci-dessous, sont reportés pour chaque taxon uniquement les résultats des tests d'écotoxicité montrant la plus forte sensibilité à la substance. Toutes les données présentées ont été validées par l'INERIS.
Ces résultats d'écotoxicité sont principalement exprimés sous forme de NOEC (No Observed Effect Concentration), concentration sans effet observé, d'EC10 concentration produisant 10% d'effets et équivalente à la NOEC, ou de EC50, concentration produisant 50% d'effets. Les NOEC sont principalement rattachées à des tests chroniques, qui mesurent l'apparition d'effets sub-létaux à long terme, alors que les EC50 sont plutôt utilisées pour caractériser les effets à court terme.
ECOTOXICITE
ECOTOXICITE AQUATIQUE AIGUË
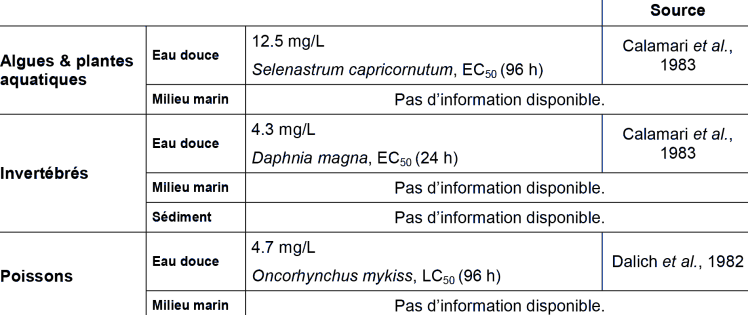
ECOTOXICITE AQUATIQUE CHRONIQUE
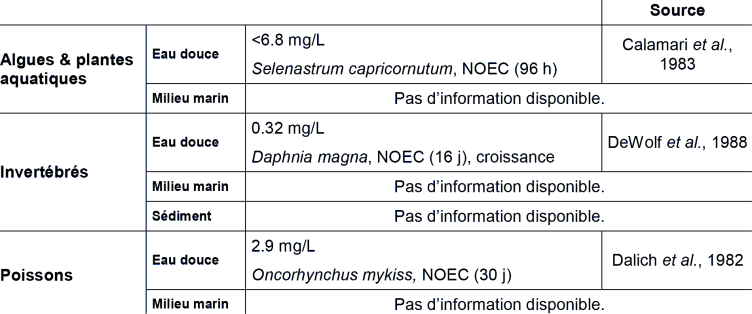
Valeurs de danger
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Synthèse
Eau douce
FDTE/VTR Importer Paramètres d’écotoxicité aiguë
Dans les essais réalisés par Calamari et al., (1983), les concentrations ont été mesurées et les essais ont été réalisés en système fermé. Les résultats sont donc valides.
Parmi les résultats d’essais poissons disponibles, seuls ceux réalisés en système dynamique ont été retenus.
De nombreux autres résultats sont disponibles qui sont d’une qualité inférieure.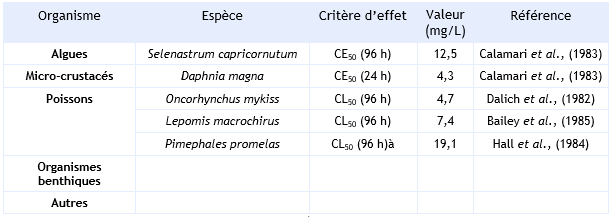
Paramètres d’écotoxicité chronique :
Dans l’essai réalisé par Calamari et co-auteurs (1983), les concentrations ont été mesurées et l’essai a été réalisé en système fermé. Les résultats sont donc valides.
Dans les essais réalisés par DeWolf et co-auteurs (1988) ainsi que Hermens et co-auteurs (1984), les concentrations ont été mesurées. Le résultat peut donc être utilisé pour l’évaluation.
L’essai de Dalich et co-auteurs (1982) a été réalisé en système dynamique. Dans l’essai réalisé par Van Leeuwen et co-auteurs (1990) les concentrations ont été mesurées. Ces résultats sont donc utilisés pour l’évaluation.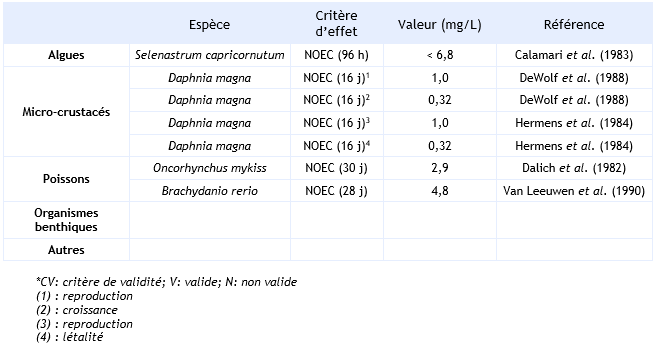
Sol
FDTE/VTR Importer Paramètres d'écotoxicité aiguë ou chronique :
Aucune donnée fiable n'a pu être trouvée concernant les essais de toxicité aiguë réalisés sur organismes terrestres.
Biote
EMPOISONNEMENT SECONDAIRE
Ce chapitre traite de la toxicité chronique induite par la substance sur les prédateurs via la consommation d'organismes aquatiques contaminés (appelés biote, i.e. poissons ou invertébrés vivant dans la colonne d'eau ou dans les sédiments). Il s'agit donc d'évaluer la toxicité chronique de la substance par la voie d'exposition orale uniquement.
Dans les tableaux ci-dessous, ne sont reportés pour chaque type de test que les résultats permettant d'obtenir les NOEC ou la valeur toxicologique de référence (VTR) les plus protectrices. N'ont été recherchés que des tests sur mammifères ou oiseaux exposés par voie orale (exposition par l'alimentation ou par gavage). Toutes les données présentées ont été validées puisqu'elles sont issues d'une source fiable.
Les résultats de toxicité sont principalement donnés sous forme de doses journalières : NOAEL (No Observed Adverse Effect Level), ou LOAEL (Lowest Observed Adverse Effect Level). NOAEL et LOAEL sont exprimées en termes de quantité de substance administrée par unité de masse corporelle de l'animal testé, et par jour.
Pour calculer la norme de qualité liée à l'empoisonnement secondaire des prédateurs, il est nécessaire de connaître la concentration de substance dans le biote n'induisant pas d'effets observés pour les prédateurs (exprimée sous forme de NOEC). Il est possible de déduire une NOEC à partir d'une NOAEL grâce à des facteurs de conversion empiriques variables selon les espèces testées. Les facteurs utilisés ici sont ceux recommandés par le projet de guide technique européen pour la détermination de normes de qualité (E.C., 2010). Les valeurs de ces facteurs de conversion dépendent de la masse corporelle des animaux et de leur consommation journalière de nourriture. Celles-ci peuvent donc varier d'une façon importante selon le niveau d'activité et le métabolisme de l'animal, la valeur nutritive de sa nourriture, etc. En particulier elles peuvent être très différentes entre un animal élevé en laboratoire et un animal sauvage.
Afin de couvrir ces sources de variabilité, mais aussi pour tenir compte des autres sources de variabilité ou d'incertitude (variabilité inter et intra-espèces, extrapolation du court terme au long terme, etc.) des facteurs d'extrapolation sont nécessaires pour le calcul de la QSbiota sec pois. Les valeurs recommandées pour ces facteurs d'extrapolation sont données dans le guide technique européen (E.C., 2010). Un facteur d'extrapolation supplémentaire (AFdose-réponse) est utilisé dans le cas où la toxicité a été établie à partir d'une LOAEL plutôt que d'une NOAEL.
Les données obtenues sur les mammifères terrestres et les oiseaux, utilisées pour la détermination des valeurs guides pour la protection des prédateurs vis-à-vis de l’empoisonnement secondaire, sont répertoriées dans les tableaux ci-dessous.
ECOTOXICITE POUR LES VERTEBRES TERRESTRES
TOXICITE ORALE POUR LES MAMMIFERES
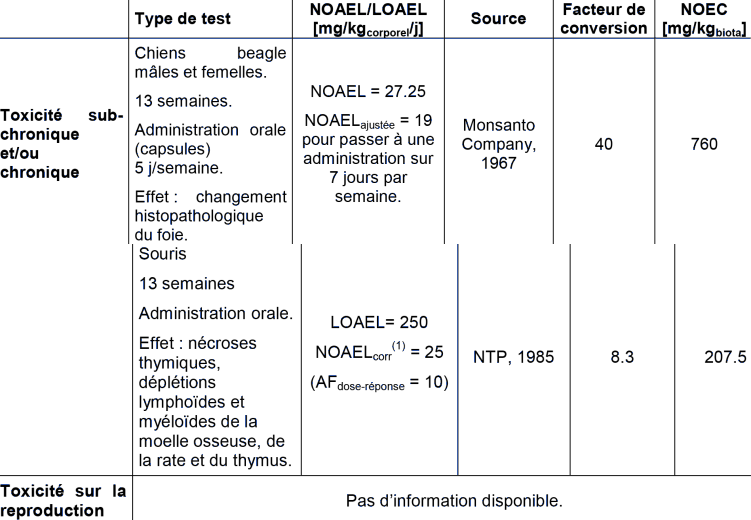
(1) La NOAELcorr correspond à la NOAEL déduite à partir de la LOAEL disponible.
TOXICITE ORALE POUR LES OISEAUX

Valeurs écotoxicologiques
Introduction
Dans cette rubrique, sont reportées des valeurs de référence pour la protection des écosystèmes aquatiques et de la santé humaine via l’environnement.
Dans cette rubrique, sont reportées des valeurs de référence pour la protection des écosystèmes aquatiques et de la santé humaine via l’environnement.
Elles peuvent avoir un statut de « Valeur réglementaire » si elles sont issues
- de réglementations européennes et issues par exemple de dossiers d’évaluation des risques dans le cadre de processus d’autorisation de mise sur le marché des substances chimiques (c’est le cas des Concentrations Prédites Sans Effet pour l’environnement (PNEC) issues des dossiers réglementaires sous REACh ou dans le cas de la réglementation des produits biocides) ou issues de « Normes de Qualité Environnementale » (NQE) de la Directive Cadre européenne sur l’Eau (DCE) ;
- de réglementations françaises telles que les arrêtés de mise en application de la DCE à l’échelle nationale.
Elles peuvent être des « Valeurs guides » lorsque ce sont des propositions scientifiques de l’INERIS qui ne sont pas reportées dans des textes réglementaires. C’est le cas de toutes les valeurs établies par l’INERIS pour guider l’évaluation de la qualité des milieux aquatiques pour les substances qui n’ont pas, ou pas encore, un statut réglementaire dans le contexte de la DCE.
Les « Valeurs Guides Environnementales » (VGE) et les « Normes de Qualité Environnementale » (NQE) sont les outils consacrés pour l’évaluation de la qualité des eaux de surface, dont l’établissement est basé sur une même méthodologie européenne dédiée (E.C., 2018).
Leur construction, d’un point de vue méthodologique, est donc similaire.
Valeurs guides
Description
NORMES DE QUALITE POUR LA COLONNE D'EAU
Les normes de qualité pour les organismes de la colonne d'eau sont calculées conformément aux recommandations du projet de guide technique européen pour la détermination des normes de qualité environnementale (E.C., 2010). Elles sont obtenues en divisant la plus faible valeur de NOEC ou d'EC50 valide par un facteur d'extrapolation (AF, Assessment Factor).
La valeur de ce facteur d'extrapolation dépend du nombre et du type de tests pour lesquels des résultats valides sont disponibles. Les règles détaillées pour le choix des facteurs sont données dans le guide technique européen (E.C., 2010).
En ce qui concerne les organismes marins, selon le projet de document guide technique pour la détermination de normes de qualité environnementale (E.C., 2010), la sensibilité des espèces marines à la
toxicité des substances organiques peut être considérée comme équivalente à celle des espèces dulçaquicoles, à moins qu'une différence ne soit montrée.
Néanmoins, le facteur d'extrapolation appliqué pour déterminer la AA-QSmarine_eco doit prendre en compte les incertitudes additionnelles telles que la sous-représentation de taxons clefs et une diversité d'espèces plus complexe en milieu marin.
Moyenne annuelle (AA-QSwater_eco et AA-QSmarine_eco) :
Une concentration annuelle moyenne est déterminée pour protéger les organismes de la colonne d'eau d'une possible exposition prolongée.
Pour le chlorobenzène, on dispose de données valides pour 3 niveaux trophiques à la fois en aigu et en chronique. En aigu comme en chronique ce sont les invertébrés les plus sensibles. La plus basse NOEC a été observée pour Daphnia magna, (NOEC 16 j à 0.32 mg.L-1). Un facteur d'extrapolation de 10 est donc appliqué (E.C., 2010). On obtient donc :
![]()
En ce qui concerne les organismes marins, aucun essai n'est disponible. Le jeu de données disponible ne permet pas de montrer une différence de sensibilité. En l'absence de taxon additionnel (mollusque, echinodermes, ...) le facteur appliqué est de 100 conformément au guide technique européen (E.C., 2010) :
![]()
Concentration Maximum Acceptable (MAC et MACmarine)
La concentration maximale acceptable est calculée afin de protéger les organismes de la colonne d'eau de possibles effets de pics de concentrations de courtes durées (E.C., 2010). On dispose de données aiguës sur les trois niveaux trophiques (algues, invertébrés, poissons), la plus faible étant celle sur Daphnia magna, EC50 (24 h) = 4.3 mg.L-1. Par défaut, un facteur d'extrapolation de 100 s'applique pour calculer la MAC. Cependant, selon le projet de document guide technique pour la détermination des normes de qualité environnementales (E.C., 2010), pour les substances qui n'ont pas de mode d'action spécifique et pour lesquelles les données disponibles montrent que la variation interspécifique est faible, le facteur peut être diminué. Pour le chlorbenzene, l'écart-type des valeurs de L(E)C50 est < 5 et cette variation peut être considérée comme faible. En conséquence, il est proposé d'abaisser le facteur d'extrapolation à 10.
![]()
![]()
![]()
VALEUR GUIDE DE QUALITE POUR LE SEDIMENT (QSSED ET QSSED-MARIN)
Un seuil de qualité dans le sédiment est nécessaire (i) pour protéger les espèces benthiques et (ii) protéger les autres organismes d'un risque d'empoisonnement secondaire résultant de la consommation de proies provenant du benthos. Les principaux rôles des normes de qualité pour les sédiments sont de :
- Identifier les sites soumis à un risque de détérioration chimique (la norme sédiment est dépassée)
- Déclencher des études pour l'évaluation qui peuvent conduire à des études plus poussées et potentiellement à des programmes de mesures
- Identifier des tendances à long terme de la qualité environnementale (Art. 4 Directive 2000/60/CE).
Aucune information d'écotoxicité pour les organismes benthiques n'a été trouvée dans la littérature.
A défaut, une valeur guide pour le sédiment peut être calculée à partir du modèle de l'équilibre de partage.
Ce modèle suppose que :
- il existe un équilibre entre la fraction de substances adsorbées sur les particules sédimentaires et la fraction de substances dissoutes dans l'eau interstitielle du sédiment,
- la fraction de substances adsorbées sur les particules sédimentaires n'est pas biodisponible pour les organismes et que seule la fraction de substances dissoutes dans l'eau interstitielle est susceptible d'impacter les organismes,
- la sensibilité intrinsèque des organismes benthiques aux toxiques est équivalente à celle des organismes vivant dans la colonne d'eau. Ainsi, la norme de qualité pour la colonne d'eau peut être utilisée pour définir la concentration à ne pas dépasser dans l'eau interstitielle.
Une valeur guide de qualité pour le sédiment peut être alors calculée selon l'équation suivante (E.C., 2010) :
![]()
Avec :
RHOsed : masse volumique du sédiment en [Kgsed.m-3sed]. En l'absence d'une valeur exacte, la valeur générique proposée par le guide technique européen (E.C., 2010) est utilisée : 1300 kg.m-3 .
Ksed-eau : coefficient de partage sédiment/eau en m3/m3 . En l'absence d'une valeur exacte, les valeurs génériques proposées par le guide technique européen (E.C., 2010) sont utilisées. Le coefficient est alors calculé selon la formule suivante : 0.8 + 0.025 * Koc soit Kpsusp-eau = 6.4 m3/m3 .
Ainsi, on obtient :
![]()
![]()
La concentration correspondante en poids sec peut être estimée en tenant compte du facteur de conversion suivant :
![]()
Avec :
Fsolidesed : fraction volumique en solide dans les sédiments en [m3solide/m3susp]. En l'absence d'une valeur exacte, la valeur générique proposée par le guide technique européen (E.C., 2010) est utilisée : 0.2 m3/m3 .
RHOsolide : masse volumique de la partie sèche en [kgsolide/m3solide]. En l'absence d'une valeur exacte, la valeur générique proposée par le guide technique européen (E.C., 2010) est utilisée : 2500 kg.m-3 .
Pour le chlorobenzène, la concentration correspondante en poids sec est :
![]()
Selon la même approche que pour le sédiment d'eau douce, une valeur guide de qualité pour le sédiment marin peut être calculée selon la formule suivante :
![]()
QSsed-marin wet weight = 15.75 µg/kg (poids humide)
La concentration correspondante en poids sec est alors la suivante :
![]()
Le LogKow de la substance étant inférieur à 5, un facteur additionnel de 10 n'est pas jugé nécessaire.
Il faut rappeler que les incertitudes liées à l'application du modèle de l'équilibre de partage sont importantes. Les sédiments naturels peuvent avoir des propriétés très variables en termes de composition (nature et quantité de matières organiques, composition minéralogique), de granulométrie, de conditions physico-chimiques, de conditions dynamiques (taux de déposition/taux de resuspension). Par ailleurs ces propriétés peuvent évoluer dans le temps en fonction notamment des conditions météorologiques et de la morphologie de la masse d'eau. Si bien que le partage entre la fraction de substance adsorbée et la fraction de substances dissoute peut être extrêmement variable d'un sédiment à un autre et l'hypothèse d'un équilibre entre ces deux fractions ne semble pas très réaliste pour des conditions naturelles.
Par ailleurs, certains organismes benthiques peuvent ingérer les particules sédimentaires, et donc être contaminés par la fraction de substance adsorbée sur ces particules, ce qui n'est pas pris en compte par la méthode.
![]()
Conditions particulières Avec un Koc de 224 L.kg-1 et un Log Kow = 2.85, la mise en œuvre d'un seuil pour le sédiment n'est pas recommandée par le projet de guide européen (E.C., 2010).
NORME DE QUALITE EMPOISONNEMENT SECONDAIRE (QSBIOTA_SEC POIS)
La norme de qualité pour l'empoisonnement secondaire (QSbiota sec pois) est calculée conformément aux recommandations du guide technique européen (E.C., 2010). Elle est obtenue en divisant la plus faible valeur de NOEC valide par les facteurs d'extrapolation recommandés (E.C., 2010).
Pour le chlorobenzène, un facteur de 90 est appliqué car la durée du test retenu (NOAEL à 25 mg/kgcorporel/j sur le rat, soit une NOEC de 207.5 mg.kg-1biota) est de 13 semaines. On obtient donc :
![]()
Cette valeur de norme de qualité pour l'empoisonnement secondaire peut être ramenée :
- à une concentration dans l'eau selon la formule suivante :
- à une concentration dans l'eau marine selon la formule suivante :
![]()
Avec :
BCF : facteur de bioconcentration,
1 BMF: facteur de biomagnification,
2 BMF: facteur de biomagnification additionnel pour les organismes marins.
Ce calcul tient compte du fait que la substance présente dans l'eau du milieu peut se bioaccumuler dans le biote. Il donne la concentration à ne pas dépasser dans l'eau afin de respecter la valeur de la norme de qualité pour l'empoisonnement secondaire déterminée dans le biote.
La bioaccumulation tient compte à la fois du facteur de bioconcentration (BCF, ratio entre la concentration dans le biote et la concentration dans l'eau) et du facteur de biomagnification (BMF, ratio entre la concentration dans l'organisme du prédateur en bout de chaîne alimentaire, et la concentration dans l'organisme de la proie au début de la chaîne alimentaire). En l'absence de valeurs mesurées pour le BMF1 et le BMF2, celles-ci peuvent être estimées à partir du BCF selon le guide technique européen (E.C., 2010).
Ce calcul n'est donné qu'à titre indicatif. Il fait en effet l'hypothèse qu'un équilibre a été atteint entre l'eau et le biote, ce qui n'est pas véritablement réaliste dans les conditions du milieu naturel. Par ailleurs il repose sur un facteur de bioaccumulation qui peut varier de façon importante entre les espèces considérées.
Pour le chlorobenzène, un BCF de 447 (sur Pimephales promelas, Veith et al. (1979) et un BMF1 = BMF2 de 1 (cf. E.C., 2010) ont été retenus. On a donc :
![]()
![]()
NORME DE QUALITE POUR LA SANTE HUMAINE VIA LA CONSOMMATION DES PRODUITS DE LA PECHE (QSBIOTA_HH)
La norme de qualité pour la santé humaine est calculé de la façon suivante (E.C., 2010) :
![]()
Ce calcul tient compte de :
- un facteur correctif de 10% (soit 0.1) : la VTR donnée ne tient compte en effet que d'une exposition par voie orale, et pour la consommation de produits de la pêche uniquement. Mais la contamination peut aussi se faire par la consommation d'autres sources de nourriture, par la consommation d'eau, et d'autres voies d'exposition sont possibles (inhalation ou contact cutané). Le facteur de correctif de 10% (soit 0.1) permet de rendre l'objectif de qualité plus sévère d'un facteur 10 afin de tenir compte de ces autres sources de contamination possibles.
- la valeur toxicologique de référence (VTR), correspondant à une dose totale admissible par jour ; pour cette substance elle sera considérée égale à 0.02 mg/kgcorporel/j (cf. tableau ci-dessus),
- un poids corporel moyen de 70 kg,
- Cons. Journ. Moy : une consommation moyenne de produits de la pêche (poissons, mollusques, crustacés) égale à 115 g par jour,
Ce calcul n'est donné qu'à titre indicatif. Il peut être inadapté pour couvrir les risques pour les individus plus sensibles ou plus vulnérables (masse corporelle plus faible, forte consommation de produits de la pêche, voies d'exposition individuelles particulières). Le facteur correctif de 10% n'est donné que par défaut, car la contribution des différentes voies d'exposition varie selon les propriétés de la substance (et en particulier sa distribution entre les différents compartiments de l'environnement), ainsi que selon les populations considérées (travailleurs exposés, exposition pour les consommateurs/utilisateurs, exposition via l'environnement uniquement). L'hypothèse cependant que la consommation des produits de la pêche ne représente pas plus de 10% des apports journalier contribuant à la dose journalière tolérable apporte une certaine marge de sécurité (E.C., 2010).
Pour le chlorobenzène, le calcul aboutit à :
![]()
![]()
- dans l'eau douce peut être estimée en tenant compte de la bioaccumulation de la substance :
- dans l'eau marine peut être estimée en tenant compte de la bioaccumulation de la substance :
![]()
Pour le chlorobenzène, on obtient donc :
![]()
QSmarin_hh food =1.22 / (447*1*1) = 0.0027 mg.L-1 = 2.7 µg.L-1
![]()
NORME DE QUALITE POUR LA SANTE HUMAINE VIA L'EAU DE BOISSON (QSdw_hh)
La norme de qualité pour l'eau de boisson est calculé de la façon suivante (E.C., 2010) :
![]()
Ce calcul tient compte de :
- un facteur correctif de 10% (soit 0.1) afin de tenir compte de ces autres sources de contamination possibles.
- la valeur toxicologique de référence (VTR), correspondant à une dose totale admissible par jour ; pour cette substance elle sera considérée égale à 0.02 mg/kgcorporel/j (cf. tableau ci-dessus),
- un poids corporel moyen de 70 kg,
- une consommation d'eau moyenne de 2 L par jour,
L'eau de boisson est obtenue à partir de l'eau brute du milieu après traitement pour la rendre potable. La fraction éliminée lors du traitement dépend de la technologie utilisée ainsi que des propriétés de la substance.
![]()
En l'absence d'information, on considèrera que la fraction éliminée est nulle et le critère pour l'eau de boisson s'appliquera alors à l'eau brute du milieu. Par ailleurs, on rappellera que ce calcul n'est donné qu'à titre indicatif et peut s'avérer inadéquat pour certaines substances et certaines populations.
Pour le chlorobenzène, on obtient :
![]()
![]()
Ce tableau comporte un trop grand nombre d'entrées pour permettre son affichage complet. Pour un affichage complet, utilisez l'une des options ci-dessus.
Synthèse
PROPOSITION DE NORME DE QUALITE ENVIRONNEMENTALE (NQE)
La NQE est définie à partir de la valeur de la norme de qualité la plus protectrice parmi tous les compartiments étudiés.
![]()
Pour le chlorobenzène, la norme de qualité pour l'eau douce et celle pour l'eau marine sont les valeurs les plus faibles pour l'ensemble des approches considérées et pour les compartiments considérés. La proposition de NQE pour le chlorobenzène est donc la suivante :
PROPOSITION DE NORME DE QUALITE ENVIRONNEMENTALE
![]()
VALEURS GUIDES POUR LE SEDIMENT
Avec un Koc de 224 L.kg-1 et un Log Kow = 2.85, la mise en œuvre d'un seuil pour le sédiment n'est pas recommandée par le projet de guide européen (E.C., 2010).
FDTE/VTR Importer Comme il existe des données long terme sur 3 niveaux trophiques, un facteur d’évaluation de 10 est utilisé pour le calcul de la PNEC eau. PNECeau = 32 µg/L
Bibliographie
Données technico-économiques
Dernière vérification le 29/03/2024
Tableaux de synthèse
Généralités
| CAS | 108-90-7 |
|---|---|
| SANDRE | 1467 |
| Substance prioritaire dans le domaine de l’eau (DCE) | non |
| Substance soumise à autorisation dans Reach | non |
| Substance soumise à restriction dans Reach | non |
| Substance extrêmement préoccupante (SVHC) | non |
| Réglementations |
FTE 2005 Importer ClassificationEn France, selon l INRS (1997), le chlorobenzène est classé comme une substance toxique (Xn, R20), nocive pour l environnement (N; R51/53). Elle est également inflammable (R10)1 . Certains conseils d'utilisation sont nécessaires à son utilisation et son stockage :
Textes législatifs de référence
En France et en Europe, le chlorobenzène n'est pas concerné par les deux textes suivants :
Seule l'OMS a édicté des directives de qualité pour l'eau de boisson (OMS, 1996) prenant en compte cette substance : teneur maximale en chlorobenzène acceptable : 300 Hg.L 1 .
[1] la classification du chlorobenzène est réglementée par l'arrêté du 20 avril 1994 relatif à la déclaration, la classification, l'emballage et l'étiquetage des substances chimiques complété par la directive 2004/73/CE de la commission du 29 avril 2004 (29ème adaptation au progrès technique de la directive). [2] Décret n°53 578 du 20 mai 1953 modifié relatif à la nomenclature des installations classées pour la protection de l'environnement mise à jour par le Ministère de l'écologie et du développement durable « Nomenclature des installations classées pour la protection de l'environnement » (2002).
Enfin, les rejets de chlorobenzène sont réglementés par les Arrêtés du 10 juillet 19904, et du 2 février 19985. Plus en détail, ces textes réglementent les rejets de chlorobenzène en tant que substance toxique, bioaccumulable ou nocive pour l'environnement. La teneur limite mensuelle dans ces rejets ne doit donc pas dépasser, 4 mg.L 1 si le rejet dépasse 10 g.j 1 . Selon l'arrêté du 20 avril 2005 relatif au programme national d'action contre la pollution des milieux aquatiques par certaines substances dangereuses, la norme de qualité des eaux a été définie pour le chlorobenzène à 32 Ng.L 1 .
Le chlorobenzène est un intermédiaire utilisé dans la production de DDT (dichlorodiphényltrichloroéthane). Ce pesticide est strictement réglementé par de nombreuses conventions internationales (Aarhus ; Genève et Stockholm). Son usage est en particulier interdit en France. [3] La liste des rubriques mentionnées est indicative et ne se veut pas exhaustive. [4] Arrêté relatif à l'interdiction des rejets de certaines substances dans les eaux souterraines en provenance d'installations classées (JO du 4 août 1990). [5] Arrêté relatif aux prélèvements et à la consommation d'eau ainsi qu'aux émissions de toute nature des installations classées pour la protection de l'environnement soumises à autorisation (JO du 3 mars 1998). |
| Classification CLP | Voir la classification CLP |
Production et utilisation
Production et ventes
Données économiques
FTE 2005 Importer
Principe de production
Le chlorobenzène est obtenu par chloration du benzène en présence d'un catalyseur (chlorure ferrique, stannique ou alumineux). On obtient ainsi un mélange de produits composé de chlorobenzène, dichlorobenzène et d'autres produits chimiquement voisins qu'il faut séparer par distillation et cristallisation.
Le chlorobenzène de qualité technique est généralement pur à 99 % et, selon un rapport édité par le Gouvernement du Canada (1992), les principales impuretés qu'il renferme sont du benzène (<0,05%) et du dichlorobenzène (<0,1%).
Production
Le déclin de la production de chlorobenzène à partir de 1960, aux USA, résulte de deux causes principales :
- abandon du chlorobenzène pour la fabrication de phénol et d'aniline,
- baisse, voire arrêt, de la production des pesticides ou insecticides (DDT) utilisant le chlorobenzène comme intermédiaire chimique dans leur fabrication.
Aujourd'hui, le phénol est produit dans le monde, à près de 90% à partir du cumène (IPPC, 2003). On en produit, en France, à partir de cette molécule, en moyenne 150 kt.an-1. La production à partir de chlorobenzène, même si elle peut toujours exister reste donc très marginale. De même, l'aniline est aujourd'hui produit en très grande majorité à partir de nitrobenzène. Dans ces conditions, la production de chlorobenzène a subi le même déclin en Europe et en France (SHD, 2005).
Selon l'ESIS (2005), les producteurs en Europe sont essentiellement Bayer, BASF (Allemagne), Monsanto (Belgique), Zeneca (Royaume Unis).
Seul le site de production français, l'usine Arkema de Jarrie a produit du chlorobenzène jusqu'en 2002. Il servait ensuite lors de la production d'herbicides et de fongicides (anti mites…). Toutefois, suite aux interdictions d'utilisation de nombreux produits issus du chlorobenzène (DDT et autres produits dérivés), le maintien des unités de production des chlorobenzènes est apparu impossible. Ces unités ont donc été démantelées et la production des chlorobenzènes n'est plus une activité du groupe Arkema. Il n'y a donc plus d'usine de production de chlorobenzène en France, sauf peut être des productions marginales. Ces informations nous ont d'ailleurs été confirmées par le Syndicat des Halogènes et Dérivés.
En revanche, l'usine Rhodia Organique (Mulhouse Dornach) semble toujours utiliser du chlorobenzène pour la synthèse de nitrochlorobenzène.
Place de la substance dans l'économie Française
En France, l'usine Rhodia Organique Mulhouse Dornach utilise du chlorobenzène pour la synthèse de nitrochlorobenzène.
L'usine Arkema de Jarrie a également produit du chlorobenzène jusqu'en 2002. Il servait en particulier à la production d'herbicides et de fongicides (anti mites…). Après des études technico économiques, le maintien des unités de production et de transformation de chlorobenzène est apparu impossible. Ces unités ont donc été démantelées et la production de chlorobenzène n'est plus une activité du groupe Arkema.
Utilisé en tant que solvant, le chlorobenzène, avec 350 t, ne représente que 1% de la consommation de solvants halogénés en France (INRS, 2005).
Impact économique des mesures de réduction
On peut estimer le coût de la réduction des émissions de COV par les industriels en étudiant le marché de la lutte contre les Composés Organiques Volatils. Celui ci a été estimé à 32,4 M€ en 2004, en augmentation de 20% par rapport à 2003. Il devrait encore continuer à augmenter de 20% en 2005, pour atteindre 38,8 M€ (Actu® environnement, 2005).
Les procédés de traitement des COV ont des coûts qui vont dépendre du type d'installation et du débit de gaz. On peut citer plusieurs installations (Alcimed, 2002) :
Tableau 5.1. Coût comparatifs de quelques installations industrielles de traitement des COV.
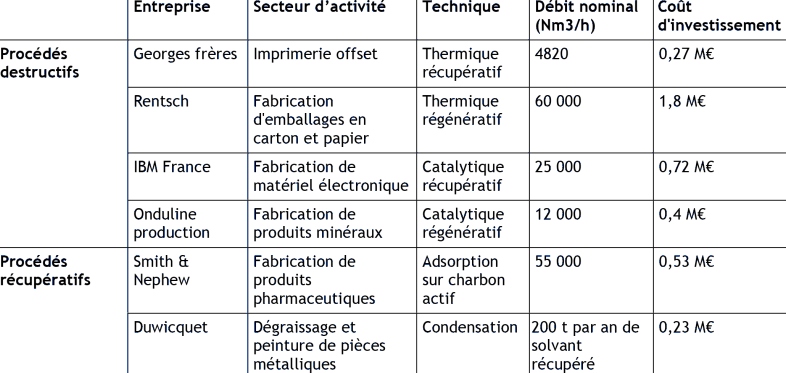
En se basant sur le prix des importations (Direction générale des douanes, 2005) le prix du cumène s'est établi en 2004 autour de 830 €.t 1. Alors que le prix du chlorobenzène s'est établit à 900 €.t 1 pour la même période. La synthèse du phénol est donc plus intéressante économiquement en utilisant du cumène. Même si nous ne connaissons pas le prix du nitrobenzène, il est intéressant de constater que le prix de l'aniline en 2004 était similaire au prix du chlorobenzène. Il semble donc plus intéressant de produire de l'aniline à partir du nitrobenzène qu'à partir du chlorobenzène. De façon générale, les substituants au chlorobenzène, utilisés comme intermédiaires réactionnels, paraissent plus intéressants économiquement.
De même, selon les industriels interrogés, le coût de la régénération et de la réutilisation des solvants est aujourd'hui plus faible que le coût d'achat d'un solvant neuf auquel il faut ajouter le coût de la destruction après utilisation.
Utilisations
Introduction
FTE 2005 Importer
Selon Srour (cité dans Euro Chlor, 1999), en 1987, un total de 97 000 t de chlorobenzène a été utilisé en Europe de l'ouest pour les usages suivants :
- fabrication des nitrochlorobenzènes 6 75 000 t (77%) ;
- autres transformations chimiques 15 000 t (16%)
- solvant de procédés 5 000 t (5%)
- Autres solvants (ex : fabrication de produits phytosanitaires) 2 000 t (2%).
Ainsi, comme le confirment diverses sources (EPA, 2005 ; Eurochlor, 1999), le chlorobenzène est, dans une large majorité des cas, utilisé comme intermédiaire réactionnel dans la fabrication d'autres produits chimiques (nitrochlorobenzène). Ces composés sont à la base de nombreuses réactions chimiques, en particulier les réactions utilisant des amines aromatiques (aniline) et les alcools aromatiques. Ces réactions ont de nombreuses applications comme la fabrication de colorants/teintures et surtout d'insecticides organiques (DDT). Toutefois dans tous ces produits finis, le chlorobenzène n'est pas présent sous une forme libre, notamment le DDT.
En outre, le chlorobenzène sert également comme solvant ou agent d'extraction dans certaines réactions chimiques (production de di isocyonate de méthylène et insecticide). Ainsi, dans son panorama sur l'utilisation des solvants, l'INRS (2005) indique que 350 t de chlorobenzène sont utilisées chaque année en France pour la formulation de préparations solvantées utilisées dans l'agrochimie. Selon le SHD (2005), ces solvants ne sont pas produits en France. En revanche, il est toujours possible d'en importer pour les utiliser dans des formulations. Le chlorobenzène peut servir également comme dégraissant dans les industries textiles et métallurgiques. Ces utilisations restent toutefois marginales. Lors de ces différentes utilisations, cette substance n'est pas présente sous forme libre dans les produits finis, mais elle peut être présente dans les effluents liquides ou gazeux.
[6] Substance utilisée pour la synthèse des produits phytosanitaires regroupés sous le nom de leur substance active : le carbofuran (Acta, 2004).
Le chlorobenzène peut également être utilisé comme solvant dans les adhésifs, les peintures, et les vernis. Dans ces derniers cas, il est directement présent dans les produits finis et peut donc se volatiliser dans l'environnement ou être rejeté dans les eaux. Toutefois cette utilisation semble avoir aujourd'hui disparu du fait des réglementations sur l'utilisation des solvants chlorés. L'INRS ne les mentionne d'ailleurs pas dans son panorama sur l'utilisation de solvants (2005).
Enfin, d'autres utilisations peuvent être mentionnées mais elles ne semblent pas représenter une quantité importante de produits. On peut ainsi citer l'utilisation de chlorobenzène dans des produits de nettoyage à sec, en tant qu'agent de gonflement des fibres dans l'industrie textile (EPA, 2005 ; INERIS, 2005), comme fluide diélectrique et fluide de transfert de chaleur (INERIS, 2005) ou encore comme répulsif à action contre les taupes.
De façon générale, le chlorobenzène est donc une substance de base utilisée lors de synthèses chimiques et 95% des quantités totales utilisées sont transformées, dans des systèmes fermés, en produits intermédiaires et finaux (Euro Chlor, 1999).
Rejets dans l’environnement
Rejets dans l'environnement
FTE 2005 Importer
Compte tenu du potentiel de dégradation par photolyse et biodégradation, le chlorobenzène est relativement peu persistant dans l'environnement.
Dans l'atmosphère, le chlorobenzène est présent sous forme de vapeur, il est dégradé par réaction photochimique sous forme de radicaux hydroxylés. Sa demi vie est de 21 jours (Atkinson, 1989).
Dans l'eau, la demi vie mesurée a été établie à 17,5 heures (eau distillée) et à 3,8 heures dans une eau de rivière (Mansour 1996). Suite à un rejet de chlorobenzène dans l'eau, la dissipation de cette substance s'effectue majoritairement par évaporation (EPA, 2005) : le temps de demi vie pour l'évaporation est de ~4,5 heures dans des conditions de vent modérées. A ce premier phénomène s'additionne l'adsorption sur les matières en suspension et les sédiments (INERIS, 2005).
Dans le sol, la mobilité du chlorobenzène est modérée à élevée (HSDB, 2003; Walton et al., 1992). La volatilisation de cette substance à partir de sols humides est donc probablement une voie de transfert privilégiée vers d'autres compartiments environnementaux.
La biodégradation du chlorobenzène dans les compartiments terrestres est variable : absence de minéralisation dans le sol après 8 mois ou des demi vies de biodégradation de 200 à 600 jours (expériences menées à partir de consortium bactérien). De plus, il a été observé que le temps de minéralisation est considérablement réduit lors d'ajout de phosphate et d'ammonium dans les sols (INERIS, 2005) ou lors de la présence d'une source de carbone pour les microorganismes (Callahan et al. 1979).
Les émissions de chlorobenzène dans l'environnement se font très majoritairement vers l'atmosphère. Elles ont pour origine les rejets industriels des usines fabricant ou utilisant le chlorobenzène. Les émissions sont dues pour l'essentiel aux pertes par volatilisation se produisant au cours de l'utilisation de chlorobenzène dans les différentes applications industrielles (INERIS, 2005 ; EPA, 2005), en particulier lorsqu'il est utilisé en tant que solvant ou dégraissant et qu'il ne subit donc pas de transformations. Pour limiter ces rejets, les modes de fabrication font intervenir des systèmes fermés, mais ces émissions ne peuvent pas être totalement évitées.
Au cours de ces différents processus industriels, le chlorobenzène peut également être rejeté dans les effluents aqueux des usines (eaux de rinçage…). Ces rejets représentent la source principale de pollution de l'eau (INERIS, 2005).
Euro Chlor (association représentant l'industrie du chlore) rapporte les émissions de chlorobenzène (Euro Chlor, 1999) par les industries européennes dans l'air (Fig. 3.1a) et dans l'eau (Fig. 3.1b).
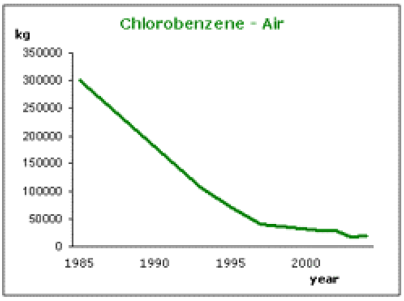
Figure 3.4. Emissions industrielles de chlorobenzène (en kg) d'après Euro Chlore (1999) : A : dans le compartiment aérien ; B : dans l'eau.
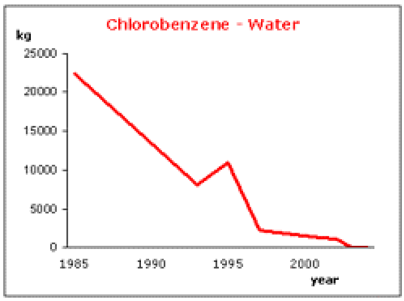
Ces graphiques confirment l'importance des rejets atmosphériques du chlorobenzène, puisque les quantités émises dans l'air sont 10 fois plus grandes que celles émises dans l'eau. Néanmoins, on constate pour l'ensemble des substances chlorées (y compris le chlorobenzène), entre 1985 et 2004, une réduction de ~99% (en masse) des quantités rejetées dans l'eau et ~93% de celles rejetées dans l'air (Euro Chlor, 1999).
Lors d'un premier inventaire des émissions polluantes réalisé entre 1991 et 2000 dans 9 régions françaises, on estimait que le flux total de chlorobenzène, émis par des installations industrielles était de 69 kg.j 1 (République française, 2005). De même, dans le cadre de l'action nationale de recherche et de réduction des substance dangereuses dans l'eau, des mesures ponctuelles ont été réalisées à la sortie de près d'un millier d'ICPE. Il apparaît que le flux total de chlorobenzène issu de ces installations est de 49 kg.j 1 en 2003/2004. Enfin, en région Rhône Alpes, où deux inventaires des rejets de micropolluants, par des établissements industriels, ont été réalisés en 1993 et 1998, on constate une baisse des émissions de chlorobenzène. Ainsi, le flux total qui représentait 67 kg.j 1 en 1993 a baissé à 8 kg.j 1 en 1998. Ces résultats, confirment tout d'abord que les émissions de chlorobenzène dans les milieux aqueux diminuent. En outre, les rejets sont dus pour l'essentiel au secteur de la chimie et de la parachimie. On retrouve en particulier des traces de chlorobenzène dans les effluents aqueux des usines Rhodia de Mulhouse (0,7 kg.j 1) et Arkema de Jarrie (DRIRE Alsace, 1998 ; DRIRE Rhône Alpes, 2004). Néanmoins, pour cette dernière, nous ne disposons pas de mesures réalisées après l'arrêt des unités de production de chlorobenzène en 2002.
Enfin, selon le gouvernement du Canada (1992), l'élimination de déchets industriels par incinération est également une source de contamination de l'environnement par le chlorobenzene. Il sont aussi détectés dans les rejets d'usines d'incinération d'ordures ménagères (ASTEE, 2003).
L'usage non industriel de produits contenant du chlorobenzène n'est pas considéré comme une voie d'émission significative (EPA, 2005). Ces rejets proviennent essentiellement des vapeurs de peintures, vernis et autres adhésifs ayant le chlorobenzène comme solvant. Un déversement de ces produits dans l'environnement pourra également entraîner une pollution de l'eau.
Pollutions historiques et accidentelles
FTE 2005 Importer
Le chlorobenzène est à la base de l'acide picrique qui fut utilisé pendant la Première Guerre Mondiale sous le nom de mélinite pour le chargement des obus.
Présence environnementale
Synthèse
FTE 2005 Importer
Le chlorobenzène présent dans l'environnement fait partie de la famille des composés organiques volatils et est d'origine anthropique. La concentration atmosphérique en chlorobenzène est évaluée à 0,1 g.m 3 dans ATSDR (1990) et Howard (1989). Des pourcentages indicatifs de partition de cette substance entre les différents compartiments de l'environnement ont été obtenus (Table 3.1) par Mackay et Patterson (1990) par modélisation.
Table 3.2. Partition du chlorobenzène entre les différents compartiments de l'environnement selon (Mackay and Patterson, 1990)
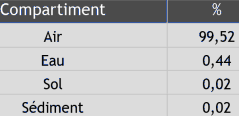
Perspectives de réduction
Réduction des rejets
Techniques de traitement des milieux pollués
FTE 2005 Importer
Traitement par ultra-sons
Des techniques de dégradation du chlorobenzène par l'usage d'ultra sons ont été expérimentées en laboratoire (Kruus et al., 1997, Jiang et al., 2002). Néanmoins, à ce jour, aucune application pratique de ces techniques n'a été rapportée.
Bioremédiation
Différentes techniques de dégradation microbienne du chlorobenzène (ou bioremédiation) présent dans des eaux souterraines ou des sols ont été testées in vitro (Alfreider et al., 2003 ; Jechorek et al., 2003 ; Muller et al., 2003 ; Vogt et al., 2004).
Epuration naturelle
Le Cemagref (2000) a prouvé, suite à des expérimentations de terrain que des zones d'herbe, implantées judicieusement sur un bassin versant à vocation agricole, sont capables de retenir une grande partie des pesticides véhiculés par les eaux de ruissellement (dont ceux contenant du chlorobenzène). L'épuration s'effectue par adsorption des substances sur la matrice minérale constituant le sol et/ou par dégradation microbienne in situ (Monferrán et al., 2005).
Ce type de système d'épuration naturelle, peut être utilisé en complément de la promotion de bonnes pratiques agricoles.
Traitement des effluents gazeux
FTE 2005 Importer
Le chlorobenzène étant un COV, le traitement des effluents gazeux contenant de tels composés est donc d'une grande importance. Nous n'avons pas identifié d'informations sur des traitements spécifiques au chlorobenzène ; on rappelle ci après quelques informations générales sur le traitement des COV.
Selon les experts du programme INTERREG III (2005), les COV sont actuellement traités selon deux grandes familles de techniques :
- Les techniques récupératrices et en particulier l'adsorption qui représente 10% des procédés en fonctionnement ;
- Les techniques destructives que sont l'oxydation thermique ou catalytique qui représentent 80% des traitement mais où l'oxydation en présence d'un catalyseur ne représentent que 5% de ce traitement.
Pourtant c'est ce dernier procédé qui semble le plus intéressant puisqu'il permet à la fois d'abaisser la température de combustion et donc de réaliser des économies d'énergie, mais aussi d'éviter la formation de NOx. Par ailleurs, la grande sélectivité de l'oxydation catalytique peut également éviter la formation de composés intermédiaires bien plus toxiques que les COV de départ ou de chlore. Cependant, les catalyseurs ont tendance à se désactiver au cours du temps.
Des études sont actuellement menées pour développer des catalyseurs permettant d'éliminer les COV chlorés par oxydation totale. Une étude est également menée pour développer une méthode de valorisation des COV par hydrodéchloration catalytique (Interreg III, 2005). Cette méthode aurait l'avantage de transformer les COV en produits chimiques organiques à valeur commerciale et/ou à contenu énergétique. Enfin une dernière étude est le développement d'adsorbants nouveaux pour la séparation et la récupération par adsorption de COV7 .
Stations d'épuration
FTE 2005 Importer
Il est difficile de trouver un procédé de traitement spécifique adapté au chlorobenzène. De plus, la décomposition de composés organiques halogénés par des traitements biochimiques peut poser quelques problèmes. Leur décomposition est parfois difficile ou impossible pour les micro organismes et la concentration des effluents doit rester la plus stable et la plus basse possible. Pour résoudre ces problèmes on peut effectuer des traitements primaires, soit avec du charbon actif, soit par un procédé thermochimique (oxydation à haute température et basse pression) (Dilla, W., et al., 1995 ). Dans ce dernier cas, on peut également utiliser des catalyseurs qui vont aider à la réaction d'oxydation. Dans le cas du charbon actif, plusieurs sources (Lenntech, chemviron Carbon, correspondance personnelle) indiquent que le chlorobenzène présente une très grande probabilité d'être efficacement adsorbé sur le charbon actif (http://www.lenntech.com/fran%C3%A7ais /adsorption.htm).
Recyclage
FTE 2005 Importer
D'autres solutions peuvent être envisagées pour réduire les rejets de chlorobenzène telles que son recyclage. Lorsqu'il est utilisé en tant que solvant lors de procédés de fabrication, il peut être envisagé de le régénérer par distillation.
[7] D'autres études de Huang Y. et al, (2003), de Ukisu Y. et al, (2000) et de Keane M.A et al, (2001) peuvent également être consultées.
Alternatives aux usages
Produits de substitution
FTE 2005 Importer
Synthèse du phénol :
Pendant longtemps, le chlorobenzène a été utilisé pour produire du phénol, intermédiaire réactionnel très utilisé en chimie. La synthèse de ce phénol consiste en une hydrolyse basique à chaud (350°C) du chlorobenzène.
A la place du chlorobenzène, le phénol peut être produit à partir du cumène8 :
Selon la Société Française de Chimie, en 1994, la capacité de production de cumène en France était de 200 000 t et était dédiée à la production de phénol à hauteur de 150 000 t. Ces deux composés sont toujours produits en France par la seule usine Rhodia de Roussillon (38).
Il est à signaler que cette synthèse du phénol à partir du cumène a diminué de façon significative les quantités de chlorobenzène utilisées aux Etats Unis à partir de 1960. Toutefois aucune étude n'a démontré une évolution semblable en Europe.
Synthèse de l'aniline
Le chlorobenzène peut être utilisé comme réactif dans la synthèse de l'aniline. Ce composé est synthétisé en chauffant de l'ammoniaque avec du chlorobenzène en présence d'un catalyseur (cuivre).
L'aniline peut également être produite à partir du benzène en deux étapes. La première étape consiste en la nitration du benzène par de l'acide nitrique. Puis le nitrobenzène ainsi formé est réduit en aniline grâce à l'ajout d'un agent de réduction (catalyseur).
Comme pour la synthèse du phénol, la synthèse de l'aniline, même si elle évite l'utilisation de chlorobenzène fait intervenir du benzène, autre substance visée par la Directive 76/464/CE de la Directive Cadre Eau. On peut donc dans ces conditions s'interroger sur l'intérêt environnemental de telles synthèses. On peut néanmoins signaler qu'elles ne font pas intervenir de composés chlorés dont la synthèse nécessite celle de chlore (souvent polluante et coûteuse en énergie).
[8] aujourd'hui, selon l'agence américaine de protection de l'environnement, le cumène ne semble pas être toxique pour l'environnement. En revanche, sa synthèse fait intervenir le benzène, inscrit à la liste des substances chimiques dangereuses prioritaires de la Directive Cadre Eau.
Synthèse du nitrochlorobenzène.
Le chlorobenzène rentre dans la production de nitrochlorobenzène. Ce composé est synthétisé par nitration de chlorobenzène grâce à l'acide nitrique et en présence d'acide sulfurique. On obtient alors un mélange de trois molécules :
- le p nitrochlorobenzène (65%) ;
- le o nitrochlorobenzène (34%) ;
- le m nitrochlorobenzène (1%).
Ces molécules de nitrochlorobenzène servent ensuite à la synthèse de pesticides, de produits intermédiaires (25%) et de colorants (40%).
En France, l'entreprise Rhodia organique Mulhouse Dornach possède une unité de fabrication de nitrochlorobenzène qui sert ensuite à la synthèse d'intermédiaires réactionnels. Toutefois, il semble que cette unité soit la seule fonctionnant en France.
A ce jour il ne semble pas exister d'autre méthode de synthèse de nitrochlorobenzène.
Autres produits de substitution.
En tant que solvant, le chlorobenzène peut être facilement substitué, que ce soit dans les peintures ou dans les produits phytosanitaires. Ainsi, certaines peintures ne contiennent pas de chlorobenzène, en particulier lorsqu'elles sont employées comme peintures fongicides dans certaines industries comme l'agro alimentaire. On peut ainsi signaler le cas de l'entreprise ARTILIN qui propose des peintures à l'eau, sans chlorobenzène, labellisées « vertes ».
De façon générale, la consommation des solvants chlorés à énormément diminué, en Europe, depuis trente ans, passant de 920 000 à 220 000 t.an-1. Cette diminution s'est traduite, le plus souvent, par l'emploi de solvants de substitution, ou par le développement de techniques sans solvant.
Conclusion
FTE 2005 Importer
Le chlorobenzène est un composé aromatique halogéné volatil. Il est utilisé essentiellement pour la synthèse du nitrochlorobenzène, et comme solvant. Toutefois, ces usages sont devenus rares, et comme la plupart des composés et solvants halogénés, sa production a été en constante diminution depuis trente ans. Il n'est d'ailleurs plus synthétisé en France depuis la fermeture des unités de production de l'usine Arkema de Jarrie. Aujourd'hui le chlorobenzène n'est plus utilisé que dans les rares cas où il n'existe pas de produits de substitution. Sa consommation comme solvant est pratiquement nulle.
Les émissions de chlorobenzène se font avant tout vers l'atmosphère, et sont dues aux rejets industriels liés à son utilisation. Ces émissions sont en diminution constante depuis de nombreuses années.
En outre, dans de nombreuses synthèses, où le chlorobenzène était utilisé comme intermédiaire réactionnels (synthèse du phénol et de l'aniline), les industriels utilisent aujourd'hui des produits de substitutions. La consommation de chlorobenzène a donc pour ces usages fortement diminué. De plus, de nombreux produits issus de la fabrication du chlorobenzène sont aujourd'hui interdits en France (DDTet dérivés). Cette substance n'est plus utilisé que dans de rares applications et pour des synthèses ou il n'existe pas d'autre substituant (nitrochlorobenzène).
Face à ces baisses de consommation, la production de chlorobenzène s'avère aujourd'hui non intéressante économiquement. Face à ce constat, et au regard des évolutions des émissions en Europe, on peut penser que les rejets de chlorobenzène continueront à baisser en France, mais modérément puisqu'ils sont déjà faibles.
Bibliographie
Archives
Dernière vérification le 29/03/2024
Documents
Exporter la substance
Choisissez le format de l'export :










